目次
📍 クイックナビゲーション
「ヌーナン症候群って聞いたことがない」「ダウン症とは違うの?」そんな疑問を持たれる方も多いでしょう。ヌーナン症候群は1963年にアメリカの心臓専門医ジャクリーン・ヌーナン博士によって報告された遺伝性疾患で、ダウン症候群に次いで2番目に多い先天性疾患です。
発症頻度は1,000〜2,500人に1人と決して稀ではなく、RAS/MAPK経路の遺伝子変異が原因です。にもかかわらず、従来のNIPTや羊水検査では発見できないという特徴があります。
- ➤ ヌーナン症候群とは何か、発症頻度と基本情報
- ➤ 心疾患・低身長・顔貌など主な症状と個人差
- ➤ PTPN11をはじめとするRAS/MAPK経路の原因遺伝子
- ➤ なぜ従来のNIPTでは検出できないのか
- ➤ ダイヤモンドプランで妊娠10週から検査できる理由
1. ヌーナン症候群とは|基本情報と発症頻度
【結論】 ヌーナン症候群はダウン症候群に次いで2番目に多い先天性疾患で、発症頻度は1,000〜2,500人に1人です。RAS/MAPK経路の遺伝子変異が原因で、特徴的な顔貌・先天性心疾患・低身長などを特徴とします。
ダウン症候群が染色体の数の異常(21トリソミー)であるのに対し、ヌーナン症候群は特定の遺伝子の変異が原因です。そのため、従来のNIPTや羊水検査では発見できないという特徴があります。
-
•
発症頻度:1,000〜2,500人に1人(ダウン症候群に次いで2番目)
-
•
原因:RAS/MAPK経路の遺伝子変異(PTPN11・SOS1・RAF1など)
-
•
遺伝形式:常染色体優性遺伝(約70%がde novo変異=新生突然変異)
-
•
男女比:ほぼ同等(やや男性に多いという報告も)
💡 RASopathy(ラソパチー)とは
ヌーナン症候群は「RASopathy(ラソパチー)」と呼ばれる疾患群の代表的な疾患です。RAS/MAPK経路は細胞の成長・分化に関わる重要なシグナル伝達経路で、この経路に関わる遺伝子の変異によって引き起こされる疾患群を総称します。コステロ症候群・心臓顔面皮膚症候群(CFC症候群)・レジウス症候群なども同じ仲間です。
2. ヌーナン症候群の特徴・症状
【結論】 ヌーナン症候群の主な症状は特徴的な顔貌・先天性心疾患(約80%)・低身長です。症状の程度には個人差が大きく、軽症の方は成人後に診断されることもあります。
ヌーナン症候群の症状は非常に多岐にわたりますが、すべての方にすべての症状が現れるわけではありません。症状の重さには大きな個人差があり、日常生活にほとんど支障がない軽症の方から、医療的ケアを必要とする方まで様々です。
主な症状一覧
❤️ 心臓の症状(約80%)
- •
肺動脈弁狭窄(約50〜60%)
- •
肥大型心筋症(約20〜30%)
- •
心房中隔欠損
- •
心室中隔欠損
📏 成長の特徴
- •
低身長(約70%)
- •
出生時は正常範囲のことが多い
- •
成人男性の平均身長:約162cm
- •
成人女性の平均身長:約153cm
🧒 発達の特徴
- •
運動発達の遅れ(約25%)
- •
言語発達の遅れ
- •
軽度の知的障害(約15〜35%)
- •
多くの方は知的に正常範囲
🩸 血液・凝固の異常
- •
出血傾向(約50〜60%)
- •
血小板減少
- •
凝固因子の異常
- •
あざができやすい
⚠️ 重要:ヌーナン症候群の症状は個人差が非常に大きいのが特徴です。軽症の方は大人になるまで診断されないケースもあり、ご家族の中に気づかれていない方がいることもあります。
3. ヌーナン症候群の顔つき・顔貌の特徴
【結論】 ヌーナン症候群には特徴的な顔貌があり、眼間開離・眼瞼下垂・低い耳介・短い首などが見られます。これらの特徴は年齢とともに変化し、成人になると目立たなくなることもあります。
ヌーナン症候群の顔貌の特徴は、年齢によって変化するのが特徴的です。乳児期と成人期では顔つきが異なり、成人になるにつれて特徴が目立たなくなる方もいます。
-
•
眼間開離(がんかんかいり):目と目の間隔が広い
-
•
眼瞼下垂(がんけんかすい):まぶたが下がって目が開きにくい
-
•
低い耳介(じかい):耳の位置が低く、後方に回転している
-
•
高い前額(ぜんがく):おでこが高く突出している
-
•
鼻根部の陥凹:鼻の付け根が平坦
-
•
翼状頸(よくじょうけい):首の側面に皮膚のひだがある
-
•
短い首、低い後頭部の髪の生え際
年齢による顔貌の変化
赤ちゃんの特徴が気になっていませんか?
ネットで調べるほど不安になることも。臨床遺伝専門医と直接お話しすることで、正確な情報と安心を得られます。
※オンライン診療も対応可能です
4. ヌーナン症候群の原因遺伝子(RAS/MAPK経路)
【結論】 ヌーナン症候群はRAS/MAPK経路の遺伝子変異が原因です。PTPN11が約50%を占め、SOS1・RAF1・KRAS・BRAFなど現在17以上の原因遺伝子が特定されています。
ヌーナン症候群の原因は染色体の数や構造の異常ではなく、特定の遺伝子の変異です。そのため、従来の染色体検査(Gバンド法やマイクロアレイ)では発見できません。
RAS/MAPK(ラス・マップキナーゼ)経路とは、細胞の増殖・分化・生存をコントロールするシグナル伝達の経路です。受容体から核へ「成長せよ」「分化せよ」というメッセージを伝えるリレーのようなもので、KRAS・RAF1・MEKなどのタンパク質が連鎖的に働きます。この経路に関わる遺伝子に変異が起きると、シグナルが過剰・異常に流れ続け、胎児発達に影響が出ます。
-
1
PTPN11:約50%(最も多い)
-
2
SOS1:約10〜13%
-
3
RAF1:約3〜17%(肥大型心筋症と関連が強い)
-
4
RIT1:約5%
-
5
KRAS:約2〜5%
-
他
BRAF・NRAS・MAP2K1・MAP2K2・SOS2など多数
💡 ダイヤモンドプランで検査可能な遺伝子
ダイヤモンドプランでは、ヌーナン症候群の原因となるPTPN11・SOS1・RAF1・RIT1・KRAS・BRAF・NRAS・MAP2K1・MAP2K2などを含む56遺伝子のde novo変異を検査可能です。COATE法により99.9%以上の精度で検出できます。
従来のNIPTでは検出できない理由
一般的なNIPTは染色体の数の異常(トリソミーなど)を検出する検査です。ヌーナン症候群は遺伝子の「塩基配列の変異」が原因のため、染色体の数は正常です。そのため、従来のNIPTや羊水検査(Gバンド法)では発見できません。
❌ 検出できない検査
- ×
一般的なNIPT(21/18/13トリソミーのみ)
- ×
羊水検査(Gバンド法)
- ×
コンバインド検査
✓ 検出できる検査
- ✓
ダイヤモンドプラン(de novo変異NIPT)
- ✓
羊水検査(遺伝子パネル検査)
- ✓
出生後の遺伝子検査
5. ヌーナン症候群の遺伝のしかた
【結論】 ヌーナン症候群は常染色体優性遺伝ですが、約70%はde novo変異(新生突然変異)で、両親のどちらにも変異がないケースです。de novo変異は父親の年齢が高いほどリスクが上昇します。
「家族に誰もヌーナン症候群の人がいないのに、どうして?」という疑問を持たれる方も多いでしょう。実は、ヌーナン症候群の多くは両親から遺伝したものではなく、受精前後に新たに発生した変異(de novo変異)が原因です。
de novo変異(デノボ変異)とは、両親のどちらにも存在しない、子どもで新たに生じた遺伝子変異のことです。精子や卵子が作られるとき、またはその後の細胞分裂の過程でDNAのコピーエラーが起きることで発生します。「遺伝した」のではなく「新たに発生した」変異であるため、家族歴がなくても発症します。
-
•
遺伝形式:常染色体優性遺伝(1コピーの変異で発症)
-
•
de novo変異(新生突然変異):約70%(両親に変異なし)
-
•
親から遺伝:約30%(特に母親からの遺伝が多い報告あり)
-
•
父親の年齢:de novo変異のリスクは父親の年齢とともに上昇
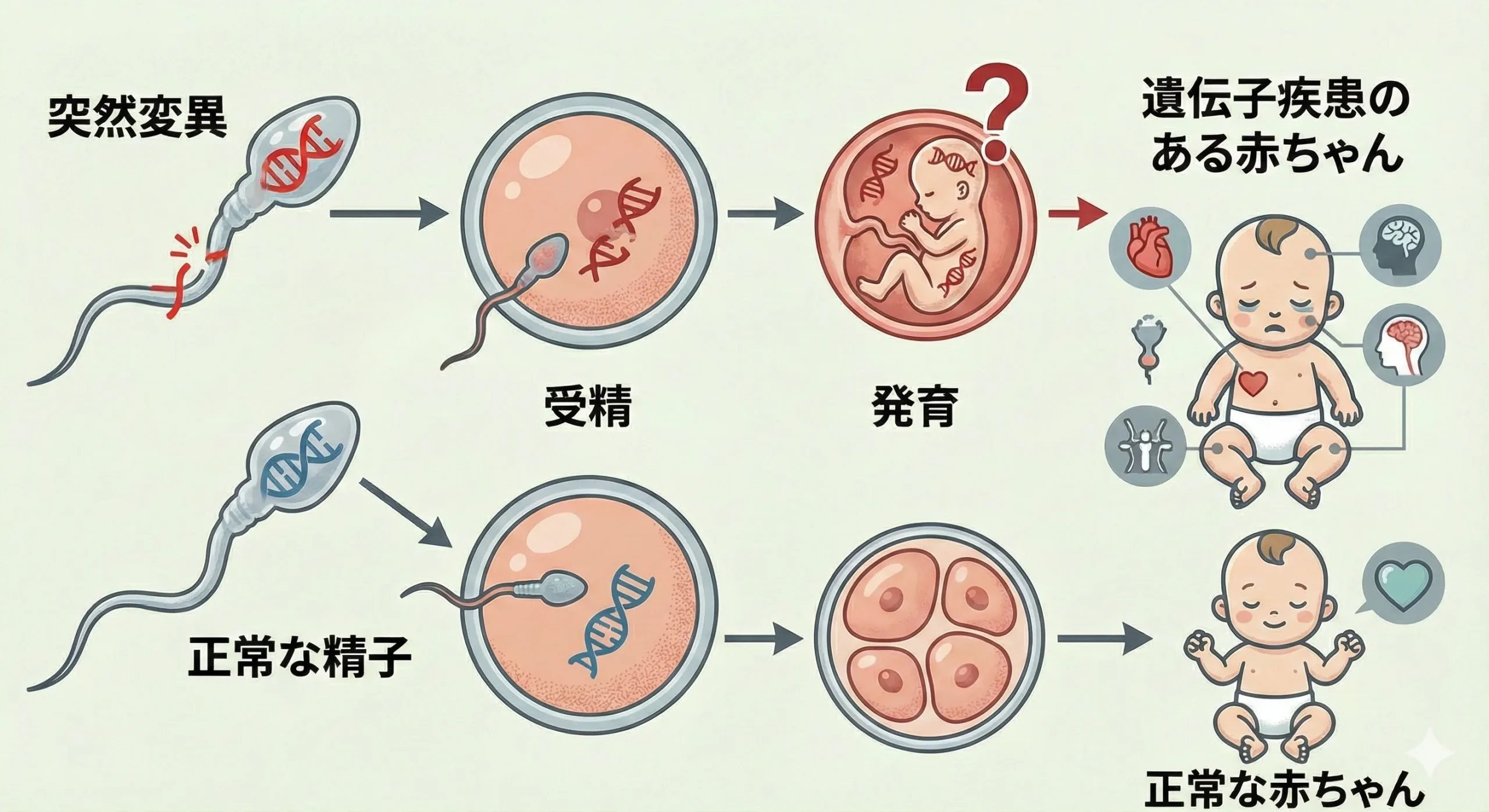
(父親由来の遺伝子変異が子へ伝わるイメージ)
de novo変異と父親の年齢の関係
精子は生涯にわたって作られ続けるため、父親の年齢が上がるほど精子のDNA複製回数が増え、変異が蓄積しやすくなります。ヌーナン症候群を含む多くのde novo変異疾患は、父親由来の変異が多いことが知られています。
⚠️ 重要:de novo変異は「誰にでも起こりうる」ものであり、特定のご夫婦だけのリスクではありません。累積リスクは1/600程度と報告されており、決して稀なことではありません。当院の検査では約60人に1人が陽性となっています。
6. ヌーナン症候群はいつわかる?診断時期と方法
【結論】 ヌーナン症候群は出生前でも出生後でも診断可能です。出生前はダイヤモンドプランで妊娠10週から検査でき、出生後は臨床症状と遺伝子検査で確定診断されます。
「ヌーナン症候群はいつわかるの?」「妊娠中に検査できるの?」という疑問を持たれる方は多いでしょう。診断のタイミングは「出生前」と「出生後」に大きく分けられます。
- ①
-
②
出生直後〜乳児期
・特徴的な顔貌・先天性心疾患・筋緊張低下などから疑い
・遺伝子検査(RASopathyパネル検査)で確定 -
③
幼児期〜成人期
・低身長・発達遅延・心疾患などから疑い
・軽症例は大人になってから診断されることも
胎児超音波検査での所見
妊娠中の超音波検査で、ヌーナン症候群を疑わせる所見が見つかることがあります。ただし、これらの所見は他の疾患でも見られるため、確定診断には遺伝子検査が必要です。
7. ヌーナン症候群の平均寿命・予後
【結論】 ヌーナン症候群の方の平均寿命は一般の方とほぼ変わらないとされています。ただし、心疾患の種類や重症度によって予後は異なります。適切な医療管理のもと、多くの方が社会生活を送っています。
「ヌーナン症候群の寿命は?」「普通に生活できるの?」という不安を持たれる方も多いでしょう。結論から言うと、多くの方は一般の方と変わらない寿命を期待でき、社会生活を送ることができます。
-
•
平均寿命:一般の方とほぼ同等(心疾患の程度による)
-
•
予後を左右する因子:心疾患の種類と重症度が最も重要
-
•
肥大型心筋症(HCM):RAF1変異に多く、予後に影響する可能性
-
•
社会生活:多くの方が就労・結婚・出産を経験
遺伝子タイプによる違い
原因遺伝子によって、症状の傾向や予後に違いがあることが報告されています。
💚 社会生活について
多くのヌーナン症候群の方は、普通学級で学び、就労し、結婚・出産を経験しています。軽度の知的障害がある場合でも、適切なサポートを受けながら社会生活を送ることができます。早期からの療育や医療的フォローが、その後の生活の質を高めることにつながります。
8. NIPTでヌーナン症候群を検査できる?
【結論】 一般的なNIPTではヌーナン症候群は検出できませんが、ミネルバクリニックのダイヤモンドプランなら妊娠10週から検査可能です。COATE法により99.9%以上の精度で、ヌーナン症候群を含む56遺伝子のde novo変異を検出できます。
「ヌーナン症候群がNIPTでわかるようになったの?」と驚かれる方も多いでしょう。従来のNIPTでは染色体の数の異常しか検出できませんでしたが、技術の進歩により遺伝子変異まで検出できるようになりました。
-
✓
56遺伝子のde novo変異を検査(ヌーナン症候群の原因遺伝子を含む)
-
✓
COATE法による99.9%以上の精度
-
✓
検査時期:妊娠10週から検査可能
-
✓
検出可能な疾患:ヌーナン症候群・軟骨無形成症・コステロ症候群など30疾患以上
-
✓
陽性率:当院では約60人に1人が陽性(累積リスク約1/600)
ダイヤモンドプランで検出可能なヌーナン症候群関連遺伝子
ダイヤモンドプランでは、ヌーナン症候群およびRASopathyの原因となる以下の遺伝子を検査できます。
🧬 検査対象遺伝子(ヌーナン症候群関連)
PTPN11・SOS1・SOS2・RAF1・RIT1・KRAS・NRAS・BRAF・MAP2K1・MAP2K2など
※上記を含む計56遺伝子を検査し、30疾患以上を検出可能です。
なぜミネルバクリニックで検査できるのか
ミネルバクリニックでは、米国の大手遺伝子検査会社と提携し、世界最先端のCOATE法を採用しています。従来のNIPTとは異なる技術で、遺伝子の塩基配列レベルの変異を検出することが可能です。
🔬 COATE法とは
COATE法は、SNP解析とターゲット融合を組み合わせた最新技術。従来法では検出困難だった微小欠失・遺伝子変異を99.9%以上の精度で検出可能です。
🏥 院内で確定検査まで
2025年6月より産婦人科を併設。陽性時の羊水検査・絨毛検査も院内で対応可能。転院不要で心理的負担を軽減できます。
9. ミネルバクリニックのサポート体制
ミネルバクリニックでは、臨床遺伝専門医の専門性を活かした診療体制を整えています。ヌーナン症候群を含む遺伝性疾患の検査から、陽性時のフォローまで一貫してサポートいたします。
🔬 世界最高水準の検査技術
スーパーNIPT(第3世代)とCOATE法を採用。ヌーナン症候群を含む56遺伝子のde novo変異を99.9%以上の精度で検出します。
🏥 院内で確定検査まで対応
2025年6月より産婦人科を併設し、羊水検査・絨毛検査も院内で実施可能に。転院の必要がなく、心理的負担を軽減できます。
💰 互助会で費用面も安心
互助会(8,000円)に加入いただくと、陽性時の確定検査(羊水検査)費用を全額カバー。上限なしで安心です。
よくある質問(FAQ)
🏥 一人で悩まないでください
ヌーナン症候群について心配なこと、検査を受けるかどうか迷っていること、
どんなことでもお気軽にご相談ください。臨床遺伝専門医があなたとご家族に寄り添います。
関連記事
参考文献
- Roberts AE, et al. Noonan syndrome. Lancet. 2013;381(9863):333-342. [PubMed]
- Tartaglia M, et al. Noonan syndrome and clinically related disorders. Best Pract Res Clin Endocrinol Metab. 2011;25(1):161-179. [PubMed]
- Romano AA, et al. Noonan syndrome: clinical features, diagnosis, and management guidelines. Pediatrics. 2010;126(4):746-759. [PubMed]
- Kong A, et al. Rate of de novo mutations and the importance of father’s age to disease risk. Nature. 2012;488(7412):471-475. [PubMed]
- Zenker M. Clinical overview on RASopathies. Am J Med Genet C Semin Med Genet. 2022;190(4):431-443. [PubMed]
- Aoki Y, et al. Germline mutations in HRAS proto-oncogene cause Costello syndrome. Nat Genet. 2005;37(10):1038-1040. [PubMed]
- National Institutes of Health – GeneReviews. Noonan Syndrome. [GeneReviews]
- American College of Medical Genetics and Genomics (ACMG). Practice guidelines. [ACMG]
- RASopathies Network. Clinical Practice Guidelines. [RASopathies Network]
- 日本小児遺伝学会. RASopathy診療ガイドライン. [日本小児遺伝学会]
















