目次
- 1 NIPT全染色体検査は意味ない?1,090人の臨床データが示す『遺伝子』を見るべき理由
NIPT全染色体検査は意味ない?
1,090人の臨床データが示す
『遺伝子』を見るべき理由
Q. NIPTで全染色体(1〜22番)を調べる必要はありますか?
A. 医学的エビデンスに基づくと、全染色体検査は推奨されません。
希少トリソミーの陽性的中率はわずか13〜25%(陽性と出ても約8割は偽陽性)、7Mb未満の微細欠失は検出困難、そして国際学会(ACMG・ISPD)も「ルーチン検査として非推奨」と明言しています。本当に見つけるべきは「染色体の数」ではなく「遺伝子の異常」です。
-
➤
希少トリソミーのPPV → 13〜25%(陽性でも約8割が偽陽性) -
➤
検出限界 → 7Mb以上の巨大欠失のみ(主要疾患の多くは3Mb程度で見逃し) -
➤
1,090人の臨床データ → その他の常染色体異常0例 vs 遺伝子疾患37例発見 -
➤
偽陽性の主原因 → 胎盤限局性モザイク(CPM)(胎児は正常なのに胎盤だけ異常) -
➤
本当に有効な検査 → COATE法(ダイヤモンドプラン)で陽性的中率>99.9%の遺伝子検査
1. NIPT全染色体検査とは?その仕組みと対象
【結論】 全染色体検査とは、1〜22番の常染色体すべてと性染色体の数的異常を調べる検査です。一見「全部調べるから安心」と思えますが、医学的には多くの問題点が指摘されています。
「全染色体を調べるなら安心では?」「項目が多い方がいいのでは?」そうお考えになる気持ちは、よくわかります。大切な赤ちゃんのために、できることは全部やりたい。その親心は当然のことです。
しかし、臨床遺伝専門医の立場から申し上げると、「検査項目が多い=良い検査」ではないのです。むしろ、不必要な項目を増やすことで偽陽性(間違って陽性と出ること)が増え、かえって不安を増大させてしまうリスクがあります。
💡 用語解説:全染色体検査(ワイドゲノム法)
ヒトの染色体は全部で46本(23対)あります。NIPTの「基本検査」では21番・18番・13番の3つの染色体(ダウン症候群・エドワーズ症候群・パトウ症候群の原因)を調べます。「全染色体検査」はこれに加えて1〜22番すべての常染色体を調べる検査です。しかし、21・18・13番以外の染色体異常は、ほとんどが流産に終わるか、生まれてくることが極めて稀です。
全染色体検査で調べる対象
| 検査対象 | 内容 | 臨床的意義 |
|---|---|---|
| 基本3トリソミー | 21・18・13番染色体 | 高い(PPV 80%以上) |
| 性染色体異常 | X・Y染色体の数的異常 | 中程度 |
| 希少トリソミー(RATs) | 1〜12、14〜17、19〜20、22番 | 低い(PPV 13〜25%) |
| 部分欠失・重複(CNV) | 7Mb以上の大きな変化 | 低い(PPV 約44%) |
💡 用語解説:陽性的中率(PPV)とは?
陽性的中率(Positive Predictive Value)とは、「検査で陽性と出た場合に、本当にその疾患がある確率」のことです。例えばPPVが25%なら、陽性と言われた4人のうち3人は実際には異常がない(偽陽性)ということになります。検査の「当たる確率」と考えるとわかりやすいでしょう。
📚 全染色体検査・詳細解説シリーズ
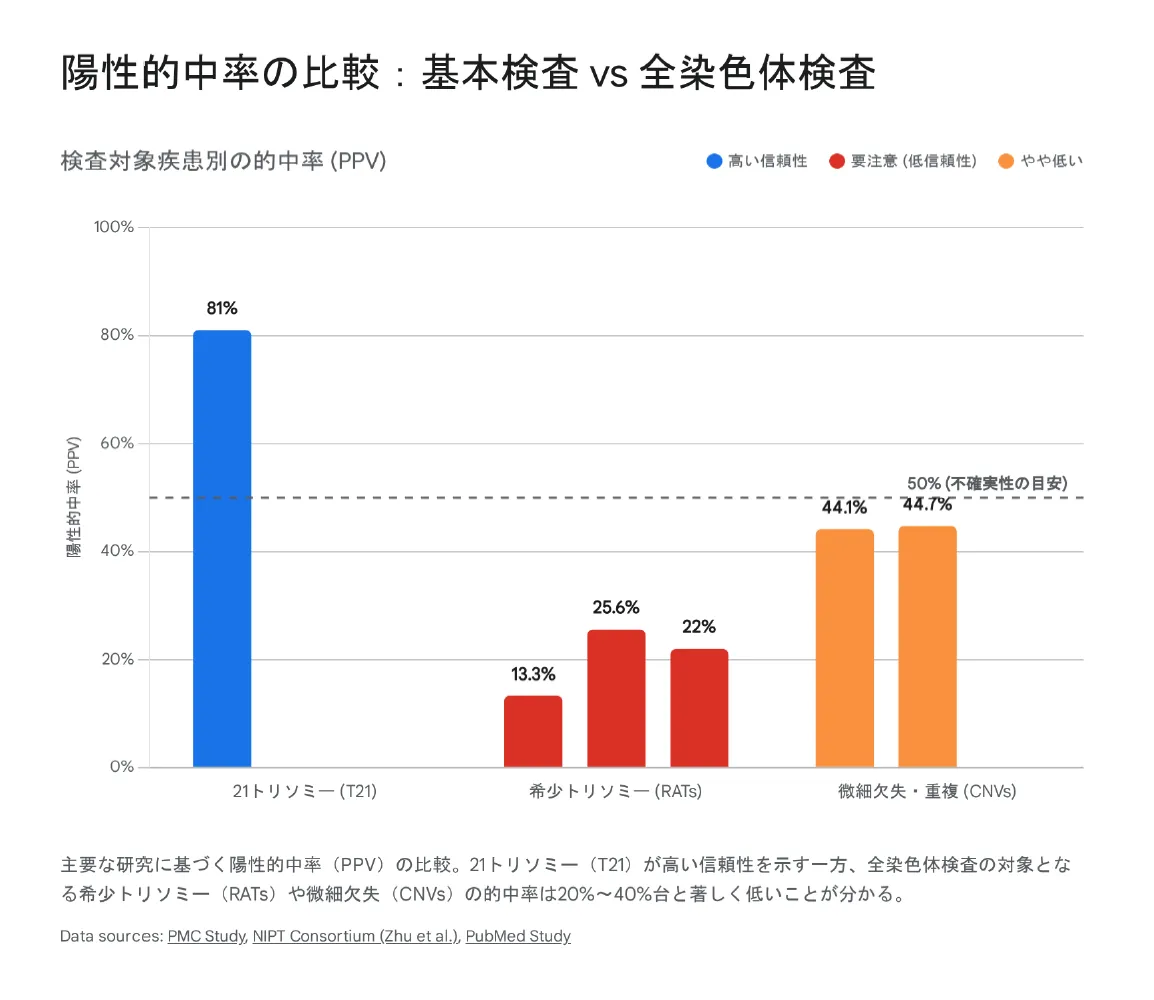
2. 衝撃の真実:陽性的中率はわずか13〜25%
【結論】 希少トリソミー(RATs)の陽性的中率はわずか13〜25%です。つまり、「陽性」と言われても約8割は偽陽性(実際は異常なし)という衝撃的なデータがあります。
「全染色体検査で陽性が出たらどうしよう」そんな不安をお持ちの方に、まず知っていただきたいのは、希少トリソミーの「陽性」は、ほとんどの場合間違いだということです。
2024年に発表された大規模研究では、6,220名の妊婦を対象にNIPT-plusの性能が評価されました。その結果は、「半分も当たらない」どころか「8〜9割外れる」という衝撃的なものでした。
-
•
21トリソミー(ダウン症):PPV 約81%(高い信頼性)
-
•
希少トリソミー(RATs):PPV わずか13.33%(約87%が偽陽性)
-
•
微細欠失・重複(CNV):PPV 約44%(半数以上が偽陽性)
-
•
7番トリソミー:PPV わずか10%(20例中2例のみ真陽性)
なぜ希少トリソミーのPPVはこれほど低いのか?
PPVが低くなる最大の理由は、対象疾患の頻度(有病率)が極めて低いからです。統計学的に、有病率が低い疾患ほど、たとえ検査の感度・特異度が高くてもPPVは低下します。
21トリソミーは約700人に1人の頻度で発生しますが、希少トリソミーの多くはそもそも生まれてくること自体が極めて稀です。ほとんどは妊娠初期に自然流産となります。つまり、「生きて生まれてくる可能性がほぼない疾患」を検査している状態なのです。
⚠️ 偽陽性がもたらす深刻な影響
希少トリソミーで「陽性」と言われた妊婦さんの80〜90%は、実際には健康な赤ちゃんを妊娠しているにもかかわらず、確定検査(羊水検査)を受けなければなりません。羊水検査には約1/300〜1/1000の流産リスクがあります。また、結果が出るまでの数週間、「重篤な異常があるかもしれない」という強い不安に晒されることになります。
3. 「7Mbの壁」:微細欠失の大半は検出できない
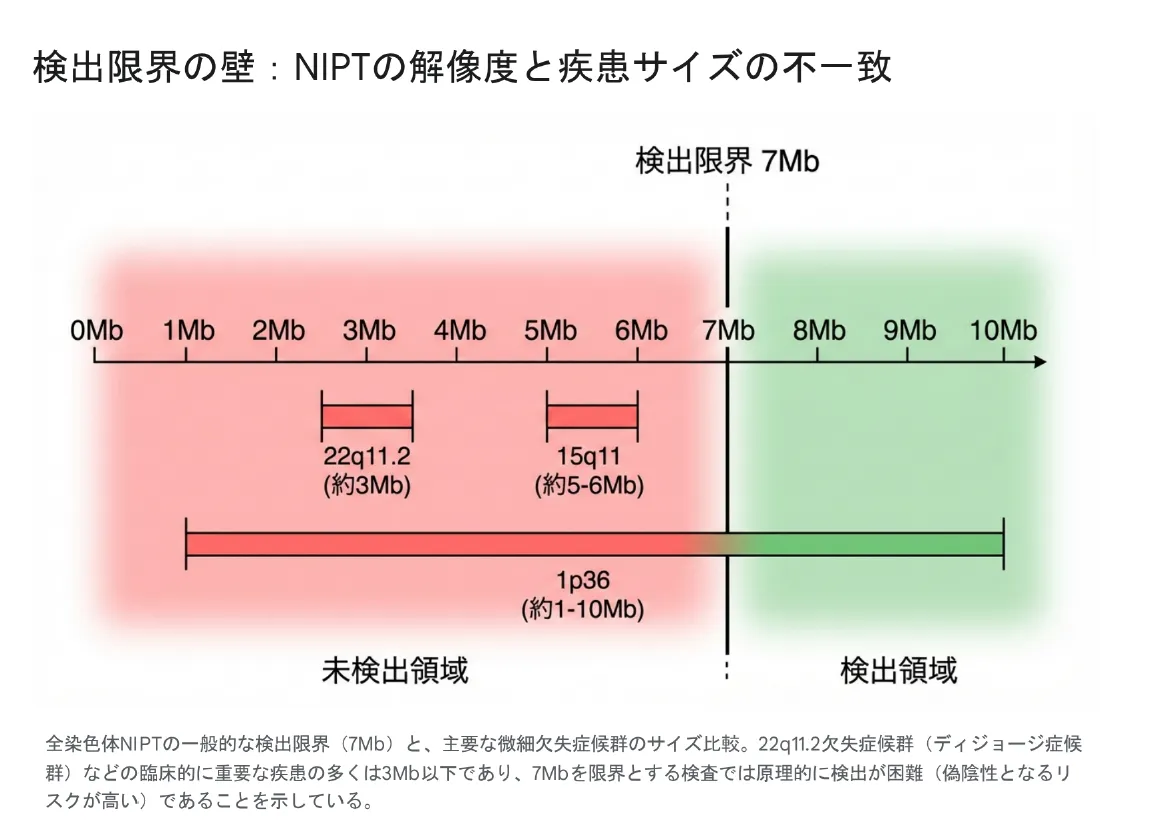
【結論】 全染色体検査(ワイドゲノム法)の検出限界は約7Mb(700万塩基対)です。しかし、臨床的に重要な微細欠失症候群(22q11.2欠失症候群など)の多くは3Mb程度であり、検出困難です。
「全染色体検査で微細欠失も調べられるなら安心」そう思われるかもしれません。しかし、ここに大きな落とし穴があります。本当に見つけたい重要な微細欠失は、そもそも検出できないのです。
💡 用語解説:Mb(メガベース)とは?
Mb(メガベース)はDNAの長さの単位で、100万塩基対を意味します。7Mbは700万塩基対、3Mbは300万塩基対です。ヒトのゲノム全体は約30億塩基対(3,000Mb)あります。7Mbというのは、ゲノム全体の約0.2%にあたる「かなり大きな」変化です。
主要な微細欠失症候群とサイズの比較
| 微細欠失症候群 | 典型的なサイズ | 頻度 | ワイドゲノム法での検出 |
|---|---|---|---|
| 22q11.2欠失症候群 (ディジョージ症候群) |
約3Mb | 1/2,000〜4,000 | 困難 |
| 15q11欠失症候群 (プラダー・ウィリ/アンジェルマン) |
5〜6Mb | 1/15,000〜20,000 | 境界 |
| 1p36欠失症候群 | 1〜10Mb(多様) | 1/5,000〜10,000 | 一部のみ |
| 5p欠失症候群 (猫鳴き症候群) |
5〜40Mb(多様) | 1/20,000〜50,000 | 大きいもののみ |
📊 検出感度の衝撃的データ
Genetics in Medicine誌に掲載された研究によると、7Mb以上のCNVに対するNIPTの検出感度は93.8%と良好でしたが、7Mb未満を含むすべてのCNVに対しては48.3%まで低下しました。つまり、実際に存在する染色体の構造異常の半分以上は見逃されているのです。
最も頻度が高く臨床的に重要な22q11.2欠失症候群(ディジョージ症候群)は、心疾患、免疫不全、口蓋裂、発達遅滞など多岐にわたる症状を呈します。この疾患の欠失サイズは約3Mbであり、7Mbの検出限界を大きく下回ります。

🩺 院長コラム【「全部調べる」の落とし穴】
検査会社の広告では「全染色体検査」「微細欠失検査」と、あたかもすべてを網羅しているかのような印象を与えます。しかし、「調べています」と「見つけられます」は全く別物です。
7Mbという検出限界は、野球場から双眼鏡でアリを探すようなものです。見えなかったからといって「アリはいない」とは言えません。本当に見つけたい重要な疾患ほど、サイズが小さく検出困難なのです。
私がダイヤモンドプランを推奨する理由は、ターゲットを絞って深く読むことで、7Mb未満の重要な変異も陽性的中率>99.9%で検出できるからです。「広く浅く」より「狭く深く」が、本当の安心につながるのです。
4. 偽陽性の主原因:胎盤限局性モザイク(CPM)
【結論】 NIPTの偽陽性の主原因は胎盤限局性モザイク(CPM)です。NIPTは「胎児のDNA」ではなく「胎盤のDNA」を見ているため、胎盤だけに異常があり胎児は正常というケースが多発します。
「なぜこんなに偽陽性が多いの?」「検査の精度が低いの?」そう疑問に思われるかもしれません。実は、偽陽性が多い理由は検査技術の問題ではなく、ヒトの発生過程における生物学的な現象に起因しています。
💡 用語解説:胎盤限局性モザイク(CPM)とは?
胎盤限局性モザイク(Confined Placental Mosaicism)とは、胎盤には染色体異常があるが、胎児自身は正常という状態です。受精卵の初期分裂でエラーが起きた後、「トリソミーレスキュー」という修復現象により胎児は正常になったものの、胎盤には異常が残っているケースです。
NIPTは「胎児」ではなく「胎盤」を見ている
NIPTの根本的な原理に関わる重要な事実があります。母体血中を流れる「胎児由来」とされるDNA(cell-free fetal DNA)は、実際には胎児本体からではなく、胎盤(絨毛の栄養膜細胞)から放出されたものなのです。
つまり、NIPTは厳密には「胎児の染色体検査」ではなく、「胎盤の染色体スクリーニング」を行っているに過ぎません。通常は胎盤と胎児の染色体構成は一致しますが、CPMの場合は食い違いが生じます。
-
•
希少トリソミー陽性例の起源:52.8%が胎盤起源(CPM)
-
•
胎児由来はわずか22.1%
-
•
残り約25%は母体由来の要因など
-
•
つまり陽性の半数以上は胎児に異常なし
希少染色体でCPMが多い理由
13・18・21番以外の染色体(希少常染色体)のトリソミーは、胎児においては致死的であることが多く、胎児自身がトリソミーを持って出生に至ることは極めて稀です。
そのため、NIPTで希少トリソミーが検出された場合、その大部分はCPMに由来する偽陽性です。これは検査の欠陥ではなく、生物学的な必然なのです。
5. 1,090人の臨床データが示す真実
【結論】 Nature Medicine 2024年掲載の1,090人のハイリスク妊娠データでは、「その他の常染色体異常」は0例でした。一方、遺伝子疾患は37例発見されています。これが「染色体の数」より「遺伝子」を見るべき医学的根拠です。
「全染色体検査は本当に不要なの?」「データで証明されているの?」そんな疑問に、明確なエビデンスをお示しします。
2024年にNature Medicine誌に掲載された研究では、1,090例のハイリスク妊娠(超音波異常や染色体異常リスクが高いと判断された妊娠)を対象に、どのような異常が見つかったかを詳細に分析しています。
-
•
対象:1,090例のハイリスク妊娠
-
•
その他の常染色体異常:0例(検出なし)
-
•
遺伝子変異(病的バリアント):37例発見
-
•
結論:「染色体の数」より「遺伝子の異常」を見るべき
このデータが意味すること
1,090人もの「ハイリスク」妊娠を調べても、21・18・13番以外の常染色体異常は1例も見つからなかったのです。これは「全染色体検査」の意義を根本から問い直す結果です。
一方で、遺伝子レベルの異常は37例も見つかっているという事実は、「染色体の数」ではなく「遺伝子の異常」にこそ注目すべきことを示しています。
全染色体検査の限界
- ✗
希少トリソミーは検出しても偽陽性だらけ
- ✗
実際に1,090人中0例
- ✗
不必要な不安と侵襲的検査のリスク
遺伝子検査の有効性
- ✓
1,090人中37例の異常を発見
- ✓
COATE法ならPPV >99.9%
- ✓
本当に知るべき情報を高精度で検出
6. 国際学会の見解:ACMG・ISPDは「非推奨」
【結論】 米国臨床遺伝・ゲノム学会(ACMG)と国際出生前診断学会(ISPD)は、希少トリソミーのスクリーニングについて「推奨するための証拠が不十分」「ルーチン検査として非推奨」と明言しています。
「本当に全染色体検査は不要なの?」「専門家の意見は?」という疑問に対して、世界的に権威ある学会のガイドラインをご紹介します。
💡 用語解説:ACMG・ISPDとは?
ACMG(American College of Medical Genetics and Genomics)は米国臨床遺伝・ゲノム学会、ISPD(International Society for Prenatal Diagnosis)は国際出生前診断学会です。いずれも遺伝医療・出生前診断分野で世界的に最も影響力のある学術団体であり、そのガイドラインは世界中の医療機関の指針となっています。
ACMG 2022年ガイドラインの内容
| 検査対象 | ACMGの推奨 | 理由 |
|---|---|---|
| 基本3トリソミー(21・18・13) | 強く推奨 | 高いPPV、臨床的有用性が確立 |
| 性染色体異常(SCA) | 選択肢として提供 | 中程度のPPV |
| 希少トリソミー(RATs) | 証拠不十分(非推奨) | 大半が偽陽性、臨床的有用性未確立 |
| 全ゲノムCNV(微細欠失) | 推奨しない | 検出限界7Mb、感度データ限定的 |
📋 ACMGの具体的な指摘
ACMGは希少トリソミー検査について、以下の理由から「推奨するための証拠が不十分」と結論づけています:
・陽性結果の多くが偽陽性(CPM)であること
・臨床的有用性が確立されていないこと
・確認検査の負担が大きいこと
ISPDの見解(2023年)
ISPDも同様に、希少トリソミーのスクリーニングは「一般的な集団に対するルーチン検査として推奨されない」と結論づけています。偽陽性の多さや結果の解釈の困難さが、メリットを上回る懸念があるためです。
7. 「染色体の数」より「遺伝子」を見るべき理由
【結論】 出生前診断で本当に見つけるべきは「染色体の数」ではなく「遺伝子の異常」です。特に父親由来の新生突然変異は、積算リスク1/600と決して稀ではなく、症候性自閉症など重篤な疾患の原因となります。
「全染色体検査がダメなら、何を調べればいいの?」という疑問にお答えします。答えは「遺伝子(DNA配列)の異常」を見ることです。
💡 用語解説:染色体異常 vs 遺伝子異常
染色体異常は染色体の「数」や「大きな構造」の変化(トリソミー、大きな欠失など)です。遺伝子異常は遺伝子(DNA配列)レベルの変化で、一つの遺伝子の中の小さな変異でも重大な疾患を引き起こすことがあります。染色体検査で「正常」でも、遺伝子に異常がある場合は疾患が生じます。
父親由来の新生突然変異(De novo mutation)
遺伝子異常の中でも特に重要なのが「父親由来の新生突然変異」です。これは父親の精子が作られる過程で新たに生じた変異で、両親には異常がなくても子どもに疾患が生じる原因となります。
-
•
ヌーナン症候群関連(PTPN11, RAF1など):頻度第2位の先天異常症候群
-
•
症候性自閉症(MECP2, CHD7など):知的障害を伴う重度の発達障害
-
•
骨系統疾患(FGFR3, COL1A1など):軟骨無形成症、骨形成不全症など
-
•
積算リスク:1/600(ダウン症1/700と同等以上)
(父親由来の遺伝子変異が子へ伝わるイメージ)
検出される疾患のランキング
| 順位 | 疾患名 | 頻度 | 検出方法 |
|---|---|---|---|
| 1位 | ダウン症候群(21トリソミー) | 約1/700 | NIPT基本検査 |
| 2位 | ヌーナン症候群関連 | 約1/1,000〜2,500 | ダイヤモンドプラン(遺伝子検査) |
| 3位 | 22q11.2欠失症候群(ディジョージ) | 約1/2,000〜4,000 | ダイヤモンドプラン(微細欠失) |
この表からわかるように、出生前診断で見つけるべき重要疾患のトップ3すべてをカバーできるのがダイヤモンドプランです。「全染色体検査」では2位・3位の疾患は検出困難または不可能です。
8. ダイヤモンドプラン:本当に有効な検査とは
【結論】 ダイヤモンドプランは、COATE法(SNP法+ターゲット法の融合技術)により、微細欠失12領域と56遺伝子を陽性的中率>99.9%で検出します。「広く浅く」ではなく「狭く深く」調べることで、本当に重要な疾患を高精度で見つけます。
💡 用語解説:COATE法とは?
COATE法は、SNP法(母体DNAと胎児DNAを識別する技術)とターゲット法(特定領域を深く読む技術)を融合した次世代NIPT技術です。ワイドゲノム法が「広く浅く」読むのに対し、COATE法は「重要な領域を狭く深く」読むことで、陽性的中率>99.9%という驚異的な精度を実現しています。COATE法のエビデンスはこちら
ダイヤモンドプランの検査対象
常染色体トリソミー(6種)
13 / 15 / 16 / 18 / 21 / 22
性染色体異数性(4種)
45,X / 47,XXX / 47,XXY / 47,XYY
微細欠失(12領域)
1p36, 2q33, 4p16, 5p15, 8q23q24, 9p, 11q23q25, 15q11.2-q13, 17p11.2, 18p, 18q22q23, 22q11.2
単一遺伝子(56遺伝子)
症候性自閉症の原因を含む30以上の単一遺伝子疾患
(PTPN11, MECP2, CHD7, FGFR3など)
ワイドゲノム法 vs COATE法(ダイヤモンドプラン)
| 比較項目 | ワイドゲノム法 | COATE法(ダイヤモンドプラン) |
|---|---|---|
| 解析深度 | 浅い(Shallow) | 深い(Targeted) |
| 検出限界 | 7Mb以上 | 3Mb以下も検出可能 |
| 希少トリソミーPPV | 13〜25% | 検査対象外(不要なため) |
| 微細欠失PPV | 約44% | >99.9% |
| 遺伝子検査 | 不可 | 56遺伝子対応 |
| 22q11.2欠失検出 | 困難(3Mb) | 高精度で検出可能 |

🩺 院長コラム【なぜ当院はダイヤモンドプランを推奨するのか】
臨床遺伝専門医として15年以上、出生前診断に携わってきました。その経験から断言できるのは、「検査項目の数」より「検査の質」が重要だということです。
全染色体検査で希少トリソミー「陽性」と言われ、泣きながら相談に来られる妊婦さんを何人も見てきました。そしてその8〜9割は偽陽性で、羊水検査の結果「正常」と分かるのです。この数週間の苦しみは、本来必要なかったものです。
当院がダイヤモンドプランを推奨するのは、米国トップ4の遺伝子検査会社が開発したCOATE法により、本当に見つけるべき疾患を、偽陽性を最小限に抑えながら検出できるからです。
検査会社ごとに技術レベルは大きく異なります。「どこで受けても同じ」ではないのです。当院の検査精度エビデンスをぜひご確認ください。
9. ミネルバクリニックのサポート体制
ミネルバクリニックでは、臨床遺伝専門医の専門性を活かした診療体制を整えています。検査から陽性時のフォローまで一貫してサポートいたします。
🏥 院内で確定検査まで対応
2025年6月より産婦人科を併設し、羊水検査・絨毛検査も院内で実施可能に。転院不要で心理的負担を軽減できます。
👩⚕️ 臨床遺伝専門医が常駐
検査前後の遺伝カウンセリングを臨床遺伝専門医が直接担当。結果の説明から今後の選択肢まで、専門家が寄り添います。
💰 互助会で費用面も安心
互助会(8,000円)に加入いただくと、陽性時の確定検査費用を上限なしで全額カバー。
💡 遺伝カウンセリング料金について
当院では遺伝カウンセリング料金33,000円が検査費用に含まれています。これは当日の説明だけでなく、陽性時の何度でものカウンセリング、妊娠経過中の心配事(サイトメガロウイルス初感染など)への相談も含まれています。「お金がかかるから相談しにくい」ということがないよう、安心して日常生活を送れる配慮をしています。
一人で悩まず、専門医を頼ってください
全染色体検査の結果で不安になっている方も、
これから検査を受けようとしている方も、
臨床遺伝専門医と直接お話しすることで、正しい選択ができます。
※オンラインNIPTで全国どこからでも受検可能です
よくある質問(FAQ)
🏥 一人で悩まないでください
全染色体検査の結果で不安になっている方、
これから検査を受けようとしている方、
どんなことでもお気軽にご相談ください。
臨床遺伝専門医があなたとご家族に寄り添います。
📚 全染色体検査・完全ガイドシリーズ
▶ 各論シリーズ
Vol.1:第1番〜第8番染色体
致死的トリソミーから8番モザイクまで。初期流産の原因を解説
Vol.2:第9番〜第16番染色体
13番パトウ・15番微細欠失・16番流産リスクの核心
▶ 関連する重要記事
参考文献
- [1] Zhu Y, et al. The evolution of cell-free fetal DNA testing: expanded non-invasive prenatal testing. Front Genet. 2024;15:1360879. [PMC]
- [2] Gregg AR, et al. Noninvasive prenatal screening for fetal aneuploidy, 2016 update: a position statement of the American College of Medical Genetics and Genomics. Genet Med. 2016;18(10):1056-1065. [PubMed]
- [3] Bianchi DW, et al. DNA sequencing versus standard prenatal aneuploidy screening. N Engl J Med. 2014;370(9):799-808. [PubMed]
- [4] Gregg AR, et al. ACMG statement on noninvasive prenatal screening for fetal aneuploidy. Genet Med. 2022;24(7):1347-1352. [PubMed]
- [5] Van der Meij KRM, et al. TRIDENT-2: National Implementation of Genome-wide Non-invasive Prenatal Testing as a First-Tier Screening Test in the Netherlands. Am J Hum Genet. 2019;105(6):1091-1101. [PubMed]
- [6] Pertile MD, et al. Rare autosomal trisomies, revealed by maternal plasma DNA sequencing, suggest increased risk of feto-placental disease. Sci Transl Med. 2017;9(405):eaan1240. [PubMed]
- [7] Dondorp W, et al. Non-invasive prenatal testing for aneuploidy and beyond: challenges of responsible innovation in prenatal screening. Eur J Hum Genet. 2015;23(11):1438-1450. [PubMed]
- [8] Wapner RJ, et al. Expanding the scope of noninvasive prenatal testing: detection of fetal microdeletion syndromes. Am J Obstet Gynecol. 2015;212(3):332.e1-9. [PubMed]
- [9] International Society for Prenatal Diagnosis (ISPD). Position Statement on the use of genome-wide sequencing for prenatal diagnosis. Prenat Diagn. 2023. [PMC]
- [10] Grati FR, et al. Outcomes in pregnancies with a confined placental mosaicism and implications for prenatal screening using cell-free DNA. Genet Med. 2020;22(2):309-316. [PubMed]