目次
- 1 出生前診断でわかること・わからないこと臨床遺伝専門医がわかりやすく解説
- 1.1 1. まず結論:出生前診断でわかること・わからないこと
- 1.2 2. 出生前診断でわかること:染色体・一部の遺伝子・形態異常
- 1.3 3. 出生前診断でわからないこと:不安を増やさない整理のしかた
- 1.4 4. 自閉症・発達障害は出生前診断でわかる?例外と限界
- 1.5 5. 出生前検査の種類:NIPT・羊水検査・絨毛検査・CMA
- 1.6 6. NIPTの精度と限界|陽性的中率(PPV)と偽陽性・偽陰性の正しい理解
- 1.7 7. 陽性・判定不能の次にすること:出生前の確定診断
- 1.8 8. 診断は「出生前」だけではありません:出生後診断と出生前診断を分けて理解
- 1.9 9. ミネルバクリニックの体制:正確性と心の安全を最優先
- 1.10 まとめ|出生前診断でわかること・わからないこと
- 1.11 よくある質問(FAQ)
- 1.12 関連記事
- 1.13 参考文献
出生前診断でわかること・わからないこと
臨床遺伝専門医がわかりやすく解説
「受けたほうがいいのか、それとも受けないほうがいいのか…」そう迷いながら、ここにたどり着いた方もいらっしゃるのではないでしょうか。
出生前診断とは、妊娠中に赤ちゃんの染色体異常や一部の遺伝子異常の可能性を調べる医療です。
この記事は、「検査を受けるかどうか」を決めるためではなく、正しい情報を整理して、ご家族が納得して選べる状態になるためのガイドです。
Q. 出生前診断で「赤ちゃんの障害」は全部わかりますか?結論だけ知りたいです
A. いいえ。出生前診断でわかるのは「一部の染色体異常・一部の遺伝子疾患・超音波で見える形態異常」などに限られます。
自閉症・発達障害・知的障害の多くは出生前に“確定”できません。また、NIPTは確定診断(診断)ではなくスクリーニングですので、陽性の場合は羊水検査・絨毛検査などの出生前の確定診断で確認します。
- ➤わかること → 染色体異常(21/18/13など)・一部の微細欠失(微小欠失)・一部の単一遺伝子疾患・超音波で見える形態異常
- ➤わからないこと → 自閉症・発達障害(ADHD等)・軽微な特性の多く・出生後にわかる疾患の多く
- ➤検査の種類 → NIPT(採血)・超音波・羊水/絨毛(出生前の確定診断)・羊水検査+CMA
- ➤精度と限界 → 検査会社・手法で差が出る理由、偽陽性/偽陰性、結果の解釈
- ➤大切な前提 → 知る権利・知らないでいる権利、非指示的(中立)な意思決定支援
- ➤当院の支え方 → 正確性重視・心理的ケア重視・院内で確定検査まで一貫
1. まず結論:出生前診断でわかること・わからないこと
妊娠中は、普段なら受け流せる言葉が胸に刺さったり、検索すればするほど不安が増えたりしますよね。「私のせいかも」「調べるべき?調べないべき?」と、ひとりで抱えてしまう方も少なくありません。
【結論】出生前診断でわかるのは、染色体異常(数的異常・一部の構造異常)、一部の微細欠失(微小欠失)や単一遺伝子疾患、そして超音波で見える形態異常などに限られます。いっぽうで、自閉症・発達障害・知的障害の多くは出生前に確定できません。そしてNIPTは確定診断ではないため、陽性の場合は出生前の確定診断(羊水検査・絨毛検査)で確認します。
出生前診断は、医学であると同時に倫理の領域でもあります。「調べるべき」「調べないべき」という正解はありません。知る権利も、知らないでいる権利も、どちらも大切です。医師の役割は決定者ではなく、情報提供者・意思決定支援者です。だからこそ当院では、結果を急いで出すことよりも、正確性と、結果の後に続く心理的・医学的フォローを重視しています。
2. 出生前診断でわかること:染色体・一部の遺伝子・形態異常
「わかること」を先に知りたい方も多いですよね。ここで大切なのは、“わかる=予後が全部決まる”ではないという点です。特に微小欠失・重複(コピー数変化:CNV)は、表現型(症状)の幅が非常に広いことがあります。
染色体の数的異常(トリソミーなど)
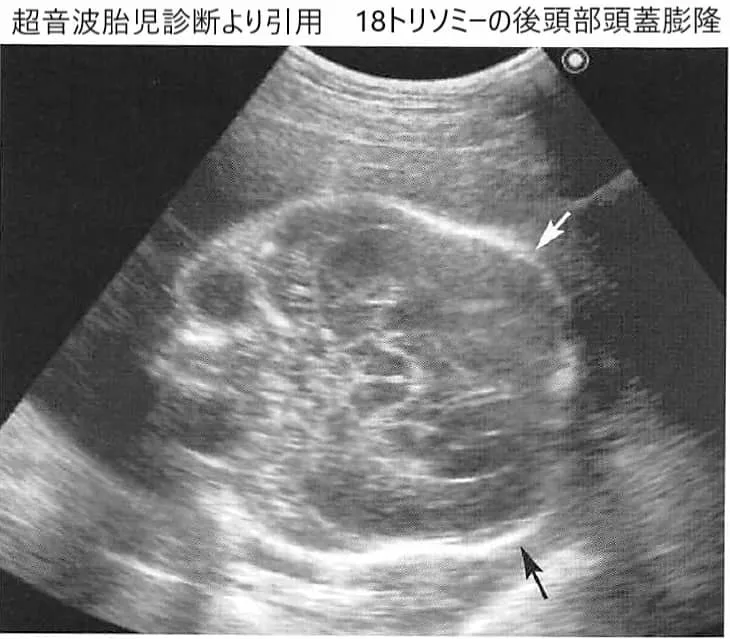
代表例は21トリソミー(ダウン症候群)、18トリソミー、13トリソミーです。詳しい疾患解説はそれぞれご参照ください:21トリソミー、18トリソミー、13トリソミー。陽性=確定ではないため、出生前の確定診断(羊水・絨毛)で確認します。
性染色体の異数性(例:45,Xなど)
性染色体の数の違いが関与します。症状の幅が広いことがあり、出生前の結果が出た場合でも、妊娠経過・超音波所見・ご家族の価値観を踏まえて情報を整理することが重要です。
微細欠失(微小欠失)・一部の単一遺伝子疾患
検査手法によっては、微細欠失(微小欠失)や単一遺伝子(特定の遺伝子変化)を評価することがあります。ただし、見つかった所見の意味づけ(予後・支援設計)は専門的で、出生前に確定できないこともあります。結果が“情報”として扱われ、結論を急がないために遺伝カウンセリングが必要です。
微細欠失(微小欠失)は、染色体の一部が小さく欠けている状態です。逆に同じ領域でコピー数が増える「重複」も検出されることがあります。CNVは表現型の幅が広く、出生前に予後を確定できないこともあります。国際的にも、生命予後に直結しない所見をどこまで出生前に検出すべきかは議論が続いています。結果が出たときは、“その情報をどう扱うか”を一緒に整理することが大切です。
3. 出生前診断でわからないこと:不安を増やさない整理のしかた
「陰性なら安心ですか?」「全部調べておけば安心ですか?」と考えてしまうのは当然です。でも、出生前診断の現実はもう少し複雑です。ここを知らないまま検査を増やしてしまうと、“わからないものを、わかった気持ちで抱える”ことが起こり得ます。
❗ 原則としてわからないもの
- ➤多因子疾患の大部分(一般的な自閉症・発達障害など)
- ➤出生後の環境要因による障害
- ➤現在の医学で原因が特定できない疾患
※一部の重度の症候性(重い)自閉症は、特定の遺伝子変化や微細欠失として検出可能な場合があります。詳しくは後述します。
❗ 明確にわからないもの
- ➤多因子疾患(自閉症・発達障害の多く)
- ➤出生後の環境要因による障害
- ➤現在の医学で原因が解明されていない疾患
- ➤自閉症(ASD)の大部分(多因子が関与し、胎児期に確定できないことが多い)
- ➤発達障害(ADHDなど)や学習の特性(環境要因も影響)
- ➤出生後の環境要因による障害(感染症・事故など)
- ➤原因が不明な知的障害の一部(多因子・非遺伝要因を含む)
- ➤出生前に所見がなくても、出生後に見つかる疾患は存在します(“陰性=100%安心”ではありません)
⚠️ 大切な視点:出生前に「見つけること」自体が、常に利益になるとは限らない領域があります。生命予後に直結しない所見や、予後の幅が非常に広い所見では、VUS(意義不明)や偶発所見が心理的負担になることも国際的に議論されています。だからこそ当院では、検査の選択を誘導せず、不確実性を正直に伝え、意思決定支援に重きを置きます。
4. 自閉症・発達障害は出生前診断でわかる?例外と限界
この質問は、本当に多いです。検索しても答えがバラバラで、余計に怖くなってしまった方もいらっしゃると思います。まずは、心を守るために結論からお伝えします。
【結論】一般的な自閉症(ASD)や発達障害(ADHDなど)の多くは、出生前診断で確定できません。ただし、重度の合併症を伴う「症候性(重い)自閉症」の一部は、特定の遺伝子変化や染色体異常に関連することがあり、検査手法によっては評価対象となる場合があります。結果の解釈は専門的支援が不可欠です。
わからない理由①:多因子が関与する
自閉症の多くは、多数の遺伝要因と環境要因が複合的に関与します。単一の遺伝子で決まるわけではないため、出生前の遺伝学的検査で「確定」することは困難です。
わからない理由②:発達の観察で診断される
ASDやADHDは、出生後の発達の経過(言語・社会性・行動パターン)を観察して診断します。胎児期にそれらを評価することはできません。
「症候性(重い)自閉症」とは、重度の知的障害やてんかん、先天異常などの合併症を伴うことが多いタイプを指す臨床的な言い方です。原因として、特定の遺伝子変化や染色体異常が関与することがあります。重要なのは、“見つかった=重症が確定”ではないこと、そして出生前に予後を確定できないケースがあることです。だからこそ当院では、結果の意味づけを丁寧に行います。
5. 出生前検査の種類:NIPT・羊水検査・絨毛検査・CMA
| 妊娠週数 | 受けられる検査 | 位置づけ |
|---|---|---|
| 妊娠6〜8週 | 早期NIPT(臨床研究) | スクリーニング |
| 妊娠9〜10週以降 | NIPT | スクリーニング |
| 妊娠11〜14週 | 絨毛検査 | 出生前の確定診断 |
| 妊娠15週以降 | 羊水検査 | 出生前の確定診断 |
検査を選ぶとき、いちばん苦しいのは「どれを選べばいいか」ではなく、違いがわからないまま決断を迫られることです。ここでは誘導はしません。意思決定の材料を、できるだけ見通しよく整えます。
| 分類 | 検査 | 方法 | 位置づけ | ポイント |
|---|---|---|---|---|
| スクリーニング | NIPT(新型出生前診断) | 採血 | 確定診断ではない | 結果は「可能性」。陽性は確定検査へ |
| 超音波・血清マーカー | エコー/採血 | スクリーニング | 所見や確率で評価 | |
| 確定診断(出生前) | 羊水検査 | 穿刺 | 出生前の確定診断 | Gバンド法で全体像、必要に応じCMA |
| 絨毛検査 | 穿刺 | 出生前の確定診断 | 妊娠早期に実施されることが多い | |
| 羊水検査+CMA | 穿刺+解析 | 確定診断 | Gバンド法では検出できない微小欠失を確定診断可能。学会指針では原則、超音波で構造異常がある場合などが対象 |
⚠️ 検査アルゴリズムの注意:ゲノム刷り込み(インプリンティング)やメチル化異常が本態となる疾患では、第一選択検査が「メチル化解析」となることがあります。CMAは、メチル化異常が確認された後の原因精査(欠失・UPD確認)として位置づけられることがあります。疾患ごとに最適な検査順序が異なるため、必要に応じて遺伝カウンセリングで整理します。
6. NIPTの精度と限界|陽性的中率(PPV)と偽陽性・偽陰性の正しい理解
「精度が高いなら、それで決めていいのでは?」そう感じる方もいらっしゃいます。でも妊娠中の不安にいちばん危険なのは、“数字の意味を取り違えたまま”結論を急いでしまうことです。ここは丁寧にいきましょう。
【結論】陽性的中率(PPV)などの数字は、母体年齢などの事前確率や、検査会社・解析手法の質で変わり得ます。だからこそ当院では、短期間で結果を出すことよりも、正確性と、その後のフォローを重視しています。
感度(Sensitivity)
実際に異常がある場合に「陽性」と出やすい度合いです。感度が高いほど、見逃し(偽陰性)が少なくなります。
特異度(Specificity)
実際に異常がない場合に「陰性」と出やすい度合いです。特異度が高いほど、偽陽性が少なくなります。
陽性的中率(PPV)
「陽性」と出た方が、実際にその異常である確率です。年齢・背景(事前確率)や検査の質で変わり得ます。
補足(とても大事):陽性的中率(PPV)は「事前確率」の影響を強く受けます。事前確率が低いほど、同じ検査精度でも偽陽性の割合が相対的に増えることがあるため、数字は必ず個別条件で解釈します。
⚠️ 重要:検査会社・解析手法で差が出ることを前提にしてください
同じ名称の検査でも、シーケンサー、解析の深さ、解析専門家(バイオインフォマティクス)の体制、品質管理の文化が異なれば、結果の信頼性は変わり得ます。だからこそ当院では、速さよりも正確性を重視し、陽性後のフォロー(心理的・医学的ケア)を大切にしています。
当院のエビデンスは以下に整理しています:スーパーNIPTのエビデンス、COATE法(ダイヤモンド/NEWプレミアム)のエビデンス。

🩺 院長コラム【「正確性」を選ぶことは、心の安全を守ること】
妊娠中の不安は、数字がひとつ増えただけでも増幅します。だから私は、検査の世界では「速さ」よりも正確性を重視したいのです。誤った陽性(偽陽性)も、見逃し(偽陰性)も、ご家族の心に深い傷を残します。
当院が大切にしているのは「結果を出すこと」ではなく、結果を受け止める時間と、その後の支えまで含めた医療です。どんな結果でも孤独にしない。そのために遺伝カウンセリングを大切にしています。
7. 陽性・判定不能の次にすること:出生前の確定診断
結果を待つ時間は想像以上に長く感じます。陽性という言葉を見るだけで息が詰まる方もいらっしゃいます。まずお伝えしたいのは、結果がどんなものであっても、次に取れる行動は必ずあるということです。
【結論】NIPTの陽性は「確定」ではありません。出生前の確定診断は羊水検査・絨毛検査です。微小欠失・重複の確定診断は「羊水検査+CMA」で行い、Gバンド法では検出できない微小欠失を確定診断可能です。ただし学会指針では原則として超音波で構造異常がある場合などが対象とされています。
💡 「確定検査」の前に大切なこと
- ➤検査結果は“情報”であり、結論を迫るものではありません
- ➤知る権利・知らないでいる権利を含め、選択は常にご家族に委ねられます
- ➤医師の役割は情報提供者であり、非指示的(中立)に意思決定を支援します
8. 診断は「出生前」だけではありません:出生後診断と出生前診断を分けて理解
「診断=出生前」と思ってしまうと、気持ちが追い詰められます。出生前診断は、あくまで選択肢のひとつです。出生後に診断し、支援を整えていく道もあります。ここは混同しないように整理します。
出生前診断(妊娠中)
- ➤NIPT:スクリーニング(確定診断ではない)
- ➤羊水検査・絨毛検査:出生前の確定診断
- ➤微小欠失の確定診断:羊水検査+CMA(学会指針では原則、構造異常がある場合などが対象)
出生後診断(赤ちゃんが生まれてから)
- ➤確定診断の中心:血液によるCMA(染色体マイクロアレイ)
- ➤Gバンド法では微小欠失の検出は困難なことが多い
- ➤結果の解釈と支援設計が重要(表現型の幅が広い)
9. ミネルバクリニックの体制:正確性と心の安全を最優先
日本には認証施設(大学病院中心)と非認証施設(民間主体)があります。非認証=質が低い、という誤解も根強いのですが、実際には体制と専門性の中身が重要です。
当院は非認証施設ですが、臨床遺伝専門医が最初から最後まで担当し、遺伝カウンセリングからNIPT判定、陽性後の対応まで一貫して行う体制を整えています。さらに2025年6月から確定検査(羊水・絨毛検査)も院内で実施できる体制を整えました。非認証でありながら、ここまで一貫体制が整った医療機関は稀有です。
🧬 臨床遺伝専門医が一貫担当
臨床遺伝専門医(2011年取得)が、30年以上の医師人生の中でのべ10万人以上のご家族の意思決定と向き合ってきた経験を踏まえ、情報提供と意思決定支援を行います。
🏥 院内で確定検査まで
羊水検査・絨毛検査を院内で実施可能です。転院による不安時間を短くし、必要な医療へつなぎます。
🔬 COATE法(ダイヤモンド/NEWプレミアム)
SNP法+ターゲット法の融合で、微細欠失の陽性的中率が従来70%台から>99.9%と報告されています(エビデンスはこちら)。必要最低胎児分画(胎児ゲノム率)は3%です。父親由来の精子の新生突然変異も評価対象となり得ます。
💰 トリプルリスクヘッジ
互助会制度(互助会費8,000円)はNIPT受検者全員に適用され、陽性時の羊水検査費用が全額補助(上限なし)されます。時間的にも心理的にも、院内完結で支えます。
(父親由来の遺伝子変異が子へ伝わるイメージ)
💎 ダイヤモンドプランのカバー範囲(記載範囲は下記のみ)
必要最低胎児分画(胎児ゲノム率)は3%です。当院のNIPTは微細欠失(微小欠失)を中心に設計されていますが、同じ領域でコピー数が増える「重複」も検出されることがあります。その場合、結果の意味づけは専門的な判断が必要となるため、遺伝カウンセリングで詳しくご説明します。
● 常染色体トリソミー(6種)
13 / 15 / 16 / 18 / 21 / 22
● 性染色体異数性(4種)
45,X / 47,XXX / 47,XXY / 47,XYY
● 微細欠失(12領域)
1p36欠失,2q33欠失,4p16欠失,5p15欠失,8q23q24欠失,9p欠失,11q23q25欠失,15q11.2-q13欠失,17p11.2欠失,18p欠失,18q22q23欠失,22q11.2欠失
● 単一遺伝子(56遺伝子)はダイヤモンドプランでカバーされます。多くが「重度の合併症を伴う症候性(重い)自閉症」に関連し得るため、結果の解釈は専門的支援が不可欠です(参考:ACMG等)。[6]

🩺 院長コラム【「話を聞いてから決める」ための時間を確保しています】
当院ではお一人あたり1.5時間の枠をお取りし、検査前に十分な遺伝カウンセリングを行います。検査の意味、結果の解釈、陽性だった場合の選択肢など、不安なまま検査を受けることがないように、丁寧に整理します。
どの検査を選ぶかは、ご家族の価値観と優先順位によって変わります。私は医師として誘導しません。「理解したうえで選べる状態」を作ることが、私の仕事です。
一人で抱え込まないでください
検査の選択は、ご家族にとって大きな決断です。
正しい情報を整理し、心を守るための準備を一緒に始めましょう。
※ご相談は可能ですが、当院受検者へのサポートを優先します
まとめ|出生前診断でわかること・わからないこと
- ➤出生前診断でわかること:染色体異常や一部の遺伝子疾患の可能性
- ➤わからないこと:多因子疾患や将来の発達特性の多く
- ➤NIPTは確定診断ではない:陽性の場合は出生前の確定診断へ
- ➤大切なのは、検査結果を一人で抱え込まないこと
出生前診断を「受けるべきかどうか」に正解はありません。大切なのは、ご家族が納得できるだけの情報を持った上で選ぶことです。
よくある質問(FAQ)
🏥 不安を、ひとりで抱えないために
出生前診断は「検査」ですが、実際には「人生の意思決定」の入口になることがあります。
だからこそ、私たちは正確性と心の安全を最優先にします。
関連記事
参考文献
- [1] American College of Obstetricians and Gynecologists (ACOG). Screening for Fetal Chromosomal Abnormalities (Practice Bulletin). [ACOG]
- [2] Gregg AR, et al. Noninvasive prenatal screening for fetal aneuploidy, 2016 update: a position statement of the ACMG. Genet Med. 2016. [PubMed]
- [3] Gil MM, et al. Analysis of cell-free DNA in maternal blood in screening for fetal aneuploidies: updated meta-analysis. Ultrasound Obstet Gynecol. 2017. [PubMed]
- [4] Wapner RJ, et al. Expanding the scope of noninvasive prenatal testing: detection of fetal microdeletion syndromes. Am J Obstet Gynecol. 2015. [PubMed]
- [5] Vora NL, et al. Prenatal exome sequencing in anomalous fetuses: opportunities and challenges. Genet Med. 2017. [PubMed]
- [6] ACMG. Policy/Guidance resources for genetic counseling and genomic testing (principles of non-directiveness and counseling). [ACMG]
- [7] International Society for Prenatal Diagnosis (ISPD). Position statements and resources. [ISPD]