この記事では、ESMOデイリーリポートから、dailyreporter.esmo.org/esmo-congress-2023/gastrointestinal-cancers/new-treatment-paradigms-may-offer-advances-in-pancreatic-cancer-treatmentsを翻訳してお伝えしたいと思います。
ネオアジュバント療法、周術期療法、分子標的療法、および併用療法は、この侵攻性疾患の患者にとって有益である可能性が示されているが、さらなる研究が必要である。
膵癌は、その侵攻性と予後不良で悪名高く、依然としてアンメット・メディカル・ニーズが最も高い領域であり、現代の腫瘍学における最大の課題の一つである。ESMO Congress 2023(マドリッド、10月20〜24日)で発表された4つの臨床試験は、膵臓がん患者の治療を改善するためのさまざまな革新的戦略を模索している。
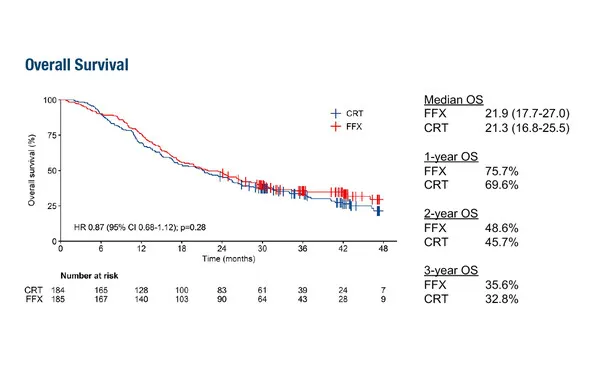
最初の試験である第III相PREOPANC-2試験では、境界切除可能および切除可能な膵腺癌(PDAC;LBA83)患者において、ネオアジュバントFOLFIRINOX療法とネオアジュバントゲムシタビンベースの化学放射線療法との比較で、主要評価項目である全生存期間(OS)の利益は示されなかった。OS中央値はそれぞれ21.9%対21.3%であった(ハザード比0.87;95%信頼区間CI:.68-1.12;p=0.28)。切除率(それぞれ77%対75%;p=0.7)と重篤な有害事象発生率(それぞれ49%対43%;p=0.26)も治療群間で同様であった。
LBA83_Westphalen_ESMO23
図. PREOPANC-2試験におけるネオアジュバントFOLFIRINOX療法とゲムシタビンベースの化学放射線療法との比較では、全生存期間は改善しなかった(ESMO Congress 2023, LBA83)。
dailyreporter.esmo.org/esmo-congress-2023/gastrointestinal-cancers/new-treatment-paradigms-may-offer-advances-in-pancreatic-cancer-treatmentsより引用。前回のPREOPANC試験(J Clin Oncol. 2022;40:1220-1230)では、切除可能および境界切除可能な膵癌において、ネオアジュバント・ゲムシタビンベースの化学放射線療法後に手術を行い、アジュバント・ゲムシタビンを投与した場合、前もって手術を行い、アジュバント・ゲムシタビンを投与した場合と比較して、OSが改善することが示された。ドイツ、ミュンヘン大学病院のBenedikt Westphalen博士は、「PREOPANC-2試験では、ネオアジュバント療法においてFOLFIRINOXがゲムシタビンベースの化学放射線療法の有効性に取って代わるかもしれないという仮説が立てられましたが、結論はそうではありませんでした。OS中央値は治療群間でほぼ一致し、切除率および重篤な有害事象発生率も同様であった。したがって、境界領域、局所進行、切除可能な膵癌の管理およびネオアジュバント治療の選択肢を検討するために、さらなる研究が必要である」。
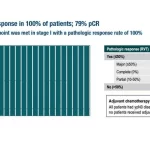
2番目の試験である単群第II相nITRO試験では、切除可能なPDAC患者107人において、周術期のNALIRIFOXは管理可能であり、有効であった(抄録番号1620P)。全体として、87人の患者が外科的切除を受け、65.3%のR0切除率が達成され、代替仮説の55%を上回った。追跡期間中央値33.1ヵ月後、intention-to-treat集団におけるOS中央値は32.3ヵ月(95%CI 27.8-44.3)であり、切除された患者のOS中央値は44.3ヵ月(95%CI 33.2-評価不能)であった。TNF-αは、奏効および生存期間と最も有意な相関を示した循環因子であった。Westphalen氏は、「切除可能なPDACの治療において、ネオアジュバントと周術期の戦略の役割は、激しい科学的議論の核心にあります。著者らは、NALIRIFOXは実行可能で効果的な周術期レジメンになりうると結論づけている。化学療法抵抗性において極めて重要なサイトカインであるTNF-αと生存成績との相関所見は、切除可能なPDACに対する治療戦略の微調整において分子経路を標的とするアプローチを支持するものである。”
膵がんにおける精密医療の役割について肯定的なデータが第Ⅱ相RAGNAR試験(抄録番号1621P)から発表され、前治療歴のある進行性/転移性膵がんで、事前に規定されたFGFR1-4遺伝子変異(14個のFGFR2、4個のFGFR1)を有する18人の患者において、エルダフィチニブ(FGFR阻害剤)の臨床的に意味のある活性が示された。全奏効率(ORR)は55.6%(95%信頼区間30.8-78.5)、OS中央値は19.7ヵ月であった。安全性データはエルダフィチニブの既知のプロファイルと一致していた。Westphalen氏によれば、「本試験で得られた注目すべきORRとOSのデータは、かなり限定された患者集団ではあるが、強力な臨床活性を示すものである。この研究は、特定の遺伝子変化に基づいて介入を調整することにより、膵臓癌の治療における識別アプローチを導入するものです」。
最後に、別の第II相試験(n=36)の予備的結果は、転移性PDAC患者における3次治療としてCBP501、シスプラチン、ニボルマブの3剤併用戦略を用いた臨床的に意義のある改善と忍容性を示した(抄録番号1625P)。3ヵ月無増悪生存(PFS)率は44%(CBP501 25mg/m2とシスプラチンおよびニボルマブ併用)、22%(CBP501 16mg/m2とシスプラチンおよびニボルマブ併用)、11%(CBP501 25mg/m2とシスプラチン併用)、33%(シスプラチンおよびニボルマブ併用)であった。ORRは3剤併用群で22%(部分奏効2例)であったが、他の群では0%であった。「PFSとORRに基づくと、CBP501、シスプラチン、ニボルマブを用いた本試験は、3次治療における役割の可能性を示しています」とWestphalen氏は指摘する。「治療成績は、その後の治療の必要性を強調していますが、化学療法と免疫療法を統合する方向に向かっているため、患者の層別化と治療成績を改善するためのレジメンの最適化の両方において、さらなる改良が必要です」。
これらの研究を総合的に精査することは、ネオアジュバント療法、周術期療法、標的療法、併用療法の可能性を強調するだけでなく、膵臓癌の最適な治療法を解明するための困難な道のりを明らかにするものでもあります。PREOPANC-2試験は、ネオアジュバントレジメンの策定と改良をより深く探求するよう腫瘍学コミュニティに呼びかけている。一方、nITROとRAGNARの有望な結果は、個別化および標的化アプローチが、患者のサブグループによりよい転帰をもたらす可能性を解明している。一方、CBP501、シスプラチン、ニボルマブで明らかになったような新しい併用療法を探求することは、進行期患者の管理に新たな地平を開くかもしれません」。

ミネルバクリニックでは、がんに罹患していないか、または、術後に再発していないか、治療効果はどうか、というモニタリングを可能な遺伝子検査を提供しています。検体は血液ですが、オンライン診療で当院を受診していただき、全国の協力施設で採血をした頂く形で検査を受けることが可能です。是非ご検討ください。
関連記事:
●がんに罹患していないか、術後に再発していないか、治療効果はあるか、のモニタリング|リキッドバイオプシー
●総合がん遺伝子検査(がんになりやすいのかを検査)