目次
- 1 1. HCFC1遺伝子とは:X染色体上に位置する転写制御のマスターハブ
- 2 2. HCF-1タンパク質の構造と独自の成熟メカニズム
- 3 3. ゲノム全体を制御する機能:CpGアイランドとX染色体不活性化
- 4 4. cblX症候群:コバラミン代謝を制御する転写因子が壊れると何が起きるか
- 5 5. X連鎖性知的障害(XLID):発現量が増えても減っても危険
- 6 6. リボソーム病・肝疾患・がんとの多面的な関与
- 7 7. 単純ヘルペスウイルス(HSV-1)によるHCFC1のハイジャック機構
- 8 8. 診断と遺伝子検査:どうやってHCFC1変異を見つけるか
- 9 9. 治療戦略:代謝補正から最新のASO療法まで
- 10 10. 遺伝カウンセリングと家族へのサポート
- 11 よくある質問(FAQ)
- 12 参考文献
- 13 関連記事
📍 クイックナビゲーション
HCFC1(Host Cell Factor C1)遺伝子は、X染色体長腕(Xq28)に位置する、全身の遺伝子発現を統括するマスターレギュレーターです。この遺伝子が産生するHCF-1タンパク質は、DNAに直接結合しないにもかかわらず、数百種類の転写因子やクロマチン修飾酵素を細胞核内の標的部位へ誘導する「分子足場(Scaffold)」として機能し、細胞周期・脳発生・コバラミン(ビタミンB12)代謝・X染色体不活性化など、生命維持に欠かせない多彩なプロセスを統合的に制御しています。HCFC1に変異が生じると、重篤な先天性代謝異常症(cblX型メチルマロン酸血症)・X連鎖性知的障害・肝疾患・さらには悪性腫瘍まで、幅広い疾患を引き起こすことが明らかになっています。
Q. HCFC1遺伝子とはどのような遺伝子ですか?まず結論だけ知りたいです
A. X染色体長腕(Xq28)に位置し、全身の遺伝子発現を統括する「転写共調節因子(HCF-1タンパク質)」をコードする遺伝子です。変異によりコバラミン代謝異常症(cblX症候群)・X連鎖性知的障害・肝疾患・がんなど多彩な疾患を引き起こします。発現量が多すぎても少なすぎても危険という「用量感受性(Dosage-sensitive)」が重要な特徴です。
- ➤遺伝子の基本情報 → Xq28・X連鎖遺伝・HCF-1タンパク質の分子足場機能
- ➤構造と成熟メカニズム → Kelchドメイン・OGT依存的タンパク質分解・ヘテロ二量体形成
- ➤cblX症候群 → MMACHC転写制御の破綻・メチルマロン酸血症・cblCとの違い
- ➤知的障害・リボソーム病 → 発現量の増減どちらも危険・リボソーム生合成不全という新たな側面
- ➤治療戦略 → コバラミン補充の限界・小分子阻害薬・次世代ASO療法の展望
1. HCFC1遺伝子とは:X染色体上に位置する転写制御のマスターハブ
HCFC1(Host Cell Factor C1)遺伝子は、ヒトX染色体長腕(Xq28)に位置し、HCF-1(Host Cell Factor 1)タンパク質をコードする遺伝子です。HCF-1は進化的に高度に保存されており、菌類から哺乳類まで幅広い生物に存在します。その名称はもともと、単純ヘルペスウイルス(HSV)の感染初期遺伝子の発現に必要な「宿主細胞因子(Host Cell Factor)」として同定されたことに由来しますが、現在ではその生物学的役割がはるかに広範であることが明らかになっています。
HCF-1タンパク質は、特定のDNA配列に自分では直接結合できないにもかかわらず、細胞核内において多数の配列特異的転写因子やクロマチン修飾酵素と物理的に相互作用し、それらを標的遺伝子のプロモーター領域へ誘導する「分子足場(Scaffold)」として機能します。この仕組みにより、HCFC1は細胞周期の進行・細胞の自己複製・アポトーシス・各種代謝応答をゲノムレベルで統合的に制御するマスターレギュレーターとして位置づけられています。
💡 用語解説:転写共調節因子(Transcriptional Coregulator)とは
「転写」とは、DNAの情報をRNAに写し取る過程のこと。「転写因子」はDNAに結合して転写を制御するタンパク質ですが、「転写共調節因子」はDNA自体には結合せず、転写因子やその他の酵素複合体と結合してそれらの活性を促進・抑制する補助的な役割を担います。HCFC1はその典型例であり、自身がDNAに触らなくても多数の転写因子を束ねることで、広範な遺伝子発現プログラムを制御します。
💡 用語解説:X連鎖遺伝(Xq28の位置)とは
ヒトの性染色体は女性がXX、男性がXYです。X染色体上に位置する遺伝子の遺伝形式を「X連鎖遺伝」と呼びます。男性はX染色体を1本しか持たないため(ヘミ接合体)、変異があれば必ず発症します。一方、女性はX染色体を2本持つため、片方のXに変異があっても、もう片方の正常なXが補うことができ(保因者)、多くの場合は無症状か軽症です。Xq28とはX染色体長腕(q)の28番バンドを指す染色体上の位置情報です。
HCFC1の重要性は、その影響を受ける疾患の多様さにも表れています。Kelchドメイン内の特定のミスセンス変異はcblX型コバラミン代謝異常症を引き起こし、5’非翻訳領域の調節変異は非症候性のX連鎖性知的障害を生じさせます。また、がん細胞ではHCFC1が過剰発現して腫瘍の悪性化を促進する一方、肝細胞でHCFC1が欠如すると急速にNAFLD(非アルコール性脂肪性肝疾患)が進行します。「多すぎても少なすぎても致命的」という用量感受性が、HCFC1を理解する上での核心です。
2. HCF-1タンパク質の構造と独自の成熟メカニズム
HCF-1は複数の機能ドメインが連結された巨大かつ複雑なタンパク質であり、機能的な複合体となるためには極めて特殊な翻訳後修飾プロセスを経る必要があります。
5つの主要ドメインとその役割
🔵 Kelchドメイン(N末端側)
タンパク質間相互作用を媒介する最重要領域。THAP11(Ronin)・ZNF143・HSV-1のVP16など多数の転写因子との結合に不可欠。疾患関連ミスセンス変異の大部分がこの領域に集中しており、その生物学的絶対性を示しています。
🟣 HCF-1PROリピート(中央部)
20〜26アミノ酸の配列が6回繰り返される「蛋白質分解ドメイン(PPD)」。後述するOGTによる特殊な切断反応の標的となる領域です。
🟡 酸性活性化ドメイン(C末端側)
アミノ酸残基1600〜1730の領域。基本転写因子複合体TFIIDのサブユニット(Taf4b・Taf6・Taf9)と直接結合し、転写開始を促進します。VP16やLZIPによるトランスアクティベーションにも不可欠。
🟢 フィブロネクチン様リピート(C末端)
HPIP(HCFC1R1)などの輸送タンパク質と相互作用し、HCF-1がCRM1依存的に核から細胞質へシャトル移動するプロセスを制御します。ウイルス感染時のVP16輸送にも重要。
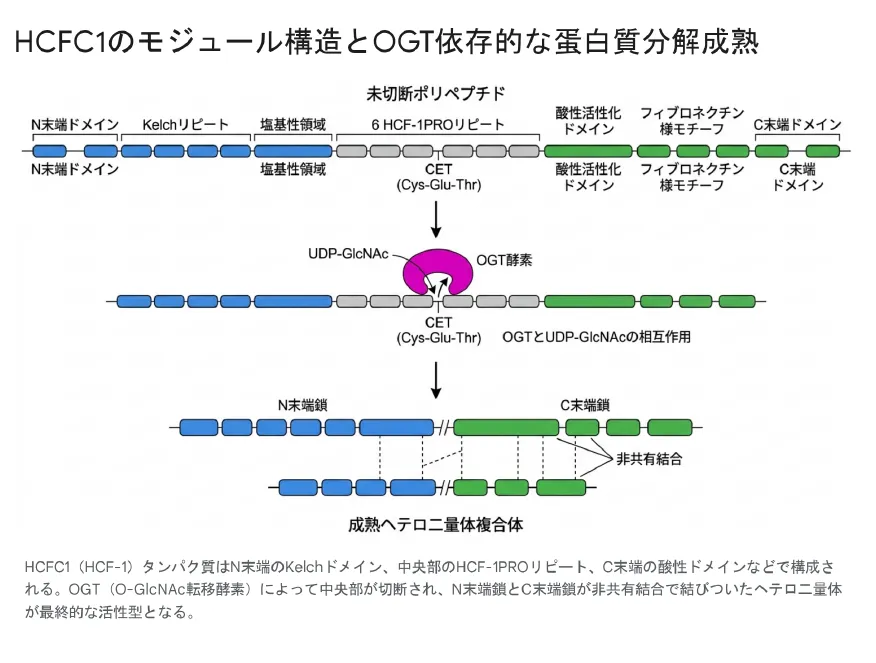
HCF-1タンパク質はN末端のKelchドメイン・中央部の6つのHCF-1PROリピート・C末端の酸性ドメインなどで構成される。OGT(O-GlcNAc転移酵素)によって中央部が切断され、N末端鎖とC末端鎖が非共有結合で結びついたヘテロ二量体が最終的な活性型となる。
OGTによる異例のプロテアーゼ活性:栄養センシングと連動した成熟メカニズム
HCF-1タンパク質が機能的な複合体へと成熟するプロセスは、生物学的に極めて稀なメカニズムに依存しています。HCF-1は中央部の6つのHCF-1PROリピートのいずれかで蛋白質分解的に切断され、N末端鎖とC末端鎖に分断されます。この切断反応を触媒するのが、通常はタンパク質に単糖(O-GlcNAc)を付加する「糖転移酵素」として知られるO-GlcNAc転移酵素(OGT)です。
OGTが他の基質に対して糖転移酵素として振る舞うのに対し、HCF-1に対しては例外的に「プロテアーゼ」として機能するという点が特筆されます。この切断にはHCF-1PROリピート内の保存されたCET(Cysteine-Glutamic acid-Threonine)配列のグルタミン酸残基がOGTの活性中心に位置づけられることで物理的な基質歪みが生じ、切断が触媒されます。また補酵素としてUDP-GlcNAcの存在が絶対的に必要であり、この物質は細胞内の糖代謝中間体です。
切断後に生じたN末端鎖とC末端鎖は互いに離れることなく非共有結合によって強固に結びつき、最終的な活性型ヘテロ二量体複合体を形成します。このUDP-GlcNAcに依存した成熟プロセスは、細胞内の栄養状態(糖代謝の中間代謝物であるUDP-GlcNAcの濃度)と細胞周期の進行やエピジェネティクス制御を直接リンクさせる、高度な細胞内栄養センシング機構として機能していると考えられています。
💡 用語解説:O-GlcNAc転移酵素(OGT)とは
OGT(O-GlcNAc transferase)は、タンパク質のセリン・スレオニン残基にN-アセチルグルコサミン(GlcNAc)という単糖を付加する酵素です。この「O-GlcNAc化」は細胞のシグナル伝達・転写制御・タンパク質安定性など多様な機能に関与します。HCFC1に対しては、この酵素が糖転移活性ではなくプロテアーゼ(タンパク質分解酵素)として働くという、生物界でも極めて稀な例外的作用を示します。この反応にはUDP-GlcNAcという補酵素が必要で、食事からの糖質摂取量が細胞内のUDP-GlcNAc濃度に影響します。
💡 用語解説:エピジェネティクスとは
DNA塩基配列そのものを変えずに、遺伝子の「読まれ方(発現量)」を制御する仕組みの総称です。DNAのメチル化・ヒストンタンパク質の修飾(メチル化・アセチル化など)が代表例。HCFC1はこれらのエピジェネティック修飾酵素を遺伝子のプロモーターに招集し、細胞の状況に応じて遺伝子発現のオン・オフを精密に制御するマスターハブとして機能します。
3. ゲノム全体を制御する機能:CpGアイランドとX染色体不活性化
HCFC1は、特定の遺伝子を局所的に制御するにとどまらず、哺乳類のゲノム全体にわたる遺伝子発現ネットワークの根幹に関与していることが、最新の研究(2025年)によって明らかになりつつあります。
クロマチン修飾酵素複合体の選択的動員
細胞周期のG1期からS期への重要な移行ポイントにおいて、HCF-1はE2F応答性プロモーターへと動員され、Set1およびMLL(Mixed-Lineage Leukemia)ヒストンメチルトランスフェラーゼ複合体(COMPASS複合体)をリクルートします。この動員によりヒストンH3の4番目のリジン残基のトリメチル化(H3K4me3)が触媒され、クロマチン構造が緩んで転写活性化状態が誘導されます。一方でHCF-1は状況に応じてSin3複合体(HDAC含む)とも結合し、転写抑制的なクロマチン環境を構築することもできます。また脱ユビキチン化酵素BAP1とも複合体を形成し、タンパク質安定性の制御も担います。
💡 用語解説:CpGアイランドとは
CpGとは、DNAの塩基配列においてシトシン(C)とグアニン(G)が隣接した部分のこと。ゲノム全体にはCpGが少ない一方で、遺伝子のスイッチ(プロモーター)付近にCpGが集中した領域(アイランド)が多数存在します。哺乳類の全遺伝子の約3分の2はプロモーター領域にCpGアイランドを持っています。これらのCpGアイランドプロモーターがどのように選択的に活性化されるかは長年の謎でしたが、2025年の研究でHCFC1がその鍵を握ることが判明しました。
2025年の革新的発見:CpGアイランド特異的コアクチベーター
2025年に発表されたプロテオーム規模の機能スクリーニング研究により、HCFC1が「CpGアイランド特異的コアクチベーター」の創設メンバーであることが特定されました。この研究は、HCFC1が数千に及ぶCGIプロモーター駆動型遺伝子の発現に不可欠であり、その特異性が精密な2段階メカニズムで達成されることを証明しました。
第一段階:CGIプロモーターに恒常的に結合しているTHAP11やZNF143などの転写因子群が、HCFC1のKelchドメインを認識してプロモーター領域へと動員します。第二段階:プロモーターに固定されたHCFC1は、自身のC末端の酸性活性化ドメインを介して基本転写因子複合体であるTFIIDのサブユニット(Taf4b・Taf6・Taf9)と直接結合します。この結合が、CGIプロモーターにおける転写開始の最大の律速段階である「TFIIDの動員」を強力に促進し、DNAに結合した転写因子群と一般転写機構を繋ぐ架け橋として機能します。
哺乳類のX染色体不活性化(XCI)を開始するトリガー
2025年のゲノムワイド解析により、HCFC1自体がX染色体上にコードされている遺伝子でありながら、X染色体不活性化(XCI)プロセスの開始を支配する極めて重要な活性化因子であることが証明されました。
💡 用語解説:X染色体不活性化(XCI)とは
女性(XX)の細胞が持つ2本のX染色体のうち1本を転写的に沈黙させる仕組みです。男性(XY)との間の遺伝子量の不均衡を是正するための必須の投与量補償メカニズムで、初期胚発生において起きます。Xist(エクシスト)という長鎖ノンコーディングRNAが不活性化されるX染色体全体を覆うことでサイレンシングが完成します。このXCIの開始にHCFC1が不可欠な役割を果たすことが2025年に明らかになりました。
XCI実行の鍵は、長鎖ノンコーディングRNAであるXistの対立遺伝子特異的な発現です。このXistの活性化プロセスにおいて、HCFC1は多機能転写因子YY1と物理的に相互作用し、ゲノム全体の調節エレメントに共動員されます。不活性化されるX染色体上では、YY1とHCFC1の複合体がXist遺伝子自体およびそのシス活性化因子(JpxやFtx)の調節領域に結合し、2つの強力なエピジェネティクス制御複合体が協調して働きます。
🧬 HCFC1とYY1によるX染色体不活性化(XCI)開始モデル
+
▶
(クロマチン開放)
(転写開始促進)
マウスでHcfc1をホモ・ヘテロ接合で欠損させると、XCIが機能不全に陥り胚性致死が引き起こされる。
💡 用語解説:ヒストン修飾(H3K4me3)とは
DNAはヒストンというタンパク質に巻き付いた「ヌクレオソーム」構造をとっています。ヒストンの特定のアミノ酸にメチル基(me)やアセチル基などの化学修飾が加わることで、DNAの巻き付きが緩んだり(転写活性化)、固まったり(転写抑制)します。「H3K4me3」とはヒストンH3の4番目のリジン(K4)に3つのメチル基がついた状態で、転写が活発な遺伝子のプロモーターに集まる「活性化マーク」です。HCFC1はCOMPASS複合体をリクルートしてこのマークを付与します。
4. cblX症候群:コバラミン代謝を制御する転写因子が壊れると何が起きるか
HCFC1遺伝子の変異がヒトにもたらす最も特徴的かつ重篤な臨床的帰結の一つが、細胞内コバラミン(ビタミンB12)代謝の先天性エラーである「cblX型メチルマロン酸血症およびホモシスチン尿症(MAHCX)」です。この疾患の発見は、先天性代謝異常症に関する従来の医学的常識を覆すものでした。
コバラミン代謝経路とMMACHC遺伝子の役割
食事から摂取されたコバラミンは、細胞内に取り込まれた後、2つの活性型補酵素形態に変換されます。アデノシルコバラミン(AdoCbl)はミトコンドリア内でメチルマロニルCoAムターゼの機能に必須であり、メチルコバラミン(MeCbl)は細胞質内でホモシステインをメチオニンに変換するメチオニン合成酵素に必須です。これら変換経路の最上流で重要な還元・脱アルキル化反応を担うのがMMACHCタンパク質です。
HCFC1は、ジンクフィンガー型転写因子であるTHAP11(Ronin)と強固な機能的複合体を形成し、ゲノム上のMMACHC遺伝子プロモーターに直接結合してその転写を強力に活性化します。HCFC1に変異が生じてこの転写活性化能が破綻すると、細胞内のMMACHCのmRNAおよびタンパク質の発現が著しく低下し、AdoCblとMeCblの合成が根元から断たれます。生化学的マーカーとして血清メチルマロン酸の顕著な上昇と高ホモシステイン血症が引き起こされます。
💡 用語解説:メチルマロン酸血症とは
メチルマロン酸(MMA)は通常、ミトコンドリア内で速やかに代謝されますが、この代謝が障害されると血中・尿中に蓄積します。MMAは神経毒性があり、新生児期から高アンモニア血症・代謝性アシドーシス・神経障害などを引き起こします。詳しくはホモシスチン尿症を伴うメチルマロン酸血症総論をご参照ください。
💡 用語解説:ホモシスチン尿症とは
ホモシステインは通常メチオニンに変換されますが、この変換が障害されると血中・尿中にホモシステインが蓄積します。血管障害・血栓症・骨粗鬆症・水晶体脱臼・神経障害などを引き起こします。メチルコバラミン(MeCbl)の欠乏により二次的に引き起こされるのがcblX症候群の特徴です。
cblC症候群とcblX症候群の比較:座乗異質性という概念の確立
コバラミン代謝異常症の中で最も発症頻度が高いのは、MMACHC遺伝子自体の常染色体潜性変異によるcblC型です。一方、生化学的検査や細胞補完アッセイではcblC型の特徴を示しながらも、MMACHC遺伝子自体には一切の変異を持たない特異な男児患者群の全エクソーム解析から発見されたのがX連鎖性の「cblX型」です。
💡 用語解説:座乗異質性(Locus heterogeneity)とは
同じ表現型(症状・検査所見)を持ちながら、原因となる遺伝子の位置(座乗)が異なる現象を座乗異質性と呼びます。cblX症候群の発見は、「代謝酵素自体ではなく、その酵素の転写を制御する転写調節因子の変異」が古典的な代謝異常症の表現型を完全に模倣するという画期的な証明となりました。この概念は先天性代謝異常症の診断において重大なパラダイムシフトをもたらしています。
| 比較項目 | cblC症候群(MMACHC変異) | cblX症候群(HCFC1変異) |
|---|---|---|
| 遺伝形式 | 常染色体潜性(劣性) | X連鎖性(主に男児に発症・ヘミ接合) |
| 分子発症機序 | 酵素(MMACHC)の直接的な機能不全 | 転写異常によるMMACHC mRNA発現低下 |
| 神経学的症状 | 発達遅滞、白質脳症、痙攣 | 難治性てんかん(点頭てんかん等)、重度の神経認知障害、小頭症、舞踏アテトーゼ |
| 形態的異常 | 一般的に稀 | 重度の頭蓋顔面異常、脳回形成異常 |
| 眼科的所見 | 牛眼状黄斑症が頻発 | 黄斑症は通常認められない |
| 生化学的所見 | 血中MMA上昇、高ホモシステイン血症 | cblCと同様(重症度は変異部位によるばらつきあり) |
cblX型の原因変異の多くは、HCFC1タンパク質のN末端にあるKelchドメイン内の高度に保存されたアミノ酸におけるミスセンス変異(A115V・A73V・A73Tなど)です。cblX症候群が単なるコバラミン代謝異常の枠に収まらない複雑な臨床像を呈するのは、HCFC1がMMACHC以外の多数の標的遺伝子をも広範に制御しているためです。関連する疾患についてはこちらもご参照ください:cblJ型・cblF型・cblD型・cblB型・cblC型ダイジェニック
5. X連鎖性知的障害(XLID):発現量が増えても減っても危険
HCFC1の異常は、代謝障害を伴わない純粋な中枢神経系の発達障害も引き起こします。その分析から、HCFC1が発現量の過剰でも過少でも壊滅的な結果を招く「遺伝子量感受性(Dosage-sensitive)」の性質を持つことが明らかになっています。
機能獲得(過剰発現):神経回路形成の異常
知的障害の大家系(MRX3ファミリー)の詳細な遺伝子解析により、HCFC1のタンパク質コード領域ではなく5’非翻訳領域(5’UTR)に位置する転写調節領域に点変異(c.0001 A-Gトランジション)が存在することが同定されました。この非コード変異は、本来HCFC1の転写を抑制している転写因子YY1の結合サイトを破壊します。YY1による抑制が外れることで、細胞内におけるHCFC1のmRNAおよびタンパク質の発現量が定常的に約1.6倍に過剰発現する結果となります。
マウスの胚性神経幹細胞および海馬ニューロンを用いた機能解析において、このHCFC1の過剰発現は深刻な神経発生異常を引き起こしました。具体的には、細胞増殖が阻害されてニューロンへの分化が抑制される一方で、アストロサイト系統への分化が異常にバイアスされ、アストロサイトの過剰産生が引き起こされます。さらに分化した海馬ニューロンでは、神経突起の成長や樹状突起の複雑な分岐(Arborization)が著しく減少し、神経細胞死が増加します。こうした神経回路網の構築不全が、MRX3家系における顔面形態異常を伴わない非症候性知的障害の直接的な原因となっています。
機能喪失(発現低下):神経前駆細胞の枯渇と小頭症
一方、HCFC1の機能喪失を引き起こすミスセンス変異もまた重度の知的障害をもたらします。Kelchドメイン内のS225N変異やA897V変異は、代謝異常を伴わずに小頭症・言語発達遅延・精神運動発達遅滞を特徴とするXLIDを引き起こします。これらの変異は胎生期の脳内で活発に分裂している神経前駆細胞(NPC)の維持に悪影響を及ぼし、NPCの異常な枯渇や細胞死の増加を通じて大脳皮質の体積減少(小頭症)をもたらします。ゼブラフィッシュを用いたノックダウンモデルでも、hcfc1b遺伝子の抑制がSOX2陽性の神経前駆細胞の異常な分化挙動を誘発することが確認されています。
💡 用語解説:機能獲得変異・機能喪失変異とは
機能喪失(Loss-of-Function:LOF)変異は、タンパク質の正常な機能が失われる変異です。一方機能獲得(Gain-of-Function:GOF)変異は、タンパク質が新たな・あるいは過剰な機能を獲得する変異です。HCFC1の場合は「発現量が1.6倍に増える」という形の量的なGOFが神経発生異常を引き起こします。同じ遺伝子でも、LOFとGOFで引き起こされる病態が異なることがあり、HCFC1はその典型例です。
6. リボソーム病・肝疾患・がんとの多面的な関与
リボソーム病という新たな側面
cblX症候群の患者に見られる頭蓋顔面異常や特定の心疾患は、古典的なコバラミン代謝異常のモデルだけでは説明が困難でした。近年のトランスクリプトーム解析とマウスモデル(Hcfc1 A115V変異マウス・Ronin F80L変異マウス)の研究により、HCFC1が引き起こす病態に「リボソーム病(Ribosomopathy)」という全く新しい側面が隠されていることが明らかになりました。
💡 用語解説:リボソーム病(Ribosomopathy)とは
リボソームはタンパク質を合成する細胞内小器官です。リボソームを構成するタンパク質サブユニットや組み立て因子の遺伝子異常によって生じる疾患群を総称して「リボソーム病」と呼びます。代表例はダイアモンド・ブラックファン貧血やShwachman-Diamond症候群など。HCFC1とTHAP11の複合体はMMACHC遺伝子のほかに、多数のリボソームタンパク質遺伝子およびリボソーム生合成因子(RBF)遺伝子の転写も直接制御することが判明し、HCFC1変異症候群がリボソーム病の側面も持つことが証明されました。
HCFC1のA115V変異やTHAP11の変異が存在すると、リボソーム関連遺伝子の発現が広範に脱制御されます。マウスモデルでは、このリボソーム生合成の破綻が翻訳効率の全体的な低下やプロテアソームを介したタンパク質分解ストレスの増大を招き、出生後早期の致死性・脳梁の顕著な菲薄化・心室心筋の重篤な発達欠損・頭蓋顔面異常という深刻な発生障害を引き起こしました。これらの知見は、HCFC1変異によって引き起こされる症候群が「コバラミン代謝の崩壊」と「リボソーム生合成不全」という2つの全く異なる細胞機能障害が重畳した複合マルチ・シンドロームであることを示しています。
肝臓の代謝ホメオスタシスとNAFLD/NASHへの関与
肝細胞特異的にHcfc1遺伝子を欠損させたマウス(hepKO)を用いた研究は、HCFC1が肝臓をNAFLD・NASHから保護するための重要な防波堤であることを示しています。通常の肝細胞において、HCF-1はKDM1A・PHF8などのヒストン脱メチル化酵素や、KAT8 MOFなどのアセチル基転移酵素と連結し、糖新生や脂質代謝に関わる遺伝子群を精密に制御しています。
Hcfc1が欠乏すると、肝細胞は酸化的リン酸化やミトコンドリアの構造・機能維持に関わる遺伝子群の発現を維持できなくなります。この遺伝子発現の破綻は重篤なミトコンドリア機能不全を引き起こし、肝細胞内への異常な脂質蓄積(脂肪肝)・慢性的な炎症の惹起・コラーゲン沈着による肝線維化といったNAFLD/NASHの全特徴が自然発生的かつ急速に進行します。さらに興味深いことに、肝再生においても性差があり、X染色体を1本しか持たない雄マウスは肝再生に全く参加できず死に至るのに対し、正常アレルを1つ持つ雌マウスはXCI モザイクによって正常肝細胞が確保され生存できます。
💡 用語解説:NAFLD/NASH(非アルコール性脂肪性肝疾患)とは
飲酒歴がないにもかかわらず脂肪肝・炎症・線維化が進行する疾患群の総称。NAFLD(非アルコール性脂肪性肝疾患)の重症型がNASH(非アルコール性脂肪肝炎)で、放置すると肝硬変・肝細胞癌へ進行することがあります。HCFC1の機能を保つことが、ミトコンドリア機能を介して肝細胞の代謝ホメオスタシスを守るうえで不可欠であることがマウスモデルで示されています。
がん(HCC・NSCLC・前立腺がん)における過剰発現
HCFC1の機能喪失が臓器変性をもたらす一方で、過剰発現は細胞の異常増殖を牽引し、悪性腫瘍の形成・悪性化を促進します。
肝細胞癌(HCC):臨床検体の大規模解析において、HCFC1のmRNAおよびタンパク質の発現レベルが正常組織と比較して有意に上昇していることが確認されています。HCFC1の高発現は、高い腫瘍ステージ・腫瘍の巨大化・低い細胞分化度・血管への浸潤・再発率の上昇と強く相関しており、特に早期ステージ患者における全生存期間(OS)および無再発生存期間(RFS)を予測する独立した不良予後因子として機能しています。
非小細胞肺がん(NSCLC):HCFC1の発現上昇が、肺がんの重要な転写因子Nkx2.1の発現亢進およびOGTおよび全体的なO-GlcNAc化の亢進と密接に連動しています。NSCLC細胞株でHCFC1をノックダウンすると、細胞増殖能力が顕著に低下することから、HCFC1を軸としたO-GlcNAc化シグナル伝達カスケードが肺がんの進行に不可欠であることが証明されています。
前立腺がん:ヒストン修飾酵素MLL5がHCF-1およびSET1と複合体を形成し、アンドロゲン受容体の転写活性をエピジェネティックに制御することで、がん細胞の増殖と治療抵抗性に寄与していることが報告されています。
7. 単純ヘルペスウイルス(HSV-1)によるHCFC1のハイジャック機構
HCFC1がもともと「宿主細胞因子」として同定された経緯は、単純ヘルペスウイルス(HSV-1)の感染研究によります。HSV-1は宿主のHCFC1を巧みに利用することで感染を成立させ、知覚神経節に潜伏感染してから再活性化を繰り返します。
💡 用語解説:単純ヘルペスウイルス(HSV-1)とHCF-1
HSV-1は口唇ヘルペスや角膜ヘルペスの原因ウイルスで、知覚神経節に潜伏感染し定期的に再活性化します。HSV-1はVP16というウイルスタンパク質を用いてHCFC1(HCF-1)に結合し、宿主細胞の核内でウイルス遺伝子の転写を活性化させます。HCFC1はウイルスがいわば「乗っ取る」宿主因子であり、この相互作用の阻害が新たな抗ウイルス戦略となり得ます。
HSV-1が宿主細胞に侵入すると、テグメントタンパク質であるVP16が細胞質内に放出されます。細胞質にプールされているHCFC1は直ちにVP16と結合し、HCF-1/HCFC1R1複合体が分子足場として機能することでVP16を核内へと迅速に輸送します。核内へ到達したVP16/HCF-1複合体は宿主の転写因子Oct-1と結合して巨大な三者複合体を形成し、HSV-1の前初期(IE)遺伝子群(ICP0・ICP4・ICP22・ICP27・ICP47)のプロモーターに存在するTAATGARAT配列に高親和性で結合します。
潜伏感染中、HSVのゲノムには転写を強力に抑制するH3K9me(ヒストンH3K9メチル化)が高密度に蓄積しています。再活性化の際、VP16-HCF-1複合体はプロモーターに結合後、脱メチル化酵素LSD1(KDM1A)およびJMJD2ファミリータンパク質をウイルスゲノム上に動員し、抑制性H3K9meマークを迅速に消去します。これと並行してSet1/MLL1メチルトランスフェラーゼ複合体を動員しH3K4me3を付与することで、「抑制マークの消去」と「活性化マークの付与」という二重のエピジェネティクス・リプログラミングによってウイルスIE遺伝子群の爆発的な転写が引き起こされます。この機序の解明は、アシクロビル耐性HSV株に対する新規抗ウイルス薬開発の糸口を提供しています。
8. 診断と遺伝子検査:どうやってHCFC1変異を見つけるか
HCFC1変異が疑われる場面として最も多いのは、cblC型の生化学所見(メチルマロン酸上昇+高ホモシステイン血症)を示す男児において、MMACHC遺伝子に変異が検出されないというパターンです。また、代謝異常を伴わずに小頭症・知的障害・難治性てんかんを呈する男児も、HCFC1変異の鑑別診断に含まれます。
遺伝子検査の選択肢
🔵 コバラミン関連遺伝子パネル検査
HCFC1・MMACHC・PRDX1・ABCD4などコバラミン代謝に関わる複数の遺伝子を網羅的に解析します。コバラミン・ホモシステイン・メチオニン遺伝子検査をご参照ください。
🟢 メチルマロン酸血症・ホモシスチン尿症パネル
コバラミン代謝異常症に関連する多数の原因遺伝子を一括検査できます。メチルマロン酸血症・ホモシスチン尿症NGSパネルで詳細をご確認いただけます。
🟣 核ミトコンドリア総合NGS検査
より広範な先天性代謝疾患の精査に対応します。核・ミトコンドリア総合NGS遺伝子検査をご覧ください。
変異の解釈においては、Kelchドメイン内の高度保存領域に位置するミスセンス変異であるかどうかの精密な評価が不可欠です。またPRDX1遺伝子の変異によるMMACHCプロモーターの過剰メチル化(エピ変異)もcblC型の原因となるため、HCFC1・MMACHC・PRDX1・ABCD4・MMAB・ACADMなど関連遺伝子も含めた包括的な遺伝子パネルでの解析が推奨されます。
9. 治療戦略:代謝補正から最新のASO療法まで
現在の代謝的アプローチとその限界
現在のcblX症候群に対する第一選択は、cblC型に対するプロトコルを踏襲した代謝的介入です。主軸はヒドロキソコバラミン(OHCbl)の非経口(筋肉内)大量投与で、一般的な推奨開始用量は1日あたり100〜200 mcg、急性期の重症例では体重あたり0.21 mg/kg/dayという極めて高用量が用いられることもあります。これに加えて、ホモシステインの再メチル化経路をバイパス活性化するためのベタインの経口投与や葉酸の補給が併用されます。
⚠️ 重要な限界:これらの集中的な代謝介入により血中MMAやホモシステイン濃度の低下といった生化学的パラメーターの改善はある程度達成されますが、最大の臨床的課題はこの治療法がcblX患者の神経学的アウトカムに対してほとんど効果を示さない点にあります。大脳皮質の形成異常やリボソーム生合成不全は出生前の胎生期から進行している不可逆的な発生障害であるため、出生後のコバラミン補充によって難治性てんかんや重度の認知障害・小頭症といった神経症状の進行を食い止めることは事実上不可能です。
低分子化合物による標的療法(がん・ウイルス感染症)
HCFC1の機能が過剰に亢進している病態では、タンパク質間相互作用や修飾酵素を標的とした低分子化合物の開発が進んでいます。肺がん(NSCLC)において、OGTに対する低分子OGT阻害剤OSMI-1を投与すると、HCFC1の切断・成熟が阻害され、下流のNkx2.1の発現レベルが低下してがん細胞の増殖が強力に抑制されることが前臨床モデルで実証されています。HSV-1感染においては、VP16-HCF-1複合体が動員するLSD1(KDM1A)やJMJD2といったヒストン脱メチル化酵素の触媒活性を特異的な低分子化合物で阻害することにより、ウイルスゲノムの抑制性クロマチンの消去を阻止し感染の成立と再活性化をブロックする戦略が有効性を示しています。
次世代の根本治療:アンチセンスオリゴヌクレオチド(ASO)療法の展望
HCFC1変異に起因する重篤な先天性神経疾患に対する最も革新的なアプローチとして現在期待を集めているのが、アンチセンスオリゴヌクレオチド(ASO)療法です。
💡 用語解説:アンチセンスオリゴヌクレオチド(ASO)とは
標的となるmRNAの特定の配列に相補的に結合するよう設計された短いDNA/RNAハイブリッド分子で、転写後レベルで遺伝子の発現量やスプライシングを精密に修飾します。脊髄性筋萎縮症(SMA)への髄腔内投与(ヌシネルセン)やALS(筋萎縮性側索硬化症)への応用など、中枢神経系への薬物送達の前臨床・臨床実績が積み重なっており、HCFC1関連神経疾患への応用が期待されています。
HCFC1関連疾患において、ASOは以下の2つの異なるメカニズムで応用可能です。
① スプライシング修飾(エクソンスキッピング)
HCFC1の塩基性ドメインを破壊するスプライシング異常変異によって引き起こされるXLID患者に対して、変異によって生じた異常なスプライシング・サイトをASOで立体障害的にマスクし、正常なエクソンの包含を誘導する療法。患者固有の変異に対する「N-of-1(個別化)」療法として実用化が進んでいます。
② 過剰発現のノックダウン
YY1結合サイトの変異によってHCFC1が定常的に過剰発現しているXLIDのケースに対して、ASOを用いて標的mRNAにRNase H依存性の分解を誘導し、HCFC1のタンパク質量を正常レベルまでダウンレギュレートする戦略。肝細胞癌(HCC)を対象としたASO薬の第I相臨床試験でも、肝臓への効率的な送達と優れた安全性・忍容性が確認されており、HCFC1関連肝代謝障害への応用も期待されます。
10. 遺伝カウンセリングと家族へのサポート
HCFC1はX連鎖遺伝子であるため、遺伝形式の理解と家族への情報提供が重要です。
- ➤男児(ヘミ接合体):X染色体を1本しか持たないため、HCFC1に変異があれば必ず発症します。cblX症候群・XLIDともに男児患者が中心です。
- ➤女性保因者(キャリア):X染色体を2本持つため、片方の正常なXが補い、多くは無症状または軽症です。ただしX染色体不活性化パターンによっては、正常なXが主に不活性化された場合に症状を呈することがあります。
- ➤再発リスク:母親が保因者の場合、息子の50%が発症し、娘の50%が保因者となります。父親が患者の場合、娘は全員保因者、息子は全員正常となります。キャリアスクリーニングの詳細はこちら
- ➤保因者診断:罹患男児の母親に対する保因者検査が推奨されます。米国人類遺伝学会(ACMG)および産科婦人科学会(ACOG)のキャリアスクリーニングに関する推奨についてはこちらをご参照ください。
- ➤出生前診断:変異が同定されている場合は、次子妊娠時に絨毛検査・羊水検査による出生前遺伝子診断が可能です。詳細はミネルバクリニックの臨床遺伝専門医にご相談ください。
よくある質問(FAQ)
🏥 HCFC1遺伝子・コバラミン代謝疾患についてご相談ください
cblX症候群・X連鎖性知的障害など先天性遺伝疾患に関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
参考文献
- [1] Yu HC, et al. An X-Linked Cobalamin Disorder Caused by Mutations in Transcriptional Coregulator HCFC1. Am J Hum Genet. 2013;93(3):506-514. [PMC3769968]
- [2] Huang J, et al. A Noncoding, Regulatory Mutation Implicates HCFC1 in Nonsyndromic Intellectual Disability. Am J Hum Genet. 2012;91(4):694-702. [PMC3484651]
- [3] NCBI Gene. HCFC1 host cell factor C1 [Homo sapiens]. Gene ID: 3054. [NCBI Gene]
- [4] Minocha S, et al. The role of HCFC1 in syndromic and non-syndromic intellectual disability. Medical Research Archives. 2021. [PMC8218923]
- [5] Epigenetic modifications in the murine liver upon depletion of HCFC1. PMC. 2025. [PMC12247444]
- [6] Mutations in Hcfc1 and Ronin result in an inborn error of cobalamin metabolism and ribosomopathy. PubMed. 2022. [PMC8748873]
- [7] HCFC1 and YY1 mediate recruitment of COMPASS and Integrator to initiate X chromosome inactivation. bioRxiv. 2025. [bioRxiv 2025]
- [8] Activator–promoter compatibility in mammals: a CpG-Island-specific co-activator directly bridges transcription factors to TFIID. bioRxiv. 2025. [bioRxiv 2025]
- [9] HCF-1 is cleaved in the active site of O-GlcNAc transferase. PMC. 2014. [PMC3930058]
- [10] Upregulation of HCFC1 expression promoted hepatocellular carcinoma progression. PMC. 2023. [PMC10240668]
- [11] Epigenetic co-regulator HCF-1 promotes lung cancer via O-GlcNAcylation-dependent pathways. PMC. 2025. [PMC12475861]
- [12] Missense and nonsense mutations of the zebrafish hcfc1a gene result in contrasting mTor and radial glial phenotypes. PMC. 2024. [PMC11373874]
- [13] The Dynamics of HCF-1 Modulation of Herpes Simplex Virus Chromatin during Initiation of Infection. PMC. 2013. [PMC3712308]
- [14] HCFC1R1 Deficiency Blocks Herpes Simplex Virus-1 Infection by Inhibiting Nuclear Translocation of HCFC1 and VP16. bioRxiv. 2020. [bioRxiv]
- [15] HCFC1 gene. MedlinePlus Genetics. [MedlinePlus]