目次
📍 クイックナビゲーション
PPP1R(プロテインホスファターゼ1制御サブユニット)は、細胞内のあらゆる生命活動を支える「脱リン酸化スイッチ」を精密にコントロールする200種類以上の遺伝子群です。心臓のリズム・脳の発達・血糖の調節・がんの進展まで、私たちの体の根幹に関わるこの遺伝子群について、最新のエビデンスをもとに臨床遺伝専門医がやさしく解説します。
Q. PPP1Rとは何ですか?まず結論だけ知りたいです
A. プロテインホスファターゼ1(PP1)という酵素に結合して、その働き場所と相手を決定する「指揮者」役の遺伝子群です。PP1は単独では基質を選べないため、200種類以上のPPP1Rがそれぞれ異なる場所・タイミングで結合し、細胞内の脱リン酸化反応の約80%を精密に制御しています。
- ➤遺伝子群の規模 → 200種類以上のメンバーが固有の機能を担う巨大ファミリー
- ➤分子メカニズム → RVxFモチーフによるPP1への係留と「立体障害」による基質選択
- ➤主要ファミリー → GADD34(ストレス応答)・MYPT1(平滑筋)・PNUTS(核内)など
- ➤関連疾患 → 心房細動・UBMS症候群・神経変性疾患・がんの進展
- ➤最新の創薬 → Sephin1・PhosTAC技術による精密医療への展望
1. PPP1Rとは:細胞内の「脱リン酸化スイッチ」を制御する巨大遺伝子群
私たちの体を構成する細胞の中では、毎瞬間、無数のタンパク質が「リン酸化」と「脱リン酸化」を繰り返しています。これは細胞内で最も普遍的なスイッチング機構であり、細胞分裂・記憶・筋収縮・血糖の調節・ストレス応答・免疫など、生命活動のほぼすべてがこの仕組みに依存しています。
💡 用語解説:リン酸化と脱リン酸化
リン酸化とは、タンパク質の特定のアミノ酸(セリン・スレオニン・チロシン)にリン酸基(−PO₃²⁻)を付ける反応のこと。スイッチを「オン」にしたり「オフ」にしたりする働きを担います。これを担うのがキナーゼ(リン酸化酵素)。逆にリン酸基を取り除く「脱リン酸化」を行うのがホスファターゼ(脱リン酸化酵素)です。両者の動的なバランスが崩れると、がん・心疾患・神経変性疾患などが引き起こされます。
ヒトのゲノムには約500種類のキナーゼがある一方で、セリン/スレオニン残基を脱リン酸化するホスファターゼ遺伝子は40種類未満しか存在しません。この圧倒的な数の不均衡があるにもかかわらず、ホスファターゼがキナーゼと同等以上の精密な特異性を発揮できる理由——それこそがPPP1R(プロテインホスファターゼ1制御サブユニット)という200種類以上の遺伝子群の存在です。
💡 用語解説:プロテインホスファターゼ1(PP1)
真核生物の細胞内で起こるセリン/スレオニン脱リン酸化反応の約80%を単独で担う主要酵素です。ヒトには3つの遺伝子(PPP1CA、PPP1CB、PPP1CC)が存在し、PP1α・PP1β/δ・PP1γ1・PP1γ2の4つのアイソフォームを生み出します。アミノ酸配列の同一性は85〜93%と非常に高いものの、それぞれ異なる細胞内局在を示します。
ここで重要なのは、PP1という酵素は単独では「どのタンパク質を脱リン酸化すべきか」を選べないということです。PP1の触媒部位は基質特異性に乏しく、これだけでは細胞のシグナル伝達を精密に制御することは到底不可能です。そこで登場するのがPPP1R——PP1に結合して「いつ・どこで・誰を」脱リン酸化するかを決定する制御サブユニット群です。
200種類以上のメンバーが固有の機能を担う
PPP1Rファミリーは、HGNC(HUGO Gene Nomenclature Committee)によって正式に分類された巨大な遺伝子グループです。代表的なメンバーには、ストレス応答を司るGADD34(PPP1R15A)、平滑筋収縮を制御するMYPT1(PPP1R12A)、核内で転写を制御するPNUTS(PPP1R10)、神経シグナルの主役DARPP-32(PPP1R1B)、糖代謝を支配するPPP1R3ファミリーなどが含まれます。それぞれが独自の細胞内局在・基質選択性・上流シグナルへの応答性を持ち、PP1という共通の触媒エンジンを使って多様な生命活動を制御しています。
2. PP1ホロ酵素の仕組み:触媒サブユニットと制御サブユニットのペア
PPP1Rを正しく理解するためには、「ホロ酵素」という概念が欠かせません。PP1は細胞内において遊離の触媒サブユニットとして存在することはなく、常に1つ以上のPPP1Rと結合してホロ酵素を形成しています。
💡 用語解説:ホロ酵素(Holoenzyme)
「触媒能力を持つ酵素本体(PP1)」と「機能を制御する補助タンパク質(PPP1R)」が結合した機能的に完結した複合体のことです。PP1単体ではエンジンを積んだだけの車のようなもの——どこへ走るかを決められません。PPP1Rが結合して初めて「目的地と運転手」が決まり、特定のタンパク質を狙って脱リン酸化できるようになります。
なぜ「組み合わせ」がここまで重要なのか
PP1のアイソフォームは4種類、PPP1Rは200種類以上。理論上は800以上の異なるホロ酵素の組み合わせが成立します。これが「数の少ないホスファターゼがキナーゼ並みの精密制御を実現できる」秘密です。組み合わせの数だけ、異なる細胞内タスクをこなせるわけです。
💡 PP1アイソフォームの細胞内局在の違い
- ➤PP1α:核マトリックス・有糸分裂期は中心体に局在
- ➤PP1γ1:核小体・有糸分裂期は紡錘体微小管に局在
- ➤PP1δ(PP1β):クロマチン全体・有糸分裂期は染色体に局在
- ➤PP1γ2:精巣特異的に発現
3. レギュラトリーコード:RVxFモチーフと立体障害による基質選択
PPP1RがどのようにしてPP1に結合し、特異的な基質を選び出すのか——その分子メカニズムを「レギュラトリーコード」と呼びます。これは細胞内で起こる生化学反応の中でも特に精緻なシステムで、複数のドッキングモチーフ(短い結合配列)が組み合わされて機能します。
RVxFモチーフ:すべてのPPP1Rに共通する係留装置
💡 用語解説:RVxFモチーフ
PPP1RがPP1に結合するために使う4文字の短いアミノ酸配列(R=アルギニン、V=バリン、x=任意のアミノ酸、F=フェニルアラニン)です。既知の約189種類のPPP1Rのうち162種類がこのモチーフを持っており、PP1の活性部位から約20オングストローム離れた疎水性ポケットに結合します。この結合自体はPP1の酵素活性を変化させず、単に「制御サブユニットをPP1に錨で固定する」役割のみを担います。一度に1つのPPP1RしかRVxFポケットに入れないため、相互排他的な結合となります。
RVxFモチーフに加えて、SILKモチーフ(−ILK配列)やMyPhoNEモチーフなどの二次的なドッキング配列も同定されています。これらの追加モチーフは結合親和性を高めるだけでなく、PP1のアイソフォーム特異性(α・β・γへの選り好み)を生み出します。
立体障害(Steric Occlusion)による基質選択
PPP1Rが基質特異性を生み出す最も独創的な方法が、「立体障害」と呼ばれるメカニズムです。多くの制御サブユニットは、PP1の活性部位そのものを直接阻害するのではなく、活性部位の周囲にある「基質結合溝」を物理的に塞ぐことで、特定の基質の接近を阻みます。
💡 用語解説:立体障害(Steric Occlusion)
物理的に「邪魔者」が入ることで、特定の分子がアクセスできなくなる現象です。PP1の活性部位は開いたままなのに、PPP1Rが特定の方向の溝をふさぐことで「この基質は通れない、こちらの基質ならOK」という選別ゲートとして機能します。スピノフィリン(PPP1R9B)はC末端側の基質結合溝を塞ぎ、PNUTS(PPP1R10)はアルギニン部位を隠蔽することで、それぞれ独自の基質選択性を生み出しています。
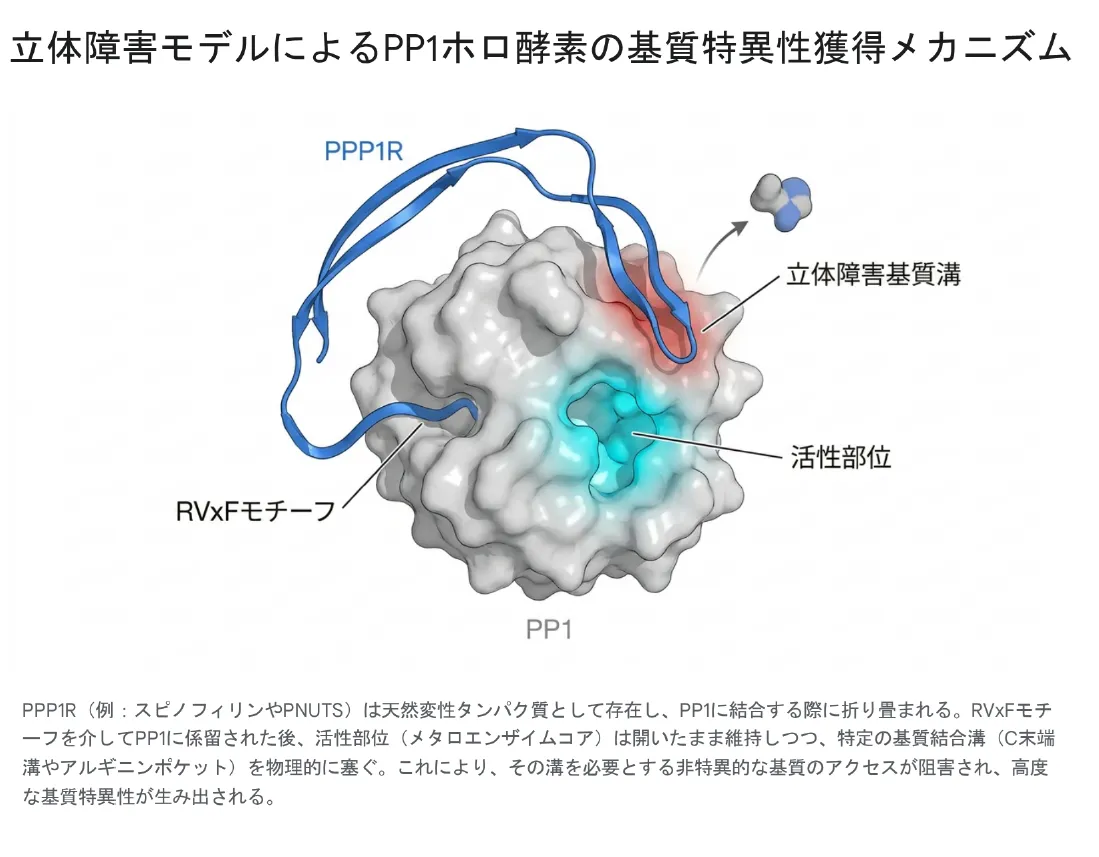
PPP1R(例:スピノフィリンやPNUTS)は天然変性タンパク質として存在し、PP1に結合する際に折り畳まれる。RVxFモチーフを介してPP1に係留された後、活性部位(メタロエンザイムコア)は開いたまま維持しつつ、特定の基質結合溝(C末端溝やアルギニンポケット)を物理的に塞ぐ。これにより、その溝を必要とする非特異的な基質のアクセスが阻害され、高度な基質特異性が生み出される。
💡 用語解説:天然変性タンパク質(IDP)
「Intrinsically Disordered Proteins」の略で、単独では決まった立体構造を持たないタンパク質のこと。多くのPPP1Rがこのタイプで、PP1に結合する瞬間に必要な形へ折り畳まれます(Folding-upon-binding)。この柔軟性こそが、PP1の広い表面に対して複数箇所で同時に結合し、高度に多様で精密な制御ネットワークを構築する基盤となっています。
4. PPP1Rファミリーの主要メンバーと機能
PPP1Rは機能的に大きく3つに分類されます——阻害型(PP1の活性を抑制)・標的化型(PP1を特定の場所へ連れて行く)・足場型(複数の分子を組み立てる)。以下では特に重要なメンバーを紹介します。
🧠 神経シグナルの司令塔
- DARPP-32(PPP1R1B):ドーパミン・cAMPで活性化される神経系の主要スイッチ
- スピノフィリン(PPP1R9B):シナプスの足場、アクチン骨格制御
- Inhibitor-1(PPP1R1A):キナーゼ応答性の強力なPP1阻害因子
💪 筋収縮の制御
- MYPT1(PPP1R12A):ミオシン軽鎖の脱リン酸化、平滑筋弛緩
- CPI-17(PPP1R14A):PKC応答性、平滑筋収縮の促進
- PPP1R12C:心房ミオシン軽鎖の脱リン酸化、心房収縮力制御
🧬 核内・転写制御
- PNUTS(PPP1R10):RNAポリメラーゼII制御、Rb・MYC安定性
- NIPP1(PPP1R8):核内PP1阻害、有糸分裂チェックポイント
- sds22(PPP1R7):核内PP1活性の主要制御因子
⚡ ストレス・代謝
- GADD34(PPP1R15A):統合的ストレス応答、eIF2α脱リン酸化
- PPP1R3ファミリー:グリコーゲン代謝の組織特異的制御
- PHI-1(PPP1R14B):リン酸化依存的PP1阻害、がん関連
統合的ストレス応答の主役:GADD34(PPP1R15A)
細胞がDNA損傷・小胞体ストレス・酸化ストレス・ウイルス感染などに直面すると、まず翻訳開始因子eIF2αがリン酸化されてタンパク質合成が一時停止します。これが統合的ストレス応答(ISR)です。GADD34は、このストレスが解除された段階でPP1をeIF2αに連れて行き、脱リン酸化することでタンパク質合成を再開させる「再起動スイッチ」として機能します。
💡 用語解説:統合的ストレス応答(ISR)
細胞が様々なストレスに直面したときに発動する共通の防衛プログラムです。eIF2αのリン酸化によって全体のタンパク質合成を急停止させ、ATF4などのストレス応答遺伝子だけを優先的に翻訳します。GADD34はこのISRを終結させるブレーキ役で、過剰な活性化はALS・シャルコー・マリー・トゥース病などの神経変性疾患に関与します。
糖代謝を支配するPPP1R3ファミリー
血糖値の変動に応じてグリコーゲンを合成・分解する反応は、PPP1R3A〜PPP1R3Gと呼ばれる7つのサブユニットによって組織特異的に制御されています。それぞれが異なる組織で発現し、絶食時と摂食時で発現量が逆転するという興味深いダイナミクスを示します。
📊 PPP1R3ファミリーの肝臓における発現ダイナミクス
PPP1R3Gの絶食時上昇は、食後血糖値の急速な感知と肝グリコーゲン合成の即時開始に必要なスタンバイ機構として機能している。
5. PPP1Rの異常と関連疾患
PPP1Rの発現異常や遺伝子変異は、心血管・神経・発生・代謝・がんなど多領域の疾患と関連します。マウスを用いたリバースジェネティクス研究により、少なくとも49種類のPPP1Rがヒト疾患関連表現型と直接結びついていることが証明されています。
心房細動(AF):PPP1R3AとPPP1R12Cの異常
心房細動は最も一般的な持続性不整脈で、血栓塞栓性脳卒中のリスクを5倍に高める深刻な疾患です。最新の分子心臓学研究により、複数のPPP1Rサブユニットの異常が心房細動の病態形成に決定的な役割を果たしていることが明らかになっています。
PPP1R3Aの発現低下
心筋細胞の筋小胞体において、PP1cをリアノジン受容体(RyR2)とホスホランバン(PLN)の近傍に固定する足場として機能。発作性および慢性心房細動患者で進行性に発現低下します。
結果としてRyR2とPLNの過剰リン酸化、SRからのCa²⁺漏出が起こり、ペーシング誘発性心房細動への感受性が亢進します。
PPP1R12Cの発現上昇
心房細動患者の右心房組織で発現が2倍に増加。心房ミオシン軽鎖2(MLC2a)の脱リン酸化を促進し、心房の収縮力低下を引き起こします。
マウスモデルでは、PPP1R12Cの心筋特異的過剰発現により左房サイズが150%増大し、心房ストレイン低下とAF誘発性亢進が確認されています。
UBMS症候群:PPP1R12A(MYPT1)の機能喪失
PPP1R12A(MYPT1)の生殖細胞系列におけるde novo変異は、泌尿生殖器および脳奇形症候群(UBMS:Urogenital and/or Brain Malformation Syndrome)を引き起こします。常染色体顕性遺伝の希少疾患で、ハプロ不全(タンパク質量の半減)が病態の根幹にあります。
💡 用語解説:de novo(デノボ)変異とハプロ不全
de novo変異とは両親には存在せず、子どもで初めて生じた新生変異のこと。ハプロ不全とは、2本ある染色体のうち1本の遺伝子が機能を失うことでタンパク質の量が半分になり、それが症状を引き起こす状態のことです。UBMSでは親が健康でも子どもに発症するため、家族歴がないケースが多いのが特徴です。
📊 PPP1R12A(UBMS症候群)の主な臨床症状と発生頻度
PPP1R12Aの機能喪失変異では、脳構造異常(特に脳梁低形成)と筋緊張低下が極めて高頻度に観察され、このサブユニットが初期の神経発生と筋発達において不可欠であることを示す。46,XYの患者ではミュラー管退縮不全による性分化疾患(DSD)も発症する。
神経変性疾患:アルツハイマー・パーキンソン・虚血性脳損傷
アルツハイマー病患者の脳では、PP1とPP2Aの活性が顕著に低下しており、これがタウタンパク質の過剰リン酸化と神経原線維変化(NFTs)の形成を促進する主要因子となっています。パーキンソン病については、2024年にLag3とAplp1の相互作用がα-シヌクレインの病的伝播を駆動することが特定され、がん免疫療法薬の転用による治療パラダイムが提示されました。虚血性脳卒中ではPPP1R17(GSBS)がYAP1を介してマイトファジーを抑制し、神経細胞ダメージを増悪させることが明らかにされています。
がんの進展・浸潤・薬剤耐性
PPP1Rの異常発現は、腫瘍血管新生・薬剤耐性・浸潤転移といったがんの悪性形質形成に深く関与します。代表例として、PHI-1(PPP1R14B)は多くのがん種で過剰発現し、発がんシグナルを活性化し腫瘍促進タンパク質を安定化させます。PPP1R14Dは肺腺癌(LUAD)で疾患進行・予後不良と強く相関し、PKCα/BRAF/MEK/ERKカスケードを介して細胞増殖と浸潤を促進します。
大腸がんなどの消化器悪性腫瘍においても、PP1ホロ酵素のシグナル伝達異常が腫瘍微小環境の制御に関与しており、遺伝性大腸がんの病態理解にも示唆を与えています。APC遺伝子関連疾患である家族性大腸腺腫症(FAP)、減弱型FAP(AFAP)、ガードナー症候群、ターコット症候群、胃腺癌・近位胃ポリポーシス症候群(GAPPS)、遺伝性デスモイド病、体細胞性肝芽腫などの腫瘍では、Wnt/β-カテニン経路を含む多層的なリン酸化制御の破綻が発がんの根幹に関与しており、PPP1Rを介した脱リン酸化制御もその文脈で重要視されています。
独創的な治療戦略として、NIPP1(PPP1R8)の過剰発現によりPP1を他の結合タンパク質から「奪い取る」(滴定効果)ことで、がん細胞を有糸分裂停止に追い込みアポトーシスを誘導する手法も研究されています。
6. 最新の標的治療:PPP1Rを狙う精密医療
長年にわたり、プロテインホスファターゼは「創薬の標的に適さない(undruggable)」と考えられてきました。PP1の触媒部位は深い窪みを持たず、強い正電荷を帯びているため低分子化合物の結合が困難だったからです。しかし、PPP1Rとのホロ酵素形成という発想の転換が、創薬の風景を一変させています。
Sephin1とGuanabenz:制御サブユニットを狙うアロステリック薬
PP1の活性部位ではなく、制御サブユニットPPP1R15A(GADD34)に結合してその立体構造を変化させる低分子化合物——それがGuanabenzとSephin1です。これらは「アロステリックモジュレーター」として機能し、R15A-PP1ホロ酵素がeIF2αをリクルートできなくします。結果として細胞は統合的ストレス応答(ISR)を長期間維持し、タンパク質フォールディング異常から保護されます。
💡 用語解説:アロステリックモジュレーター
酵素の活性部位(実際に化学反応が起こる場所)ではなく、それとは離れた別の場所に結合して、酵素全体の形を変化させる薬剤のことです。Sephin1はPP1ではなくPPP1R15Aに結合するため、他のPP1ホロ酵素には影響を与えず、副作用を最小限に抑えながらストレス応答経路だけを精密にコントロールできます。
マウスモデルでは、Sephin1はシャルコー・マリー・トゥース病(CMT-1B)やSOD1変異型筋萎縮性側索硬化症(ALS)などの神経変性疾患の進行を効果的に防止することが確認されました。これは「PPP1Rが極めて有効かつ安全性の高い創薬標的」であることを決定づけた歴史的な発見です。
PhosTAC技術:標的タンパク質を狙い撃ちで脱リン酸化する革新
💡 用語解説:PhosTAC(Phosphorylation Targeting Chimera)
2024年に登場した革新的な創薬技術です。標的タンパク質分解を誘導するPROTACの概念を脱リン酸化に応用し、任意のタンパク質の特定のリン酸化部位だけを狙って脱リン酸化することができます。極めて高い親和性でPP1に結合する人工ペプチド(PhosTAP)を使い、PP1を任意の標的タンパク質の近傍に強制的にリクルートする仕組みです。キナーゼ阻害剤を使わずにシグナル伝達を精密にモジュレートできるため、薬剤耐性克服や副作用低減への応用が期待されます。
PhosTAC技術によって、これまでのホスファターゼ生物学の定説を覆す発見も次々と報告されています。多くのPPP1Rが単なる足場や阻害因子ではなく、PP1自身の脱リン酸化基質でもあること、PP1が有糸分裂キナーゼと直接拮抗してHaspinキナーゼを脱リン酸化することなど、PPP1Rネットワークの新たな顔が明らかになっています。
7. PPP1R関連疾患の遺伝子検査と遺伝カウンセリング
PPP1Rファミリーの遺伝子変異が関与する疾患は多岐にわたるため、単一遺伝子検査ではなく包括的な解析手法が推奨されます。特にUBMS症候群やNSLH2のような多発奇形症候群では、トリオ全エクソーム解析(Trio-WES)が診断の中心です。
🧬 全エクソーム解析(WES)
タンパク質コード領域全体を網羅。両親も含めたトリオ解析でde novo変異を確実に検出。原因不明の多発奇形症候群や知的障害の精密診断に第一選択。
🩸 血栓性疾患パネル
凝固制御に関わる遺伝子群を網羅。PP1関連シグナルが関与する血小板機能・血管内皮機能異常の評価に有用。
🧠 てんかん包括パネル
UBMSなどPPP1R変異関連疾患でも高頻度(約51%)に発症するてんかんの原因遺伝子を網羅的に検査。
🤰 単一遺伝子疾患の出生前診断
家族内で既知の変異が同定されている場合、絨毛検査・羊水検査による胎児の遺伝子診断が可能。
遺伝カウンセリングのポイント
PPP1R関連疾患の多くは常染色体顕性遺伝を示し、UBMS症候群のように生殖細胞モザイクの理論的可能性から再発リスクが約1%程度と見積もられるケースもあります。確定診断後の家族への説明では、以下の項目が重要です:
- ➤遺伝形式と再発リスク:de novo変異が大多数だが、患者本人の挙児希望時には50%の遺伝確率を考慮。
- ➤キャリアスクリーニング:キャリアスクリーニング検査による潜性遺伝疾患の保因者確認も、挙児前の重要な選択肢。
- ➤米国基準のガイドライン:米国人類遺伝学会(ACMG)が推奨するキャリアスクリーニングに基づく包括的アプローチ。
- ➤出生前診断:単一遺伝子疾患の出生前診断により、次子妊娠時の確実な診断が可能。
希少遺伝性疾患を抱えるご家族の体験談として、副腎白質ジストロフィー保因者検査を受けた姉妹の経験や、ALDと家族計画における選択肢もぜひ参考にしてください。同様の遺伝学的相談プロセスがPPP1R関連疾患でも適用されます。
8. よくある誤解
誤解①「ホスファターゼは特異性がない」
かつての教科書の記述は誤りでした。PPP1Rが200種類以上存在することで、PP1ホロ酵素はキナーゼと同等以上の精密な基質特異性を発揮します。「組み合わせ」が特異性を生む独自のシステムです。
誤解②「PP1阻害=ホスファターゼ全体の阻害」
特定のPP1ホロ酵素だけを狙うことが可能です。Sephin1がPPP1R15Aだけを狙って他のPP1機能には影響を与えないように、PPP1R特異的な薬剤設計により副作用を最小化できます。
誤解③「PPP1R変異は希少だから関係ない」
UBMS症候群のような単一遺伝子疾患は確かに希少ですが、PPP1Rの発現異常は心房細動・がん・神経変性疾患など、頻度の高い疾患の病態に深く関与しています。
誤解④「ホスファターゼは創薬できない」
2010年代までの常識でしたが、PPP1Rを標的としたアロステリックモジュレーターやPhosTAC技術の登場により、ホスファターゼ系薬剤の開発は急速に現実化しています。
9. 臨床遺伝専門医からのメッセージ
よくある質問(FAQ)
🏥 希少疾患の診断・遺伝カウンセリングについて
PPP1R関連疾患をはじめとする希少遺伝性疾患・多発奇形症候群に関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
関連記事
参考文献
- [1] HGNC. Gene group: Protein phosphatase 1 regulatory subunits (PPP1R). [HGNC]
- [2] Bollen M, et al. The extended PP1 toolkit: designed to create specificity. Trends Biochem Sci. 2010;35(8):450-458. [PMC3131691]
- [3] Choy MS, et al. Understanding the antagonism of retinoblastoma protein dephosphorylation by PNUTS provides insights into the PP1 regulatory code. PNAS. 2014. [PNAS]
- [4] Heroes E, et al. Structural Basis for Protein Phosphatase 1 Regulation and Specificity. FEBS J. 2013. [PMC3350600]
- [5] Korrodi-Gregório L, et al. Protein phosphatase 1 catalytic isoforms: specificity toward interacting proteins. Transl Res. 2014. [PMC7114192]
- [6] Alsina FC, et al. PPP1R12C Promotes Atrial Hypocontractility in Atrial Fibrillation. Circ Res. 2024. [Circ Res]
- [7] Reiken S, et al. Loss of Protein Phosphatase 1 Regulatory Subunit PPP1R3A Promotes Atrial Fibrillation. Circulation. 2019. [PMC6699925]
- [8] Hauser AS, et al. PPP1R12A-Related Urogenital and/or Brain Malformation Syndrome. GeneReviews. 2021. [GeneReviews NBK573670]
- [9] Das R, et al. A protein phosphatase 1 specific phosphatase targeting peptide (PhosTAP) to identify the PP1 phosphatome. PNAS. 2024. [PNAS 2024]
- [10] Das I, et al. Preventing proteostasis diseases by selective inhibition of a phosphatase regulatory subunit (Sephin1). Science. 2015. [ACS Central Science]
- [11] Wang Y, et al. Rediscovery of PHI-1/PPP1R14B: Emerging Roles of Cellular PP1 Signaling in Multiple Cancers. Front Oncol. 2025. [PMC11939891]
- [12] Luo Y, et al. Fasting-Induced Protein Phosphatase 1 Regulatory Subunit Contributes to Postprandial Blood Glucose Homeostasis (PPP1R3G). Diabetes. 2011. [PMC3292316]
- [13] Foley K, et al. Protein Phosphatase 1 Regulatory Subunit 17 (PPP1R17) Regulates Cerebral Ischemia. Mol Neurobiol. 2025. [ResearchGate]
- [14] Mahmood T, et al. Molecular Role of Protein Phosphatases in Alzheimer’s and Other Neurodegenerative Diseases. Int J Mol Sci. 2024. [PMC11117500]
- [15] McConnell JL, Wadzinski BE. Targeting Protein Serine/Threonine Phosphatases for Drug Development. Mol Pharmacol. 2009;75(6):1249-1261. [ACS Chemical Biology]