目次
本記事では、「ゲノム病」という用語を中心に、その原因、診断、治療法に関する最新の研究成果と医療技術の進展を紹介します。ゲノム解析技術の発展からゲノム病の特定、予防、そして治療に至るまでの過程を、病理学の視点を交えながら詳細に解説し、医療現場での応用例を通じてその有用性を探ります。
第1章: ゲノム病の基本概念
ゲノム病とは何か:定義と概要
ゲノム疾患は、染色体またはDNAの物質的な損失や獲得、すなわちコピー数変動(copy number variations;CNV)に起因する疾患を指します。これらの変動は、遺伝子のコピー数に異常が生じることで、個体の発達や健康状態に影響を与えます。ゲノム疾患は、その発生メカニズムに基づいて、主に欠失症候性(コピー数の減少)と重複症候性(コピー数の増加)の2つのカテゴリーに分類されます。
●欠失症候性ゲノム疾患
欠失症候性ゲノム疾患は、遺伝子のコピー数が通常より少ない状態によって引き起こされます。このタイプの疾患では、特定のDNAセグメントが欠けているため、その遺伝子がコードするタンパク質の正常な生産が妨げられます。この結果、体の発達や機能に必要な過程が正常に行われなくなり、さまざまな健康問題が発生します。例えば、ウィリアムズ症候群は7番染色体の特定の領域が欠失することで引き起こされる欠失症候性のゲノム疾患です。
●重複症候性ゲノム疾患
一方、重複症候性ゲノム疾患は、特定の遺伝子のコピー数が増加することによって生じます。この増加により、関連する遺伝子製品が過剰に生産され、体の調節機構が乱れることがあります。これもまた、発達上の遅れや健康上の問題を引き起こす可能性があります。例えば、いくつかの神経発達障害は、特定の遺伝子のコピー数が異常に増加することによって引き起こされると考えられています。
ゲノム病に対する理解の深化と技術の進歩により、将来的にはより効果的な診断方法と治療法が開発されることが期待されています。
ゲノム病の原因:遺伝子変異とその影響
ゲノム病の原因は主に遺伝子変異によるものです。遺伝子変異とは、DNA配列に生じる変更のことを指し、これが細胞の機能に影響を及ぼし、最終的には病気の原因となり得ます。遺伝子変異はさまざまな形で起こり得ますが、主なタイプには以下のようなものがあります。
●点変異: DNA配列の単一塩基が別の塩基に置換される変異。小さな変更ですが、タンパク質の機能に重大な影響を及ぼすことがあります。
●挿入および欠失: DNA配列に一つ以上の塩基が追加されたり、欠けたりする変異。これにより、タンパク質の構造が大きく変わることがあります。
●重複: DNA配列の一部が一回以上余計に複製される変異。タンパク質の過剰な生産や機能不全を引き起こす可能性があります。
●転座: 染色体の一部が別の場所に移動する変異。遺伝子の発現調節に影響を及ぼし、疾患を引き起こすことがあります。
これらの遺伝子変異は、細胞分裂の過程での誤り、外部からの放射線や化学物質の影響、あるいはウイルスの感染などによって生じることがあります。また、遺伝子変異は親から子へ遺伝することもあります。
遺伝子変異によって引き起こされるゲノム病の影響は非常に多岐にわたります。例えば、システィック・フィブローシス、サルコイドーシス、ハンチントン病などがあり、これらの病気は特定の遺伝子変異によって引き起こされます。症状は軽度から重度までさまざまで、影響を受ける遺伝子や体系、そして個人の遺伝的背景によって異なります。
遺伝子変異の影響を理解することは、ゲノム病の診断、治療、予防において非常に重要です。近年のゲノム編集技術の進歩により、遺伝子変異に基づく病気の治療法が開発されつつあります。これにはCRISPR-Cas9などの技術が用いられ、特定の遺伝子変異を正確に修復することが可能になりつつあります。
ゲノム解析技術の役割
ゲノム病におけるゲノム解析技術の役割について説明します。
ゲノム解析技術は、遺伝子の変異や異常が原因で起こるゲノム病の診断、治療、予防において重要な役割を果たしています。ここでは、その主な役割をいくつか紹介します。
1. 疾患の診断
ゲノム解析技術を用いることで、個々の患者のDNA配列を詳細に調べ、特定の遺伝子変異を同定することができます。これにより、多くの遺伝性疾患やゲノム病の正確な診断が可能になります。例えば、システム生物学的アプローチを用いた全ゲノムシークエンシングは、希少疾患や未診断疾患の原因遺伝子を特定するのに有効です。
2. パーソナライズドメディシン
患者固有のゲノム情報を基にしたパーソナライズドメディシンの実現には、ゲノム解析技術が不可欠です。特定の遺伝子変異に基づいて、最も効果的な治療法や薬剤を選択することができます。例えば、特定のゲノム変異を持つがん患者に対して、特定の標的療法薬を選択することがあります。
3. リスク評価と予防
遺伝子検査により、特定の疾患に対する遺伝的なリスクを評価することができます。これにより、リスクが高い個人に対して予防的な措置を講じることが可能になります。例えば、BRCA1やBRCA2の変異を持つ女性は乳がんや卵巣がんのリスクが高く、定期的なスクリーニングや予防的手術の選択が可能です。
4. 新しい治療法の開発
ゲノム解析技術は、疾患の根本的な原因を理解し、新しい治療法や薬剤の開発に寄与しています。遺伝子療法やCRISPR/Cas9などのゲノム編集技術は、特定の遺伝子変異を直接修正することで疾患を治療するアプローチを提供します。
5. 疫学研究
ゲノム解析技術は、疫学研究においても重要な役割を果たしています。大規模なゲノムデータを解析することで、特定の疾患の発生に関与する遺伝的要因や環境要因の相互作用を理解することができます。
ゲノム解析技術は、これらの役割を通じて、ゲノム病の診断、治療、予防に革命をもたらしています。この技術の進展により、より効率的で精度の高い医療の提供が可能になっています。
第2章: ゲノム病の診断と病理学的研究
ゲノム解析による病気の早期発見
ゲノム解析は、ゲノム病の早期発見において重要な役割を果たしています。この技術により、疾患を引き起こす可能性のある遺伝子の変異やコピー数変動(CNVs)を精密に特定し、病気の予防や早期治療につなげることが可能になります。
●ゲノム解析のプロセス
ゲノム解析では、個人のDNAサンプルから遺伝情報を抽出し、全ゲノム配列解析(WGS)や全エクソーム配列解析(WES)などの手法を用いて、ゲノム全体または特定の遺伝子領域の配列を決定します。このデータから、正常な配列と比較して、変異やコピー数変動が検出されます。
●早期発見の重要性
ゲノム病の多くは、遺伝的な要因によって生じるため、生まれつきのリスクを持っています。ゲノム解析による早期発見は、以下の点で特に重要です。
予防とリスク管理: 特定の遺伝子変異の存在を知ることで、その人が将来、特定のゲノム病を発症するリスクが高いかどうかを評価できます。この情報をもとに、ライフスタイルの変更や予防策を講じることが可能です。
早期介入: 病気が発症する前や初期段階での治療を開始することで、病気の進行を遅らせたり、重症化を防いだりすることができます。
個別化医療: 個々の遺伝的背景に基づいた治療計画を立てることで、より効果的で副作用の少ない治療が可能になります。
●ゲノム解析の応用例
新生児スクリーニング: 新生児の段階でゲノム解析を行い、生まれつきの代謝異常や遺伝性疾患のリスクを評価します。
がんリスクの評価: BRCA1やBRCA2など、特定のがんのリスクが高まる遺伝子変異のスクリーニングを通じて、がんの早期発見や予防策を講じます。
家族性遺伝病のリスク評価: 家族歴から遺伝性のリスクを持つ個人に対して、遺伝カウンセリングとともにゲノム解析を提供します。
ゲノム解析技術の発展と普及により、ゲノム病の早期発見と予防がより実現可能になり、個々の健康管理と医療の質の向上に大きく貢献しています。
病理学におけるゲノム病の分類と研究
病理学におけるゲノム病の分類と研究は、疾患の原因を遺伝子レベルで理解し、それに基づいた治療法や診断法を開発することを目的としています。ゲノム病は遺伝子の変異によって引き起こされるため、その性質上、分類と研究は複雑で幅広いアプローチが必要です。ここでは、ゲノム病の分類とその研究方法について概説します。
ゲノム病の分類
ゲノム病は、その遺伝子変異の型や疾患の表現型に基づいて分類されます。主な分類は以下の通りです。
単一遺伝子疾患 (モノジェニック疾患): 一つの遺伝子の変異によって引き起こされる疾患。例えば、システィック・フィブローシスやハンチントン病などがこれに該当します。
多因子遺伝疾患 (ポリジェニック疾患): 複数の遺伝子の変異と環境因子が組み合わさって発症する疾患。例えば、心疾患、糖尿病、多くのがんの種類などがこれに含まれます。
染色体異常: 染色体の構造や数の変化によって引き起こされる疾患。ダウン症候群やターナー症候群などが例として挙げられます。
ミトコンドリア遺伝疾患: ミトコンドリアDNAの変異によって引き起こされる疾患。これらは主にエネルギー産生に関わる細胞機能に影響を及ぼします。
ゲノム病の研究方法
ゲノム病の研究には多様な方法があり、これらは疾患の原因の解明、診断、治療に貢献しています。
ゲノムシーケンシング: 高度なシーケンシング技術を用いて、個人の全ゲノムまたは特定の遺伝子領域を解析し、変異を特定します。これにより、疾患関連遺伝子の同定が可能になります。
バイオインフォマティクス: 大量の遺伝情報を解析し、疾患関連の遺伝子変異やパターンを特定するためのコンピューター技術。
機能ゲノミクス: 遺伝子変異が細胞や生物の機能にどのように影響するかを研究するアプローチ。CRISPR-Cas9などのゲノム編集技術がこの分野の研究を加速させています。
表現型解析: 遺伝子変異と疾患の臨床的表現型との関係を研究する方法。このアプローチは、特定の遺伝子変異がどのように疾患の特定の症状を引き起こすかを理解するのに役立ちます。
遺伝子治療: 遺伝子変異を正すために、正常な遺伝子を患者の細胞に導入する研究。一部のゲノム病に対する治療法として実際に使用されています。
これらの研究方法は、ゲノム病の理解を深め、より効果的な治療法の開発に繋がる可能性を秘めています。病理学におけるゲノム病の研究は、個別化医療への道を開く重要なステップとなっています。
ケーススタディ:特定のゲノム病の病理学的分析
嚢胞性線維症
嚢胞性線維症(システィック・ファイブローシス、CF)の病理学的分析について再度説明します。嚢胞性線維症は、CFTR(Cystic Fibrosis Transmembrane Conductance Regulator)遺伝子の変異によって引き起こされる遺伝性の疾患です。この疾患は、特に肺や消化器系に影響を及ぼし、粘液の過剰な粘度と生産が特徴です。
●疾患概要
嚢胞性線維症は、体内の塩分輸送メカニズムに関わるCFTR遺伝子の変異により発症します。この変異により、体の外に分泌される液体が通常よりも粘り気があり、気道や消化管などが詰まりやすくなります。これが慢性的な呼吸器感染症や消化不良を引き起こし、長期的には肺や膵臓などの器官に損傷を与える原因となります。
●病理学的分析
遺伝子変異の同定:嚢胞性線維症の診断には、CFTR遺伝子の変異を特定することが重要です。エクソームシークエンシングやターゲットシークエンシングなどのゲノム解析技術が、このプロセスに利用されます。
●表現型の理解:CFTR遺伝子の変異は、塩分と水分の輸送異常を引き起こし、体内の粘液が通常よりも粘り気を増します。肺では、この粘液が気道を塞ぎ、慢性的な呼吸器感染症や肺の損傷を引き起こします。消化器系では、膵臓の管が塞がれ、消化酵素の分泌が妨げられ、栄養吸収不良を引き起こします。
●治療法への影響:CFTR遺伝子の変異を特定することは、治療法の選択にも重要です。例えば、特定の変異に対して効果的なCFTRモジュレーター薬剤が存在し、これらは患者の症状の改善に役立ちます。また、遺伝子療法や新規薬剤の開発が進められています。
●結論
嚢胞性線維症(システィック・ファイブローシス)の病理学的分析は、遺伝子変異の同定から始まり、その変異が体内でどのように機能障害を引き起こすかを理解することが重要です。この理解を基にして、より効果的な治療法の選択や新規治療法の開発につながります。ゲノム解析技術は、このプロセスにおいて不可欠なツールであり、個別化医療の実現に向けた重要なステップを提供します。
22番染色体長腕(q)近位部
22番染色体長腕(q)近位部では分節重複間の不均等再構成による欠失や重複が複数みられ、ゲノム病の一般原則を示しています。
特に頻度の高い微細欠失は22q11.2で起こり、DiGeorge症候群、 口蓋帆・心・顔症候群(velo-cardiofacial syndrome)、 円錐動脈幹異常顔貌症候群(conotruncalanomaly face syndrome)と関連しています。
この3つの症候群は臨床的に多様で常染色体優性遺伝形式をとり、22番染色体の一方のコピー上の22q11.2内の約3Mbの欠失により生じます。
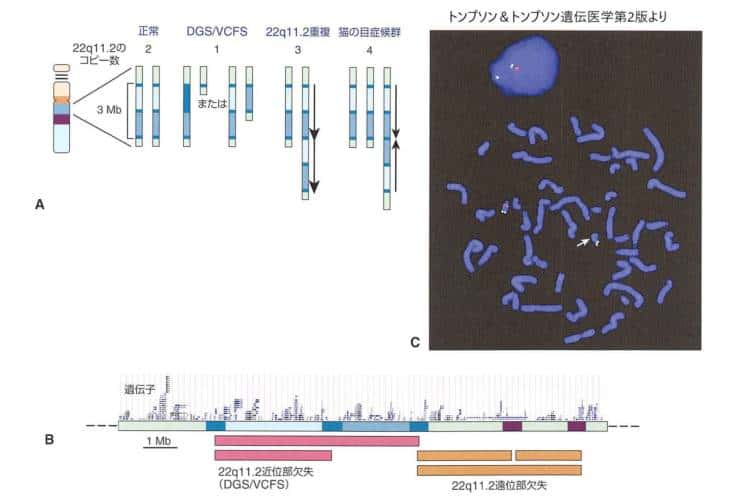
分節重複間の相同組換えによる22q11.2での欠失・重複・再構成を示した図です。
A:正常核型は2コピーの22q11.2をもち、それぞれが当該領域内に分節重複(濃青色)のコピーを多数含んでいます。
DiGeorge症候群(DGS)や口蓋帆・心・顔症候群(VCFS)では, 一方の相同染色体の3Mbの領域が欠失していて、約30の遺伝子が失われています。患者の約10%では1.5Mbの領域が欠失しています。重複はdup(22)(q11.2q11.2)の核型をもつ患者にみられ、22q11.2のテトラソミーは猫の目症候群の患者にみられます。猫の目症候群患者の重複領域は dup(22) 患者でみられる重複とは向きが逆(逆位)で、これらの分節重複に関連してより複雑なゲノム再構成が起こっていることがわかります。
B:22q11.2領域の拡大図です。一般的なDGS/VCFS患者の欠失領域(赤)と同じく分節重複の組換えにより生じる他の表現型の患者でみられるより遠位の欠失領域をオレンジ色で示しています。
C:DGSの発端者の2色FISH解析では,相同染色体の一方に22q11.2の欠失がみられています。緑色のシグナルは22番染色体長腕遠位部に対照プローブがハイブリダイズ(相補的な配列にくっつく)していています。赤色のシグナルは22番染色体長腕近位部の領域にハイブリダイズしていて、この領域は一方の22番染色体にはみられますが、他方の22番染色体では欠失しています。(矢印) 。
この領域の微細欠失と他の構成は、この領域の分節重複間の相同組換えによって生じるものです。
欠失はおよそ4,000生産児に1人の割合で認められ、重要な表現型に関連した最も一般的なゲノム再構成の1つとなっています。患者は特徴的な頭蓋顔面の形態異常、知的障害、免疫不全先天性心疾患をもち、通常この領域にある数十の遣伝子のうち1つ以上のハプロ不全(2つあるべき遺伝子が一つになることにより産生されるタンパクが減ってしまうことで機能不全を起こし症状が出る)を反映しています。
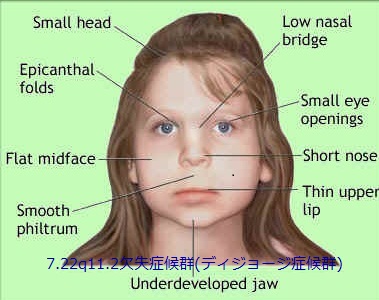
22q11.2欠失症候群(22q11.2 deletion syndrome)におけるTBX1遣伝子の欠失は、すべての先天性心疾患の5%に関与していると考えられ、特に左室流出路の形態異常の原因となることが多いとされています。
22ql 1.2の欠失の頻度が比較的高いのに対して、重複ははるかに稀となっていて、特徴的な形態異常と先天性疾患を呈する22q11.2重複症候群(22q11.2 duplication syndrome)となります。この重複の診断には一般に間期核FISHかマイクロアレイが必要となります。
22q 11.2に関連した疾患についての一般原則は、 他の染色体疾患やゲノム病にも当てはまりその代表的なものや重要なものについての概要はこのページの一番上の表にあります。
このような繰り返しみられる症候群は、人類遺伝学と遺伝医学のいくつかの重要な原則を示している。
第3章: ゲノム病の治療法と医療技術の進歩
分子レベルでの治療アプローチ
個別化医療とゲノム病
分子レベルでのゲノム病治療アプローチは、ゲノム病の原因となる遺伝子や分子メカニズムを直接的に対象とします。この種の治療は、ゲノム病の根本的な原因に焦点を当て、遺伝子の異常を修正したり、その影響を緩和することを目指しています。以下に、代表的な分子レベルでの治療アプローチを紹介します。
1. 遺伝子治療
遺伝子治療は、病気を引き起こす遺伝子の異常を修正することを目的としています。これには、異常な遺伝子を正常な遺伝子で置き換える、遺伝子の機能を抑制する、または異常な遺伝子の活性を修正する技術が含まれます。CRISPR-Cas9のようなゲノム編集技術は、特定のDNA領域を非常に正確に編集することができるため、遺伝子治療の分野で大きな可能性を秘めています。
2. RNA干渉(RNAi)技術
RNA干渉(RNAi)技術は、病気を引き起こす特定の遺伝子が作り出すmRNAを標的とし、その遺伝子の発現を抑制することで病気の進行を遅らせるまたは阻止することを目指します。この方法は、遺伝子の機能を「沈黙」させることにより、病気の影響を緩和することができます。
3. アンチセンスオリゴヌクレオチド(ASO)治療
アンチセンスオリゴヌクレオチド(ASO)は、特定のmRNA分子に結合し、そのmRNAからタンパク質が生成されるのを防ぐ短いDNAまたはRNAの断片です。この結合により、病気に関連する遺伝子の発現を下げることができ、症状の改善につながります。
4. 小分子薬物
小分子薬物は、特定の分子パスウェイを標的とし、病気の進行に重要な役割を果たすタンパク質の活動を変化させます。これらの薬物は、病気の原因となる分子やタンパク質の機能を直接的に修正することで、症状の軽減を目指します。
5. モノクローナル抗体
モノクローナル抗体治療は、病気の原因となる特定のタンパク質や細胞を標的とする抗体を使用します。これらの抗体は、病気を引き起こす分子プロセスをブロックしたり、異常な細胞を破壊することにより、病気の進行を防ぐか、症状を軽減します。
これらの分子レベルの治療アプローチは、ゲノム病の管理と治療において大きな希望を提供しています。しかし、これらの治療法はまだ研究段階にあるものも多く、臨床応用にはさらなる研究と開発が必要です。
新しい治療法の開発状況
個別化医療(パーソナライズドメディシン)は、個々の患者の遺伝的プロファイル、生活習慣、環境要因を考慮して、最適な治療法を提供する医療アプローチです。ゲノム病における個別化医療の進展は、疾患の予防、診断、治療に革命をもたらしています。
●個別化医療の重要性
疾患の早期発見と予防: 個人の遺伝的リスクを特定することで、特定の病気に対する予防措置を講じることが可能になります。たとえば、遺伝的スクリーニングにより、がんや心臓病の高リスク個体を早期に識別できます。
カスタマイズされた治療: 患者の遺伝的プロファイルに基づいて治療をカスタマイズすることで、効果を最大化し、副作用を最小限に抑えることができます。例えば、特定の遺伝子変異を持つ患者には、その変異に対応する特定の薬剤が推奨されます。
治療の効率性: 患者ごとの遺伝的特徴に基づく治療の選択は、不必要な治療や時間の浪費を避け、治療効果を迅速に得ることを可能にします。
●ゲノム病における応用
遺伝子標的治療: 特定の遺伝子変異をターゲットとした薬剤を用いて、ゲノム病を効果的に治療します。例えば、特定の変異を持つ乳がん患者に対して、HER2ターゲット療法が有効です。
ゲノム編集: CRISPR-Cas9などのゲノム編集技術を使用して、病気を引き起こす遺伝子変異を直接修正します。これにより、根本的な治療が可能になる可能性があります。
薬物遺伝子組み換え: 個人の遺伝的な違いに基づいて、薬物の種類や用量を最適化します。これにより、治療の有効性を高め、副作用のリスクを減らすことができます。
●挑戦と展望
個別化医療とゲノム病の研究は、多くの可能性を秘めていますが、実装にはいくつかの課題があります。これには、高額なコスト、データのプライバシー問題、遺伝的知識の不平等なアクセスなどが含まれます。しかし、技術の進歩と研究の深化により、これらの課題を克服し、より多くの人々が個別化医療の恩恵を受けられるようになることが期待されています。
ゲノム病に対する個別化医療の発展は、患者にとってより効果的で安全な治療オプションを提供する新たな時代を切り開いています。これにより、患者一人ひとりに最適な医療ケアを実現することができるようになります。
第4章: ゲノム病の予防と公衆衛生への影響
ゲノム病の予防策と生活習慣の調整
ゲノム病(遺伝的疾患)の予防と生活習慣の調整に関しては、遺伝的要因に基づく疾患のリスクを理解し、可能な限りそのリスクを減少させることが目標です。以下は、ゲノム病の予防策と生活習慣の調整に役立ついくつかのアプローチです。
ゲノム病の予防策
遺伝カウンセリング: 家族歴に基づいて、遺伝的なリスクを評価します。遺伝カウンセラーは、遺伝的検査の選択肢、リスクの理解、および予防策についての情報を提供できます。
遺伝的スクリーニング: 特定の遺伝的疾患のリスクが高い場合、遺伝的スクリーニングを通じて早期発見を目指します。これには、胎児期のスクリーニングや新生児スクリーニングが含まれる場合があります。
ライフスタイルの変更: 遺伝的リスクを持つ一部の疾患は、生活習慣の変更によってその発症リスクを減少させることが可能です。たとえば、心臓病や糖尿病のリスクを減らすためには、健康的な食事、定期的な運動、禁煙などが推奨されます。
生活習慣の調整
バランスの取れた食事: 健康的な食事は、遺伝的疾患のリスクが高い人々にとって特に重要です。野菜、果物、全粒穀物、良質のタンパク質を多く含む食事を心がけましょう。
定期的な運動: 定期的な運動は、多くの遺伝的疾患のリスクを減少させることができます。週に数回、中強度から高強度の運動を行うことが推奨されます。
禁煙と節度ある飲酒: タバコとアルコールの過剰な摂取は、遺伝的リスクを持つ疾患の発症リスクを高める可能性があります。
ストレス管理: 過度のストレスは健康に悪影響を及ぼし、疾患のリスクを高める可能性があります。瞑想、深呼吸、趣味、運動などを通じてストレスを管理しましょう。
定期的な健康診断: 早期発見と治療は、遺伝的疾患の管理において重要です。定期的な健康診断を受け、推奨される検査を実施しましょう。
これらのアプローチは、遺伝的なリスクを完全に取り除くことはできませんが、リスクを管理し、健康を維持するために役立ちます。遺伝的疾患のリスクが高い場合は、専門家の指導のもとで適切な予防策を講じることが重要です。
病気の予防における遺伝子検査の重要性
遺伝子検査は、病気の予防における革命的な進歩を遂げています。遺伝子には、私たちの身体の働きや健康に影響を与える情報が詰まっており、その情報を読み解くことで、将来的に発症する可能性のある病気を予測し、適切な予防策を講じることが可能になります。
●遺伝子検査のメカニズム
遺伝子検査は、DNAの一部または全体を分析することにより、遺伝的な疾患や状態のリスクを特定します。これにより、個々の遺伝子変異が持つ健康への影響を理解し、その人に特定の病気が発症するリスクが高いかどうかを知ることができます。
●病気の予防におけるその重要性
遺伝子検査により得られる情報は、病気の予防において極めて価値があります。特定の遺伝的リスクを知ることで、個々に合わせた予防策を立てることが可能になり、生活習慣の改善、定期的な健康診断の受診、予防的な治療の開始などを通じて、病気の発症を遅らせるか、完全に防ぐことができる場合があります。
●例としてのがん予防
例えば、BRCA1やBRCA2といった遺伝子の変異は、乳がんや卵巣がんのリスクを高めることが知られています。このような遺伝的リスクを早期に知ることで、高リスクの個人はより頻繁なスクリーニングを受けたり、リスクを低減するための手術を選択したりすることが可能になります。
●個別化医療への貢献
遺伝子検査は、個別化医療の実現にも寄与しています。個人の遺伝的プロファイルに基づいて最適な予防策や治療法を選択することができるため、より効果的で効率的な医療提供が可能になります。
●結論
遺伝子検査による病気の予防は、現代医療における重要な進歩の一つです。遺伝的リスクの特定により、個別化された予防策を講じることができ、病気の発症を未然に防ぎ、健康な生活を送るための重要な手段となっています。このような技術の進歩は、将来的にさらに多くの人々が健康で充実した人生を送るための鍵となるでしょう。
公衆衛生におけるゲノム病の管理と教育
公衆衛生におけるゲノム病の管理と教育は、21世紀の医療分野における重要な課題の一つです。ゲノム病、すなわち遺伝子の変異によって引き起こされる疾患は、個人の健康だけでなく、公衆衛生にも大きな影響を与えます。したがって、これらの疾患の予防、診断、治療においてゲノム医学の知識と技術が不可欠となっています。本稿では、公衆衛生におけるゲノム病の管理と教育の重要性について詳述します。
●ゲノム病の管理
ゲノム病の管理には、遺伝性の疾患を早期に発見し、予防策を講じることが含まれます。遺伝カウンセリングは、家族歴や遺伝的リスクに基づいて、個人にカスタマイズされた情報と支援を提供する重要な手段です。また、新生児スクリーニングや出生前診断などの技術は、特定の遺伝病のリスクが高い場合に早期介入を可能にします。
公衆衛生の観点からは、集団レベルでの遺伝的スクリーニングプログラムの開発が重要です。これにより、特定の遺伝病に対する感受性が高い集団を特定し、予防策を講じることができます。さらに、ゲノム編集技術の進歩により、将来的には遺伝病の根本的な治療が可能になることも期待されています。
●教育の役割
ゲノム病の効果的な管理には、医療従事者だけでなく、一般の人々に対する教育も非常に重要です。医療従事者に対しては、ゲノム医学の最新の知識と技術を提供する継続的な教育が必要です。これにより、遺伝カウンセリングや遺伝的テストの適切な利用が促進されます。
一方、一般の人々に対しては、遺伝的リスクに関する正確な情報の提供と、遺伝病の予防や管理に関する意識の向上が求められます。ゲノム病に関する知識を広めることで、不必要な恐怖や誤解を減らし、遺伝的テストや治療へのアクセスを改善することができます。
●まとめ
公衆衛生におけるゲノム病の管理と教育は、遺伝子の変異によって引き起こされる疾患への対策を強化するために不可欠です。遺伝カウンセリング、遺伝的スクリーニング、および教育プログラムを通じて、ゲノム病の予防、早期発見、そして効果的な管理を実現することが可能です。医療従事者と一般の人々双方への教育を強化することで、ゲノム医学の可能性を最大限に活用し、公衆衛生の改善に貢献することができます。
第5章: ゲノム病の社会的、倫理的考察
ゲノム情報のプライバシーと倫理
ゲノム情報のプライバシーと倫理に関する議論は、現代医学と社会において極めて重要なテーマです。ゲノム情報は、個人の遺伝的特性、疾患のリスク、家族歴など、非常に個人的かつ敏感なデータを含んでいます。この情報がもたらす潜在的な利益は計り知れないものがありますが、同時に、プライバシー侵害や不公正な扱いへのリスクもはらんでいます。以下では、ゲノム情報のプライバシーと倫理について考慮すべき主要な側面を探ります。
●ゲノム情報のプライバシー保護
ゲノム情報のプライバシー保護は、個人の権利と尊厳を守る上で不可欠です。遺伝的データの不適切な利用や共有は、保険加入の拒否、雇用上の差別、社会的スティグマの原因となり得ます。したがって、ゲノム情報を扱う際には、高度なセキュリティ措置と厳格なプライバシー保護ポリシーの実施が求められます。また、個人は自身のゲノム情報に対して知る権利と、どのように使用されるかを決定する権利を持つべきです。
●情報の同意と利用
ゲノム情報を収集・分析する際には、対象者からの明確な同意が必要です。同意プロセスには、情報の使用目的、潜在的なリスクと利益、プライバシー保護の措置についての詳細な説明が含まれるべきです。さらに、研究目的でのゲノム情報の利用に際しては、倫理的なガイドラインに従い、個人の同意に基づくべきです。
●データの共有と利用
ゲノムデータの共有は、科学研究の進展と新たな治療法の開発に貢献します。しかし、このような共有は、個人のプライバシーを保護するための厳格な条件のもとで行われるべきです。データの匿名化や擬似匿名化は、個人を特定されるリスクを減少させる一方で、完全な匿名性を保証することは困難であるため、倫理的な配慮が必要です。
●社会的責任と公正性
ゲノム情報の利用は、全ての個人に平等に利益をもたらすべきです。遺伝的情報に基づく差別を防ぐために、法律や政策で保護措置を講じることが重要です。また、ゲノム研究は多様な人口集団を対象とすることで、研究の公正性を確保し、特定の集団に偏らない治療法の開発を目指すべきです。
●結論
ゲノム情報のプライバシーと倫理は、科学的探求と社会的責任の間でバランスを取る必要がある複雑な問題です。個人の権利を守りつつ、ゲノム科学の進歩を促進するためには、透明性、公正性、そして全ての人々の尊厳を尊重することが不可欠です。適切なガイドラインと規制を通じて、ゲノム情報のポテンシャルを最大限に活用し、同時にそのリスクを最小限に抑えることが、私たちの社会に課せられた重要な課題です。
遺伝子編集技術とゲノム病
遺伝子編集技術は、科学と医療の分野で急速に発展しており、ゲノム病の治療法に革命をもたらす可能性を秘めています。ゲノム病とは、個人のゲノム内の遺伝子変異によって引き起こされる疾患のことで、遺伝性疾患や多くのがんなどがこれに含まれます。遺伝子編集技術の中でも特に注目されているのが、CRISPR-Cas9システムです。この技術を用いることで、科学者たちはDNAの特定の部分を非常に正確に切り取り、削除、または置換することが可能になり、ゲノム病の根本的な原因に直接介入できるようになりました。
●遺伝子編集のメカニズム
CRISPR-Cas9は、バクテリアがウイルスの攻撃から自身を守るための免疫システムの一部として自然界に存在します。科学者たちはこのシステムを利用して、生物のゲノムを編集する強力なツールを開発しました。この技術では、ガイドRNA(gRNA)が特定のDNA配列を認識し、Cas9酵素がその場所でDNAを切断します。その後、細胞の自然な修復プロセスを利用して、DNAに変更を加えることができます。
●ゲノム病への応用
遺伝子編集技術は、特に遺伝性疾患の治療において大きな希望を提供しています。例えば、シクル細胞性貧血や筋ジストロフィーなどの病気は、特定の遺伝子変異によって引き起こされます。CRISPR-Cas9を用いることで、これらの変異を持つ遺伝子を正常な形に修正することが可能になり、病気の治療や予防が現実的な選択肢となり得ます。
●倫理的な考慮
遺伝子編集技術の応用は、倫理的な問題も伴います。特に、生殖細胞(精子や卵子)や胚に対する編集は、修正された遺伝情報が次世代に伝わるため、深刻な倫理的懸念を引き起こします。また、ゲノム編集がもたらす長期的な影響や予期せぬ結果についても、十分な理解がないことが問題となります。
●まとめ
遺伝子編集技術は、ゲノム病の治療における大きな突破口となりうるものです。CRISPR-Cas9をはじめとする技術は、特定の遺伝子変異を正確に修正し、遺伝性疾患の治療や予防に新たな可能性を開くものです。しかし、この技術の安全性や倫理性については、社会全体での広範な議論と合意形成が必要です。遺伝子編集が持つ可能性を最大限に活用しつつ、そのリスクを適切に管理するバランスを見つけることが、今後の課題となるでしょう。
社会におけるゲノム病の認識と対応
社会におけるゲノム病の認識と対応は、近年、医学技術の進歩に伴い、ますます重要性を増しています。ゲノム病は、遺伝子の変異によって引き起こされる疾患であり、その多様性と複雑性は、社会全体における包括的な理解と対策を必要としています。本稿では、社会におけるゲノム病の認識の向上と、それに対応するためのアプローチについて探求します。
●ゲノム病に対する認識の向上
ゲノム病に対する社会的認識の向上は、教育と情報の普及から始まります。一般市民に対して、遺伝子の基本的な知識や、ゲノム病が個人や家族に与える影響についての理解を深めることが重要です。また、ゲノム病に関する正確な情報を提供し、誤解や偏見を解消する取り組みも必要です。
医療従事者に対しては、ゲノム医学の教育を強化し、最新の研究成果や治療法に関する知識を更新することが求められます。これにより、遺伝カウンセリングの質の向上や、遺伝的テストの適切な利用が促進されます。
●社会における対応の多様化
ゲノム病に対する社会の対応は、多面的であるべきです。以下は、その対応のいくつかの例です。
政策立案と法規制: 遺伝情報のプライバシー保護や、遺伝的テストに関する倫理的なガイドラインの策定が含まれます。遺伝情報に基づく差別を防止するための法的枠組みも重要です。
保険制度の改善: 遺伝的リスクが高い個人でも、医療保険の適用を受けられるようにするための制度設計が求められます。
支援システムの構築: ゲノム病を持つ個人やその家族を支援するためのシステムを構築します。これには、心理的サポートや、情報提供、経済的支援が含まれます。
公衆衛生プログラム: 遺伝的スクリーニングや健康教育プログラムを通じて、ゲノム病の早期発見と予防を目指します。
●まとめ
社会におけるゲノム病の認識と対応は、多様なステークホルダーが関与する複雑なプロセスです。教育と情報の普及、政策の策定、保険制度の改善、そして支援システムの構築など、多方面からのアプローチが必要です。ゲノム病に対する社会全体の理解を深め、適切な対応を行うことで、公衆衛生の向上と、ゲノム病を持つ個人及びその家族の生活の質の向上が期待できます。
第6章: ゲノム病研究の未来と展望
研究の最新動向と将来の方向性
ゲノム病の研究は、急速に進化し続けている分野であり、新たな技術の発展によって、疾患の理解、診断、治療が大きく変わりつつあります。以下では、ゲノム病の研究における最新動向と将来の方向性について概観します。
●最新動向
CRISPR-Cas9を用いた遺伝子編集: CRISPR-Cas9技術は、特定の遺伝子を正確に編集することを可能にします。この技術は、遺伝性疾患の治療法の開発に革命をもたらしており、既に一部の疾患に対する臨床試験が行われています。
全ゲノムシークエンシング: 全ゲノムシークエンシングのコストが大幅に低下したことで、個々のゲノムを詳細に分析し、疾患の原因となる遺伝子変異を特定することがより実用的になっています。これは、個別化医療の実現に向けた重要なステップです。
バイオインフォマティクスとデータ解析: 大量の遺伝的データを解析し、疾患の原因や治療標的を特定するために、バイオインフォマティクスと高度なデータ解析技術が活用されています。
多様な人口集団での研究: 研究対象となる人口集団の多様性を増やすことで、疾患の理解を深め、より幅広い患者群に適用可能な治療法の開発が進められています。
●将来の方向性
個別化医療の拡大: 患者個々の遺伝的特徴に基づいた治療法の開発が進むことで、より効果的で副作用の少ない治療が可能になることが期待されます。
遺伝子治療の進化: CRISPR-Cas9をはじめとする遺伝子編集技術の進化により、遺伝性疾患の根本的な治療が現実のものとなります。安全性と効果の確立が、今後の大きな課題です。
疾患予防への応用: 遺伝的リスクの早期識別により、生活習慣の改善や予防的治療によって、疾患の発症を防ぐ取り組みが強化されます。
レア疾患の研究促進: レア疾患の原因となる遺伝子変異の特定が進むことで、これまで治療法のなかった疾患に対する新たな治療法が開発されます。
エピジェノミクスの探求: 遺伝子の発現を制御するエピジェネティックな変化の理解を深めることで、新たな治療標的が明らかになることが期待されます。
ゲノム病の研究は、倫理的、社会的な課題にも直面しています。プライバシーの保護、遺伝情報に基づく差別の防止、治療への公平なアクセスなど、技術的進歩と同様に、これらの課題に対処することが、研究の進展と社会の受容性を高める上で重要です。将来的には、遺伝学的知見を活用した疾患の予防、診断、治療が一般化し、より多くの人々の健康と生活の質の向上に寄与することが期待されます。
ゲノム科学の進歩が医療にもたらす可能性
ゲノム科学の進歩は、医療分野に革命的な変化をもたらす可能性を秘めています。人間のゲノムを理解し操作する能力が向上するにつれて、疾患の予防、診断、治療が根本的に変わりつつあります。以下に、ゲノム科学の進歩が医療にもたらす可能性について詳しく解説します。
1. 個別化医療の実現
ゲノム情報の詳細な分析により、個人の遺伝的特性に基づいた個別化医療が実現します。これにより、患者一人ひとりに最適な治療法を提供できるようになり、効果が高く副作用が少ない治療が可能になります。例えば、がん治療において、腫瘍の遺伝子プロファイルを分析して、最も効果的な薬剤を選択するアプローチが取られています。
2. 疾患の早期発見と予防
遺伝子検査を用いて遺伝性のリスクを早期に識別することで、疾患の予防や早期発見が可能になります。たとえば、BRCA1やBRCA2遺伝子の変異を持つ人は乳がんや卵巣がんのリスクが高いとされており、リスクを知ることで定期的なスクリーニングや予防策を取ることができます。
3. 新たな治療法の開発
ゲノム編集技術の進歩により、遺伝子療法が現実のものとなっています。CRISPR-Cas9などの技術を用いて、遺伝子の変異を直接修正し、遺伝性疾患の根本的な原因を治療する新たな方法が開発されています。これにより、これまで治療法がなかった疾患に対しても、治療の可能性が開かれます。
4. 疾患理解の深化
ゲノム科学の進歩により、疾患の原因となる遺伝子変異やそのメカニズムの理解が深まります。これにより、疾患の分子的な基盤に基づいた新しい診断法や治療法の開発が加速されます。
5. パーソナライズされた予防策
遺伝子情報を活用することで、個人の遺伝的傾向に基づいた予防策を立てることができます。生活習慣の改善や食事、運動などの予防策が、個人のゲノム情報に基づいてカスタマイズされます。
結論
ゲノム科学の進歩は、医療分野において前例のない変革をもたらしています。これにより、疾患のより良い予防、診断、治療が可能になり、より健康で質の高い生活を送ることができるようになります。しかし、これらの進歩には倫理的な考慮が伴います。個人の遺伝情報の取り扱い、遺伝子編集の倫理性、健康格差の問題など、様々な課題を解決するための社会的な議論と枠組みの構築が求められています。ゲノム科学の進歩を最大限に活用し、その恩恵を公平に享受するためには、これらの課題に対する注意深い取り組みが不可欠です。
患者と社会にとっての意味と影響
ゲノム病の患者と社会にとっての意味と影響は、医学的、心理的、社会的、経済的な多様な側面を含んでいます。ゲノム病は、個人の遺伝子の変異に起因する病気であり、その性質上、患者本人だけでなく家族や社会全体に深い影響を及ぼすことがあります。
●個人と家族への影響
医学的影響: ゲノム病は、生活に大きな制限をもたらすことがあり、治療法が限定されている場合も多いです。患者は、病気の進行を遅らせるために、生涯にわたる治療や管理が必要になることがあります。
心理的影響: 診断を受けた個人は、不安、孤独感、ストレス、そして時には抑うつを経験することがあります。また、遺伝的な側面から、自分の子どもに病気が遺伝する可能性についての心配も生じます。
社会的影響: 社会における誤解やスティグマは、ゲノム病の患者が直面する大きな障壁です。これにより、就職、保険加入、さらには個人関係においても差別や不平等が生じることがあります。
経済的影響: ゲノム病の診断と治療は、患者及びその家族にとって重大な経済的負担となることがあります。高額な医療費、治療に伴う時間的制約、仕事の喪失など、経済的な困難を招く原因は多岐にわたります。
●社会への影響
医療システムへの負担: ゲノム病の患者が増えることは、医療システムに対する需要の増加を意味し、診断、治療、遺伝カウンセリングなどのサービスへのアクセスに影響を与えます。
経済的負担: ゲノム病の管理と治療に関わる高額な医療費は、社会保障システムに大きな負担をかける可能性があります。また、患者や家族の生産性の低下も、社会経済に影響を及ぼします。
法的・倫理的課題: 遺伝情報の取り扱いや、遺伝的スクリーニング、ゲノム編集技術などに関連する法的および倫理的な問題は、社会にとって重要な課題です。これらの技術の適切な利用と管理には、継続的な議論と政策の更新が必要です。
教育と意識向上: ゲノム病に関する社会全体の認識と理解を深めることは、スティグマの解消と患者への支援を強化する上で重要です。これには、教育プログラムや啓発活動が不可欠です。
●まとめ
ゲノム病の患者と社会にとっての意味と影響は、多方面にわたります。これらの病気に対する総合的なアプローチは、医学的治療だけでなく、心理的サポート、社会的インクルージョン、経済的援助、そして教育と情報提供にも焦点を当てる必要があります。個人の尊厳と権利を守りつつ、ゲノム病の患者とその家族が直面する課題に対処するための社会的支援の強化が求められています。
【関連記事】
- 染色体異常【23】染色体分析法1
- 染色体異常【24】染色体分析法2高精度染色体解析
- 染色体異常【25】染色体分析法3蛍光in situハイブリダイゼーション
- 染色体異常【26】染色体分析法4:マイクロアレイ
- 染色体異常【27】染色体分析法5:全ゲノムシーケンス
- 染色体異常染色体異常【28】染色体異常の種類
- 染色体異常【29】遺伝子量:どうして染色体が3本になると人間は疾患になるのか
- 染色体異常【30】染色体の数的異常
- 染色体異常【31】染色体の構造異常1.総論
- 染色体異常【32】染色体の構造異常2.均衡型構造異常
- 染色体異常【33】染色体の構造異常3.不均衡型構造異常








