目次
この記事では、DNAからRNAへの転写プロセスの基本から、セントラルドグマ、ポリメラーゼの働き、そして生物学の大謎を解決するSpring-8での最新研究まで、わずか5分で理解できるコンパクトでスムーズな流れを紹介します。
第1章: 転写の基礎
DNAとRNAの基本
生物学における遺伝情報の暗号
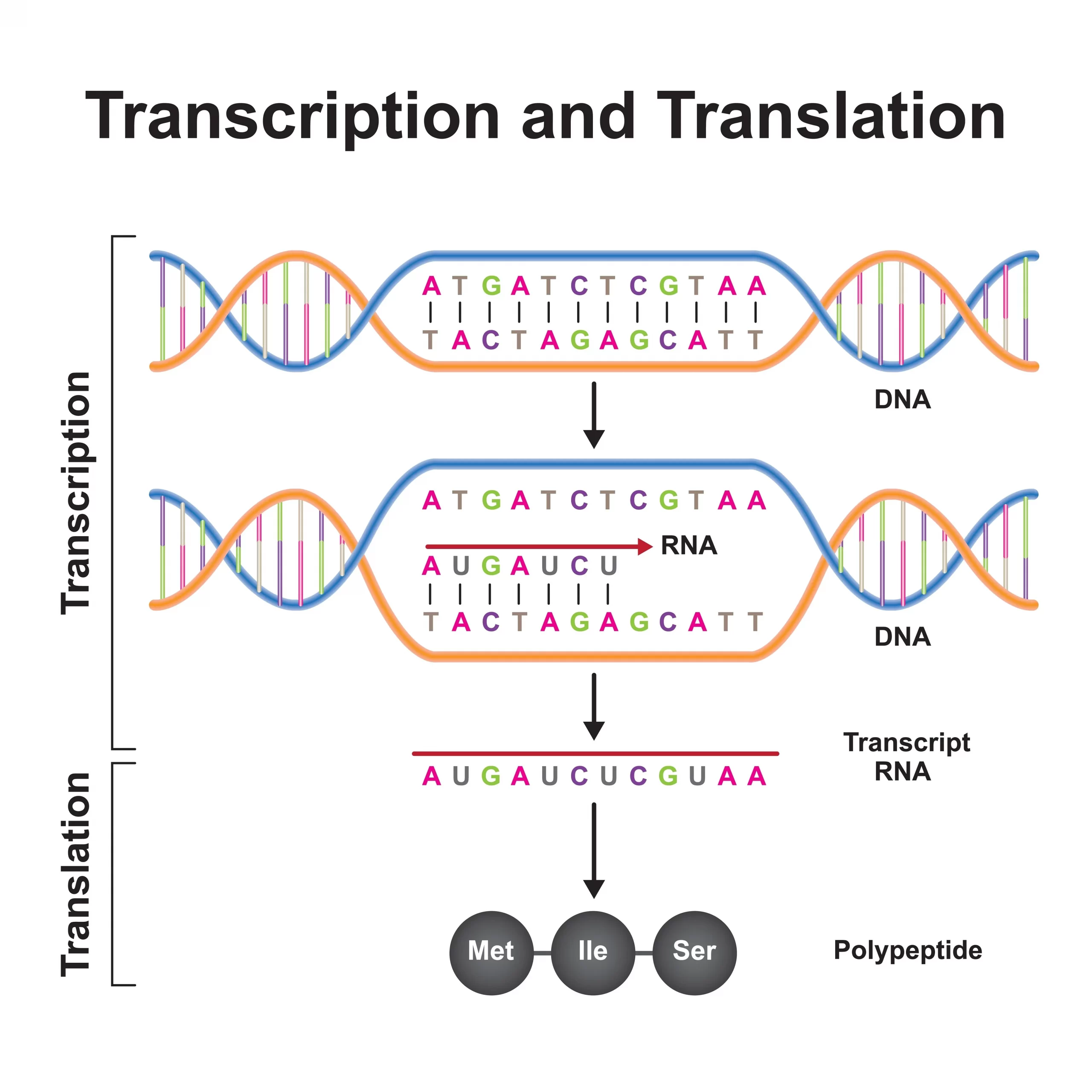
生物学における遺伝情報の暗号は、DNAに含まれる塩基配列によって定義されます。この配列は、アデニン(A)、チミン(T)、グアニン(G)、シトシン(C)の4種類の核酸塩基によって構成され、生命の設計図として機能します。遺伝情報は、DNAからRNAへと転写され、その後、RNAがタンパク質へと翻訳されることで、細胞の構造、機能、および調節メカニズムを形成します。この一連のプロセスは「セントラルドグマ」として知られ、遺伝情報がどのようにして生物学的特徴や機能に変換されるかを説明しています。各塩基配列は、特定のアミノ酸をコードし、これらのアミノ酸が連結してタンパク質を形成します。このようにして、DNAの塩基配列は生物の形質や振る舞いを決定する遺伝情報の暗号として機能するのです。
セントラルドグマの概要
セントラルドグマは、分子生物学の基本原則であり、遺伝情報の流れを説明しています。この理論は、DNAからRNAへ、そしてタンパク質へという情報の一方向性の流れを示しています。まず、DNAの遺伝情報は転写によってmRNA(メッセンジャーRNA)に転写されます。次に、このmRNAは翻訳プロセスを通じてアミノ酸の連鎖体であるタンパク質に翻訳されます。セントラルドグマは、生物学的情報の伝達と遺伝子の機能発現の基本的な枠組みを提供し、遺伝情報の安定性と制御の理解に寄与しています。ただし、この理論には例外もあり、逆転写やRNAエディティングなどのプロセスを通じて、RNAからDNAへの情報の逆流も可能です。
転写の流れ
遺伝子からmRNAへの情報伝達
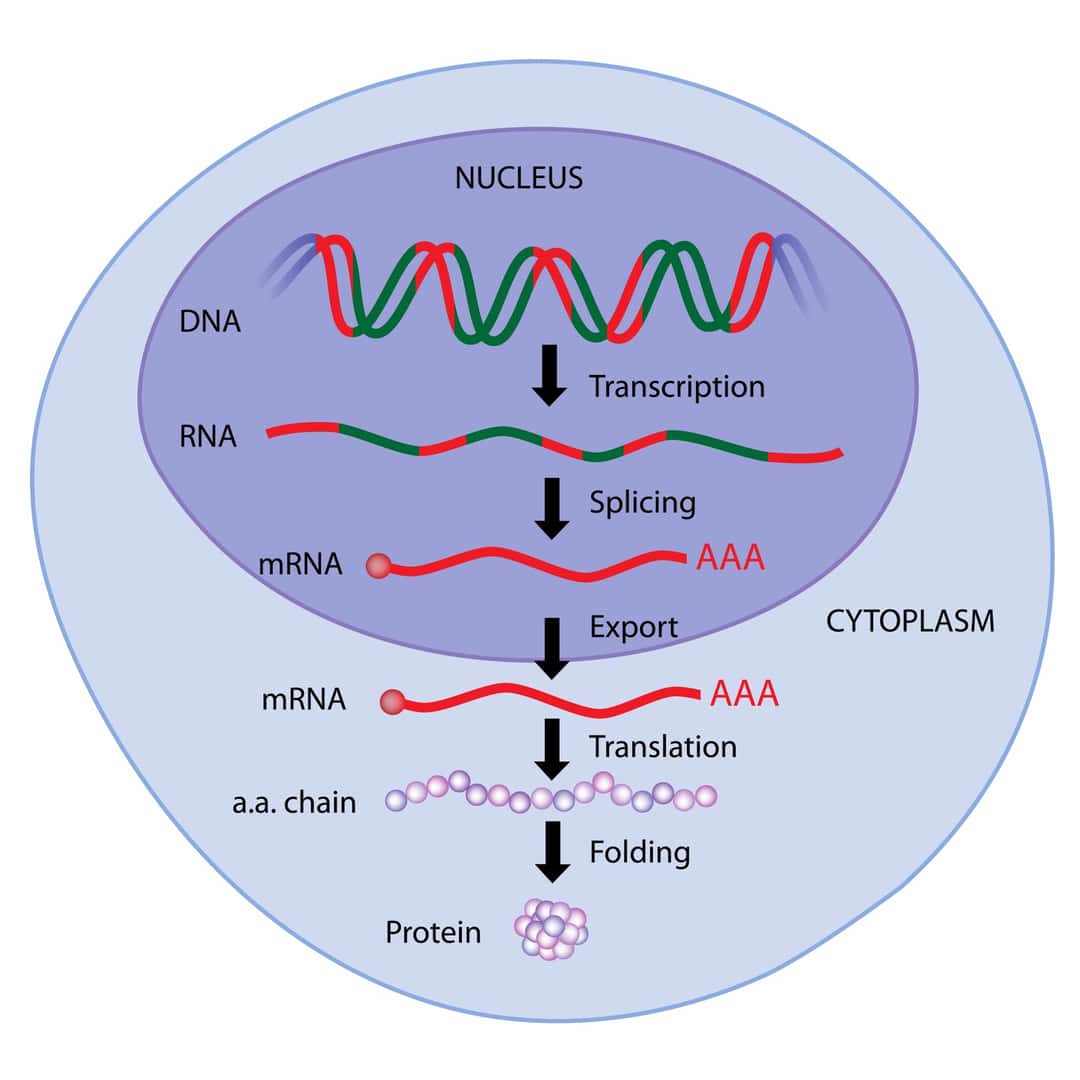
遺伝子からmRNAへの情報伝達は、転写というプロセスを通じて行われます。この過程で、DNAの遺伝情報がRNAポリメラーゼ酵素によってmRNAに「転写」されます。まず、RNAポリメラーゼがDNAのプロモーター領域に結合し、DNA鎖を開いて転写を開始します。次に、DNAのテンプレート鎖に沿って、補完的なmRNA鎖が合成されます。転写が終わると、初期mRNAはキャッピング、スプライシング、ポリアデニル化といったプロセシングを受け、成熟したmRNAが形成されます。この成熟したmRNAは細胞質へと移動し、リボソームでのタンパク質合成へと繋がる情報を運びます。この一連のプロセスによって、遺伝子の情報が生物の形質として現れるタンパク質へと翻訳されます。
ポリメラーゼの役割と仕組み
ポリメラーゼは、DNAやRNAの塩基配列を合成する酵素であり、生命の遺伝情報伝達に不可欠な役割を果たします。DNAポリメラーゼは、細胞分裂時にDNAを複製する過程で活動し、新しいDNA鎖の合成を担います。一方、RNAポリメラーゼは、DNAの遺伝情報を使ってmRNAを合成する転写プロセスに関与します。このプロセスでは、RNAポリメラーゼがDNA鎖を開き、テンプレート鎖に沿って新しいRNA鎖を合成します。酵素は特定のプロモーター領域に結合し、そこから転写を開始し、終結信号で転写を終了します。ポリメラーゼの活動により、遺伝情報は正確にRNAへと転写され、このRNAがタンパク質合成の指示書として機能します。このようにポリメラーゼは、遺伝情報の正確なコピーと伝達を保証し、生物の生存と発達に欠かせない酵素です。
第2章: 転写の詳細なプロセス
遺伝子発現の開始
遺伝子発現の開始は、細胞が特定の遺伝子からタンパク質を合成するプロセスを始める重要なステップです。この過程は、RNAポリメラーゼと呼ばれる酵素がDNAの特定領域、すなわちプロモーターに結合することから始まります。プロモーターは、遺伝子の上流に位置し、遺伝子の転写を開始する信号を提供します。RNAポリメラーゼの結合により、DNA二重螺旋が局所的に開かれ、酵素がテンプレート鎖に沿って新しいRNA鎖を合成することが可能になります。このプロセスは転写の開始と呼ばれ、特定の転写因子によって調節されます。これらの転写因子は、遺伝子の発現を増加させるか抑制するかを制御し、細胞のニーズに応じて遺伝子発現の精密な調節を可能にします。遺伝子発現の開始は、生物の成長、発達、応答メカニズムなど、多くの生物学的プロセスにおいて中心的な役割を果たします。
プロモーター領域と転写因子の結合
プロモーター領域は、遺伝子の転写を開始するためのDNA配列であり、転写因子と呼ばれる特定のタンパク質が結合するサイトを含んでいます。転写因子は遺伝子の発現を調節する役割を担い、特定のプロモーター領域に結合することで転写の開始を促進または抑制します。この結合は、細胞の状態や発達段階、外部からのシグナルに応じて遺伝子の発現を精密に制御するために重要です。転写因子がプロモーター領域に結合することにより、RNAポリメラーゼIIなどの転写酵素が遺伝子の転写開始点に正確に位置づけられ、遺伝情報がmRNAへと転写されるプロセスが開始されます。この相互作用は、生物学的多様性と細胞特異的な機能の実現に不可欠であり、遺伝子発現のダイナミクスを理解する上で中心的な役割を果たしています。
RNAポリメラーゼIIの活性化
RNAポリメラーゼII(Pol II)の活性化は、転写の開始と遺伝子の発現調節に不可欠です。この活性化プロセスは、特定の転写因子がDNA上のプロモーター領域に結合することから始まります。これらの転写因子は、Pol IIが正しい位置に結合し、転写を開始できるようにする役割を果たします。さらに、メディエーター複合体などの調節因子が介在し、Pol IIと転写因子の相互作用を促進します。この相互作用により、Pol IIのC末端ドメイン(CTD)が特定のリン酸化パターンを受け、活性化されます。リン酸化されたCTDは、さまざまな転写調節因子やRNAプロセシング因子を引き寄せ、転写の開始、RNAのプロセシング、およびmRNAの成熟を効率的に進行させます。このようにして、RNAポリメラーゼIIの活性化は、遺伝子の正確な発現と細胞機能の調節に重要な役割を果たします。
伸長と終結
RNA鎖の伸長プロセス
RNA鎖の伸長プロセスは、遺伝子の転写において核心的な段階です。このプロセスでは、RNAポリメラーゼがDNAのテンプレート鎖に沿って新しいRNA鎖を合成します。転写の開始後、RNAポリメラーゼはDNAを解読し、対応するリボヌクレオチドを連結させてRNA鎖を伸長させます。この段階で、酵素はDNAの塩基配列に基づいて、アデニン(A)、ウラシル(U)、グアニン(G)、シトシン(C)の4種類のリボヌクレオチドを適切に選択し、RNA鎖に加えていきます。伸長過程では、RNAポリメラーゼが一定の速度でDNA鎖を移動し、連続的にRNAを合成します。このプロセスは、遺伝子の終結信号に到達するまで続けられ、そこでRNAポリメラーゼはDNAから解離し、新しく合成されたRNA鎖が放出されます。伸長プロセスを通じて、遺伝情報が正確にRNAに転写されることで、後のプロセスである翻訳において、このRNAがタンパク質の設計図として機能することになります。
転写終結とRNAの成熟
転写終結は、RNAポリメラーゼがDNAテンプレート沿いの転写を停止し、新たに合成されたpre-mRNAが放出されるプロセスです。この段階は、特定の終結信号に従って精密に制御され、遺伝子の正確な転写を保証します。転写終結後、pre-mRNAは成熟mRNAに加工されるための一連の修飾を受けます。これには5’キャップの付加、3’末端のポリアデニル化、およびイントロンの除去が含まれます。特に、スプライシングと呼ばれるプロセスによってイントロンが除去され、エクソン同士が連結されます。これらの修飾は、mRNAの安定性を高め、細胞質への輸送を可能にし、翻訳の効率を向上させる重要な役割を果たします。成熟したmRNAは、タンパク質合成のためのリボソームへと輸送され、遺伝情報がタンパク質へと翻訳される準備が整います。このプロセス全体は、遺伝子の発現調節と細胞機能の実現に不可欠です。
第3章: 転写の調節メカニズム
遺伝子発現の細かな調節
エピジェネティクスとヌクレオソームの構造
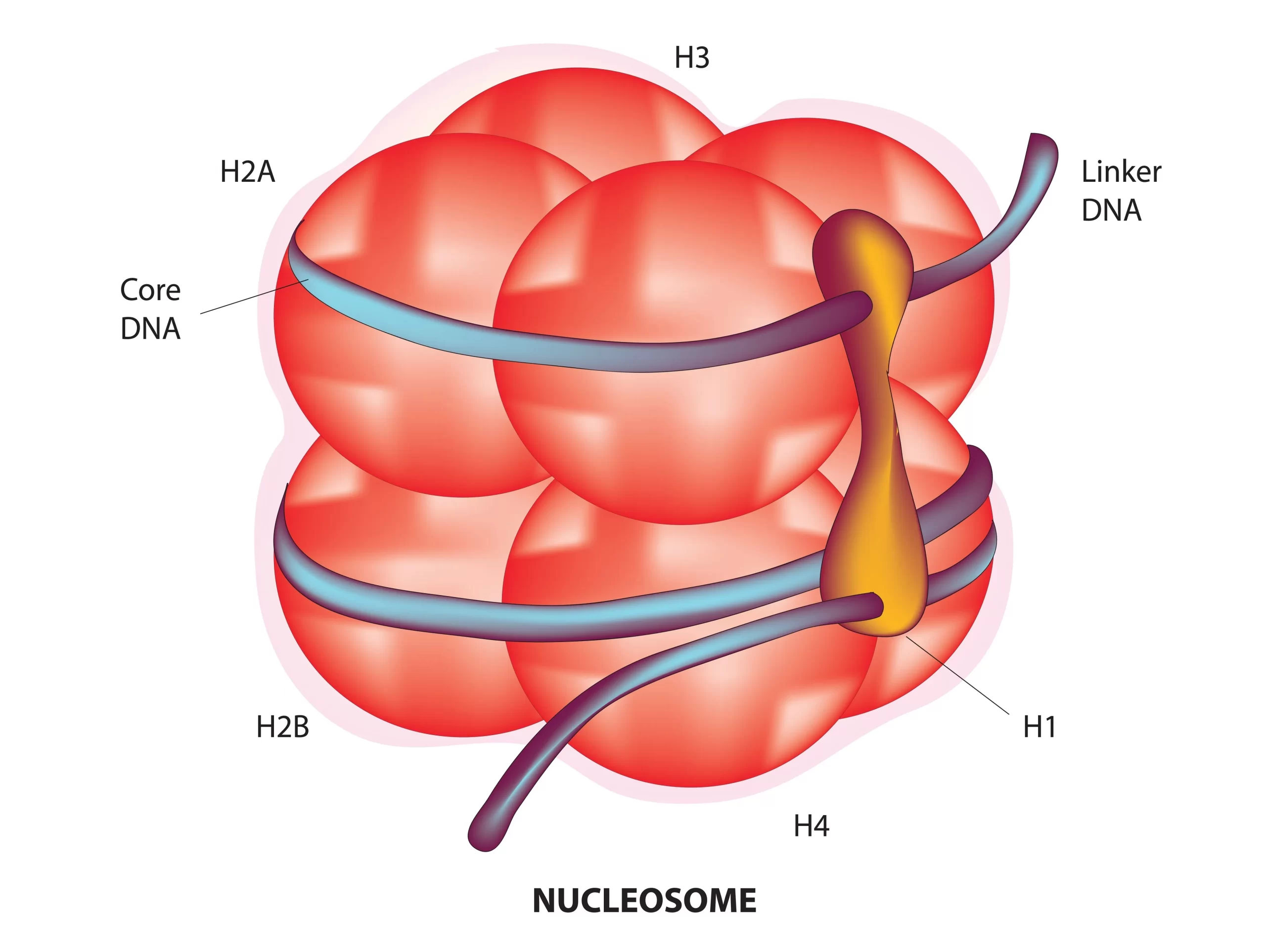
エピジェネティクスは、遺伝子の活性を変化させるがDNA配列そのものは変えない、遺伝情報の調節機構を指します。この調節は、DNAメチル化、ヒストンの修飾、クロマチンのリモデリングなどを通じて行われます。ヌクレオソームの構造は、エピジェネティクス調節の基本的な単位であり、この構造が遺伝子のアクセシビリティと活性を決定する重要な役割を果たします。
ヌクレオソームは、DNAとヒストンタンパク質から成る複合体で、DNAが約147塩基対の長さでヒストンオクタマー(2つのH2A、H2B、H3、H4ヒストンの各ペアからなる)を中心に約1.65回螺旋を描いて巻き付いた構造をしています。この構造により、DNAはコンパクトに折りたたまれ、細胞核内での遺伝物質の収納が可能になります。
エピジェネティクスの観点から、ヒストン修飾(アセチル化、メチル化、リン酸化など)はヌクレオソームのダイナミクスに直接影響を与えます。例えば、ヒストンのアセチル化はクロマチン構造を緩め、遺伝子が転写因子により容易にアクセスされるようになり、遺伝子の発現が促進されます。逆に、ヒストンのメチル化はクロマチンを凝縮させ、遺伝子のアクセスを制限し、発現を抑制することがあります。
このように、エピジェネティクスとヌクレオソームの構造は密接に関連しており、遺伝子の発現パターンを決定する上で重要な役割を果たします。細胞の特定の時期や環境条件下での遺伝子のオン/オフは、このエピジェネティックな調節メカニズムによって細かくコントロールされています。
スプライシングとRNA修飾
スプライシングとRNA修飾は、eukaryotic cellsにおいてpre-mRNA(前駆体mRNA)が成熟したmRNAに変換される過程で重要な役割を果たします。これらのプロセスは、遺伝情報の正確な表現とタンパク質の多様性を確保するために不可欠です。
●スプライシング
スプライシングは、pre-mRNAからイントロン(非コーディング領域)を取り除き、エクソン(コーディング領域)を連結させる過程です。このプロセスはスプライソソームと呼ばれる大きなリボヌクレオプロテイン複合体によって媒介されます。スプライシングにより、同じpre-mRNAから異なるスプライシングバリアントが生み出されることがあり、これによってタンパク質のアイソフォームの多様性が生じます。この現象はアルタナティブスプライシングと呼ばれ、細胞タイプ、発達段階、環境条件に応じて異なるタンパク質を生産することを可能にします。
●RNA修飾
RNA修飾は、RNA分子に様々な化学的変更が加えられる過程を指します。これには5’キャッピング、3’のポリアデニル化、そしてRNA分子内の特定ヌクレオチドの修飾(例:メチル化)が含まれます。5’キャッピングは、mRNAの安定性とリボソームによる翻訳の効率を高めます。3’ポリアデニル化もまたmRNAの安定性に寄与し、細胞質への輸送を助けます。その他のRNA修飾(例:メチル化)は、RNAの構造と機能に影響を与え、スプライシング、翻訳効率、RNAの分解などに関与しています。
スプライシングとRNA修飾は、遺伝子の正確な発現とタンパク質の機能的多様性を実現するための複雑な調節メカニズムを形成しています。これらのプロセスの異常は、多くの遺伝的疾患やがんなどの病態に関連しているため、生命科学と医学の研究において重要な研究対象となっています。
転写の制御と生物学的重要性
細胞特異的な遺伝子発現の調節
細胞特異的な遺伝子発現の調節は、生物の発達、分化、および機能的な多様性を支える基本的な生物学的プロセスです。この調節は、細胞が特定のタイプに分化する過程で、特定の遺伝子がオンまたはオフに切り替わることにより行われます。この過程には、複数の調節機構が関与しています。
転写因子の結合: 細胞特異的な遺伝子発現は、特定の転写因子がDNA上の特定の配列(プロモーターやエンハンサー領域)に結合することで調節されます。これにより、特定の遺伝子の転写が活性化または抑制されます。転写因子は細胞タイプや発達段階、さらには外部からのシグナルに応じて異なります。
エピジェネティクス的調節: DNAメチル化やヒストン修飾(アセチル化、メチル化など)によるクロマチンの構造変化は、遺伝子のアクセシビリティを変化させ、細胞特異的な遺伝子発現を調節します。これらの修飾は、遺伝子がアクティブな状態かサイレントな状態かを決定する重要な役割を果たします。
RNAプロセシングの調節: RNAスプライシング、エディティング、および輸送は、mRNAの多様性と細胞内での局在を調節し、細胞特異的なタンパク質発現パターンを形成します。これにより、同じ遺伝子から異なる細胞タイプで異なるタンパク質が生産されることがあります。
非コーディングRNAによる調節: miRNAやlncRNAなどの非コーディングRNAは、mRNAの安定性や翻訳を調節し、細胞特異的な遺伝子発現パターンを形成します。これらのRNA分子は、特定のmRNAを標的として分解させたり、翻訳を抑制することで、遺伝子発現を微調整します。
これらの調節機構は相互に作用し合い、細胞の特定の状況やニーズに応じた適切な遺伝子発現パターンを確立します。このようにして、遺伝的情報は細胞タイプ、組織、器官、および生物全体のレベルで異なる機能的なコンテキストに適応することが可能となります。
環境応答と遺伝子のオンオフ
第4章: 研究の最前線とSpring-8の成果
Spring-8による転写プロセスの撮影
Spring-8は、日本にある世界最高峰の放射光施設の一つで、非常に強力なX線を利用して物質の微細構造を解析することが可能です。この技術は、タンパク質結晶や生物学的構造の詳細な観察に広く用いられており、転写プロセスのような生命科学の基本的な現象を理解するのに役立ちます。
転写プロセスの撮影において、Spring-8の放射光を用いることで、RNAポリメラーゼがDNAの特定の領域に結合し、RNA鎖を合成する過程を、原子レベルで観察することができます。このような詳細な構造解析は、転写開始、エロンゲーション(伸長)、終結など、転写の各段階における分子間相互作用の理解を深めるのに非常に有効です。
具体的には、Spring-8を利用した研究によって、転写因子やその他の調節タンパク質がRNAポリメラーゼやDNAとどのように相互作用するか、またこれらの分子がどのようにして転写の制御を行っているかについての貴重な洞察が得られます。これらの情報は、遺伝子発現の精密な調節メカニズムの解明に寄与するだけでなく、遺伝病やがんなどの疾患の治療法開発に向けた基盤となり得ます。
Spring-8による転写プロセスの撮影は、分子生物学と構造生物学の分野における研究を大きく前進させる可能性を秘めており、生命の本質を解明するための重要な手段となっています。
構造生物学における画期的な解析
構造生物学は、生物分子の3次元構造を解明し、その機能を理解する学問です。
転写プロセスの撮影を含む構造生物学における研究では、Spring-8の提供する高輝度X線がタンパク質や複合体の立体構造を原子レベルで解明するのに不可欠です。
転写プロセスは、DNAからmRNAへの情報伝達を含む生命現象の根幹をなすものです。この過程には、RNAポリメラーゼという酵素が関与しており、その動的な構造変化が転写の各段階を制御しています。Spring-8を使用して転写プロセスを「撮影」することで、科学者たちはRNAポリメラーゼの動作メカニズムや、転写を開始、進行、終了させるために必要なタンパク質やRNAとの相互作用について深い理解を得ることができます。
このような研究は、特にX線結晶構造解析やX線自由電子レーザー(XFEL)技術を使用して行われます。これらの技術により、非常に高い解像度で転写複合体のスナップショットを捉えることが可能となり、転写過程における瞬間的な構造変化を明らかにすることができます。これらの解析結果は、遺伝子発現の精密な制御メカニズムの理解を深めるだけでなく、転写関連疾患の治療法開発にも寄与する可能性があります。
Spring-8による転写プロセスの解析は、生命科学の基礎研究を大きく前進させる画期的な成果をもたらしています。これらの進歩は、将来的に新しい医薬品の開発や遺伝子療法の改善に繋がることが期待されます。
RNAポリメラーゼと遺伝子発現の謎の解明
最新の研究成果とその影響
RNAポリメラーゼ2(RNAP2)は、真核生物の遺伝子発現を担う重要な酵素です。最近の研究により、RNAP2が遺伝子転写の際にDNAの巻き取り構造であるヌクレオソームを一時的にほどき、その後再構築する仕組みが解明されました 。
具体的には、RNAP2はさまざまなタンパク質と結合して複合体を形成し、ヌクレオソームに入り、DNAをヒストンから徐々にほどいて解体していきます。ヌクレオソームの中央を通過すると、ヒストンを転写が終わったDNAの方へと移し、ヌクレオソームを組み立て直すことが確認されています。このプロセスには「ヒストンシャペロン」である「ファクト(FACT)」というタンパク質も関与しており、DNAからはがされたヒストンが離れていかないようにつなぎ止めています。
この研究成果は、遺伝子発現とクロマチン構造の維持を両立させる仕組みを理解する上で重要であり、将来的には疾患の解明や新たな医薬品の開発にも寄与することが期待されています。
生物学における未解決問題への新たなアプローチ
RNAポリメラーゼと遺伝子発現の謎の解明に対する新たなアプローチは、生物学における未解決問題への突破口となっています。RNAポリメラーゼはDNAからmRNAへ情報を転写する酵素であり、その活動は遺伝子発現の初期段階を制御しています。しかし、このプロセスにおける詳細なメカニズムや、特定の遺伝子発現パターンがどのように決定されるかは長らく大きな謎の一つでした。
新たなアプローチと技術
高解像度構造生物学: X線結晶構造解析やクライオ電子顕微鏡(cryo-EM)技術の進歩により、RNAポリメラーゼの複合体の高解像度構造を明らかにする研究が進んでいます。これにより、転写開始、伸長、終了の各段階での酵素の構造的変化や、DNAおよびRNAとの相互作用が詳細に解析されています。
ゲノムワイドアプローチ: シーケンシング技術とゲノム編集技術(CRISPR-Cas9など)の組み合わせにより、遺伝子発現の制御に関わる新たな要素が発見されています。これらの技術を用いて、特定の転写因子やエピジェネティックな修飾が遺伝子発現にどのように影響するかを大規模に解析することが可能になりました。
ライブセルイメージング: 高度な顕微鏡技術を使用して、実際の細胞内でのRNAポリメラーゼの動きや遺伝子発現のダイナミクスをリアルタイムで観察する研究が増えています。このアプローチにより、転写の過程が細胞の状態や環境変化にどのように応答するかを理解することができます。
期待される影響
これらの新たなアプローチにより、RNAポリメラーゼの働きと遺伝子発現の調節メカニズムの理解が深まりつつあります。これは、遺伝子発現の異常が原因である多くの疾患、例えばがんや遺伝性疾患などの治療法開発に直接的な影響を与える可能性があります。また、この知識は合成生物学や遺伝子療法の分野での応用を通じて、新しい治療戦略の開発に繋がることも期待されています。
RNAポリメラーゼと遺伝子発現に関するこれらの研究は、生物学の基礎をなす重要な謎を解き明かすだけでなく、医学、バイオテクノロジー、合成生物学の分野における革新的な進歩を促す原動力となっています。
【関連記事】
- 遺伝病を理解するためのヒトゲノム入門編【1】ヒトゲノムから染色体へ
- 遺伝病を理解するためのヒトゲノム入門編【2】DNAの構造
- 遺伝病を理解するためのヒトゲノム入門編【3】染色体の構造
- 遺伝病を理解するためのヒトゲノム入門編【4】ヒトゲノムを構成するもの
- 遺伝病を理解するためのヒトゲノム【5】ゲノム情報伝達の仕組み:基礎編
- 遺伝病を理解するためのヒトゲノム【6】ゲノム情報伝達の仕組み:細胞周期
- 遺伝病を理解するためのヒトゲノム【7】ゲノム情報伝達の仕組み:減数分裂
- 遺伝病を理解するためのヒトゲノム【8】ゲノム情報伝達の仕組み:配偶子形成と受精減数分裂