目次
- 1 1. ASS1遺伝子とは:基本情報とゲノム上の位置
- 2 2. 酵素機能:尿素サイクルとアンモニア解毒の要
- 3 3. 免疫応答での働き:マクロファージのNO産生とフェイルセーフ機構
- 4 4. ASS1遺伝子変異が引き起こす疾患:シトルリン血症1型(CTLN1)
- 5 5. ASS1とがん:多種多様な悪性腫瘍で発現が抑え込まれる
- 6 6. なぜがん細胞はあえてASS1を切るのか:ピリミジン合成のハイジャック
- 7 7. アルギニン枯渇療法:ペガルギミナーゼ(ADI-PEG20)という革新
- 8 8. アルギニン枯渇療法への耐性メカニズムと克服戦略
- 9 9. 新たな研究領域:胎盤発生・ぶどう膜炎バイオマーカー
- 10 10. ASS1遺伝子検査と臨床診療:誰がいつ受けるべきか
- 11 よくある質問(FAQ)
- 12 関連記事
- 13 参考文献
📍 クイックナビゲーション
ASS1遺伝子は、第9染色体長腕(9q34.11)に位置し、生体内の窒素代謝の中核を担う「アルギニノコハク酸合成酵素」をコードする極めて重要な遺伝子です。肝臓におけるアンモニア解毒から、免疫細胞の病原体撃退、さらにはがん細胞の代謝的弱点を突く新世代の標的治療まで、現代医学の幅広い領域で注目を集めています。
Q. ASS1遺伝子はどんな働きをしていて、なぜ医学的に重要なのですか?
A. ASS1は、有毒なアンモニアを無害化する「尿素サイクル」の鍵酵素をコードする遺伝子です。機能が失われると新生児期から重篤な高アンモニア血症(シトルリン血症1型)を引き起こす一方、多くのがん細胞ではこの遺伝子の発現が意図的に抑え込まれており、それが現在のがん代謝標的治療の重要なターゲットとなっています。
- ➤遺伝子の位置と構造 → 第9染色体9q34.11、機能するコピーは1つのみ
- ➤酵素の働き → シトルリンとアスパラギン酸からアルギニノコハク酸を合成する
- ➤関連疾患 → シトルリン血症1型(常染色体劣性遺伝、新生児期発症型〜成人発症型)
- ➤がん治療標的 → ペガルギミナーゼ(ADI-PEG20)による「アルギニン枯渇療法」
- ➤最新の知見 → 胎盤発生、ぶどう膜炎バイオマーカー、耐性克服戦略
1. ASS1遺伝子とは:基本情報とゲノム上の位置
ASS1(Argininosuccinate Synthase 1)遺伝子は、第9染色体長腕の9q34.11領域に位置するヒト遺伝子です。窒素代謝とアミノ酸生合成において中心的役割を担う「アルギニノコハク酸合成酵素」というタンパク質をコードしています。
興味深いことに、進化の過程で生じた遺伝子重複の結果、ヒトゲノムにはASS1の偽遺伝子(pseudogenes)を含めて約10〜14個のコピーが様々な染色体上に散在しています。しかし、機能的なアルギニノコハク酸合成酵素タンパク質を産生できるのは、第9染色体上のこの単一コピーのみです。この遺伝子からは同一のタンパク質をコードする2種類の転写バリアントが生成されます。
💡 用語解説:アルギニノコハク酸合成酵素(ASS)とは
シトルリンとアスパラギン酸を結合させて「アルギニノコハク酸」という分子を合成する酵素です。この反応にはエネルギー源であるATPが必要で、生体内のアルギニン生合成経路における「ボトルネック(律速段階)」として機能します。肝臓では尿素サイクルを介したアンモニア解毒、その他の組織では局所的なアルギニン供給を担う、極めて多機能な酵素です。
どこで発現しているのか:全身組織での広範な存在
かつてASS1は「肝臓の尿素サイクル専用の酵素」と考えられていましたが、現在では哺乳類のほぼすべての組織で発現していることが明らかになっています。具体的には消化器系、中枢神経系、皮膚などの外皮系、腎臓を含む後腎、感覚器など、多様な解剖学的部位に分布しています。
細胞内では主にミトコンドリア外膜・細胞体線維・核周部に局在し、エネルギー代謝と物質輸送のハブとして機能します。さらに、ASS1の活性は概日リズム(サーカディアンリズム)の制御下にあり、CLOCKタンパク質によるアセチル化を介して尿素生成プロセスに日内変動をもたらすことも報告されています。
2. 酵素機能:尿素サイクルとアンモニア解毒の要
ASS1がコードする酵素は、肝臓のミトコンドリア外膜の外側に結合した状態で存在し、ミトコンドリア内部と細胞質をまたぐ「尿素サイクル」を空間的・生化学的に橋渡しする位置にあります。タンパク質の分解やアミノ酸の代謝で絶え間なく生じる強力な神経毒「アンモニア」を、水溶性で無害な「尿素」へと変換し、腎臓を経由して体外へ排出する——この生命維持に不可欠な代謝経路の中核を、ASS1が担っているのです。
💡 用語解説:尿素サイクル(オルニチン回路)とは
タンパク質代謝で生じる有毒なアンモニアを、無害な尿素に変換するための代謝経路です。肝臓のミトコンドリアと細胞質をまたぐ形で、6つの酵素反応を通じて段階的に進行します。アンモニアは血液脳関門を容易に通過し、ごくわずかな濃度上昇でも脳浮腫や意識障害を引き起こすため、このサイクルは生命維持の根幹をなす経路といえます。
ASS1が触媒する具体的な反応
ASS1酵素の働きを化学反応として表すと、次のようになります。
生成されたアルギニノコハク酸は、次の酵素であるアルギニノコハク酸リアーゼ(ASL)によってアルギニンとフマル酸に分解され、アルギニンはさらにアルギナーゼによってオルニチンと尿素に変換されます。ASS1とASLの協調的な働きが、体内組織におけるアルギニンの生合成を担保する中核的な仕組みです。
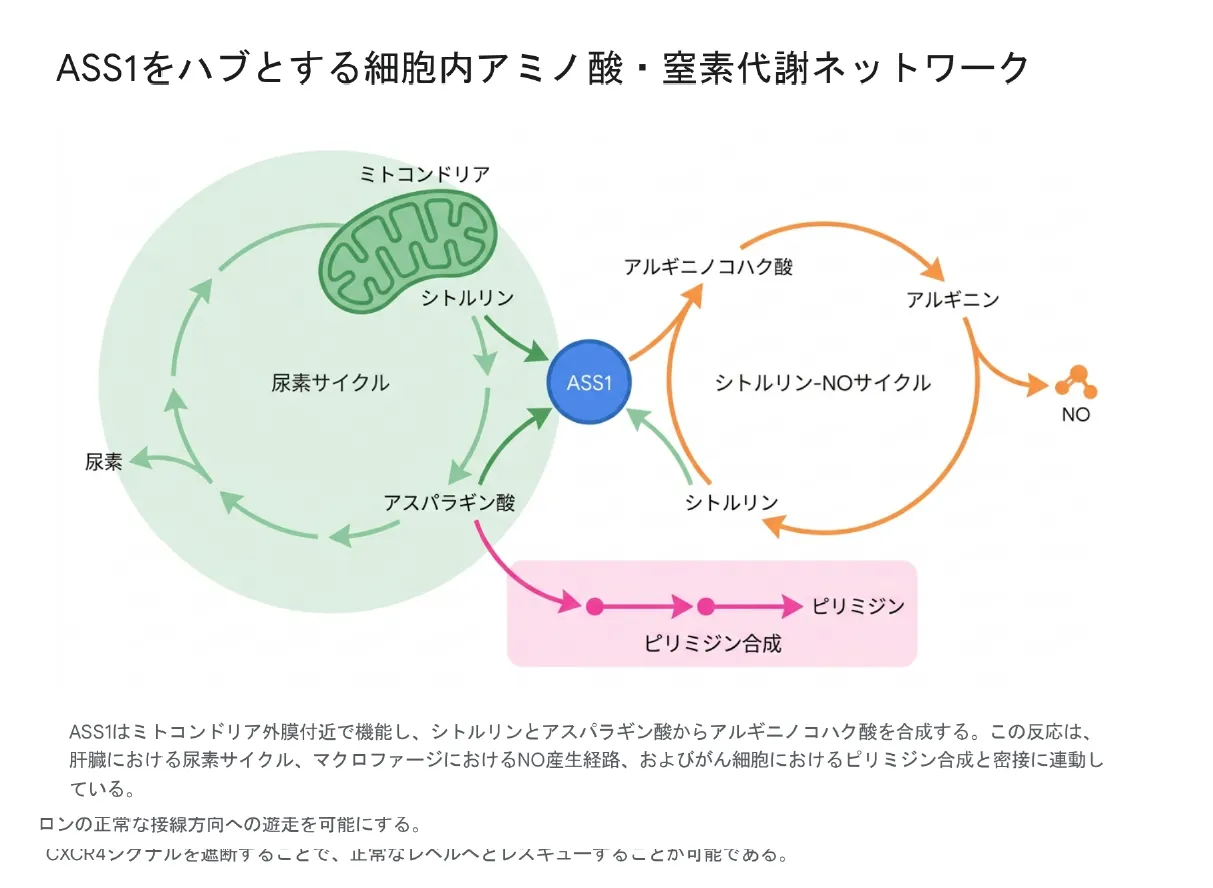
下図は、ASS1を中心としたアミノ酸・窒素代謝ネットワーク全体を視覚化したものです。ASS1がミトコンドリア外膜付近で機能し、尿素サイクル・シトルリン-NOサイクル・ピリミジン合成という3つの主要経路の交差点(ハブ)として働いていることが一目でわかります。
ASS1はミトコンドリア外膜付近で機能し、シトルリンとアスパラギン酸からアルギニノコハク酸を合成する。この反応は、肝臓における尿素サイクル、マクロファージにおけるNO産生経路、およびがん細胞におけるピリミジン合成と密接に連動している。
「細胞内アルギニンプール」を提供するハブ酵素
ASS1の重要性は単に肝臓のアンモニア処理だけにとどまりません。ASS1の酵素活性は、一酸化窒素(NO)合成酵素やポリアミン合成酵素など、アルギニンを基質とする他の代謝酵素に対して独立した「細胞内アルギニンプール」を供給する役割を果たしています。このコンパートメント化された局所的アルギニン合成は、細胞のシグナル伝達や増殖制御において欠かせない仕組みです。
🔍 関連記事:遺伝形式|常染色体優性劣性・X染色体連鎖・ミトコンドリア遺伝・多因子遺伝 — 常染色体劣性遺伝の仕組みについて詳しく解説しています。
3. 免疫応答での働き:マクロファージのNO産生とフェイルセーフ機構
肝臓での尿素合成という古典的な役割とは別に、免疫系(特にマクロファージ)においてASS1は抗菌防御の要として全く異なる働きを見せます。これは、ASS1が単なる代謝酵素ではなく、生体防御の最前線に立つ多機能タンパク質であることを示す代表例です。
💡 用語解説:一酸化窒素(NO)と免疫
一酸化窒素(NO)は強力な殺菌作用を持つ反応性窒素種の前駆体であり、マクロファージが侵入してきた細菌や寄生虫を撃退するための「化学兵器」として機能します。NOはアルギニンを原料に「誘導型一酸化窒素合成酵素(iNOS / NOS2)」によって産生され、副産物として「シトルリン」が生じます。このシトルリンを再びアルギニンに戻すのがASS1の役割です。
シトルリン-NOサイクルというフェイルセーフ機構
感染初期、マクロファージは周囲に存在する細胞外アルギニンを大量に取り込み、爆発的なNOバーストを起こして病原体を攻撃します。しかし高出力のNO産生が続くと、やがて細胞外のアルギニンは枯渇してしまいます。
この絶望的なアルギニン枯渇状態において、マクロファージはASS1とASLの発現を強力に誘導し、一度排出したシトルリンを再び細胞内に取り込んで自力でアルギニンを再合成し始めます。これが「シトルリン-NOサイクル」と呼ばれる、慢性感染において持続的なNO産生を維持するための究極のフェイルセーフシステムです。
実際に、結核菌(マイコバクテリウム)感染モデルでは、ASS1を遺伝的に欠損させたマクロファージはアルギニン枯渇後にシトルリンを再利用できず、NOレベルが急減し、感染を制御できなくなることが証明されています。ASS1は単なる代謝酵素ではなく、慢性感染症から身を守るための司令塔でもあるのです。
4. ASS1遺伝子変異が引き起こす疾患:シトルリン血症1型(CTLN1)
ASS1遺伝子の機能喪失型変異(Loss-of-function)は、尿素サイクルの進行を決定的に阻害し、毒性代謝産物が血中・組織内に異常蓄積する重篤な先天性代謝異常症「シトルリン血症1型(Citrullinemia Type I:CTLN1)」を引き起こします。古典型シトルリン血症とも呼ばれるこの疾患は、常染色体劣性遺伝形式をとります。
💡 用語解説:常染色体劣性(潜性)遺伝とは
「常染色体」とは性染色体(X・Y)以外の染色体です。「劣性(潜性)」とは、2本の染色体の両方に変異がある場合に初めて症状が現れる遺伝形式を指します。片方だけに変異がある人は「保因者(キャリア)」と呼ばれ、通常は症状が出ません。両親がともに保因者の場合、子どもが発症する確率は理論上25%です。CTLN1はこの遺伝形式に従う代表的な疾患の一つです。
病態の核心:高アンモニア血症と神経毒性
ASS1酵素の機能不全により、肝臓は過剰な窒素を尿素へと処理できなくなり、その結果として毒性の高いアンモニアが血中に蓄積(高アンモニア血症)します。アンモニアは血液脳関門を容易に通過し、中枢神経系に対して強力な毒性を発揮するため、細胞浸透圧の不均衡による重篤な脳浮腫や不可逆的な神経細胞損傷を招きます。
臨床型のスペクトラム
CTLN1の臨床表現は、発症年齢と重症度に応じて連続的なスペクトラムを形成します。残存するASS酵素活性が正常の8%以下では重篤な急性発症型に、8%を超える場合は比較的軽度な遅発型になる傾向があります。
🚨 新生児急性型(古典型)
最も重篤な形態。出生時は正常に見えるが、生後数日以内に哺乳不良・嘔吐・進行性嗜眠が出現。神経筋緊張亢進・痙攣など頭蓋内圧亢進兆候が急速に悪化。生後1週間以内に67%が発症。即座の血液透析・アンモニア除去療法を要し、生存例でも重度神経学的欠損が残るリスクが高い。
⚠️ 遅発型
小児期以降〜成人期に発症する軽症型。激しい頭痛・暗点・運動失調・不明瞭発語などの神経症状を伴う高アンモニア血症エピソードを反復。近年では神経症状より先に「原因不明の肝不全」が初発症状として現れるケースが認識されている。
🤰 妊娠期・産褥期発症型
幼少期から無症状だった女性が、妊娠や分娩に伴う急激な代謝的ストレスやタンパク質異化の亢進を契機に、急性肝不全を含む重篤な高アンモニア血症を突然発症。母子ともに生命の危機に瀕する可能性があり、速やかな集中治療が必要。
😴 無症候型
新生児マススクリーニングなどで発見される軽度のシトルリン血症などの生化学的異常を持つが、少なくとも10歳まで、あるいは生涯にわたって臨床症状を呈さない個体。発症リスクはゼロではないため予防的経過観察が推奨される。
🔍 関連記事:シトルリン血症(シトリン欠損症)の詳細解説 — シトルリン血症1型・2型の症状、診断、治療について専門医がさらに詳しく解説しています。
診断の決め手:生化学検査と分子遺伝学的検査
CTLN1の診断は、以下の生化学的特徴の組み合わせから疑われます。
- ➤血漿アンモニア濃度の著しい上昇(通常150 µmol/L以上、急性期には2000〜3000 µmol/Lに達することも)
- ➤血漿シトルリン濃度の顕著な上昇(通常500 µmol/L以上)
- ➤アルギニノコハク酸の血中検出なし(後続酵素ASLの欠損疾患との鑑別点)
- ➤培養線維芽細胞でのASS酵素活性測定による残存活性評価(重症度予測)
最終的な確定診断は、ASS1遺伝子に生じた両アレル性の病的バリアントを分子遺伝学的検査で同定することによって行われます。中東・中国・日本など世界中の多様な民族集団において多数の病的変異が同定されており、遺伝子型と表現型の相関関係の解明が進められています。
5. ASS1とがん:多種多様な悪性腫瘍で発現が抑え込まれる
がん生物学の領域において、ASS1は今や単なる代謝酵素ではなく、がん細胞の増殖戦略と脆弱性を決定づける「代謝のマスターレギュレーター」として認識されています。驚くべきことに、非常に多くの種類の悪性腫瘍でASS1の遺伝子発現が意図的に低下、あるいは完全に消失していることが明らかになっています。
ASS1発現が低下する主ながん種
悪性胸膜中皮腫、メラノーマ(悪性黒色腫)、肝細胞がん、腎細胞がん、前立腺がん、粘液線維肉腫、卵巣がん、上咽頭がん、フィラデルフィア染色体陽性(Ph+)/Ph-likeのB細胞性急性リンパ芽球性白血病(B-ALL)、食道腺がん、膠芽腫、平滑筋肉腫、急性骨髄性白血病(AML)など
💡 用語解説:エピジェネティック・サイレンシング
DNA塩基配列そのものを変えずに、遺伝子の「読まれ方」を抑え込んで発現をオフにする現象です。代表的な仕組みが「DNAメチル化」で、遺伝子のスイッチ領域(プロモーター)に化学的なマーク(メチル基)が付くことで、その遺伝子を読み取るための機械が近づけなくなります。多くのがんで、ASS1のプロモーターはこのメチル化によって「ロック」されています。
最近の非小細胞肺がん(NSCLC)研究では、強力な発がん性ドライバー変異である「KRAS変異」の活性化が、エピジェネティックなサイレンシングを起動してASS1の転写を直接抑制することが発見されました。つまり、強力な発がんシグナルが自発的に窒素代謝経路を書き換えているのです。
「アルギニン要求性」というがん細胞のアキレス腱
ASS1がサイレンシングされると、がん細胞は自力でシトルリンからアルギニンを合成する能力を失います。急速増殖のために大量のアミノ酸を必要とするがん細胞は、生存に必要なアルギニンを「細胞外からの取り込み」に100%依存しなければなりません。
💡 用語解説:アルギニン要求性(Arginine Auxotrophy)
細胞がアルギニンを自分で作れず、外部から取り込まなければ生きていけない状態を指します。正常細胞はASS1が機能しているため、シトルリンからアルギニンを合成できますが、ASS1欠損がん細胞はこの能力を失っており、外部供給が絶たれると死滅します。この弱点こそが、後述する「アルギニン枯渇療法」のターゲットとなります。
6. なぜがん細胞はあえてASS1を切るのか:ピリミジン合成のハイジャック
「なぜがん細胞は自らの生存に必要なアミノ酸の合成経路をわざわざ遮断するのか?」——長年の謎でした。近年の画期的な研究により、ASS1のサイレンシングはアルギニン不足という代償を払ってでも、核酸合成を爆発的に加速させるための「積極的な代謝再プログラミング」であることが解明されました。
アスパラギン酸の「シャント(方向転換)」
ASS1が触媒する正常反応では、シトルリンとアスパラギン酸が消費されます。ASS1の発現が抑制されると、余ったアスパラギン酸が細胞内にだぶつき、がん細胞はこの余剰アスパラギン酸を、DNAやRNAの構成要素を生産する「ピリミジン合成経路」へと大規模に方向転換させます。
ASS1はCAD酵素を分解する「腫瘍抑制因子」だった
さらに踏み込んだ最新研究で、ASS1はピリミジン合成の律速酵素であるCAD(Carbamoyl-phosphate synthetase 2など3酵素を持つ複合酵素)と直接結合し、E3ユビキチンリガーゼ「STUB1」を呼び寄せてCADをユビキチン化・分解する働きを持つことが発見されました。
つまり、ASS1はCADを破壊することでピリミジン合成にブレーキをかける、強力な「腫瘍抑制因子」として機能していたのです。肝細胞がん患者でASS1が低下すると、CADは分解を免れて異常に蓄積し、ピリミジン合成が暴走します。臨床データでは、「低ASS1・高CAD発現」の患者は最も予後が不良であることが確認されています。
7. アルギニン枯渇療法:ペガルギミナーゼ(ADI-PEG20)という革新
ASS1欠損がんが抱える「アルギニン要求性」という弱点は、がん細胞だけを選択的に兵糧攻めにする「アルギニン枯渇療法」という革新的アプローチを生み出しました。この分野を牽引するファースト・イン・クラス(画期的)の標的薬が「ペガルギミナーゼ(Pegargiminase / ADI-PEG20)」です。
💡 用語解説:ペガルギミナーゼ(ADI-PEG20)とは
細菌由来のアルギニン分解酵素「アルギニンデイミナーゼ(ADI)」に、ポリエチレングリコール(PEG)を化学結合させた標的抗がん剤です。静脈内投与すると血中アルギニンを酵素的に分解してシトルリンに変換します。正常細胞はASS1が機能しているためシトルリンから自力でアルギニンを再合成できますが、ASS1欠損がん細胞はそれができず、アミノ酸飢餓状態に陥ってアポトーシス(細胞死)に至ります。
ATOMIC-Meso第III相試験:中皮腫で全生存期間を延長
ペガルギミナーゼの臨床的有効性は、最も治療困難ながんの一つである「悪性胸膜中皮腫(MPM)」を対象としたグローバル第III相試験「ATOMIC-Meso試験」によって決定的に証明されました。中皮腫の中でも「肉腫様」「二相性」と呼ばれる非上皮型サブタイプは特に予後不良ですが、同時にASS1発現が欠如している頻度が極めて高いという特徴があります。
- 全生存期間(OS)中央値:ペガルギミナーゼ併用群9.3ヶ月 vs プラセボ群7.7ヶ月
- 3年生存率:ペガルギミナーゼ群はプラセボ群の4倍
- 平均6ヶ月以上にわたる病勢安定(Stable Disease)達成
- グレード3以上の有害事象:28.8% vs 16.9%(多くは管理可能な血液毒性)
この結果を受け、ペガルギミナーゼの臨床応用範囲は急性骨髄性白血病(AML)、膠芽腫、肝細胞がん、平滑筋肉腫、食道腺がん、B細胞性急性リンパ芽球性白血病(B-ALL)など、ASS1欠損を特徴とする多様な悪性腫瘍へと急速に拡大しています。さらに、がん領域を超えて非アルコール性脂肪肝炎(NASH)の治療薬としての評価も進行中です。
精密医療の鍵:ASS1免疫染色によるバイオマーカー診断
食道腺がんを対象とした最新研究では、97腫瘍の免疫組織化学染色解析の結果、6.2%の患者がASS1の完全喪失、さらに6.2%が低発現を示しました。つまり食道腺がん患者の約12.4%がアルギニン枯渇療法の適格基準を満たす可能性があります。ASS1の免疫染色を生検評価に組み込むことが、術前補助療法の戦略最適化のための精密医療バイオマーカーとして重要であることを強く示唆しています。
🔍 関連記事:リキッドバイオプシーforモニター — 血液中のがん由来DNAを解析することで、治療効果や再発を低侵襲かつ定量的にモニタリングできる革新的検査です。
8. アルギニン枯渇療法への耐性メカニズムと克服戦略
ペガルギミナーゼは優れた抗腫瘍ポテンシャルを持ちますが、長期投与により多くのがん細胞(特に肉腫など)が驚くべき適応能力を発揮し、薬剤耐性を獲得することが臨床上の最大の壁となっています。耐性メカニズムは多岐にわたり、それぞれに対する克服戦略が研究されています。
耐性① ASS1の自律的再発現
メカニズム:飢餓ストレス下でASS1プロモーターの脱メチル化が起こり、c-MycがHIF-1αを打ち破ってASS1転写を再起動。アルギニンを自力で合成できるようになる。
対応策:エピジェネティック修飾薬、c-Mycシグナル経路阻害薬の検討。
耐性② 代謝経路の再配線
メカニズム:アルギニン枯渇下で、TCAサイクルを回し続けるためにグルタミン代謝への依存度が極端に高まる。
対応策:グルタミナーゼ(GLS1)阻害剤の併用による「合成致死」誘導。
耐性③ 腫瘍微小環境からの救済
メカニズム:周囲の線維芽細胞が放出する細胞外小胞をマクロピノサイトーシスで貪食し、オートファジーで分解してアルギニンを再利用。
対応策:イミプラミン(抗うつ薬)またはクロロキン(抗マラリア薬)による補給路遮断。
耐性④ ピリミジン合成の暴走
メカニズム:ASS1欠損によるCAD安定化と余剰アスパラギン酸により、核酸合成が爆発的に促進される。
対応策:カペシタビン、ペメトレキセドなどのピリミジン合成阻害剤を併用。
💡 用語解説:マクロピノサイトーシスとオートファジー
マクロピノサイトーシス(細胞の飲作用)とは、細胞が周囲の液体や大きな分子を無差別に飲み込むプロセスです。オートファジー(自食作用)は、取り込んだ物質を細胞内のリソソームで分解し、アミノ酸などに再利用する仕組みです。アルギニン枯渇に苦しむがん細胞は、これら2つの機構を組み合わせて、周囲の正常細胞のタンパク質を「食べる」ことで生き延びていたのです。
特筆すべきは、これらの非カノニカル耐性メカニズムが、FDAによって既に承認されている安全で安価な既存薬(イミプラミン・クロロキン)によって完全にブロックできることが証明されている点です。これらを現行のペガルギミナーゼ療法に追加する新たな臨床試験設計が強く推奨されており、患者の予後を飛躍的に向上させる可能性を秘めています。
9. 新たな研究領域:胎盤発生・ぶどう膜炎バイオマーカー
ASS1の役割はがんと先天性代謝異常の領域にとどまりません。近年の研究は、ASS1が他の重要な生理学的プロセスや炎症性疾患の進行を示す高感度バイオマーカーとしても機能していることを明らかにしています。
胎盤形成における低酸素応答と分化制御
初期妊娠における正常な胎盤形成と発達には、ASS1由来の一酸化窒素(NO)産生が不可欠です。妊娠第1三半期の胎盤において、ASS1タンパク質は増殖能を維持する細胞群「絨毛細胞栄養膜」に高発現していますが、細胞外栄養膜への分化が進むにつれて意図的にダウンレギュレーションされることが確認されています。
これらの過程の破綻や低酸素応答の異常は、流産・妊娠高血圧腎症(PE)・胎児発育遅延(IUGR)といった重篤な妊娠合併症の根本原因となる可能性が指摘されています。胎児期の肺発生プロセスにおいてもASS1の関与が示唆されており、ASS1の発生学的役割は今後さらに研究が進展する分野です。
ぶどう膜炎の活動性バイオマーカー
眼科領域において、ASS1は重篤な眼内炎症性疾患「ぶどう膜炎(Uveitis)」の臨床的バイオマーカーとして特定されています。前房水・硝子体液・涙液を用いたプロテオミクス解析でASS1レベルの変動が眼内の炎症状態を反映するため、免疫抑制剤の安全な休薬時期を見極めるための客観的指標として注目されています。
10. ASS1遺伝子検査と臨床診療:誰がいつ受けるべきか
ASS1遺伝子検査が必要となる場面は、大きく以下の3つに分類されます。
① 確定診断目的(CTLN1が疑われる場合)
新生児マススクリーニングでシトルリン高値が指摘された場合、または重篤な高アンモニア血症エピソードを呈する乳幼児・小児・成人において、ASS1遺伝子の両アレル性病的変異の同定が確定診断となります。妊娠期に突然発症した急性肝不全・脳症の鑑別においても重要です。
② 保因者(キャリア)診断と家族計画
CTLN1は常染色体劣性遺伝のため、家系内に患者がいる場合の他の家族員の保因者診断、および結婚・妊娠を考えるカップルのキャリアスクリーニングが重要です。両親がともに保因者であった場合、子どもの発症リスクは25%、保因者となるリスクは50%です。
🔍 関連記事:キャリアスクリーニングとは / 米国人類遺伝学会の推奨内容 — 妊娠前・妊娠初期に受けるキャリアスクリーニングについて、専門医が詳しく解説しています。
③ がん診療における腫瘍特性評価
悪性胸膜中皮腫・肝細胞がん・特定の白血病など、アルギニン枯渇療法の適応を検討する際のバイオマーカー検査として、腫瘍組織におけるASS1免疫染色や発現解析が行われます。今後はASS1メチル化状態を血液で評価する非侵襲的モニタリング(リキッドバイオプシー)も期待されています。
出生前診断という選択肢
家系内にCTLN1患者がいて、両親の病的変異が同定されている場合、羊水検査や絨毛検査による出生前遺伝子診断が選択肢として存在します。次子の妊娠を計画している方は、妊娠前から臨床遺伝専門医に相談することをお勧めします。
よくある質問(FAQ)
🏥 ASS1遺伝子検査・遺伝カウンセリングについて
ASS1遺伝子検査・シトルリン血症1型のご相談・
がん診療における腫瘍特性評価まで、臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
関連記事
参考文献
- [1] NCBI Gene Database. ASS1 argininosuccinate synthase 1 [Homo sapiens] (Gene ID: 445). [NCBI Gene]
- [2] UniProtKB. ASS1 – Argininosuccinate synthase – Homo sapiens (Human). [UniProt P00966]
- [3] Quinonez SC, Thoene JG. Citrullinemia Type I. GeneReviews®. University of Washington, Seattle. [GeneReviews / NBK1458]
- [4] Husson MC, et al. Argininosuccinate synthase: at the center of arginine metabolism. Int J Biochem Cell Biol. [PMC3074183]
- [5] Qualls JE, et al. Sustained generation of nitric oxide and control of mycobacterial infection requires argininosuccinate synthase 1. Cell Host Microbe. [PMC3444824]
- [6] Rabinovich S, et al. Diversion of aspartate in ASS1-deficient tumours fosters de novo pyrimidine synthesis. Nature. 2015. [PubMed 26560030]
- [7] ASS1 inhibits liver cancer by promoting CAD ubiquitination. Hepatology Communications. [PMC12363443]
- [8] Beddowes E, Szlosarek PW, et al. Pegargiminase Plus First-Line Chemotherapy in Patients With Nonepithelioid Pleural Mesothelioma: The ATOMIC-Meso Randomized Clinical Trial. JAMA Oncol. [PMC10870227]
- [9] Sun N, Zhao X. Argininosuccinate synthase 1, arginine deprivation therapy and cancer management. Front Pharmacol. 2022. [PMC9335876]
- [10] Discovery and Targeting of a Noncanonical Mechanism of Sarcoma Resistance to ADI-PEG20 Mediated by the Microenvironment. Cancer Discov. [PMC10425734]
- [11] Innate and adaptive resistance mechanisms to arginine deprivation therapies in sarcoma and other cancers. Front Oncol. [PMC8992531]
- [12] Downregulation of argininosuccinate synthase 1 (ASS1) is associated with hypoxia in placental development. Histochem Cell Biol. [PubMed 36995581]
- [13] Errera FIV, et al. Protein Biomarkers in Uveitis. Front Immunol. [PMC7744561]
- [14] MedlinePlus Genetics. ASS1 gene. [MedlinePlus]
- [15] Chu YD, et al. Unlocking the Potential of Arginine Deprivation Therapy: Recent Breakthroughs and Promising Future for Cancer Treatment. Int J Mol Sci. 2023. [PMC10341449]