目次
AP1S2遺伝子は、X染色体短腕(Xp22.2)に位置し、細胞内でタンパク質を正確な目的地に届ける「AP-1複合体」のσ1B(シグマ1B)サブユニットをコードする遺伝子です。全身の細胞で広く発現しながらも、その変異が脳神経系にのみ集中した重篤な障害を引き起こすという生物学的に興味深い特性を持ちます。AP1S2の機能喪失変異は、X連鎖劣性遺伝形式をとる稀少な神経発達障害「Pettigrew症候群(ペティグルー症候群)」の直接的な原因遺伝子として確立されています。
Q. AP1S2遺伝子とはどのような遺伝子ですか?まず結論だけ知りたいです
A. X染色体短腕(Xp22.2)に位置し、細胞内タンパク質輸送を担うAP-1複合体のσ1Bサブユニットをコードする遺伝子です。全身に広く発現しながらも脳神経系で不可欠な特異的役割を果たし、この遺伝子の変異がX連鎖性稀少神経発達障害「Pettigrew症候群」を引き起こします。
- ➤遺伝子の基本情報 → X染色体Xp22.2に位置し、複数の転写バリアントを持ち、脳・精巣上体で際立った高発現
- ➤AP-1複合体の構造 → ヘテロ四量体の4サブユニット構成と、Arf1・PI(4)Pによる膜上での活性化メカニズム
- ➤σ1Bの特異的機能 → ジロイシンモチーフを持つカーゴタンパク質を正確に認識し、小胞形成を誘導する分子メカニズム
- ➤機能的冗長性のパラドックス → 末梢ではAP1S1・AP1S3が代償できるが、脳ではσ1B固有の要件が存在する理由
- ➤Notchシグナルとの接点 → 神経幹細胞の運命決定を支配するNotchシグナル分子の空間的統制とAP1S2の役割
- ➤関連疾患・遺伝子検査 → Pettigrew症候群・アダプチン異常症の概念と、利用できる遺伝子検査の選択肢
1. AP1S2遺伝子の基本プロフィール
AP1S2(Adaptor Related Protein Complex 1 Subunit Sigma 2)遺伝子は、ヒトゲノムにおいてX染色体短腕のXp22.2バンドにマッピングされており、物理的座標としておよそ15,825,806塩基対(bp)から15,854,931 bpの領域を占めています。マウスにおけるオルソログはマウスX染色体のF5バンドに位置しており、哺乳類全般にわたって高度に保存された遺伝子座です。ゼブラフィッシュ(Danio rerio)でもCRISPR/Cas9によるノックアウトラインが構築されており、受精後24〜48時間に特定の脳領域で顕著な発現が確認されています。
💡 用語解説:遺伝子座・バンド(Xp22.2)とは
染色体を特殊な染料で染色すると、明暗のバンドパターンが現れます。「Xp22.2」は「X染色体(X)・短腕(p)・第2領域2番バンド(22.2)」を示す番地です。X染色体に乗った遺伝子は、男性(XY)は1本しか持たないため変異があると症状が出やすく、女性(XX)は2本持つため片方が正常なら症状が出にくい(保因者)という特徴があります。
転写産物の多様性:選択的スプライシングとアイソフォーム
AP1S2遺伝子は選択的スプライシングおよび選択的ポリアデニル化シグナルを利用して複数の転写バリアントを生成します。遺伝子近傍にはENSG00000289237などの長鎖ノンコーディングRNA(lncRNA)やAP1S2P1という偽遺伝子が存在し、このゲノム領域の複雑な制御構造を示しています。
💡 用語解説:選択的スプライシングとアイソフォーム
遺伝子のDNAがmRNAへ転写された後、タンパク質をコードしない「イントロン」が除かれ「エクソン」がつなぎ合わされます。この「つなぎ方のパターン」を変えることを選択的スプライシングと言い、1つの遺伝子から構造・機能が少しずつ異なる複数のタンパク質(アイソフォーム)が生み出されます。AP1S2では脳と末梢でアイソフォームの使い分けがあり、これが「脳特異的機能」を理解する重要な鍵です。
組織発現プロファイル:脳と精巣上体で際立つ高発現
Human Protein AtlasやBgeeデータベースのRNA発現データによると、AP1S2はユビキタスな(全身性の)発現パターンを持ちながら、脳組織と精巣上体で特に発現レベルが際立って高くなっています。脳内では黒質・視床下部室傍核・弓状核・乳頭体・橋核・神経節隆起などで最高レベルの発現が観察されます。これらの領域は自律神経機能・運動制御・高次内分泌制御に深く関与しており、後述するPettigrew症候群の多様な神経症状の発生基盤と解剖学的に一致します。大脳皮質を含むほとんどの脳領域でニューロンの細胞体に顆粒状のタンパク質局在が確認されており、小胞輸送ネットワークの中心として機能していることが形態学的にも裏付けられています。
2. AP-1複合体の生化学的構造と活性化メカニズム
AP1S2遺伝子が単独で機能することはなく、細胞内では「AP-1複合体(アダプタータンパク質複合体1)」と呼ばれる大きなタンパク質集合体(ヘテロ四量体)の一員として機能します。全身の細胞内膜系で働き、必要なタンパク質を正しい場所に届ける「仕分けシステム」の中核です。
💡 用語解説:AP-1複合体とは
AP-1複合体(Adaptor Protein complex 1)は、細胞内の膜系——特にトランスゴルジ網(TGN)やエンドソーム——に存在し、輸送すべきタンパク質(カーゴ)を認識してクラスリン被覆小胞の形成を誘導するタンパク質複合体です。荷物を仕分けして配達車(小胞)に積み込む「仕分けセンター」のスタッフにたとえられます。AP複合体にはAP-1からAP-5まで5種類あり、それぞれ異なる細胞内区画で機能します。
💡 用語解説:トランスゴルジ網(TGN)とクラスリン被覆小胞
トランスゴルジ網(TGN)はゴルジ体の出口側に位置する膜構造で、タンパク質が合成・加工された後に「どこに送るか」を最終的に仕分けする場所です。
クラスリン被覆小胞はTGNやエンドソームの膜から出芽して形成される輸送ベシクル(小胞)で、クラスリンというタンパク質が籠状に外側を覆います。AP-1複合体がこの小胞形成を誘導し、AP1S2はその中核的なサブユニットです。
ヘテロ四量体の構成:4サブユニットの役割分担
| サブユニット | 該当するタンパク質 / 遺伝子 | 主な役割 |
|---|---|---|
| ラージサブユニット1 | γ1(AP1G1)またはγ2(AP1G2) | クラスリンの動員、膜への繋留、アクセサリータンパク質の結合 |
| ラージサブユニット2 | β1(AP1B1) | クラスリン重鎖との直接的な相互作用(ヒンジ・イヤー領域) |
| ミディアムサブユニット | μ1A(AP1M1)またはμ1B(AP1M2) | チロシンベース選別シグナル(YXXØ)の認識 |
| スモールサブユニット | σ1A(AP1S1)、σ1B(AP1S2)、σ1C(AP1S3) | ジロイシンベース選別シグナル(XXXL[LI])の認識、複合体全体の構造的安定化 |
スモールサブユニット(σ1)にはAP1S1(σ1A)・AP1S2(σ1B)・AP1S3(σ1C)という3種類のアイソフォームが存在し、細胞の種類や状態に応じて使い分けられます。このサブユニット構成の多様性が、AP1S2欠損時に脳以外では機能が代償される一方、脳神経系では代償されにくいという「機能的冗長性のパラドックス」の根本原因です。
Arf1とPI(4)Pによる膜上でのアロステリック活性化
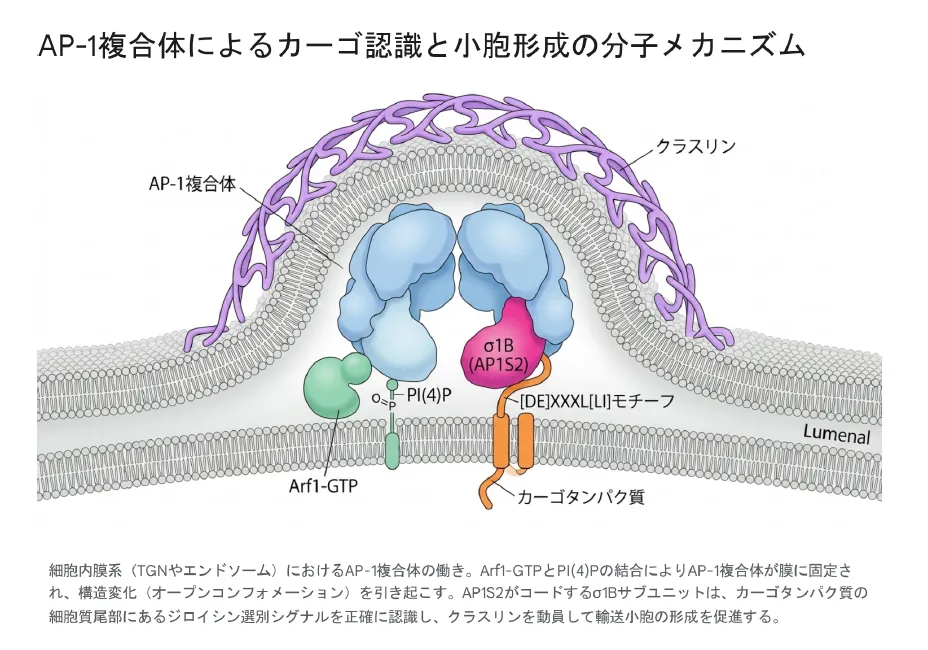
AP-1複合体は通常、不活性な「閉じた」コンフォメーションで細胞質に溶けて存在しています。TGNやエンドソームの膜上で活性化されるには2つの引き金が必要です。① GTP結合型のArf1(低分子量GTPアーゼ)と② 膜上のPI(4)P(ホスファチジルイノシトール4-リン酸)が同時に結合すると、複合体は劇的な立体構造変化(アロステリック変化)を起こし「オープンコンフォメーション」へ移行します。この構造変化により、μサブユニットとσサブユニット(AP1S2)のカーゴ結合ポケットが露出し、輸送すべきタンパク質との相互作用が可能になります。
細胞内膜系(TGNやエンドソーム)におけるAP-1複合体の働き。Arf1-GTPとPI(4)Pの結合によりAP-1複合体が膜に固定され、構造変化(オープンコンフォメーション)を引き起こす。AP1S2がコードするσ1Bサブユニットは、カーゴタンパク質の細胞質尾部にあるジロイシン選別シグナルを正確に認識し、クラスリンを動員して輸送小胞の形成を促進する。
3. AP1S2(σ1B)による特異的なカーゴ認識
AP-1複合体の標的となるカーゴタンパク質は多岐にわたりますが、AP1S2がコードするσ1Bサブユニットは、カーゴタンパク質の細胞質領域に存在する特定の「住所タグ」を読み取ることで正しい仕分けを実現しています。
💡 用語解説:ジロイシンベースシグナルとカーゴ認識
細胞内を輸送されるタンパク質(カーゴ)には、「どこへ送るか」を示す特定のアミノ酸配列が存在します。σ1Bが認識するのは「ジロイシンベースシグナル(XXXL[LI])」——ロイシン(L)またはイソロイシン(I)が並んだ特徴的な配列です。この特定の配列を読み取ることでタンパク質を正しいエンドソームや細胞膜へ仕分けます。このタグの読み間違いが「ミスソーティング(誤選別)」と呼ばれ、AP1S2変異による細胞機能障害の直接的なメカニズムです。
AP1S2が管理するカーゴタンパク質は細胞の種類によって異なります。脂肪細胞においてはソルチリン(sortilin)と呼ばれるタンパク質の仕分けを介して脂肪細胞の分化を制御しており、ニューマン・ピック病C型に関与するタンパク質群の輸送にもAP-1を介した細胞内トラフィックが関与しています。
一方、神経細胞においてσ1Bが担当するカーゴには、シナプス後部受容体・イオンチャネル・Notchシグナル関連タンパク質(Sanpodoなど)など、脳機能に直結する分子群が含まれます。これらは末梢では別のアイソフォームによって代替可能ですが、脳ではσ1B(AP1S2)でなければ仕分けできないという厳密な要件が存在します。
4. 機能的冗長性のパラドックス:なぜ脳だけが障害を受けるのか
AP1S2遺伝子の最も興味深い特性の一つは、全身の細胞で広く発現し基本的な小胞輸送に不可欠でありながら、その機能喪失が主に脳神経系に限定された重篤な表現型をもたらすという「機能的冗長性のパラドックス」です。
💡 用語解説:機能的冗長性とは
機能的冗長性(Functional Redundancy)とは、ある遺伝子やタンパク質が失われても、他の類似した分子が同じ機能を肩代わりできる状態です。AP-1複合体のスモールサブユニットには3種類(σ1A・σ1B・σ1C)があり、末梢組織ではこれらが互いに代替可能です。しかし特定の細胞タイプや高負荷の状況では「代替不可能な固有の要件」が存在します。
脳神経系でσ1B(AP1S2)が代替されにくい理由
① 超高速・超高頻度のトラフィック
シナプス形成や高頻度の神経伝達が行われる脳では、小胞輸送のトラフィック量は末梢細胞の比ではありません。σ1Bが代替されても「量」が間に合わない状況が生じます。
② σ1B依存性の特異的カーゴ
神経細胞には、σ1B(AP1S2)単独に依存する特定のカーゴ分子や輸送経路が存在し、σ1Aやσ1Cでは物理的に代替できません。
Pettigrew症候群の患者から採取された線維芽細胞では、AP1S2変異によりσ1Bが欠失していてもAP-1複合体全体の安定性・小胞輸送機能に致命的な異常は観察されませんでした。これはAP1S1・AP1S3が代償できるためです。しかし脳では複数の理由から代償が成立せず、微小かつ脳特異的なAP-1依存性タンパク質トラフィックの破綻が蓄積して不可逆的な神経ネットワーク異常へとつながります。
5. 神経発生・脳機能におけるAP1S2の特異的役割
神経系の完全性は、分子レベルのロジスティクスであるAP-1複合体の機能に全面的に依存しています。AP1S2が欠損した状態では以下の主要な神経生理学的プロセスが直接的な悪影響を受けます。
5-1. ソマトデンドリティック極性輸送とシナプス小胞の再構築
💡 用語解説:ソマトデンドリティック極性輸送とシナプス小胞
ソマトデンドリティック極性輸送とは、ニューロン(神経細胞)の細胞体で合成された受容体やイオンチャネルを、軸索(信号を送る側)ではなく樹状突起(信号を受け取る側)へと選択的に輸送する仕組みです。この輸送が乱れるとシナプスに必要な分子が正しく配置されず、脳の情報処理能力が大きく低下します。
シナプス小胞は神経伝達物質(グルタミン酸やGABAなど)を格納する直径約40nmの小さな膜袋です。神経伝達物質を放出した後、膜に吸収(エンドサイトーシス)されて再び新しいシナプス小胞として再構築(リサイクル)されます。この再構築プロセスにAP1S2が深く関与します。
σ1B欠損マウス(Ap1s2 KOマウス)を用いた実験では、高頻度の神経刺激を与えるとシナプス小胞の再構築が間に合わず、シナプス前終末の内部に巨大なエンドソーム中間体が異常蓄積し、シナプス小胞の総数が減少することが電子顕微鏡解析で確認されています。その結果、学習障害・長期空間記憶の重度な欠損・運動協調性の低下が引き起こされます。
5-2. 銅トランスポーター(ATP7A)の軸索輸送への影響
AP-1複合体は銅イオンを輸送するP型ATPaseであるATP7Aの細胞内トラフィックも制御しています。AP-1による制御が損なわれるとATP7Aが軸索や細胞膜へと異常に放出され、末梢性運動ニューロパチーの病態生理学的基盤となることが指摘されています。ただし、AP1S1変異によるMEDNIK症候群のような広範な銅代謝障害はPettigrew症候群では生じない点が重要な鑑別点です(詳細はセクション7)。
5-3. 神経幹細胞の運命決定とNotchシグナル伝達の統制
💡 用語解説:Notchシグナル伝達と神経幹細胞の運命決定
Notchシグナル伝達経路は、隣接する細胞同士のNotch受容体とリガンドの相互作用によって細胞の運命(何の細胞になるか)を決定する重要なシグナル経路です。哺乳類の大脳皮質発生では、放射状グリア細胞(RGC)と呼ばれる神経幹細胞が非対称分裂を繰り返し、タイミングよく多様なニューロンを生み出します。Notchシグナルがこのタイミングと運命決定を厳密に制御しており、乱れると分化のタイミングが狂って脳構築が異常をきたします。
Notchシグナルの活性化状態は「Sanpodo」や「Numb」と呼ばれるタンパク質の細胞内局在によって決定されます。AP-1複合体による極性輸送が欠損するとSanpodoの局在が乱れ、Notchシグナルが不適切に活性化または阻害されます。AP1S2の欠損は「輸送の停滞」にとどまらず、細胞運命を左右するマスターシグナル(Notch)の空間的統制を崩壊させ、生み出されるべきニューロンの多様性の喪失や脳構造の構築異常を直接的に引き起こします。先天性水頭症・PVNH・Dandy-Walker奇形といったPettigrew症候群の脳形態異常の根本には、この分子レベルの崩壊があると考えられています。
6. がん・腫瘍学研究との新たな接点
AP1S2をはじめとするAP-1複合体は主に神経機能の文脈で研究されてきましたが、近年のバイオインフォマティクス解析により、がんの病態や進展においても重要な役割を果たしていることが明らかになってきています。
- ➤AP1M1はB型肝炎ウイルスによって発現が亢進し、がん細胞の増殖促進や脳転移のバイオマーカーとなる可能性が指摘されています。
- ➤AP1M2は上皮細胞の基底膜におけるβ1インテグリンの輸送を制御し、転移を抑制する「細胞固有の抗がんメカニズム」として機能する側面を持ちます。
- ➤AP1G1の発現レベルが高い患者群では、活性酸素種(ROS)による細胞死誘導に対する生存率が高く、AP-1複合体のがん細胞に対する内因性防御への関与が示唆されています。
- ➤AP1S2・AP1S3を含む他のサブユニットも、細胞周期の制御・低酸素応答(Hypoxia)・上皮間葉移行(EMT)における発現変動が示されています。
AP1S2を直接ターゲットとしたがん治療への応用研究は現時点では発展途上にありますが、AP複合体全体のネットワークが腫瘍微小環境においても重要な機能を担っている可能性が示されています。
7. AP1S2変異と関連疾患:アダプチン異常症の世界
AP-1複合体のサブユニットに生じた遺伝的欠陥によって引き起こされる疾患群は、総称して「アダプチン異常症(Adaptinopathies)」と呼ばれます。AP1S2の病態を正確に理解するためには、パラログ遺伝子であるAP1S1などの変異がもたらす疾患との比較が不可欠です。
💡 用語解説:アダプチン異常症(Adaptinopathies)とは
AP複合体を構成するサブユニット遺伝子の変異によって引き起こされる疾患群の総称です。各サブユニットが認識する特異的なカーゴタンパク質の種類が異なるため、どのサブユニットに変異が生じるかによって全く異なる臓器・システムが障害を受ける独自の臨床像が現れます。これは「カーゴ特異性の違いが疾患特異性を生む」という精密な分子レベルの分業を示しています。
| 疾患名 | 原因遺伝子 | 主な病態メカニズム | 主要な臨床症状 |
|---|---|---|---|
| Pettigrew症候群(PGS) | AP1S2(σ1B) | シナプス小胞再構築障害・樹状突起への極性輸送障害・Notchシグナル分子の局在異常。銅代謝障害は生じない | 重度知的障害、水頭症、Dandy-Walker奇形、大脳基底核石灰化、てんかん発作、運動障害 |
| MEDNIK症候群 | AP1S1(σ1A) | 銅トランスポーターATP7A・ATP7BのTGNから細胞膜へのトラフィック異常。広範な銅代謝障害 | 精神遅滞、腸症、難聴、末梢神経障害、魚鱗癬、メンケス病+ウィルソン病様症状 |
| KIDAR症候群 | AP1B1(β1) | ラージサブユニットの異常。ATP7Aのトラフィック異常が見られるが肝毒性には至らない | 角膜炎、魚鱗癬、難聴 |
| Usmani–Riazuddin症候群 | AP1G1(γ1) | AP-1複合体の膜繋留・クラスリン動員の阻害。常染色体優性遺伝 | 神経・発達関連の異常 |
AP1S1変異のMEDNIK症候群とAP1S2変異のPettigrew症候群の決定的な違いは「銅代謝異常の有無」です。MEDNIK症候群ではATP7A/Bのミスソーティングにより血清銅濃度の上昇と肝臓への銅蓄積が生じるのに対し、Pettigrew症候群ではこのような広範な銅代謝障害は報告されていません。これは進化的に獲得されたアイソフォーム間の厳密な機能分担とカーゴ特異性を明確に裏付けています。
AP1S2変異タイプと症状発現傾向:遺伝子型と表現型の相関
これまでに特定されたAP1S2変異の大半はナンセンス変異またはスプライシング変異です。変異の種類と発現しやすい症状の間に相関関係が明らかになってきています。
AP1S2変異タイプと主要症状の発現傾向
小頭症(Microcephaly)
スプライス部位変異
ナンセンス変異
過去に報告されたAP1S2変異患者の臨床データ分析(NCBI・MedNexusを参考に作成)
スプライス部位変異 → てんかん発作が多い
「不完全だが存在するAP1S2タンパク質」が正常なAP-1複合体の形成を阻害するドミナント・ネガティブ効果を発揮し、神経伝達物質の受容体局在を著しく乱すことで、てんかん原性ネットワーク(PVNHなど)を形成しやすくなると考えられています。
ナンセンス変異 → 小頭症が多い
タンパク質の完全な喪失により、神経幹細胞の増殖期におけるNotchシグナル依存的な細胞分裂や生存そのものが深刻な打撃を受け、発生初期段階から脳容積全体の成長が停止して小頭症に至ると推論されています。
💡 用語解説:X連鎖劣性遺伝とは
X連鎖劣性遺伝(X-linked recessive)とは、X染色体上の遺伝子に変異がある場合、男性(XY)は変異したX染色体を1本しか持たないため症状が現れやすく、女性(XX)は正常なX染色体がもう1本あれば症状が出にくい(保因者)という遺伝形式です。AP1S2変異によるPettigrew症候群は、この遺伝形式をとるため罹患者のほとんどが男性となります。患者の多くは変異を持ちながら無症状の「保因者の母親」から変異を受け継いでいます。
8. AP1S2に関連する遺伝子検査と遺伝カウンセリング
原因不明の重度X連鎖性知的障害・先天性水頭症・大脳皮質形成異常(PVNH)を呈する患者に対しては、次世代シーケンシング(NGS)を用いた遺伝子検査が推奨されます。AP1S2は国際的な「X連鎖性知的障害パネル」に必須項目として含まれており、Blueprint Genetics社などが提供するパネルにも収載されています。
ミネルバクリニックで利用できる関連検査
X連鎖遺伝疾患の保因者(キャリア)である女性へ
AP1S2変異の保因者(キャリア)である女性は通常症状を呈しませんが、男児に変異を伝える確率が50%あるため、妊娠前または妊娠中の遺伝カウンセリングが強く推奨されます。ミネルバクリニックでは保因者検査から出生前診断まで一貫した体制でサポートしています。妊娠前の遺伝子検査については専用ページもご覧ください。
X連鎖劣性遺伝疾患の保因者として診断を受けた方の心理的体験や家族計画の考え方については、副腎白質ジストロフィー(ALD)に関する以下のコラムが参考になります(ALDはABCD1遺伝子による別の疾患ですが、X連鎖劣性遺伝で母親が保因者となるメカニズムはAP1S2と共通しています)。
キャリアスクリーニングが自分にとって必要かどうかについては、「キャリアスクリーニングとは」のページで詳しく解説しています。
よくある質問(FAQ)
🏥 AP1S2遺伝子・Pettigrew症候群に関するご相談
希少遺伝性疾患・X連鎖遺伝・保因者検査について、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
関連記事
参考文献
- [1] GeneCards. AP1S2 Gene — AP1S2 Protein / AP1S2 Antibody. [GeneCards]
- [2] NCBI Gene. AP1S2 adaptor related protein complex 1 subunit sigma 2 [Homo sapiens (human)]. Gene ID: 8905. [NCBI Gene]
- [3] Bonifacino JS, et al. New directions for the clathrin adaptor AP-1 in cell biology and human disease. J Cell Biol. 2022. [PMC9187608]
- [4] Bhavnani S, et al. Adaptor Proteins in Neurological Disorders. Journal of Bio-X Research. 2023. [MedNexus]
- [5] Glyvuk N, et al. AP-1/σ1B-adaptin mediates endosomal synaptic vesicle recycling, learning and memory. EMBO J. 2010;29(8):1318-1330. [PMC2868567]
- [6] Tarpey PS, et al. Mutations in AP1S2 Cause X-Linked Mental Retardation. Am J Hum Genet. 2006;79(6):1119-1124. [PMC1698718]
- [7] Cacciagli P, et al. Clinical, cellular, and neuropathological consequences of AP1S2 mutations. Am J Med Genet A. 2008. [PubMed 18428203]
- [8] Li H, et al. Role of adaptin protein complexes in intracellular trafficking and their impact on diseases. Cell Commun Signal. 2021. [PMC8806629]
- [9] Martinelli D, et al. Direct interactions of adaptor protein complexes 1 and 2 with the copper transporter ATP7A. Mol Biol Cell. 2015. [PMC4383858]
- [10] Lesca G, et al. A novel splice site mutation in AP1S2 gene for X-linked mental retardation syndrome. Mol Genet Genomic Med. 2019. [PMC6422709]
- [11] ERN ITHACA. Understanding AP1S2-related disorders. European Reference Network. [ERN ITHACA]
- [12] NCBI MedGen. Pettigrew syndrome (Concept Id: C0796254). [NCBI MedGen]