目次
- 1 1. ピュリノソームとは?——2008年、細胞の中に「代謝の工場」が発見された
- 2 2. ピュリノソームの分子アーキテクチャ——コア・周辺・シャペロンの三層構造
- 3 3. 細胞内の「住所」と代謝チャネリングの驚異——通常の7倍の効率
- 4 4. 形成メカニズムの解明:液-液相分離(LLPS)とユビキチン化制御
- 5 5. 動的制御:細胞周期・mTOR・CK2・GPCRとの連動
- 6 6. がんとピュリノソーム——「依存症」と次世代の治療戦略
- 7 7. 神経発達とピュリノソーム——大脳皮質形成異常・難治性てんかんとの関わり
- 8 8. ピュリノソーム関連の遺伝子検査・臨床応用
- 9 よくある質問(FAQ)
- 10 参考文献
- 11 関連記事
📍 クイックナビゲーション
ピュリノソーム(プリノソーム、英: Purinosome)とは、細胞がDNAやRNAの材料となるプリン塩基をゼロから合成するときに限って出現する、特殊な多酵素複合体です。6種類の酵素が時空間的に精密に集合し、まるで「小さな工場」のように代謝反応を効率化します。2008年の発見以来、がん・神経発達・希少遺伝性疾患との深い関わりが次々と明らかになり、現在では次世代の精密医療の重要な研究対象として世界的に注目を集めています。
Q. ピュリノソーム(プリノソーム)とは何ですか?まず結論だけ知りたいです
A. 細胞がプリン塩基をゼロから合成する「デノボ合成」を行うとき、6種類の酵素が動的に集合して形成される超分子複合体(メタボロン)です。プリン枯渇時に出現し、合成効率を通常の最大7倍に高める機能を持ちます。がん増殖・脳発達・希少遺伝性疾患にも深く関わる、細胞の生存戦略の要です。
- ➤発見の経緯 → 2008年Benkovic研究チームによる画期的な可視化、「メタボロン」仮説の実証
- ➤分子構成 → コア酵素(PPAT・GART・FGAMS)と周辺酵素(PAICS・ADSL・ATIC)の二層構造+シャペロン群
- ➤形成メカニズム → 液-液相分離(LLPS)とASB11–PAICS–UBAP2ユビキチン化制御軸
- ➤がんとの関係 → 「ピュリノソーム依存症」とDRP-104を用いた合成致死戦略
- ➤神経発達との関係 → Nwd1–PAICS相互作用と大脳皮質形成異常・難治性てんかんとの関わり
1. ピュリノソームとは?——2008年、細胞の中に「代謝の工場」が発見された
💡 用語解説:プリン塩基とは
プリン塩基(プリン)とは、アデニン(A)とグアニン(G)の総称で、DNAやRNAの構成要素です。ATP(細胞のエネルギー通貨)・GTP・cAMP(細胞内シグナル)など、生命維持に不可欠な多くの分子の基盤となっています。細胞がプリンを得る方法は大きく2つあります。①サルベージ経路:使い終わった塩基をリサイクルする(省エネ)、②デノボ合成経路:ゼロから新規に合成する(エネルギーコストは高い)——ピュリノソームはこの「デノボ合成」の現場に登場する分子工場です。
私たちの細胞は、増殖・DNA修復・シグナル伝達のためにプリン塩基を絶え間なく必要としています。通常の状態では、使い終わったプリンをリサイクルするサルベージ経路が主役を担いますが、急速な細胞増殖や胚発生、あるいはがん化が起きてプリン需要が急増すると、細胞は「ゼロからプリンを作る」デノボプリン合成(DNPB)を強力に稼働させます。
このデノボ合成は10段階もの連続する酵素反応からなる複雑な経路で、出発原料のホスホリボシルピロリン酸(PRPP)から共通のプリン前駆体であるイノシン5′-一リン酸(IMP)が合成されます。長年、生化学者たちはこれらの酵素が細胞質に無秩序に浮遊しているはずがない——もっと高度に組織化されているのではないかという「メタボロン仮説」を提唱してきました。
💡 用語解説:メタボロン(Metabolon)とは
代謝経路に関わる複数の酵素が物理的に集合し、中間代謝物を次の酵素へ直接受け渡す「代謝の超複合体」のことです。バケツリレーのように中間産物を外に逃がさず効率的に受け渡すことで、反応速度を飛躍的に高め、不安定な中間体が細胞質に拡散して悪影響を与えることを防ぎます。ピュリノソーム(プリノソーム)は、哺乳類細胞において生きた細胞内で初めて可視化されたメタボロンとして歴史的な位置づけを持ちます。
この数十年来の仮説を実証したのが、2008年のStephen J. Benkovic研究チームによる画期的な研究です。ヒト細胞内においてデノボプリン合成に関わる6種類の主要酵素が、プリン枯渇という特定の条件下で一箇所に集まり、動的な多酵素複合体を形成することを蛍光顕微鏡で初めて視覚的に証明しました。この複合体に「ピュリノソーム(プリノソーム、Purinosome)」と名付けられたのです。
2. ピュリノソームの分子アーキテクチャ——コア・周辺・シャペロンの三層構造
ピュリノソーム(プリノソーム)は単に酵素が偶然集まったものではなく、精緻な役割分担に基づく三層構造を持つことが明らかになっています。
ピュリノソームの三層構造(概略図)
分子シャペロン(構造安定化・液滴流動性制御)
周辺酵素
周辺酵素
周辺酵素
コア(足場)酵素群 — 複合体の骨格
プリン枯渇時、ミトコンドリアと微小管の界面に形成。コア酵素を中心に周辺酵素・シャペロンが動的に集合し、代謝フラックスを最大7倍に高める。
コア酵素群:複合体全体の「骨格」となる3種
コア酵素群は、ピュリノソーム全体の構造的完全性を保つための強固な足場(スキャフォールド)です。互いに強力かつ持続的な相互作用を形成し、複合体の「芯」となります。
PPAT
ホスホリボシルピロリン酸アミドトランスフェラーゼ。デノボ合成の第1段階(律速段階)を触媒。スキャフォールドの核となる。プリンが豊富な環境でのみAKTリン酸化(Thr397)を受けることが最近判明。
GART(TGART)
第2・3・5段階を一手に担う三機能性酵素。複数の機能領域を1本のポリペプチドに統合した、真核生物特有の多機能酵素の典型例。
FGAMS(PFAS)
ホルミルグリシンアミジンリボヌクレオチドシンターゼ。第4段階を触媒し、コア足場の中心的一翼を担う。ミトコンドリア分画からも共単離される。
周辺酵素群:環境に応じて動的に集合・解離する3種
PAICS
二機能性酵素で第6・7段階を担う。ASB11によるK6ユビキチン化の標的となり、液-液相分離(LLPS)を引き起こす引き金となる重要な分子。
ADSL
アデニロコハク酸リアーゼ。第8・13段階を担う。ADSL遺伝子の変異はアデニロサクシナーゼ欠損症を引き起こす。
ATIC
二機能性酵素で第9・10段階(最終2段階)を担い、IMP合成を完結させる。経路の「締め」を担う重要な周辺酵素。
分子シャペロン:複合体の「品質管理と流動性制御」を担う
ピュリノソームにはHSP70・HSP90・DnaJA1・DnaJc7といった熱ショックタンパク質(分子シャペロン)が恒常的に組み込まれています。これらは単にタンパク質の折りたたみを助けるだけでなく、ピュリノソームという巨大超分子複合体の立体構造を安定化させ、液滴としての流動性を積極的に制御するという役割を担います。Hsp90を阻害する薬剤(17-AAGなど)を投与すると、ピュリノソームは直接崩壊します。
💡 AlphaFold3でも再現できない「アロステリックな構造最適化」
AI構造予測ツールAlphaFold3でPAICSの三次元構造を予測すると、実験的に解明された実際の構造(PDB: 7ALE)と基質チャネルの配置・対称軸に重大な不一致が生じます。その理由は、ピュリノソームの各酵素が単独では不完全な構造を持ち、他の5酵素と複合体を形成することで初めて正確な触媒コンフォメーションが完成する(アロステリックな構造最適化)からだと考えられます。ピュリノソームが単なる「酵素の集合」ではなく、高度に協調した超分子システムであることを示す証拠です。
3. 細胞内の「住所」と代謝チャネリングの驚異——通常の7倍の効率
ピュリノソーム(プリノソーム)が細胞質のどこに形成されるかは、決して無作為ではありません。超解像顕微鏡を用いた精密なイメージング研究により、ピュリノソームはミトコンドリアの表面と微小管細胞骨格の界面に特異的に局在することが明らかになっています。
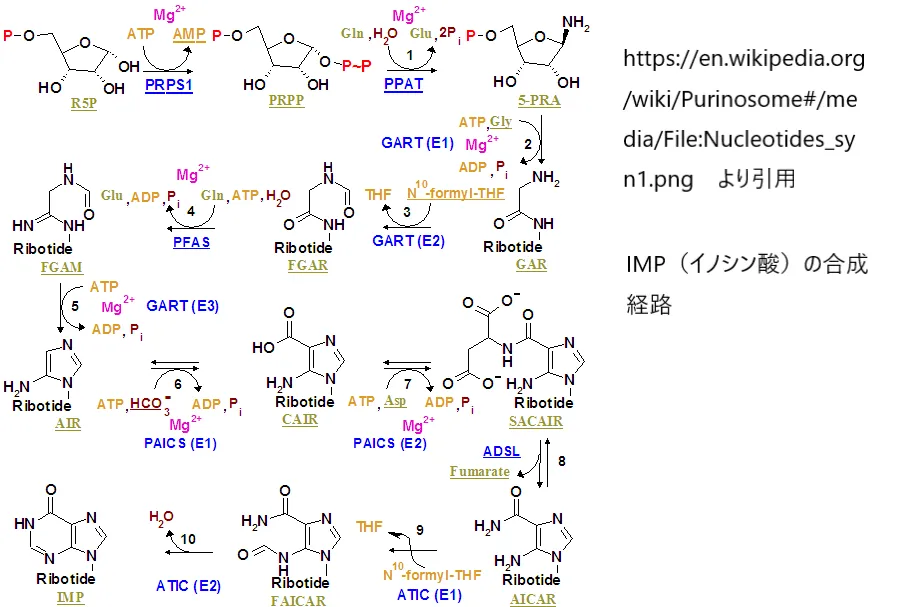
デノボプリン合成経路(PRPP→IMP)の10段階。各ステップをコア酵素・周辺酵素が担い、ピュリノソーム内で連続的に反応が進む。
💡 用語解説:基質チャネリング(Substrate Channeling)とは
ある酵素反応で生じた中間産物(基質)が、細胞質溶液に拡散することなく直接隣の酵素へ受け渡される現象です。バケツリレーのようなイメージです。これにより、①反応速度が飛躍的に向上、②不安定・有毒な中間体による細胞へのダメージを防ぐ、③競合する別の代謝経路への「横取り」を防ぐ——という3つの利点が同時に実現されます。
ミトコンドリアとの関係は特に重要です。ミトコンドリアの機能が障害されたり、呼吸鎖阻害剤(アンチマイシンAなど)にさらされると、細胞はこれをエネルギー危機として認識し、代償的にピュリノソームの形成を増強してデノボ経路を活性化させます。ミトコンドリアがピュリノソームの組み立てを監督する「センサー」として機能している可能性があります。
最先端の代謝物マッピング技術(GCIB-SIMS)を用いた解析では、ピュリノソームが形成されている細胞内領域でATPが異常に高濃度で濃縮されていることが確認されました。この基質チャネリングにより、プリン枯渇下のHeLa細胞ではデノボ合成経路全体の代謝フラックスが最大7倍向上することが報告されています。
4. 形成メカニズムの解明:液-液相分離(LLPS)とユビキチン化制御
💡 用語解説:液-液相分離(LLPS:Liquid-Liquid Phase Separation)とは
油と水が混ざらずに分離するように、細胞内でタンパク質や核酸が多価相互作用を介して自己集合し、高濃度の液滴(凝縮相)と周囲の希薄溶液へと自発的に分離する可逆的なプロセスです。脂質膜を持たずに区画化された微小環境を作り出す「膜なしオルガネラ(Membraneless organelle)」を形成します。ストレス顆粒やP-bodyと同じ原理で成立し、ピュリノソームもこの「液滴形成」によって組み立てられることが確立されています。
顕微鏡下でピュリノソーム(プリノソーム)を観察すると、均一な球状の集合体として振る舞い、互いに近づくと水滴が合体するように融合します。この流動的な液滴としての特性こそが、「固い不溶性の凝集体ではないか?」という初期の批判を退け、機能的なメタボロンとして確立する決定的な根拠となりました。
ASB11–PAICS–UBAP2制御軸:ユビキチン化が液滴形成を引き起こす
2023年のブレイクスルーで解明されたのが、ASB11–PAICS–UBAP2という分子軸です。ピュリノソーム形成のトリガーとなる精緻な翻訳後修飾カスケードを順に説明します。
STEP 1:ASB11の発現上昇
代謝ストレスを細胞が検知すると、エピジェネティックな仕組みを通じてCul5ユビキチンリガーゼ複合体の認識アダプター「ASB11」の発現が顕著に増加する。
STEP 2:PAICSへのK6ユビキチン化
ASB11がPAICSの74番目のリジン残基(K74)にK6結合型ポリユビキチン鎖を付加する。分解シグナル(K48型)ではなく「空間的組織化のシグナル」として機能する点が重要。
STEP 3:UBAP2の動員
K6ユビキチン鎖を足場として、無秩序領域(IDR)を多数持つ「UBAP2」タンパク質が呼び寄せられ、多価相互作用ネットワークの物理的な原動力となる。
STEP 4:液滴(LLPS)の形成
UBAP2がLLPSを引き起こす。ユビキチン化されたPAICSを核として高濃度の液滴が急速に形成され、機能的なピュリノソームが組み立てられる。
💡 用語解説:ユビキチン化とは(K6型 vs K48型の違い)
「ユビキチン」という小さなタンパク質を標的に連結する修飾です。一般にK48型はタンパク質を分解するシグナルとして知られますが、今回のピュリノソーム形成で機能するK6型は「タンパク質の空間的組織化・相分離の誘導」というまったく別の目的で働きます。「ユビキチン化=分解」という常識を覆す発見として注目されています。
5. 動的制御:細胞周期・mTOR・CK2・GPCRとの連動
ピュリノソーム(プリノソーム)は一度形成されれば永続する静的な構造体ではなく、細胞内外の環境に応じて極めて迅速かつ可逆的に集合と解離を繰り返す動的実体です。光回復後蛍光褪色法(FRAP)による解析でも、酵素群はピュリノソーム領域へ絶え間なく流入・流出していることが確認されています。
集合と解離の主な制御因子
| 制御の方向 | 主な因子・薬剤 | 作用メカニズム |
|---|---|---|
| 集合(形成促進) | プリン枯渇環境 | サルベージ経路の供給不足→デノボ合成への需要急増 |
| HPRT欠損(レッシュ・ナイハン症候群) | サルベージ経路の完全遮断→デノボ合成への全依存 | |
| CK2阻害剤(DMAT・TBI・TBB) | キナーゼカスケード調節によりIMP産生量が約1.5倍増加 | |
| GPCRアゴニスト(α2A-AR・P2Y・PGなど) | Gαi経路→mTORC2活性化→代謝フラックス増大 | |
| ミトコンドリア呼吸鎖阻害(アンチマイシンA等) | エネルギー危機への代償的代謝リプログラミング | |
| 解離(形成阻害) | プリン補充 | 外部供給の充足→デノボ合成需要の低下 |
| Hsp90阻害剤(17-AAG・NVP-AUY922) | 複合体の折りたたみ・流動性を担うシャペロン機能の喪失 | |
| mTOR阻害(ラパマイシン) | PRPP産生抑制+ミトコンドリアとの共局在の破壊 |
💡 用語解説:mTOR(哺乳類ラパマイシン標的タンパク質)とは
細胞の栄養状態・エネルギー状態・成長因子シグナルを感知し、タンパク質合成・細胞成長・代謝全般を統括する重要なキナーゼです。mTORC1はペントースリン酸経路(PRPP産生経路)の遺伝子発現を刺激するとともに、ピュリノソームのミトコンドリアへの共局在を制御します。mTORC1の阻害剤ラパマイシンを投与するとピュリノソーム形成が顕著に抑制されることから、mTORC1が「ピュリノソーム形成を許可するマスタースイッチ」として機能していると考えられます。
ピュリノソームの形成ダイナミクスは細胞周期の進行とも精密に同期しています。HeLa細胞の解析では、DNA複製の準備期であるG1期においてピュリノソーム保有細胞の割合がピークに達し、G1→S期移行時にはプリン産生速度が最大5倍に達することが確認されています。
6. がんとピュリノソーム——「依存症」と次世代の治療戦略
がん細胞は正常細胞とは根本的に異なる代謝特性を持ちます(代謝リプログラミング)。異常な増殖を続けるために膨大なプリン塩基を必要とするがん細胞にとって、ピュリノソームによる代謝フラックスの増大は生存に直結する「ライフライン」です。多くのがん種においてデノボプリン合成酵素群が過剰発現しており、ピュリノソームの活性亢進が腫瘍の悪性化を支えています。
メラノーマが獲得した「ピュリノソーム依存症」
💡 用語解説:ピュリノソーム依存症(Purinosome Addiction)とは
特定のがん細胞が、生存・増殖・腫瘍形成能力のすべてをピュリノソームの存在に依存している状態を指します。悪性黒色腫(メラノーマ)では、液滴形成のトリガーとなるASB11が恒常的に過剰発現しており、プリン枯渇という外部ストレスがなくてもピュリノソームが常時形成された状態(構成的集合)になっています。この「がん細胞が進化の過程で得た強み」が、同時に「致命的な弱点(Vulnerability)」にもなります。
DRP-104+ドセタキセル:「がん細胞の適応行動を逆利用する」合成致死戦略
① DRP-104でプリン供給を遮断
プロドラッグDRP-104がデノボプリン合成を強力に阻害し、がん細胞に強烈なプリン枯渇ストレスを誘発する。
② がん細胞が「適応」しようとする
生存のため、がん細胞は急遽微小管上にピュリノソームを組み立て代謝効率を限界まで高めようとする。この適応によりピュリノソームが微小管に強く依存した状態になる。
③ ドセタキセルが致命打を与える
微小管安定化薬「ドセタキセル」を投与すると、ピュリノソームを微小管に依存しているがん細胞は通常より劇的に高い感受性を示し、致命的なダメージを受ける(合成致死)。
④ 免疫活性化とのシナジー
プリン枯渇によるDNA損傷蓄積がcGAS-STING経路を活性化し、抗腫瘍免疫を誘導。免疫療法との相乗効果も期待されている。
また、肝臓がんの研究では「ピュリノソームスコア」が高い患者群ほど免疫療法に対する臨床的反応が良好であるという正の相関が報告されており、ピュリノソームの形成度合いが免疫療法の効果予測バイオマーカーになりうる可能性が注目されています。
7. 神経発達とピュリノソーム——大脳皮質形成異常・難治性てんかんとの関わり
ピュリノソーム(プリノソーム)の重要性はがんにとどまりません。哺乳類の脳の発達においても、ピュリノソームは決定的な役割を果たしていることが明らかになっています。
マウスの大脳皮質発達研究から、生後0日目(P0)前後を境に、未熟な脳のプリン供給がデノボ経路からサルベージ経路へと切り替わることがわかっています。胚生期の神経幹細胞・前駆細胞(NSPC)が適切なタイミングで増殖し、大脳皮質プレートへ正確に移動するためには、ピュリノソームを介した精密なプリン代謝の時空間的調節が不可欠です。
Nwd1–PAICS相互作用:神経幹細胞でのピュリノソーム形成の調整役
この神経発生特異的なプロセスを制御する重要な因子が、神経幹細胞に高発現するタンパク質「Nwd1(NACHT and WD repeat domain-containing 1)」です。NwD1はPAICSと直接タンパク質間相互作用を形成し、生理的な条件下でのNSPC内ピュリノソーム形成のタイミングと量を厳密に調節しています。
Nwd1の発現を実験的に抑制(ノックダウン)すると、神経幹細胞内でのピュリノソームの正常な組み立てが著しく阻害されます。その結果として起こる連鎖は以下の通りです。
① ピュリノソーム形成の失敗
Nwd1欠如→PAICSの正常な集合が阻害→ピュリノソームが形成されない
② プリン供給の局所的枯渇
神経幹細胞の増殖に必要なプリン塩基の局所供給が不足する
③ NSPCの異常な早期分化
本来増殖すべきタイミングで神経幹細胞が分化してしまい、細胞周期を未熟なまま離脱する
④ 大脳皮質形成異常(PH様)
ニューロンが正しい層に到達できず脳室周囲に停留→脳室周囲結節状異所性灰白質(PH)
💡 用語解説:脳室周囲結節状異所性灰白質(PH)とは
本来なら大脳皮質の特定の層に移動すべきニューロンが、移動に失敗して脳室周囲に塊(結節)として停留した状態の大脳皮質形成異常です。ヒトでは難治性てんかん・重度の精神遅滞の主要な原因となる脳奇形です。ピュリノソームの形成失敗がこのPH様異常を引き起こすという事実は、プリン代謝と脳奇形の間の意外な関係を示すものとして注目されています。
ADSL遺伝子をはじめとするピュリノソーム関連酵素の遺伝的欠損も、同様に神経発達に重篤な影響をもたらします。アデニロサクシナーゼ欠損症では、知的障害・自閉症スペクトラム・てんかんが主要な臨床像となり、遺伝子パネルを用いた早期診断が管理方針の決定に重要です。PAICSやATICの欠損も、小頭症や神経新生障害を引き起こすことがモデル動物で確認されています。
8. ピュリノソーム関連の遺伝子検査・臨床応用
ピュリノソームを構成する酵素をコードする遺伝子の変異は、代謝疾患・神経発達疾患・てんかんとして顕在化します。以下に、関連する主な検査オプションをまとめます。
よくある質問(FAQ)
🏥 プリン代謝異常・希少遺伝性疾患について専門医に相談する
ピュリノソーム関連疾患(アデニロサクシナーゼ欠損症など)をはじめ、
代謝疾患・神経発達疾患・遺伝子検査に関するご相談はミネルバクリニックへ。
参考文献
- [1] An J, et al. Potential Mechanisms Connecting Purine Metabolism and Cancer Therapy. Front Immunol. 2018;9:1697. [Frontiers in Immunology]
- [2] Yamada H. Purinosomes and Purine Metabolism in Mammalian Neural Development: A Review. PMC. 2024. [PMC11231565]
- [3] Verrier F, et al. The purinosome, a multi-protein complex involved in the de novo biosynthesis of purines in humans. PMC. 2014. [PMC3877848]
- [4] Benkovic SJ, et al. Purinosome. Sites at Penn State – Benkovic Lab. [Penn State Benkovic Lab]
- [5] French JB, et al. Spatial Colocalization and Functional Link of Purinosomes with Mitochondria. PMC. 2016. [PMC4881839]
- [6] Pedley AM, Benkovic SJ. The Purinosome: A Case Study for a Mammalian Metabolon. PMC. 2022. [PMC9531488]
- [7] Yamada H, et al. Nwd1 Regulates Neuronal Differentiation and Migration through Purinosome Formation in the Developing Cerebral Cortex. PMC. 2020. [PMC7186558]
- [8] Purine biosynthetic enzymes assemble into liquid-like condensates dependent on HSP90. PMC. 2022. [PMC9034097]
- [9] Zhou L, et al. PAICS ubiquitination recruits UBAP2 to trigger phase separation for purinosome assembly. PubMed. 2023. [PubMed 37848033]
- [10] Doigneaux C, et al. Hypoxia drives the assembly of the multienzyme purinosome complex. Purinosome formation as a function of the cell cycle. PNAS. 2015. [PNAS]
- [11] Pedley AM, et al. A New View into the Regulation of Purine Metabolism – The Purinosome. PMC. 2017. [PMC5272809]
- [12] Zhao H, et al. Resilience and vulnerabilities of tumor cells under purine shortage. PMC. 2025. [PMC12399269]