目次
一過性新生児糖尿病2型(TNDM2)は、染色体11p15.1に位置するABCC8遺伝子の機能獲得型変異によって引き起こされる、極めて稀な単一遺伝子性糖尿病です。生後数日から数週間という早期に深刻な高血糖として発症しながらも、乳児期に一旦「寛解(症状が落ち着く時期)」を迎えるという独特の経過をたどります。しかしその名称に含まれる「一過性」という言葉が、この疾患において最大の落とし穴となっています——思春期以降に再発するリスクは50%以上あり、誤診されたまま何十年も不適切な治療を受け続けたケースが実際に報告されています。
Q. 一過性新生児糖尿病2型(TNDM2)とはどのような疾患ですか?
A. ABCC8遺伝子(染色体11p15.1)の機能獲得型変異によって膵臓ベータ細胞のKATPチャネルが正常に閉じられなくなり、インスリンが分泌できなくなる希少な遺伝性糖尿病です。新生児期に重篤な高血糖として発症し、乳児期に一旦寛解しますが、思春期以降に再発するリスクが50%以上あります。経口スルホニル尿素薬(SU薬)への移行によって、患者自身の膵臓のインスリン分泌能を回復させる劇的な治療改善が期待できます。
- ➤疾患の定義 → OMIM #610374、常染色体優性遺伝、ABCC8遺伝子ヘテロ接合性変異
- ➤分子メカニズム → KATPチャネルの機能獲得型変異によるインスリン分泌障害
- ➤鑑別の鍵 → 出生体重が正常範囲・巨舌症なし・臍ヘルニアなし(TNDM1との違い)
- ➤治療の革新 → 経口SU薬への移行で約90〜95%がインスリン注射から解放
- ➤長期管理の重要性 → 「完治」ではなく再発リスクを踏まえた生涯フォローアップが必要
1. 一過性新生児糖尿病2型(TNDM2)とは
新生児糖尿病(NDM)は、生後6ヶ月未満という非常に早い時期に発症する稀な遺伝性糖尿病の総称です。国際的な疫学調査によれば、出生約95,000〜400,000人に1人という極めて稀な頻度で発症し、発症に性別や人種による偏りは確認されていません。
💡 用語解説:新生児糖尿病(NDM)とは
生後6ヶ月未満に発症する糖尿病を「新生児糖尿病(NDM: Neonatal Diabetes Mellitus)」と呼びます。一般的な1型糖尿病(自己免疫性)とは異なり、特定の遺伝子の変異が直接の原因となる「単一遺伝子性疾患」です。膵臓の自己抗体(GAD抗体など)は陰性であることが多く、遺伝子検査によって確定診断されます。NDMは長期的な経過によって、インスリン治療が生涯必要な「永続性(PNDM)」と、乳児期に一旦治療が不要になる「一過性(TNDM)」に分類されます。
TNDMはさらに、遺伝的な原因の違いによって3つのサブタイプに分類されます。その中でTNDM2はABCC8遺伝子変異が原因のタイプ(OMIM #610374)で、TNDMの約13〜15%を占めます。
| サブタイプ | 原因遺伝子・染色体座 | メカニズム | 頻度 |
|---|---|---|---|
| TNDM1 | 6q24(PLAGL1・HYMAI) | 父方インプリンティング異常 | 約60〜70% |
| TNDM2 ★ | 11p15.1(ABCC8/SUR1) | KATPチャネル機能獲得型変異 | 約13〜15% |
| TNDM3 | 11p15.1(KCNJ11/Kir6.2) | KATPチャネル機能獲得型変異 | 約13〜15% |
★本記事で取り上げるTNDM2。TNDM2とTNDM3は合わせてTNDM全体の約30%を占める。
💡 用語解説:インプリンティングとは(TNDM1との違いを理解するために)
私たちは両親から1本ずつ、合計2本の染色体を受け継ぎ、通常はどちらのコピーも働きます。しかし一部の遺伝子では、お父さん由来のコピーだけ、またはお母さん由来のコピーだけが働くという特殊な仕組みがあります。これを「インプリンティング(刷り込み)」と呼びます。TNDM1(全TNDMの60〜70%)はこのインプリンティングの異常が原因ですが、TNDM2はインプリンティングとは無関係なABCC8遺伝子の直接的な変異が原因です。この根本的な違いが、治療法の選択にも直結します。
TNDM2はTNDM1と比べ、出生体重が正常範囲であること、巨舌症(舌が大きくなる症状)や臍ヘルニアなどの先天性奇形を伴わないことが重要な特徴です。これらの違いが、臨床現場での初期鑑別において大きな手がかりとなります。一過性新生児糖尿病(TNDM)の全体像や永続性新生児糖尿病(PNDM)についての詳細ページもあわせてご覧ください。
2. 原因遺伝子ABCC8とKATPチャネルのメカニズム
TNDM2を引き起こすABCC8遺伝子の変異は、膵臓のベータ細胞にある「KATPチャネル」という特殊なスイッチを狂わせます。このスイッチが正常に閉じられなくなることで、インスリンが血液中に分泌できなくなり、重篤な高血糖が引き起こされます。
💡 用語解説:ABCC8遺伝子とSUR1タンパク質
ABCC8(ATP Binding Cassette Subfamily C Member 8)遺伝子は、染色体11p15.1に位置し、膵臓ベータ細胞のKATPチャネルを構成するSUR1(スルホニル尿素受容体1型)というタンパク質をコードしています。SUR1はチャネルの「調節役」として機能し、スルホニル尿素薬(SU薬)が結合する部位でもあります。SUR1に異常が生じると、インスリン分泌のスイッチが適切に働かなくなります。詳細はABCC8遺伝子ページもご参照ください。
💡 用語解説:KATPチャネルの正常な役割
KATPチャネル(ATP感受性カリウムチャネル)は、膵臓ベータ細胞の「血糖センサー」です。2種類のタンパク質からなる8量体の複合体で、中心のポア(穴)部分をKir6.2(KCNJ11遺伝子産物)が4つ、外側の調節部分をSUR1(ABCC8遺伝子産物)が4つ囲んでいます。血糖が上がると細胞内のATPが増え、このチャネルが閉じます。閉じると細胞が興奮してインスリンの袋(顆粒)を放出します。つまり、KATPチャネルは「血糖値が高い!」を感知してインスリン放出の引き金を引く重要なスイッチです。
正常なインスリン分泌の流れ
血糖値が上昇 → グルコースがベータ細胞内に取り込まれ、分解される
細胞内のATP(エネルギー分子)が増える → KATPチャネルが閉じる
細胞膜の電位が変化(脱分極)→ カルシウムチャネルが開く
カルシウムが流入 → インスリン顆粒が放出される
TNDM2での異常:「開きっぱなし」のチャネル
TNDM2を引き起こすABCC8変異は「機能獲得型変異(Activating mutation)」と呼ばれるタイプです。変異したSUR1が組み込まれたKATPチャネルは、血糖値がどれだけ上がってATPが増えても、チャネルが閉じません。チャネルが開きっぱなしのため、カリウムイオンが細胞外へ流れ続け、細胞膜が脱分極せず、カルシウムが流入せず、インスリンが分泌されない——という連鎖的な機能不全が起きます。
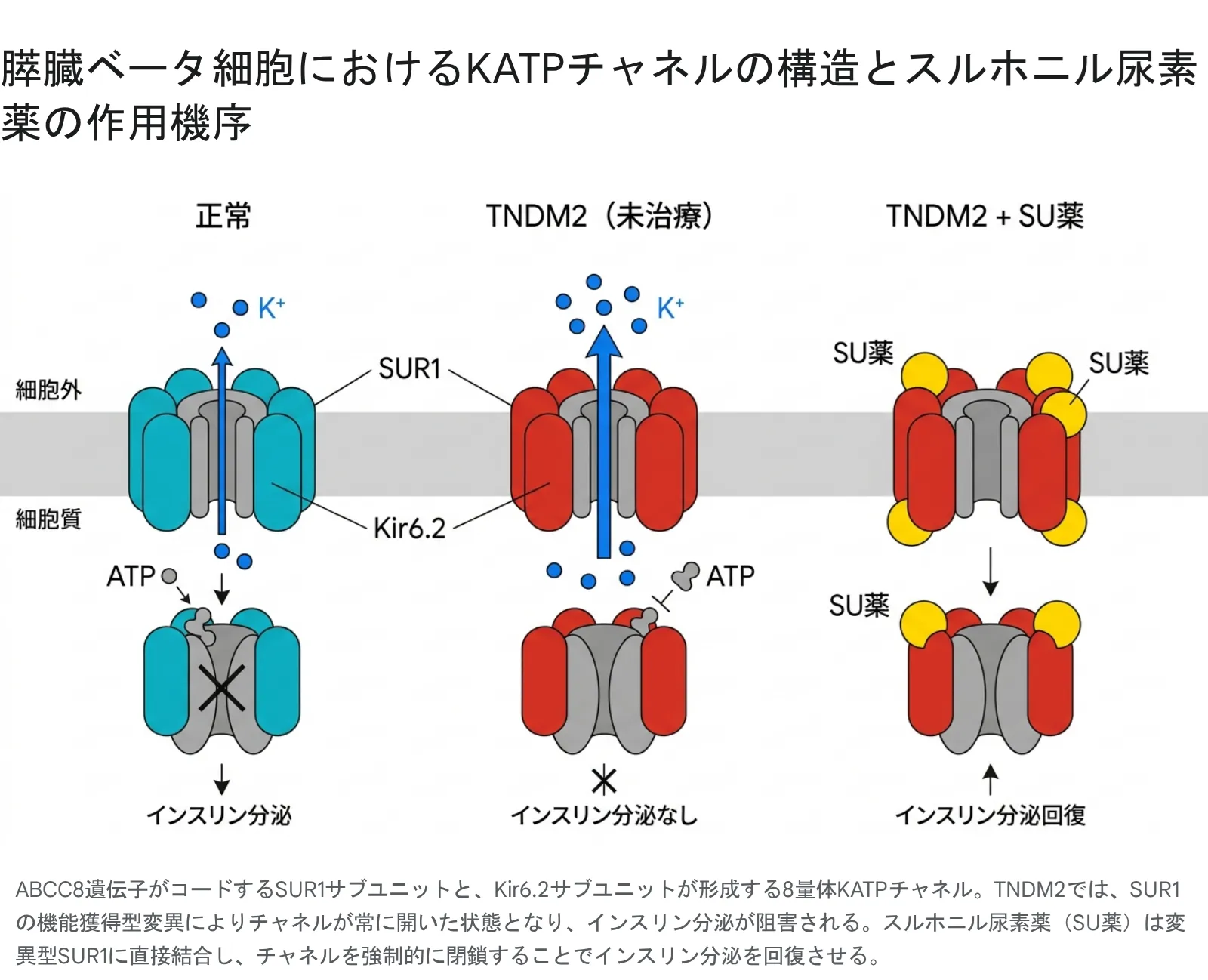
正常なベータ細胞ではATPによってKATPチャネルが閉じインスリンが分泌される(左)。TNDM2(未治療)ではABCC8変異によりチャネルが開きっぱなしとなりインスリン分泌が阻害される(中)。SU薬は変異SUR1に直接結合しチャネルを強制的に閉鎖、インスリン分泌を回復させる(右)。
💡 用語解説:機能獲得型変異とは
遺伝子変異には大きく分けて「機能喪失型(Loss of Function)」と「機能獲得型(Gain of Function)」があります。機能喪失型は遺伝子の働きが弱まる変異ですが、機能獲得型は本来あるべき機能が「過剰に」または「不適切に」発揮される変異です。TNDM2では、本来血糖が高い時だけ閉じるべきKATPチャネルが、機能獲得型変異によって血糖に関係なく「常に開いた状態」になります。この「開きっぱなし」状態がインスリン分泌の根本的な障害を引き起こします。
KATPチャネルは膵臓ベータ細胞だけでなく、脳神経系・骨格筋・心筋にも存在します。そのため、TNDM2では代謝異常だけでなく、一部の患者でジストニア(不随意運動)や視覚的統合障害などの神経発達的異常が報告されています。KCNJ11変異のTNDM3で特に顕著な「DEND症候群(発達遅滞・てんかん・新生児糖尿病)」のスペクトラムの一部が、TNDM2でも出現しうることが確認されています。
💡 用語解説:DEND症候群
DEND症候群は「Developmental delay(発達遅滞)・Epilepsy(てんかん)・Neonatal Diabetes(新生児糖尿病)」の頭文字をとった名称です。KATPチャネルが脳でも機能不全を起こした場合に現れます。主にKCNJ11変異のTNDM3に関連しますが、ABCC8変異のTNDM2でも軽症型(intermediate DEND)が認められることがあります。SU薬は血液脳関門を通過できるため、インスリンでは治療できなかった脳内のチャネル異常も是正し、神経発達予後を改善する可能性が示唆されています。
3. 主な症状と発症時期
TNDM2の症状は、胎児期からのインスリン不足による成長障害と、生後すぐからの重篤な高血糖の2つから構成されます。発症は生後3日〜74日の間に確認されるケースが大半を占め、医学的緊急事態としての迅速な対応が求められます。
🔵 主な代謝症状
- 顕著な高血糖(持続的に高い血糖値)
- 多尿(浸透圧利尿による)
- 多飲(異常なほどの水分要求)
- 重篤な脱水症状
- 糖尿病性ケトアシドーシス(DKA)のリスク
🔴 成長に関する症状
- 軽度〜中等度の低出生体重
- 子宮内発育遅延(TNDM1より軽度)
- 体重増加不良
🟣 神経学的症状(一部の患者)
- ジストニア(不随意な筋緊張異常)
- 視覚的統合障害
- 空間的認識障害
- 軽症型DENDスペクトラム
💡 用語解説:糖尿病性ケトアシドーシス(DKA)
インスリンが全く分泌されないと、細胞はエネルギーを得るために脂肪を過剰に分解し、「ケトン体」という酸性の物質が大量に産生されます。これが血液を酸性に傾け(アシドーシス)、意識障害・呼吸困難・嘔吐などを引き起こす緊急状態が糖尿病性ケトアシドーシス(DKA)です。6q24インプリンティング異常によるTNDM1ではDKAはまれとされますが、TNDM2(ABCC8変異)では生命を脅かす重度のDKAを伴って救急搬送されるケースも報告されています。ケトアシドーシスの存在はTNDM2/3またはPNDMを強く疑う根拠となります。
4. 鑑別診断:TNDM1・PNDMとどう見分けるか
新生児期に高血糖が見つかった際、臨床医が最初に直面する問いは「これはTNDM1か、TNDM2か、TNDM3か、それともPNDMか」という鑑別です。正確な診断が治療方針を左右するため、以下の臨床的特徴を見極めることが重要です。
| 特徴 | TNDM1(6q24) | TNDM2(ABCC8) | PNDM |
|---|---|---|---|
| 出生体重 | 著しく低い(SGA) | 正常〜軽度低下 | 様々 |
| 巨舌症・臍ヘルニア | 約50%に巨舌症 | 極めて稀 | 原因次第 |
| DKAのリスク | 低い | あり | あり |
| 寛解 | あり | あり | なし(永続) |
| SU薬への移行 | 困難〜不可 | 約90〜95%が可能 | ABCC8変異なら可能 |
特に重要な臨床的ポイントとして、出生体重が正常範囲で、巨舌症・臍ヘルニアなどの先天性奇形を伴わずに生後1ヶ月前後で高血糖と脱水を発症した新生児に出会った場合、臨床医はTNDM2(またはTNDM3)を最優先で疑うべきです。膵島自己抗体(GAD抗体・IA-2抗体など)が陰性で、血中インスリンおよびC-ペプチドが血糖値に反して著しく低い場合、単一遺伝子性NDMの強い根拠となります。
5. 診断・遺伝子検査のプロセス
TNDM2の確定診断には、臨床所見による疑いの段階と、分子遺伝学的な確定診断の2段階があります。現在の世界標準では、NDMが疑われるすべての患者において可能な限り早期に遺伝子検査を実施することが推奨されています。診断の確定が、治療方針(インスリンからSU薬への移行)を決定づけるためです。
段階的な診断アプローチ
重度IUGRや巨舌症を伴う場合(生後3週間未満)
→ 染色体6q24領域のインプリンティング異常を検出するメチル化特異的MLPA法(MS-MLPA)を最優先で実施(TNDM1の除外)
出生体重が正常で奇形を伴わない場合(または生後3週間以降の発症)
→ 次世代シーケンシング(NGS)を用いた遺伝子パネル検査でABCC8およびKCNJ11変異解析を最優先で実施
💡 用語解説:次世代シーケンシング(NGS)とは
「次世代シーケンシング(NGS: Next Generation Sequencing)」とは、DNAの塩基配列を大量かつ高速に読み取る技術の総称です。従来のサンガー法では1〜2個の遺伝子しか解析できませんでしたが、NGSを用いた遺伝子パネル検査では複数の遺伝子を同時に解析できます。新生児糖尿病の原因遺伝子(ABCC8・KCNJ11・INS・GCKなど)を網羅的に調べることができ、迅速かつ正確な確定診断に貢献します。
💡 用語解説:持続血糖測定(CGM)の役割
CGM(Continuous Glucose Monitoring:持続血糖測定)は、皮下の間質液中のグルコース濃度を5分ごとなど高頻度で連続測定する機器です。新生児の頻回採血による苦痛を避けながら、血糖の変動をリアルタイムで把握できます。TNDM2の急性期管理においてはインスリン量の精密な調整に、また寛解期の判定(インスリン中止後に正常血糖が維持されていることの客観的確認)にも活用されます。低血糖アラームの設定により、重症低血糖を未然に防ぐことも可能です。
ミネルバクリニックでは、MODY・新生児糖尿病に関連する遺伝子を網羅した検査を提供しています。MODY・新生児糖尿病遺伝子検査および高インスリン血症遺伝子検査の詳細もご確認ください。
6. 治療:インスリンからスルホニル尿素薬(SU薬)へのパラダイムシフト
TNDM2の治療において最も重要な知識は、ABCC8変異が確定した場合、経口スルホニル尿素薬(SU薬)への切り替えによってインスリン注射を中止できる可能性が非常に高いという事実です。大規模な国際的追跡調査により、ABCC8変異を有する患者の約90〜95%がこの移行に成功し、インスリン注射を完全に中止できることが証明されています。
💡 用語解説:スルホニル尿素薬(SU薬)とは
スルホニル尿素薬(SU薬)はグリベンクラミド(グリブリド)・グリクラジド・トルブタミドなどを含む、経口で服用できる糖尿病薬のグループです。SU薬はSUR1タンパク質に直接結合し、ATPの有無に関わらずKATPチャネルを強制的に閉鎖させます。これにより、変異によって「開きっぱなし」になっていたチャネルが物理的に閉じられ、ベータ細胞の正常なインスリン分泌カスケードが再起動します。外からホルモンを補充するインスリン注射とは異なり、SU薬は患者自身の膵臓が持つインスリン分泌能力を「回復・復元」させるという革新的な作用を持ちます。
SU薬移行の臨床データ:症例ごとの多様性
以下の表は、ABCC8変異を有するTNDM2患者の発症から寛解に至るまでの実際の臨床経過を示しています。寛解に至るまでの期間は患者によって大きく異なることがわかります。
| 症例 | 発症(生後日齢) | 治療の経過 | 寛解まで |
|---|---|---|---|
| Case 1 | 36日 | インスリン→SU薬移行 | 24ヶ月 |
| Case 2 | 50日 | インスリン→SU薬移行 | 6ヶ月 |
| Case 3 | 35日 | インスリン→SU薬移行 | 14ヶ月 |
| Case 4 | 270日 | インスリン単独 | 48ヶ月 |
| Case 8 | 60日 | インスリン単独 | 4ヶ月 |
| Case 9 | 105日 | インスリン単独(8歳で再発) | 3.5ヶ月 |
| Case 10 | 35日 | インスリン→SU薬移行 | 22ヶ月 |
| Case 11 | 74日 | インスリン→SU薬移行 | 1ヶ月 |
出典:Transient diabetes mellitus with ABCC8 variant successfully treated with sulfonylurea (PMC11346097) をもとに作成
SU薬による治療はインスリン注射と比較して、重症低血糖リスクの軽減・HbA1cの有意な低下・長期的な血糖コントロールの安定化をもたらすことが長期フォローアップデータで示されています。また、KATPチャネルは脳にも存在するため、血液脳関門を通過できるSU薬は脳内のチャネル異常も是正し、神経発達予後を改善する可能性も示唆されています。
7. 寛解・再発のダイナミクスと生涯フォローアップ
TNDM2の患者は適切な治療のもとで血糖値が正常化し、外からのインスリン投与やSU薬の内服を一切必要としない「寛解(Remission)」状態に至ります。寛解の時期は患者ごとに大きく異なりますが、平均して生後8ヶ月前後で訪れ、大部分は生後18ヶ月までに治療が不要になります。
しかし、ここで最大の注意が必要です。「一過性」という名称は「完治」を意味しません。TNDM2では乳児期の寛解後、50%以上の確率で糖尿病が再発(Relapse)します。この再発の事実を見落とすことが、長年にわたる誤診と不適切治療という「悲劇」につながります。
📋 再発のトリガー
- 思春期(平均15歳前後、2〜45歳の幅)
- 重篤な感染症罹患時
- 女性の妊娠期(妊娠糖尿病として発症)
⚠️ 再発時の誤診リスク
- 1型糖尿病と誤診される
- 若年発症2型糖尿病と誤診される
- MODYと混同される
- 乳児期の病歴が伝わらない
🚨 実際に報告された誤診例
生後7日でTNDM2を発症し、インスリンで寛解した女性が13歳で再発した際、過去の既往歴が伝わらず「インスリン依存型糖尿病」と誤診されました。その後25年間にわたって不十分な血糖コントロールのままインスリン強化療法を余儀なくされました。のちにABCC8変異が特定された後にSU薬へ切り替えたところ、速やかに正常血糖(Euglycemia)が達成され、内因性インスリン分泌能の改善まで認められています。
このような悲劇を防ぐために、寛解後も少なくとも年1回のHbA1c測定を含む長期的な内分泌学的フォローアップが絶対に不可欠です。また成人科医が若年で非定型的な糖尿病患者を診察した際には、「乳児期に一時的な高血糖があったか」という病歴聴取が、正確な診断への最重要な鍵となります。
8. 遺伝カウンセリング:家族全体を視野に入れた支援
TNDM2は常染色体優性遺伝の疾患です。患者(発端者)のABCC8変異を持つ子どもは、男女を問わず50%の確率で同じ変異を受け継ぎます。変異を受け継いだ場合、新生児期の糖尿病、あるいは後に成人発症型の糖尿病を発症する高いリスクを負います。
💡 用語解説:常染色体優性遺伝
「常染色体」は性染色体以外の染色体、「優性(顕性)」は2本のうち1本に変異があるだけで発症することを意味します。TNDM2は1つの変異コピーを持つだけで発病するリスクがある常染色体優性遺伝です。TNDM1(6q24関連)の遺伝リスクがインプリンティングの性別依存性によって複雑に変化するのとは異なり、TNDM2ではシンプルに子への50%の遺伝リスクが存在します。
親世代の「2型糖尿病」がABCC8変異の可能性
TNDM2において特に重要な現象が「表現型の多様性(Phenotypic variability)」と「不完全浸透性(Incomplete penetrance)」です。TNDM2の新生児が診断された際に両親の遺伝子スクリーニングを行うと、父親または母親が同じABCC8変異を保持しながら、新生児期の糖尿病を発症せず成人後に「2型糖尿病」や「妊娠糖尿病」として発症していたケースが多く報告されています。
つまり、ABCC8遺伝子の変異は新生児期の重篤な糖尿病から成人発症型の軽症な糖尿病まで、同じ変異でも全く異なる年齢・重症度で発症する広いスペクトラムを形成しています。小児科医は患児単独の診断にとどまらず、家族全体の糖尿病歴(特に若年発症の2型糖尿病や妊娠糖尿病の既往)を詳細に確認し、必要に応じて血縁者への遺伝子スクリーニングとカウンセリングを提供する責任があります。
9. よくある誤解
誤解①「一過性=完治した」
乳児期の寛解は完治ではありません。思春期・妊娠期に50%以上の確率で再発します。生涯にわたる定期的なHbA1c測定と内分泌フォローが不可欠です。
誤解②「インスリンしか治療法がない」
ABCC8変異が確定した場合、約90〜95%の患者が経口SU薬への移行に成功し、インスリン注射を中止できます。遺伝子診断なしには、この選択肢が存在すること自体知られません。
誤解③「思春期の糖尿病再発は普通の1型・2型だ」
TNDM2の再発は肥満を伴わず自己抗体も陰性なため、MODYや若年発症2型糖尿病と混同されます。「乳児期の高血糖の既往歴」という病歴聴取が鑑別の決め手となります。
誤解④「両親が健康なら遺伝ではない」
同じABCC8変異を持つ親が「成人の2型糖尿病」として発症しているケースが多く報告されています。表現型の多様性により、親が「健康」に見えても変異を保持している場合があります。
🏥 新生児糖尿病・遺伝子検査のご相談
TNDM2をはじめとする新生児糖尿病・単一遺伝子性糖尿病に関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
よくある質問(FAQ)
参考文献
- [1] Orphanet. Transient neonatal diabetes mellitus. [Orphanet ORPHA:99886]
- [2] OMIM. #610374 Diabetes Mellitus, Transient Neonatal, 2. Johns Hopkins University. [OMIM]
- [3] Edghill EL, et al. Neonatal diabetes mellitus: a disease linked to multiple mechanisms. Horm Res. 2007;67(suppl 1):e5-e11. [PMC1847805]
- [4] Docherty LE, et al. Transient neonatal diabetes mellitus. Orphanet J Rare Dis. 2010. [Orphanet]
- [5] Khulan B, et al. Transient neonatal diabetes mellitus caused by a novel mutation in the ABCC8 gene. J Surg Med. 2019. [Journal of Surgery and Medicine]
- [6] KEGG DISEASE. Transient neonatal diabetes mellitus (H00513). [KEGG]
- [7] ABCC8. Open Targets Platform. [Open Targets Platform]
- [8] Wambach JA, et al. Chromosome 6q24-related diabetes mellitus. GeneReviews. 2018. [PMC5897580]
- [9] Gao X, et al. Transient diabetes mellitus with ABCC8 variant successfully treated with sulfonylurea: Two case reports and review of literature. Front Endocrinol. 2024. [PMC11346097]
- [10] Bowman P, et al. Long-term Follow-up of Glycemic and Neurological Outcomes in an International Series of Patients With Sulfonylurea-Treated ABCC8 Permanent Neonatal Diabetes. Diabetes Care. 2021. [PMC7783935]
- [11] Demirbilek H, et al. A case with relapsed transient neonatal diabetes mellitus treated with sulfonylurea, ending chronic insulin requirement. Endocrinol Diabetes Metab Case Rep. 2018. [EDM Case Reports]
- [12] MedlinePlus Genetics. ABCC8 gene. [MedlinePlus]
- [13] Reactome. Defective ABCC8 can cause hypo- and hyperglycemias. [Reactome]
- [14] Senniappan S, et al. Neonatal Diabetes Mellitus: An Update on Diagnosis and Management. J Pediatr Endocrinol Metab. 2018. [PMC5928785]