目次
- 1 1. AGXT遺伝子の概要:ゲノム上の位置と発現の特異性
- 2 2. AGT酵素の生化学的機能とペルオキシソームへの輸送
- 3 3. グリオキシル酸代謝経路の破綻と全身性シュウ酸症
- 4 4. AGXT遺伝子変異の種類と4つの病態メカニズム
- 5 5. G170R変異とP11L多型の相乗効果:ミトコンドリア誤局在の分子機構
- 6 6. 診断アプローチ:生化学検査から遺伝子解析まで
- 7 7. ピリドキシン(ビタミンB6)療法:薬理学的シャペロンの仕組み
- 8 8. RNA干渉(RNAi)治療薬:基質合成抑制療法の革命
- 9 9. 次世代遺伝子編集治療:Once-and-Doneへの挑戦
- 10 10. 遺伝カウンセリングの意義と家族スクリーニング
- 11 よくある質問(FAQ)
- 12 関連記事
- 13 参考文献
📍 クイックナビゲーション
AGXT遺伝子は、ヒト第2染色体長腕(2q37.3)に位置し、肝臓の肝細胞だけに発現するという、ほかに類を見ない特異的な遺伝子です。コードされるアラニン-グリオキシル酸アミノトランスフェラーゼ(AGT)酵素は、体内で絶えず生成される有毒代謝中間体「グリオキシル酸」を無害なグリシンへと変換する、生命維持に不可欠な役割を担います。この酵素が変異によって機能を失うと、シュウ酸が全身に蓄積して腎不全や多臓器不全を招く重篤な難病「原発性高シュウ酸尿症1型(PH1)」が発症します。かつては肝臓と腎臓の同時移植しか根治策がなかったこの疾患も、近年のRNA干渉(RNAi)治療薬の登場や世界初のin vivo遺伝子編集治療の臨床応用により、疾患のパラダイムは劇的な変革を遂げつつあります。
Q. AGXT遺伝子とはどのような遺伝子ですか?まず結論だけ知りたいです
A. 肝臓の肝細胞だけに発現し、有毒な「グリオキシル酸」を無害な「グリシン」へと変換するAGT酵素をコードする遺伝子です。変異によって酵素が機能を失うと、シュウ酸が過剰産生されて腎臓や全身の臓器に沈着し、原発性高シュウ酸尿症1型(PH1)を引き起こします。近年はRNAi治療薬2種が承認され、CRISPR遺伝子編集治療も臨床試験段階に入っています。
- ➤遺伝子の基本情報 → 染色体2q37.3・11エクソン・肝細胞特異的発現・RefSeq: NM_000030
- ➤酵素の機能 → PLP依存性アミノトランスフェラーゼ・ペルオキシソームに局在・グリオキシル酸→グリシン
- ➤主な変異 → G170R(全アレルの約30%)・I244T(北アフリカ系に高頻度)など200以上の病原性バリアント
- ➤治療の最前線 → ピリドキシン療法(30〜50%有効)・RNAi治療薬2種承認・CRISPR遺伝子編集(臨床試験中・70%シュウ酸低下達成)
- ➤遺伝形式 → 常染色体潜性(劣性)遺伝・家族スクリーニングが予防において重要
1. AGXT遺伝子の概要:ゲノム上の位置と発現の特異性
AGXT遺伝子(正式名称:Alanine-Glyoxylate Aminotransferase)は、ヒト第2染色体長腕末端近くの2q37.3バンドに位置しています。米国国立生物工学情報センター(NCBI)のゲノムアセンブリ(GRCh38.p14)における座標は第2染色体の240,868,824塩基対から240,880,500塩基対にわたる、約11.6キロベース(kb)の領域です。この領域は11の連続したエクソンから構成され、進化的に高度に保存された機能ドメインを形成しています。主要なメッセンジャーRNAのRefSeqアクセッション番号はNM_000030、翻訳されるタンパク質のアクセッション番号はNP_000021として登録されています。
💡 用語解説:遺伝子(Gene)とは
遺伝子とは、DNA(デオキシリボ核酸)の特定の領域に記されたタンパク質を作るための「設計図」のことです。ヒトの全遺伝子数は約2万個とされています。AGXT遺伝子の「設計図」に従って作られるのがAGT酵素であり、この設計図に誤り(変異)が生じると、作られる酵素の形や機能が変わってしまいます。遺伝子は両親から各1コピー(合計2コピー)受け継がれるため、AGTXのように常染色体潜性遺伝の場合は、2コピー両方に変異が生じたときに初めて発症します。
AGXT遺伝子が持つ最大の特徴は、その組織特異的な発現様式にあります。人体の様々な組織の中で、AGXT遺伝子は専ら肝臓の肝細胞においてのみ発現します。これは、肝臓が全身のグリオキシル酸代謝と糖新生の中心的ハブとして機能しているという生物学的要求を反映しています。この発現の場所の偏りが、PH1が「肝疾患」ではなく「肝臓の代謝エラーが全身に波及する疾患」という独特な病態を生み出す根本的な理由でもあります。
💡 用語解説:常染色体潜性(劣性)遺伝とは
「常染色体」とは、性染色体(X・Y染色体)以外の22対の染色体のことです。「潜性(劣性)」とは、2コピーある遺伝子の両方に変異があるときだけ発症する遺伝形式を意味します。変異を1コピーだけ持つ人は「保因者(キャリア)」と呼ばれ、自身は発症しません。PH1はこの遺伝形式をとるため、両親がともに保因者である場合、子どもが発症する確率は25%となります。血縁関係のある両親の間での発症リスクが高くなる傾向があるのも、この遺伝形式の特徴です。
2. AGT酵素の生化学的機能とペルオキシソームへの輸送
AGXT遺伝子がコードするアラニン-グリオキシル酸アミノトランスフェラーゼ(AGT)は、ビタミンB6の活性型であるピリドキサール5′-リン酸(PLP)を補酵素として必要とする、PLP依存性アミノトランスフェラーゼです。細胞内では2つの同一サブユニットが結合した「ホモダイマー(二量体)」として機能し、単量体の状態では触媒活性を発揮できません。
💡 用語解説:PLP(ピリドキサール5′-リン酸)とは
PLPはビタミンB6の体内活性型です。AGT酵素にとって「なくてはならない相棒」の存在で、アミノ基(-NH₂)の転移反応を触媒する際の中心的な役割を果たします。PLPがAGTにしっかり結合することで、タンパク質の立体構造が安定化され、正しい二量体(ダイマー)が形成されます。後述するピリドキシン(ビタミンB6)療法が機能する理由は、まさにこの「PLPによるタンパク質安定化」の作用にあります。
AGT酵素が担う主要な触媒反応
AGTが行う最も重要な反応は、L-アラニンからアミノ基(-NH₂)をグリオキシル酸へと転移させることで、ピルビン酸とグリシンを生成する反応です。これにより、極めて毒性の高い代謝中間体であるグリオキシル酸が、無害かつ再利用可能なアミノ酸(グリシン)へと速やかに解毒されます。さらにAGTは、L-セリンとピルビン酸の間のアミノ基転移反応も触媒し、糖新生(体が糖を新たに合成するプロセス)にも寄与しています。酵素の至適pHは7.5〜8.5の弱アルカリ性領域であり、1mMのアミノオキシ酢酸(AOA)によって97.5%という強力な阻害を受けることが知られています。
💡 用語解説:ペルオキシソームとは
ペルオキシソームは細胞内に存在する小さな袋状の構造体(細胞小器官)で、脂肪酸の分解や有毒物質の解毒など、特定の酸化還元反応を「隔離」して行う場所です。正常な肝細胞では、AGT酵素はペルオキシソームの内部に局在しており、そこでグリオキシル酸をグリシンへと変換します。ペルオキシソームはグリオキシル酸が生成される場所でもあるため、「酵素とその基質が出会う場所」として絶妙に機能しています。この局在がずれると、酵素は機能していても代謝的には意味をなさなくなります。
ペルオキシソームへの正確な輸送メカニズム:PTS1とPex5p
細胞の核から離れたリボソームで翻訳されたAGTタンパク質は、細胞内の「宅配システム」によってペルオキシソームへと正確に届けられます。この輸送に不可欠な鍵となるのが、タンパク質のC末端(タンパク質の端)に存在するペルオキシソーム移行シグナル1(PTS1)という特定のアミノ酸配列です。
💡 用語解説:PTS1シグナルとPex5pとは
PTS1(Peroxisome Targeting Signal 1)とは、タンパク質の末端に存在する「宛先ラベル」のようなアミノ酸配列です。細胞質に存在する受容体タンパク質「Pex5p」が、このPTS1ラベルを特異的に認識してAGTをペルオキシソームへと案内します。重要なのは、PTS1の認識はAGTが完全に正しく折り畳まれた(folded)ホモダイマー構造になっていることが前提である点です。わずかなタンパク質の形の乱れでさえ、Pex5pによる認識を妨げ、本来の局在を失わせるには十分です。このメカニズムの精妙さが、変異によって引き起こされる多様な病態を生み出します。
3. グリオキシル酸代謝経路の破綻と全身性シュウ酸症
AGXT遺伝子の変異によりAGT酵素が欠損または著しく低下すると、グリオキシル酸の無毒化プロセスが破綻します。これがPH1の病態生理学的トリガーです。正常な代謝経路と、PH1での代謝経路の違いを以下のCSSダイアグラムで示します。
✅ 正常な肝細胞
❌ PH1肝細胞(AGXT変異あり)
ペルオキシソーム内でグリオキシル酸が代謝されなくなると、細胞質へと流出したグリオキシル酸は、乳酸脱水素酵素(LDH、特にLDHA)の基質となってシュウ酸へと不可逆的に変換されます。ヒトの体内にはシュウ酸を分解する酵素が存在しないため、産生されたシュウ酸はすべて血流に乗り、腎臓から尿中へ排泄されるしかありません。
尿中のシュウ酸濃度が上昇すると、カルシウムイオンと結合してシュウ酸カルシウム結晶が形成され、腎結石や腎石灰化を引き起こします。さらに腎機能が低下してeGFRが30〜45 mL/min/1.73 m²を下回ると、血漿中のシュウ酸濃度(POx)が急激に上昇し、シュウ酸カルシウムは腎臓以外の全身臓器にも沈着し始めます。これが「全身性シュウ酸症(Systemic Oxalosis)」という致死的な病態です。
🦴 骨格系・関節
骨痛、多発性骨折、関節炎、脊柱管狭窄症、滑膜炎
❤️ 心臓・循環器
致死的不整脈、拡張能障害、弁膜異常、動脈硬化、脳卒中
🔵 皮膚・眼
難治性皮膚潰瘍、網状皮斑、網膜シュウ酸塩沈着、視力障害
🧠 神経・筋肉
軸索喪失、脱髄、ミオパチー、多発神経根ニューロパチー
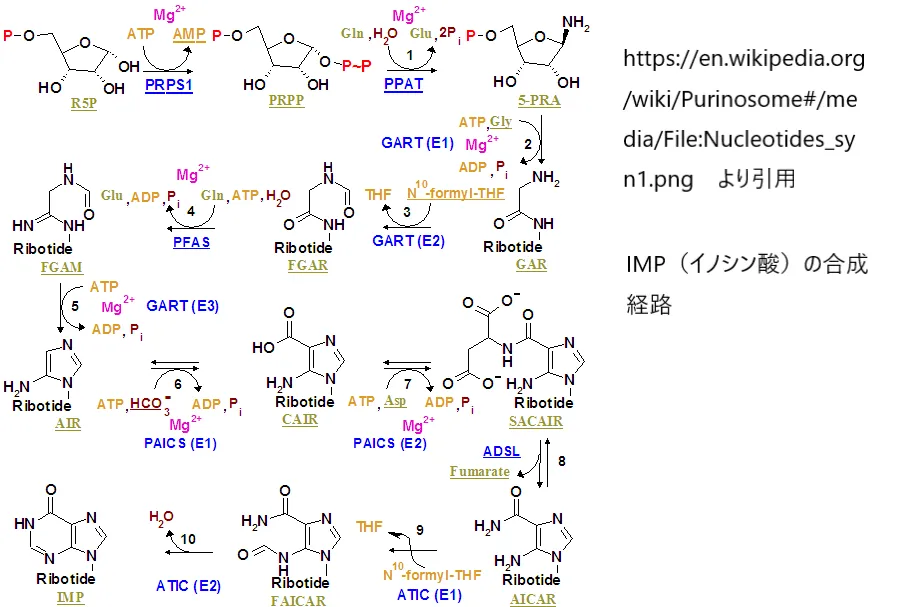
以下の画像は、細胞の代謝ネットワークがいかに精緻に相互接続されているかを示す参考資料です。グリオキシル酸はグリシンやセリンなどのアミノ酸代謝とも密接に関わっており、AGTはこれらの広大な代謝ネットワークの中核にあるハブとして機能しています。
4. AGXT遺伝子変異の種類と4つの病態メカニズム
これまでに200以上の異なる病原性または病原性の可能性が高いバリアントがAGXT遺伝子上に報告されており、これらがPH1の表現型の多様性(重症度や発症年齢の違い)を生み出しています。変異はエクソン1・エクソン4・エクソン7に特に集中しており、この3エクソンのスクリーニングだけで約77%の診断感度が得られます。全遺伝子シーケンスでは感度が98%に達します。
💡 用語解説:ミスセンス変異とフレームシフト変異
ミスセンス変異:DNA塩基が1つ変化し、対応するアミノ酸が別の種類に置き換わる変異です。タンパク質の形や機能が変わりますが、タンパク質自体は一応作られます。AGXT遺伝子では最も多くみられる変異タイプです。
フレームシフト変異:DNAの塩基が1〜2個挿入または欠失することで、以降のアミノ酸の「読み枠」がずれてしまう変異です。結果として本来とは全く異なる(多くは機能しない)タンパク質が作られるか、早期に合成が止まります。強力な機能喪失変異(Loss-of-function)として分類されます。
AGXT変異による酵素不全の4つのメカニズム
① 細胞内誤局在
Subcellular Mistargeting
酵素は合成されるが、ペルオキシソームではなくミトコンドリアなど別の細胞小器官に誤って輸送される。最も多いG170R変異のメカニズム。
② タンパク質の凝集
Protein Aggregation
折り畳み(フォールディング)の異常により不溶性の凝集体を形成し、速やかに細胞内で分解される。G41R変異が代表例。
③ 触媒欠陥
Catalytic Defects
タンパク質の構造や局在は保たれるが、活性中心のアミノ酸変異により触媒機能そのものを喪失する。酵素が存在しても反応が起きない状態。
④ 合成欠陥
Synthesis Defects
フレームシフト変異やナンセンス変異により、機能的なタンパク質が全く合成されない。c.832del、c.26_27insAなどのフレームシフト変異が該当。
臨床的に重要な主要バリアント
| バリアント | 変異の種類 | 主な特徴・頻度 | 病態メカニズム |
|---|---|---|---|
| c.508G>A (p.Gly170Arg / G170R) |
ミスセンス変異 | 最多(全アレルの約30%)。世界中で広く見られる | P11L多型との相乗効果でミトコンドリアへ誤局在 |
| p.Ile244Thr (I244T) |
ミスセンス変異 | 全体の約9%、北アフリカ系集団で極めて高頻度(モロッコで84%) | G170Rと同様にミトコンドリア誤局在 |
| p.Gly41Arg (G41R) |
ミスセンス変異 | 著明なタンパク質凝集を引き起こす | タンパク質凝集・触媒活性の完全喪失 |
| c.33_34insC c.832del(p.Leu278fs)など |
挿入・欠失変異(フレームシフト) | 診断スクリーニングで高頻度に検出 | 合成欠陥・短縮タンパク質・機能完全喪失 |
| p.Ser223Arg (S223R) |
ミスセンス変異 | 高度保存残基の変異。エクソーム解析で同定 | 構造的不安定性を惹起 |
5. G170R変異とP11L多型の相乗効果:ミトコンドリア誤局在の分子機構
PH1の病態生理学において、分子レベルで最も精緻に解明されているのが「酵素のミトコンドリアへの誤局在」メカニズムです。最も多いG170R変異を例にとると、この変異単独ではミトコンドリアへの誤局在は起きません。そこには、ある「共犯者」が関わっています。
💡 用語解説:P11L多型(マイナーアレル多型)とは
p.Pro11Leu(P11L)とは、AGXT遺伝子の11番目のアミノ酸がプロリン(Pro)からロイシン(Leu)に変わる変異で、健常な一般集団にも約20%のマイナーアレル頻度で存在するありふれた「多型(polymorphism)」です。これ単独では疾患を引き起こさず、酵素は正常にペルオキシソームへ輸送されます。しかしP11L置換はタンパク質のN末端領域に、ミトコンドリア移行シグナル(MTS)として機能し得る「潜在的(Cryptic)な配列」を形成してしまうのです。
G170Rによるフォールディング遅延——「潜伏したMTS」が露わになる瞬間
P11L多型と同一アレル(シス配置)にG170R変異が加わると、事態は劇的に変わります。G170R変異はAGTタンパク質が二量体(ダイマー)を形成する際のフォールディングプロセスに重大な欠陥を誘発し、単量体(モノマー)状態が細胞質内に長期間留まる状態を引き起こします。
この単量体が長時間細胞質に存在すると、Hsc70などの分子シャペロンとの相互作用が異常に増大します。そして、P11L多型によってN末端に形成されていた「潜在的なミトコンドリア移行シグナル(MTS)」が、単量体状態であることで細胞質に曝露(アンマスク)されます。結果として、本来ペルオキシソームへ向かうべきAGT酵素が、ミトコンドリアのトランスロケーター機構に捕捉され、誤ってミトコンドリア内部へとインポートされてしまうのです。
6. 診断アプローチ:生化学検査から遺伝子解析まで
PH1は発症年齢によって著しい多様性を示します。反復するカルシウム結石・腎石灰化を呈し、特に腎機能低下や家族歴を伴うあらゆる年齢の患者において、AGXT遺伝子の変異を疑うことが重要です。
年齢層ごとの典型的な臨床像
👶 乳児期(12か月未満)
最も重篤。びまん性腎石灰化・体重増加不良・成長遅滞。早期に末期腎不全へ至るリスクが高い。
🧒 小児〜青年期(1〜17歳)
初回の腎結石発作や反復するシュウ酸カルシウム結石で発見。約30%は画像診断時に腎石灰化あり。
🧑 成人期(18歳以上)
反復性の両側カルシウム結石、または原因不明の腎機能低下として遅発的に診断されるケースも。
🏥 腎移植後の発見
腎単独移植後に移植腎が早期廃絶し、生検でシュウ酸カルシウム結晶が同定されて初めて診断される例もある。
確定診断のための検査ステップ
- ➤24時間尿中シュウ酸測定:0.5 mmol/24時間(体表面積1.73 m²補正)を超えれば高シュウ酸尿症と判定。小児では随時尿のシュウ酸/クレアチニン比を年齢別基準値と比較。
- ➤血漿シュウ酸濃度(POx):20 µmol/Lを超えればPH1と矛盾せず、50 µmol/Lを超える場合は極めて強くPH1が示唆される。eGFR低下患者で特に重要。
- ➤結石成分分析:排出された結石が100%シュウ酸カルシウム一水和物(Calcium oxalate monohydrate)であればPH1の可能性が高い。
- ➤AGXT遺伝子解析(確定診断):両アレル性の病原性バリアントを同定。かつて必要だった肝生検は、遺伝子解析技術の進歩により現在では省略可能になっています。
7. ピリドキシン(ビタミンB6)療法:薬理学的シャペロンの仕組み
PH1の治療において、特定の変異を持つ患者に対する第一選択のひとつがピリドキシン(ビタミンB6)療法です。ピリドキシンは、単なる補酵素の補充にとどまらず、変異AGTタンパク質に対する「薬理学的シャペロン」として機能します。
💡 用語解説:薬理学的シャペロン(Pharmacological Chaperone)とは
「シャペロン」とは、タンパク質が正しく折り畳まれる(フォールディングする)のを助ける分子のことです。薬理学的シャペロンとは、薬として投与することでタンパク質の立体構造を安定化させ、機能を回復させる化合物を指します。大量のピリドキシン投与によって細胞内のPLP濃度が上昇し、PLPが変異AGTモノマーに強固に結合することで、正常な二量体形成プロセスが加速されます。結果として、P11L+G170R変異によって誤局在を引き起こす「潜在的MTSの露出」が回避され、変異AGTの一部がペルオキシソームへと正しく輸送されます。
臨床データによれば、PH1患者の約30〜50%がピリドキシン療法に対して反応性を示し、尿中シュウ酸排泄量の大幅な低下が確認されています。反応性は遺伝子型に強く依存しており、G170RおよびF152Iのホモ接合型を持つ患者で最も高い効果が得られます。
臨床的意義の高い研究データ:G170Rホモ接合型の患者5名を対象とした追跡研究(移植時年齢中央値39歳、追跡期間中央値8.5年)では、腎臓単独移植後もピリドキシン療法を継続することで、尿中シュウ酸レベルは0.5 mmol/24 hr未満を維持し、移植腎における結晶沈着もごくわずかに抑えられ、良好な移植成績が達成されました。すなわち、ピリドキシン反応性患者では侵襲性の高い肝・腎同時移植を回避できる可能性があります。
国際的なガイドラインでは、少なくとも一つのミスセンス変異を有するすべてのPH1患者に対して、確定診断後速やかに高用量ピリドキシン投与試験を実施し、反応性を評価することが強く推奨されています。
8. RNA干渉(RNAi)治療薬:基質合成抑制療法の革命
ピリドキシンに反応しない過半数の患者にとって、2020年代に相次いでFDAから承認された「RNA干渉(RNAi)」技術に基づく治療薬は画期的な福音となりました。RNAi治療薬は欠損したAGT酵素を直接修復するのではなく、グリオキシル酸やシュウ酸を産生する「上流の代謝経路」を遮断するという基質合成抑制療法(SRT)のアプローチをとります。
💡 用語解説:RNA干渉(RNAi)と基質合成抑制療法(SRT)とは
RNA干渉(RNAi)とは、特定のメッセンジャーRNA(mRNA)を標的にして分解させることで、そのmRNAからタンパク質が作られるのを阻止する自然の遺伝子制御メカニズムです。siRNA(小さな干渉RNA)という分子を投与することで、特定の遺伝子の「スイッチを切る」ことができます。
基質合成抑制療法(SRT)とは、病気の原因となる有害な物質(基質)の産生を、その上流で遮断することで症状を抑える治療アプローチです。PH1の場合、欠陥のあるAGTを修復する代わりに、シュウ酸の前駆体であるグリオキシル酸をそもそも作らせないようにします。
承認済み2剤の比較:ルマシランとネドシラン
9. 次世代遺伝子編集治療:Once-and-Doneへの挑戦
RNAi療法はPH1の予後を劇的に改善しましたが、「生涯にわたる定期投与の継続」という課題が残ります。この根本課題を解決するため、DNAレベルで疾患を永続的に修復する「Once-and-Done(生涯に一度の治療)」アプローチとして、遺伝子補充療法と遺伝子編集技術の開発が最終段階へと進んでいます。
💡 用語解説:CRISPR/Casとアデニン塩基編集(ABE)
CRISPR/Casとは、特定のDNA配列を「はさみ」のように切断できる遺伝子編集ツールです。標的遺伝子を不活性化(ノックアウト)したり、正しい配列に修復したりすることができます。
アデニン塩基編集(ABE)は、CRISPRの応用技術の一つで、DNAを切断せずに特定の塩基だけをピンポイントで別の塩基に書き換えることができる、より精密なアプローチです。G170R変異(c.508G>A)のような1塩基変化を直接修正することが可能です。
前臨床での注目成果:ABEによるG170R変異の直接修復
G170R変異を持つiPS細胞由来の肝細胞様モデルに対し、脂質ナノ粒子(LNP)に内包したABEのmRNAとガイドRNAを導入したところ、変異した塩基をピンポイントで修復することに成功しました。この修復によりAGT酵素がミトコンドリアからペルオキシソームへと正しい局在を取り戻し、シュウ酸の蓄積が劇的に減少しました。ラットモデルを用いた解析では、約44%の編集効率で尿中シュウ酸排泄を正常化できるという、臨床応用への重要なベンチマークも特定されています。
YOLT-203:世界初のin vivo遺伝子編集治療薬の臨床データ
現在最も注目されているのが、YolTech Therapeutics社が開発したYOLT-203です。CRISPR/Cas12システムを脂質ナノ粒子(LNP)に内包して静脈内投与することで、肝細胞内のHAO1遺伝子(グリコール酸オキシダーゼをコード)のDNA配列を直接切断・永続的に不活性化(ノックアウト)する戦略を採用しています。
🔬 YOLT-203 第1相試験の主要成果(2025年2月発表)
- ✅有効性:高用量コホートで1回の静脈内投与により24時間尿中シュウ酸が約70%低下。この抑制効果は16週間の観察期間中も一切減弱せず持続。
- ✅安全性:全用量群において良好な忍容性。重篤な有害事象(SAE)・治療中止・離脱例はゼロ。
- ✅規制上のマイルストーン:2026年2月2日にFDAより「再生医療先端医療(RMAT)」指定を取得。グローバルピボタル試験(第3相相当)のIND申請もFDAにクリアされ、本格的な開発が進行中。
10. 遺伝カウンセリングの意義と家族スクリーニング
AGXT遺伝子の変異は常染色体潜性(劣性)遺伝で受け継がれます。PH1は浸透度の高い遺伝性疾患であるため、発端者(患者)が同定された場合、その兄弟姉妹に対する迅速な家族スクリーニングの実施が強く推奨されます。早期診断によって腎機能が保たれている段階からRNAi療法等を介入させることで、腎結石や末期腎不全の発症を予防できる可能性があります。
- ➤再発リスクの説明:両親がともに保因者の場合、次子が発症する確率は25%(保因者となる確率は50%)。両親の遺伝子検査によってリスク評価が可能です。
- ➤出生前診断の選択肢:既知の変異が同定されている場合、絨毛検査・羊水検査による出生前遺伝子診断が可能です。
- ➤妊娠中の管理:ルマシラン・ネドシランなどのRNAi治療薬はヒトでの安全性データが不足しているため、妊娠前および妊娠中の投与中止が推奨されます。腎臓内科および産科の専門医による密な管理が不可欠です。
- ➤生活上の注意:十分な水分摂取、NSAIDsの過剰摂取の回避、ビタミンCの過剰摂取の禁止、ルバーブ・チョコレートなど高シュウ酸食品の大量摂取の制限が、生涯を通じた支持療法として重要です。
また、PH1の家族歴がなくても、パートナーとのご結婚・妊活にあたって保因者スクリーニング(キャリアスクリーニング)を検討されることで、将来のリスクを事前に知ることができます。特に近親婚の多い集団や、特定の民族背景を持つ方では保因者頻度が高い場合があります。
遺伝性疾患に向き合うご家族の体験は一人ひとり異なります。別の遺伝性疾患ではありますが、キャリア検査を経験された患者さんご家族の体験談や、遺伝性疾患と家族計画についてのコラムも、遺伝カウンセリングを検討される際の参考にしていただければ幸いです。
よくある質問(FAQ)
🏥 AGXT遺伝子・PH1・遺伝子検査について
遺伝子変異・原発性高シュウ酸尿症・キャリアスクリーニングに関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
関連記事
参考文献
- [1] MedlinePlus Genetics. AGXT gene. National Library of Medicine. [MedlinePlus]
- [2] NCBI Gene. AGXT alanine–glyoxylate aminotransferase [Homo sapiens (human)]. Gene ID: 189. [NCBI Gene]
- [3] Hoppe B. An update on primary hyperoxaluria. Nat Rev Nephrol. 2012;8(8):467-475. GeneReviews® [Internet]. Primary Hyperoxaluria Type 1. [NCBI Bookshelf]
- [4] GeneCards. AGXT Gene – GeneCards | AGT1 Protein. [GeneCards]
- [5] UniProtKB. AGXT – Alanine–glyoxylate aminotransferase – Homo sapiens. Accession: P21549. [UniProtKB]
- [6] Cellini B, et al. Protein Homeostasis Defects of Alanine-Glyoxylate Aminotransferase: New Therapeutic Strategies for Primary Hyperoxaluria Type I. Biomed Res Int. 2013. [PMC3730394]
- [7] Fodor K, et al. Molecular Requirements for Peroxisomal Targeting of Alanine-Glyoxylate Aminotransferase as an Essential Determinant in Primary Hyperoxaluria Type 1. PLoS Biol. 2012. [PLOS Biology]
- [8] Purdue PE, et al. Four of the Most Common Mutations in Primary Hyperoxaluria Type 1 Unmask the Cryptic Mitochondrial Targeting Sequence of Alanine:glyoxylate Aminotransferase Encoded by the Polymorphic Minor Allele. J Biol Chem. 2013. [PMC3554916]
- [9] Santana A, et al. Pyridoxine Responsiveness in a Type 1 Primary Hyperoxaluria Patient With a Rare (Atypical) AGXT Gene Mutation. Front Genet. 2020. [PMC7270974]
- [10] Fargue S, et al. Sustained Pyridoxine Response in Primary Hyperoxaluria Type 1 Recipients of Kidney Alone Transplant. Kidney Int. 2015. [PMC4543374]
- [11] Sas DJ, et al. Lumasiran for primary hyperoxaluria type 1: What we have learned? Pediatr Nephrol. 2023. [PMC9871624]
- [12] Frishberg Y, et al. Long-term lumasiran therapy final results from a Phase 2 open-label extension study in primary hyperoxaluria. Nephrol Dial Transplant. 2025;41(3):575. [Oxford Academic]
- [13] Garrelfs SF, et al. Nedosiran: First Approval. Drugs. 2024. [PMC10803381]
- [14] Genetic Correction of the Most Common Mutation Causing Primary Hyperoxaluria Restores Enzyme Localization and Oxalate Metabolism. PMC. 2025. [PMC12672195]
- [15] YolTech Therapeutics. FDA Regenerative Medicine Advanced Therapy (RMAT) Designation for YOLT-203. 2026年2月. [YolTech公式]
- [16] Salido E, et al. Primary hyperoxaluria type 1: pathophysiology and genetics. Clin Kidney J. 2022;15(Suppl 1):i4–i12. [Oxford Academic]