目次
- 1 多発性外骨腫(HME/HMO)とは?症状・原因から悪性化リスクと最新治療まで徹底解説
- 1.1 1. 疾患の概要と歴史的変遷、疫学
- 1.2 2. 分子遺伝学的基盤と病態生理学的メカニズム(骨軟骨腫はなぜ形成されるのか)
- 1.3 3. 遺伝子型と表現型の相関、および日本人集団における特異的特徴
- 1.4 4. 臨床症状と多角的な整形外科的合併症
- 1.5 5. 前腕変形に関する病態と進化した新分類システム(2025年最新知見)
- 1.6 6. 画像診断基準と類似疾患との厳格な鑑別
- 1.7 7. 最大の脅威:悪性転化(二次性軟骨肉腫)のリスクとMRI診断
- 1.8 8. 外科的介入戦略と慢性疾患としてのQOL(生活の質)への影響
- 1.9 9. 新規分子標的治療の展望とパロバロテン臨床試験からの教訓
- 1.10 よくある質問(FAQ)
- 1.11 関連記事
- 1.12 参考文献
多発性外骨腫(HME/HMO)とは?
症状・原因から悪性化リスクと最新治療まで徹底解説
多発性外骨腫(Hereditary Multiple Exostoses: HME)は、骨格系の発育過程において、腕や脚などの長管骨の「骨幹端部(Metaphysis)」や扁平骨に、多数の良性骨腫瘍が多発する希少な常染色体優性(顕性)遺伝性の疾患です。全身に多発する硬い腫瘤は、単なる美容的な問題にとどまらず、骨格の成長障害、慢性的な疼痛、関節可動域の制限、さらには神経や血管への物理的圧迫を引き起こします。
🔖 専門用語:常染色体優性(顕性)遺伝
両親のどちらかが原因となる遺伝子変異を持っている場合、50%の確率で子どもに引き継がれ、性別に関係なく発症する遺伝の仕組みです。なお、現在では「優・劣」という誤解を避けるため「顕性(けんせい)・潜性(せんせい)」という呼称が推奨されています。本疾患では、親からの遺伝ではなく、受精卵ができた時に偶然起こる「新生突然変異(孤発例)」も約10%を占めます。
加えて、患者様が直面する最大の脅威として、成人期以降に既存の良性腫瘍が「軟骨肉腫」へと悪性転化(がん化)するリスクが生涯を通じて伴うため、長期かつ慎重な医学的サーベイランスが不可欠となります。
本記事では、多発性外骨腫の歴史的背景と診断基準の変遷から始まり、EXT1遺伝子およびEXT2遺伝子を中心とした腫瘍形成の分子メカニズム(ヘパラン硫酸の欠乏と細胞極性の喪失)、日本人集団における特有の遺伝的傾向、生活の質(QOL)への深刻な影響を深く掘り下げます。さらに、整形外科領域で2025年に提唱された前腕変形を予測する画期的な「新三層分類システム」、そしてパロバロテンの臨床試験(MO-Ped試験)から得られた教訓と次世代の分子標的治療の展望まで、臨床遺伝専門医の視点から最新の医学的知見を網羅して徹底的に解説します。
1. 疾患の概要と歴史的変遷、疫学
多発性外骨腫の病態概念は医学史において非常に古くから認識されてきました。1786年にスコットランドの著名な外科医John Hunterによって単発性と多発性の外骨腫の差異が初めて詳細に記述され、その後1814年にはフランスのAlexis Boyerによって「家族内集積性を持つ遺伝性疾患」として学術的に報告されました。さらに1964年、Solomonによる包括的な遺伝学的研究を経て、現在の疾患の遺伝的基盤が確立されるに至りました。
歴史的に本疾患は「多発性軟骨性外骨腫(Multiple cartilaginous exostoses)」「骨幹端全域異常(Diaphyseal aclasis)」「遺伝性変形性軟骨異形成症(Hereditary deforming chondrodysplasia)」あるいは「Ehrenfried病」など、多数の同義語で呼称されてきた背景があります。しかし、近年の病理学的および分子生物学的な理解の目覚ましい進展により、形成される病変が単なる骨の出っ張り(Exostosis)ではなく、表面に「硝子軟骨のキャップ(軟骨帽)」を有し、正常な骨の成長と同じ「内軟骨性骨化」のプロセスを伴って成長する真の腫瘍性病変(Osteochondroma)であることが明らかとなりました。
🔖 専門用語:内軟骨性骨化(ないなんこつせいこっか)
骨が形成されるプロセスの一つです。最初に「軟骨」でできた骨の鋳型(モデル)が作られ、そこに血管が入り込むことで徐々に硬い「骨組織」へと置き換わっていきます。腕や脚の長い骨など、人間の骨格の大部分はこの仕組みで成長します。
この病理学的実態を正確に反映するため、現在では世界保健機関(WHO)の基準を含め、国際的に「遺伝性多発性骨軟骨腫症(Hereditary Multiple Osteochondromas: HMO)」という呼称の使用が強く推奨されています。
💡 疫学的な発症頻度と診断時期の自然史
多発性外骨腫の発生頻度は、欧米の集団において約50,000人から100,000人に1人と推定されています。無症状のまま診断されない潜在的な患者が存在するため正確な罹患率の算出は困難ですが、臨床報告においては男性の罹患率が女性の約1.5倍から最大で3倍に達するというデータが複数存在します。
臨床的な診断時期については、出生直後や新生児期には病変が視認できず無症状であることが一般的です。しかし、骨格の成長に伴って腫瘍も同時に増大するため、小児期早期に異常が顕在化します。統計によれば、診断年齢の中央値は3歳であり、5歳までに約50%の患者様で視認可能または触知可能な腫瘍が形成され、10歳までに約80%、そして事実上ほぼすべての罹患者が12歳までに確定診断に至ります。
2. 分子遺伝学的基盤と病態生理学的メカニズム(骨軟骨腫はなぜ形成されるのか)
多発性外骨腫の根本的な原因は、細胞内の微細な遺伝子変異に起因します。主要な分子病態は、第8染色体長腕(8q24.11)に位置するEXT1遺伝子、または第11染色体短腕(11p11.2)に位置するEXT2遺伝子の「ヘテロ接合性機能喪失型変異(Loss-of-function mutation)」です。これらの遺伝子は「常染色体優性(顕性)遺伝」の形式をとりますが、家族歴のない孤発例も少なくなく、全症例の約10%は親からの遺伝ではなく、生殖細胞系列における新生突然変異(De novo mutation)によって発症することが確認されています。
2.1 へパラン硫酸の生合成と腫瘍形成における「ツーヒット仮説」
細胞内において、EXT1遺伝子とEXT2遺伝子は、ゴルジ体に局在する「グリコシルトランスフェラーゼ(糖転移酵素)」をコードしています。これらのタンパク質は強固なポリメラーゼ複合体を形成し、細胞の生理機能に不可欠なヘパラン硫酸(Heparan Sulfate: HS)という多糖類の生合成において中心的な役割を果たします。生成された成熟したヘパラン硫酸は細胞表面および細胞外マトリックスへと輸送され、軟骨や骨の形成に関与する多様なシグナル伝達分子(IHH、FGF、BMP、WNTなど)の濃度勾配を厳密に制御する重要な「足場」として機能します。
ここで多発性外骨腫の病態を理解する上で極めて重要なのが、がん抑制遺伝子におけるKnudsonの「ツーヒット仮説(Second-hit theory)」に類似した分子的事象の関与です。患者様は全身の細胞に一つの機能不全遺伝子(ファーストヒット)を持って生まれますが、これにより細胞内のヘパラン硫酸生合成能力が約50%低下したとしても、直ちには骨軟骨腫の形成には至りません。成長板の特定の軟骨細胞において、残存する野生型アレルに対する「後天的なランダムな体細胞変異(セカンドヒット)」が生じることで、その細胞におけるヘパラン硫酸合成能力が完全に喪失し、初めて病変の起点となるのです。
🔖 専門用語:ツーヒット仮説(Two-hit hypothesis)
がん抑制遺伝子によく見られる発症メカニズムです。HMEの患者様は、生まれつき全身の細胞のEXT遺伝子の片方に変異(1回目のヒット)を持っています。しかしこれだけでは腫瘍はできず、成長する過程で偶然、成長板の軟骨細胞に残っているもう片方の正常な遺伝子にも変異(2回目のヒット)が起こることで、初めてヘパラン硫酸が作れなくなり、腫瘍の形成がスタートします。
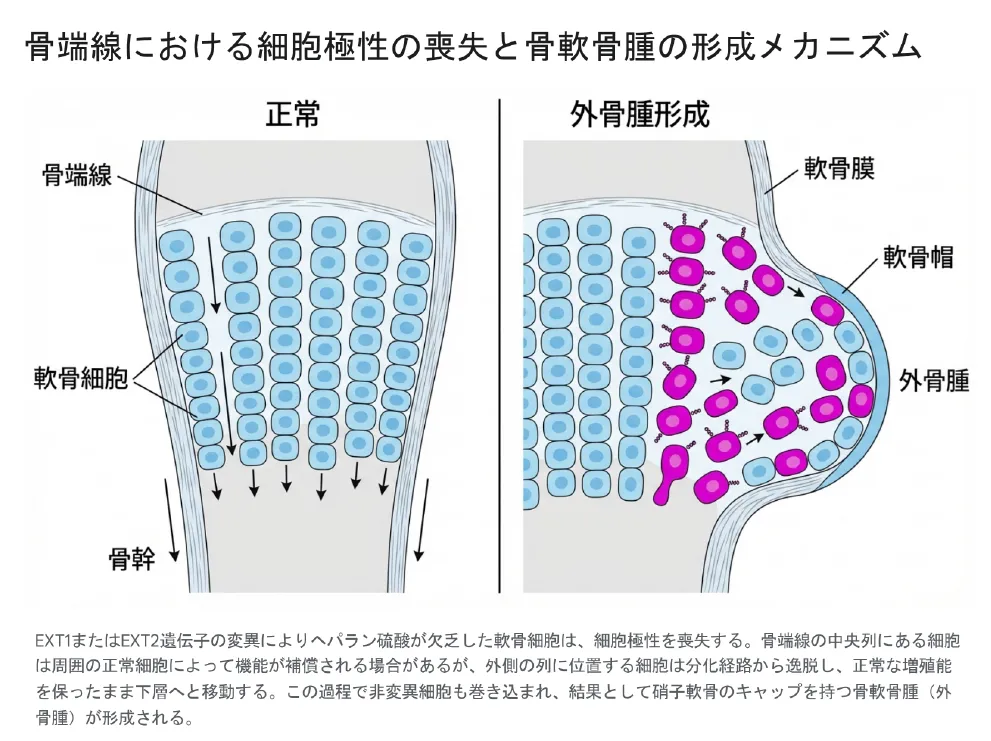
2.2 骨端線における細胞極性の喪失と外骨腫の形成過程
ヘパラン硫酸が完全に欠乏した軟骨細胞は、骨の成長を司る「骨端線(成長板)」において致命的な機能不全に陥ります。正常な状態において、軟骨細胞はインディアン・ヘッジホッグ(IHH)などのシグナルに導かれ、骨の長軸方向(骨端から骨幹へ)に向かって整然と配列し、成熟していきます。
🔖 専門用語:細胞極性(さいぼうきょくせい)
細胞が持つ「方向性」のことです。成長板の軟骨細胞は、本来「縦方向(骨が伸びる方向)」に綺麗に並んで増殖する極性を持っています。ヘパラン硫酸が不足するとこの「細胞のコンパス」が壊れてしまい、細胞が向かうべき方向を見失います。
シグナル伝達ネットワークが破綻すると、骨端線の外周列(軟骨膜に近い領域)に位置する変異細胞は、増殖の方向性を決定づける「細胞極性」を完全に喪失します。その結果、下方向へ進むべき軟骨細胞が横方向へと増殖のベクトルを変え、周囲の非変異(正常)細胞をも巻き込んでキメラ状の細胞塊を形成し始めます。最終的にこの細胞塊が骨皮質を突き破って外側へと突出します。この突出部の先端が新たな成長板として機能する「軟骨帽」となり、その下部で内軟骨性骨化が進行することで、母床の骨と連続した形態を持つ骨軟骨腫が完成するのです。
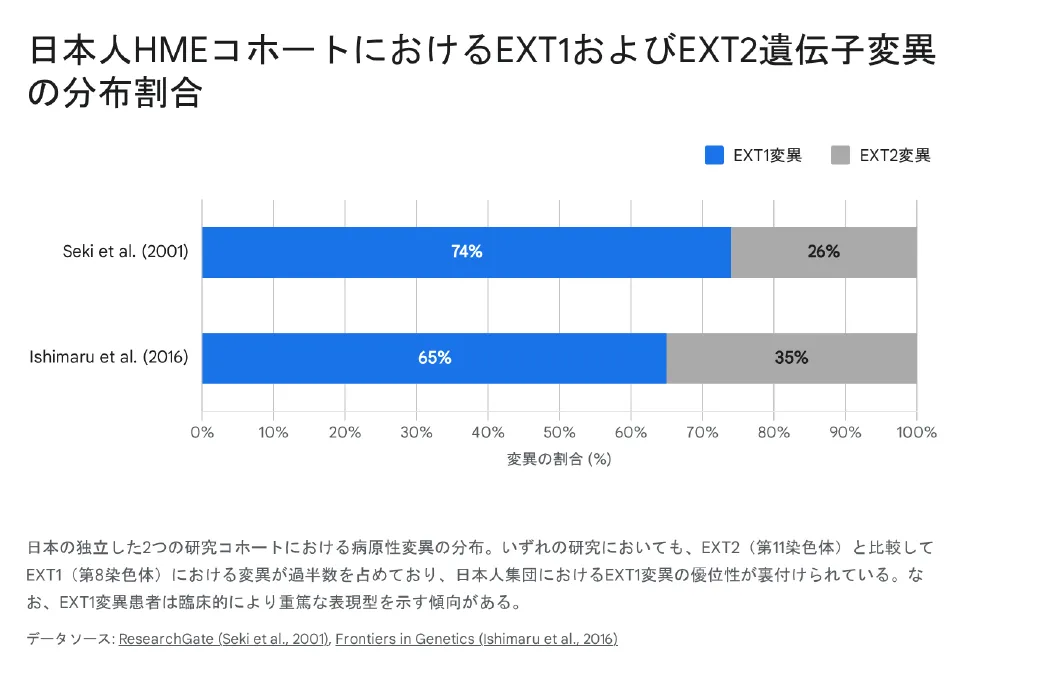
3. 遺伝子型と表現型の相関、および日本人集団における特異的特徴
原因遺伝子の違いは、臨床的な重症度に明確な差をもたらすことが近年の大規模な臨床ゲノム研究により明らかになりつつあります。概して、EXT1遺伝子に変異を持つ患者様は、EXT2遺伝子に変異を持つ患者様と比較して、臨床的に重症化しやすい傾向があります。具体的には、EXT1変異群では形成される外骨腫の総数が有意に多く、それに伴う骨格の変形や低身長の度合いが深刻であり、さらに後述する軟骨肉腫への悪性転化率も高いことが示されています。
🔖 専門用語:ミスセンス変異とR340(コドン340のアルギニン残基)
ミスセンス変異とは、DNAの暗号が1文字変わることで、作られるタンパク質の部品(アミノ酸)が別のものに置き換わってしまう変異です。日本人のEXT1遺伝子変異において、この部品の置き換わりが「340番目のアルギニン(R340)」という特定の場所に集中していることが発見されました。ここは酵素の働きにとって急所となる非常に重要な領域です。
なお、現在の標準的な遺伝子検査(全エクソームシーケンス等)を駆使しても、全患者の約4%から最大33%においてEXT1またはEXT2の病原性変異を特定できない「分子学的に未診断の症例」が存在します。これらに対しては、染色体19p領域に連鎖する未同定の第3の原因遺伝子(EXT3)の存在、発生初期の体細胞モザイク現象、あるいは標準検査では検出不可能な深部イントロン領域の制御バリアントの存在などが強く示唆されており、現在も活発に研究が進められています。
4. 臨床症状と多角的な整形外科的合併症
多発性外骨腫の臨床的プレゼンテーションは患者様によって極めて多様です。無症状のまま他の目的で撮影されたX線検査で偶然発見される症例も存在しますが、大部分の患者様は骨盤、膝周辺(大腿骨遠位や脛骨近位)、肩関節周辺などの関節近傍に多数の硬く非可動性の腫瘤を呈します。腫瘍は骨格の成長と並行して増大し、思春期を経て骨端線が閉鎖し骨格が成熟するとともに、腫瘍自体の成長も停止するのが本疾患の基本的な自然史です。
これらの良性腫瘍がもたらす直接的な臨床症状は、主に物理的な空間占拠効果によるものです。
- 慢性疼痛と滑液包炎:関節の屈曲や伸展時に腱や筋肉が腫瘍と摩擦を生じることで、慢性的な疼痛や滑液包炎が生じ、関節可動域が著しく制限されます。また、外骨腫自体が骨折を起こし、急性の疼痛を引き起こすこともあります。
- 神経・主要血管への物理的圧迫:より深刻な合併症として、腫瘍の先端が隣接する末梢神経や主要血管を圧迫・損傷することが挙げられます。中国の医療機関からの報告では、11歳の男児に対する右大腿骨の骨軟骨腫切除術において、術前に外骨腫によって右大腿動脈が破裂していたことが判明し、緊急の血管修復術が行われました。これは術中の綿密な神経血管構造の評価がいかに重要であるかを如実に物語っています。
- 全身的な骨格変形と成長阻害:骨端線近傍の異常増殖は、長管骨の正常な長軸方向への成長を物理的および生化学的に阻害します。その結果、罹患していない家族と比較して最終身長が有意に低くなる(低身長)傾向があります。また、下肢における非対称な成長は、外反膝や内反膝などのアライメント異常、左右の脚長差(Limb length discrepancy)による歩行障害や代償性の側弯症を誘発します。
5. 前腕変形に関する病態と進化した新分類システム(2025年最新知見)
多発性外骨腫において、機能的障害が最も顕著に現れる部位の一つが「前腕」です。前腕には橈骨(とうこつ)と尺骨(しゃっこつ)という2つの骨が並走していますが、尺骨は橈骨に比べて成長板の総面積が狭いため、遠位尺骨に生じた外骨腫は尺骨の縦方向の成長をより強く遅延させます。この非対称な成長障害が連鎖的な解剖学的破綻を引き起こし、尺骨の相対的短縮、代償的な尺骨の弯曲変形、手関節の著しい尺屈変形、そして手首や肘の機能(回内・回外運動)を決定的に阻害する橈骨頭の脱臼(Radial head dislocation: RHD)へと発展します。
5.1 古典的Masada分類の限界
長年にわたり、整形外科領域においてこの複雑な前腕変形を評価し、手術方針を決定するための標準的指標として「Masada分類(Type I〜IVb)」が広く使用されてきました。これは外骨腫の発生部位と脱臼の有無に基づく形態学的な分類です。しかし、2024年に『Journal of Hand Surgery』で発表されたChanらの大規模な後方視的コホート研究により、275の前腕変形例を再評価した結果、既存のMasada分類を適用した場合、実に全体の34.5%(95例)が提示された基準のいずれにも合致しない「分類不能(Unclassifiable)」となることが判明し、形態記述に依存する従来のシステムの臨床的限界が露呈しました。
🔖 専門用語:比例的尺骨長(Proportional ulna length)
レントゲン画像から尺骨(前腕の小指側の骨)の長さを評価し、正常な成長割合と比較する指標です。外骨腫により尺骨の成長が著しく妨げられるとこの数値が小さくなります。新分類では、この値が「0.95以下」になると将来脱臼するリスクが極めて高いと予測します。
5.2 橈骨頭脱臼リスクに基づく新三層分類システム(比例的尺骨長)
Masada分類の限界を克服し、外科的介入のタイミングを逃さないための「予後予測」に重点を置いた新たな分類システムがChanらによって提唱され、2025年に向けて注目を集めています。多変量ロジスティック回帰分析の結果、最も重篤な機能障害であるRHDを引き起こす最大の解剖学的要因は「遠位尺骨の病変」であることが特定されました。さらに、RHDの発生と統計的に最も有意な関連を示す放射線学的パラメータとして「比例的尺骨長」が特定され、予測の理想的な閾値は「0.95以下」と算出されました。
💡 Chanらによる新三層分類システム(脱臼予測モデル)
- 【Type 1A(高リスク群)】遠位尺骨に骨軟骨腫が存在し、かつ「比例的尺骨長が0.95以下」を満たす前腕。RHDへの進行リスクが極めて高く、最も厳重な警戒と早期の外科的介入(創外固定器を用いた尺骨延長術など)が推奨される。
- 【Type 1B(中等度リスク群)】遠位尺骨に骨軟骨腫は存在するが、「比例的尺骨長が0.95を超える」前腕。直ちに脱臼する危険性は低いが、成長に伴う骨比率の変化を注視する必要がある。
- 【Type 2(低リスク群)】遠位尺骨に骨軟骨腫が存在しない前腕。前腕の相対的短縮による脱臼のメカニズムが生じにくいため、保存的観察が主となる。
この新しい分類体系は、形態的な「結果」を記述するだけでなく、将来の脱臼を未然に防ぐための「アットリスク基準」を明確にした点で、今後の多発性外骨腫の臨床管理ガイドラインを大きく変革するポテンシャルを秘めています。
あわせて読みたい関連記事
6. 画像診断基準と類似疾患との厳格な鑑別
多発性外骨腫の初期診断は、特徴的なX線画像によって確定されます。世界保健機関(WHO)の診断基準では「長管骨の傍骨端部(Juxta-epiphyseal region)に、放射線学的に確認可能な骨軟骨腫が少なくとも2つ以上存在すること」が必要とされています。
診断において最も重要なプロセスの一つは、類似の臨床所見や放射線学的外観を呈する他の骨・軟骨系異形成症候群との厳格な鑑別です。疾患ごとに原因遺伝子、病変の成長方向、そして何より悪性化のリスクプロファイルが全く異なるため、正確な鑑別診断は治療方針の決定において不可欠です。
🔍 HMEと鑑別すべき主要な疾患群の決定的な違い
- メタコンドロマトーシス (PTPN11変異): 外側へ突出する外骨腫に加えて、骨髄内の「内軟骨腫」が同時に多発します。病変は手足の指に好発し、HMEとは逆に関節に向かって成長します。長管骨の著しい短縮は引き起こしません。
- Ollier病 / Maffucci症候群: 病変が骨の「外側」への突出ではなく、「内側(髄腔内)」に多数の良性硝子軟骨性腫瘍が形成されます。原則として非遺伝性です。
- Trevor病 (Dysplasia Epiphysealis Hemimelica): 病変が骨幹端部ではなく、関節軟骨と連続した「骨端部」そのものの片側に形成され、重度の関節変形を来します。
- Langer-Giedion症候群 / Potocki-Shaffer症候群: それぞれEXT1、EXT2の微小欠失を含む隣接遺伝子症候群であり、HME単独では見られない特異な顔貌、頭蓋骨の骨化遅延、知的障害を伴います。
- 進行性骨化性線維異形成症 (FOP / ACVR1変異): 骨の異常な突出ではなく、筋肉や腱の中に異所性骨(Heterotopic ossification)が進行性に形成され、「フレアアップ」と呼ばれる急性の疼痛と腫脹発作を繰り返す、全く異なるメカニズムの疾患です。
7. 最大の脅威:悪性転化(二次性軟骨肉腫)のリスクとMRI診断
多発性外骨腫の自然史において、患者様の生命を直接的に脅かす最も深刻な合併症が、既存の良性骨軟骨腫が「二次性末梢性軟骨肉腫(Secondary peripheral chondrosarcoma)」へと悪性転化(Malignant transformation)することです。
孤発性(単発性)の骨軟骨腫が悪性化するリスクが約1%程度であるのに対し、多発性外骨腫の患者様が生涯にわたって悪性転化を経験するリスクは、推計で約2%から最大10%に達し、加齢とともにその危険性は増大します。悪性化は通常、腫瘍の表面を覆っている「軟骨帽(Cartilage cap)」の深部または内部で発生します。発症の平均年齢は約31歳とされており、10歳未満の小児期における発症は極めて稀です。また、病変の発生部位によって悪性化のリスクには明確な差があり、四肢の遠位(手足)よりも、骨盤、腸骨、肩甲骨、近位大腿骨といった体幹部に近い部位(Central skeleton)に存在する病変ほど、悪性転化の発生率が高いことが広く認知されています。
7.1 悪性化を疑うべき臨床サインとMRIによる軟骨帽の評価
骨格の成長が終了し、成長板が完全に閉鎖した成人患者様において、「長年にわたってサイズの変わらなかった既存の骨軟骨腫が再び増大し始めた」、あるいは「病変の周囲に新たな安静時痛や運動時痛が出現した」場合は、いかなる場合であっても直ちに悪性転化の可能性を強く疑い、迅速な精密検査へ移行しなければなりません。
悪性化の確定診断および除外診断において、最も信頼性の高いゴールドスタンダードはMRI(磁気共鳴画像法)です。MRIの最大の目的は、軟骨肉腫の発生源となる「軟骨帽の厚さ」をミリメートル単位で正確に測定することです。
🔖 専門用語:軟骨帽(Cartilage cap)
骨軟骨腫(外骨腫)の表面をキャップのように覆っている硝子軟骨の層です。成長期にはここから腫瘍が大きくなります。大人になると通常は数ミリの厚さに退縮しますが、これが再び分厚くなることが悪性化(がん化)の最も重要なサインとなります。
臨床的なカットオフ閾値は、患者様の骨格成熟度(年齢)によって厳密に区別されます。
- 成人患者の閾値:成人の良性骨軟骨腫の軟骨帽は通常数ミリ程度に退縮しています。したがって、MRIにおいて軟骨帽の厚さが1.5cm(15mm)〜2.0cmを超える場合、悪性化の疑いが極めて強い(Highly suspicious of malignancy)とみなされます。
- 小児患者の閾値:成長期にある小児では、活発な内軟骨性骨化が行われているため、軟骨帽が自然に厚くなるのが正常な生理的現象です。成人の閾値を適用すると偽陽性が多発するため、小児においては厚さが3.0cm(30mm)を超える場合が、悪性化を疑う境界線となります。
さらに、T2強調MRI画像において軟骨基質内にガドリニウム造影剤の異常な取り込みが認められる場合や、近年補助的に用いられるFDG-PETスキャンにおいて腫瘍の糖代謝活性(SUV_max)が「2.0」を超えることは、悪性化の強力な傍証となります。万が一悪性転化が確認された場合は、直ちに骨軟部腫瘍の専門センターにて、腫瘍本体と周囲の安全域(Tumor-free margins)を確保した広範な一括切除(En-bloc resection)が必要となります。
💡 寿命・予後についてのご不安へ
「がん化」と聞くと非常に怖いイメージを持たれるかもしれませんが、過度に絶望する必要はありません。定期的なMRIで早期発見し、適切に切除できれば、命に関わる事態(寿命への影響)は十分に防ぐことが可能です。生涯にわたる検査は、患者様の命と未来を守るための前向きなアクションです。
8. 外科的介入戦略と慢性疾患としてのQOL(生活の質)への影響
現在、多発性外骨腫の根本原因であるヘパラン硫酸の欠乏を修復し、外骨腫の形成そのものを完全に食い止める承認された原因療法(内服薬など)は存在しません。したがって、臨床管理の主体は、物理的障害に対する対症療法的な外科手術と、悪性転化の早期発見を目指した長期的なサーベイランスです。
無症状の病変に対して、単なる美容上の懸念を理由とした予防的切除は推奨されません。良性外骨腫の単純切除を行う際、術後の局所再発を防ぐための絶対的な外科的原則は、「軟骨帽と、それを覆っている軟骨膜(Overlying perichondrium)を完全に含めて一塊として切除すること」です。軟骨膜の細胞がわずかでも残存すれば、そこから新たな腫瘍が再生する危険性が高いためです。
9. 新規分子標的治療の展望とパロバロテン臨床試験からの教訓
外科的手術以外の選択肢がなかった本疾患において、病態の根本を直接標的とし、外骨腫の発生そのものを抑制する「生物学的アプローチに基づく薬理学的介入」は次世代のフロンティアです。
パロバロテン(Palovarotene)の挑戦と治験中止の深い理由
近年、世界中の研究者と患者様から最も熱い注目を集めた化合物が「パロバロテン」です。この薬剤は元々、全く別の超希少難病である進行性骨化性線維異形成症(FOP)の治療薬として開発されました。FOPはBMPシグナルが過剰に活性化し筋肉が骨に置き換わる疾患であり、パロバロテンはBMPシグナル経路を直接的に阻害する作用でFDA承認を獲得しました。
🔖 専門用語:BMPシグナル(骨形成タンパク質シグナル)
細胞に対して「骨や軟骨を作りなさい」という強力な指令を伝える情報伝達の経路です。多発性外骨腫では、ヘパラン硫酸が不足することでこのシグナルが暴走し、不要な腫瘍(外骨腫)が作られてしまうと考えられていました。
多発性外骨腫(HME)の腫瘍形成プロセスにも、ヘパラン硫酸欠乏によって制御不能となったBMPシグナルの関与が強く疑われており、マウスモデルで強力な予防効果が確認されたため、14歳以下の小児HME患者様を対象とした国際第2相臨床試験(MO-Ped試験)が開始されました。しかし、最終的な結果は非常に厳しいものでした。パロバロテンは小児HME患者様に対して骨軟骨腫の発生を抑制するという明確な有効性を示すことができず、全身性レチノイド特有の有害事象プロファイルが確認されたため、試験は早期中止に至りました。
この治験の失敗は、FOPの「異所性骨化」とHMEの「内軟骨性腫瘍形成」が、一見似たようなBMPシグナル異常を背景に持ちながらも、その根底にある細胞駆動メカニズムが全く異なることを示す極めて重要な教訓をもたらしました。
次世代の代替分子標的と将来の方向性
パロバロテンの限界が明らかになった現在、基礎研究の関心は、よりHMEの特異的な病態生理(ヘパラン硫酸欠乏環境)に根ざした別のシグナル伝達経路の調節へとシフトしています。
- ヘパラナーゼ拮抗薬(SST0001など): 細胞外のヘパラン硫酸鎖を酵素的に切断するヘパラナーゼを阻害し、残存するヘパラン硫酸を守るアプローチ。in vitro研究で軟骨形成プロセスの抑制が確認され、有望視されています。
- ヘッジホッグシグナル伝達拮抗薬(HhAntag): 成長板における細胞の増殖と分化の中核を担うIHH経路を直接的にブロックするアプローチ。
- 全トランス型レチノイン酸(ATRA): P63などの軟骨特異的分子をダウンレギュレートすることで、間葉系細胞の異常な軟骨形成を抑制する作用が基礎研究で確認されています。
多発性外骨腫の完全な克服への道程は平坦ではありませんが、世界的なゲノム解析の進展と新たな分子標的の探求は確実に前進しています。今後の疾患管理においては、ご自身の遺伝的背景を正確に把握するための遺伝子検査(NGSパネルなど)の活用と、成人後の厳密なサーベイランス体制の構築が何よりも重要です。
よくある質問(FAQ)
関連記事
参考文献
- [1] Hereditary Multiple Exostoses-A Review of the Molecular Background, Diagnostics, and Potential Therapeutic Strategies – Frontiers [Link]
- [2] Multiple Hereditary Exostoses: Genetics, Multimodality Imaging Features, Complications, Differential Diagnosis, and Treatment – LWW [Link]
- [3] Hereditary multiple osteochondromas in a child: a case report and discussion of postoperative complication management – Frontiers [Link]
- [4] Hereditary Multiple Osteochondromas – GeneReviews® – NCBI Bookshelf [Link]
- [5] A New Classification System for Forearm Deformities Caused by Hereditary Multiple Osteochondromas – PubMed [Link]
- [6] Palovarotene for patients with multiple hereditary exostosis: results of MO-Ped, a terminated, randomized, placebo-controlled, double-blind phase 2 trial – PMC [Link]