目次
重症早期発症型網膜ジストロフィ(EOSRD)は、生後まもない乳幼児期から始まる急速かつ不可逆的な視力の喪失を特徴とする、遺伝性網膜疾患の総称です。原因となる遺伝子は数百種類にのぼり、診断には次世代シーケンシングを用いた網羅的な遺伝子解析が不可欠です。本記事では、非症候群性EOSRDの主因遺伝子であるABCA4と、しばしば混同されるABCD4の決定的な違いを含め、症状・診断・治療まで臨床遺伝専門医がわかりやすく解説します。
Q. 重症早期発症型網膜ジストロフィとは何ですか?まず結論だけ知りたいです
A. 出生後まもなく〜若年期に発症し、網膜の光受容体細胞が急速に失われていく遺伝性眼疾患の総称です。原因遺伝子は数百種類にのぼり、最も頻度が高い非症候群性(全身症状を伴わない)タイプの主因はABCA4遺伝子変異です。一部に「ABCD4遺伝子変異によるEOSRD」という記述が流通していますが、これはデータベース上の注釈エラーに起因する誤りであり、真のABCD4変異は全身性の代謝異常症(cblJ欠損症)の中で二次的に網膜障害を引き起こします。
- ➤疾患の定義 → OMIM C1855465、LCA・スターガルト病・錐体杆体ジストロフィと重複する表現型群
- ➤ABCA4とABCD4の決定的な違い → 細胞内局在・分子機能・疾患の性質がまったく異なる
- ➤主な症状 → 急速な視力低下・眼振・夜盲・視野狭窄・ERG異常
- ➤診断アプローチ → 次世代シーケンシング(遺伝子パネル・全エクソーム解析)+代謝マーカー評価
- ➤治療戦略 → 原因遺伝子によって治療法が根本的に異なる・誤診は治療の誤りに直結する
1. 重症早期発症型網膜ジストロフィ(EOSRD)とは
重症早期発症型網膜ジストロフィ(Early-Onset Severe Retinal Dystrophy:EOSRD)は、出生直後から若年期にかけて発症し、網膜の光受容体細胞(視細胞)および網膜色素上皮(RPE)が進行性かつ不可逆的に変性する遺伝性網膜疾患の総称です。単一の疾患ではなく、複数の遺伝子変異によって引き起こされるさまざまな病態を包括する概念です。
💡 用語解説:網膜ジストロフィとは
「網膜ジストロフィ(Retinal Dystrophy)」とは、遺伝子の変異によって網膜の細胞が徐々に壊れていく疾患群の総称です。網膜は眼球の奥に広がる薄い膜で、光を感じる「視細胞(光受容体細胞)」が密集しており、ここで受け取った光の信号が脳に送られることで「見える」が成立します。ジストロフィとは「栄養失調性変性」を意味し、遺伝子の異常によって細胞の維持に必要なタンパク質が正常につくられなくなることで、細胞が少しずつ死んでいく状態を指します。
臨床的には、レーバー先天黒内障(LCA)・早期発症型スターガルト病・進行性の錐体杆体ジストロフィといった複数の表現型と重複し、視力喪失・求心性視野狭窄・網膜電図(ERG)の著明な異常を特徴とします。これまでに数百の遺伝子変異が関連付けられており、次世代シーケンシング(NGS)を用いた網羅的な解析が診断の要となっています。
💡 用語解説:レーバー先天黒内障(LCA)
EOSRDの中でも特に重篤な表現型の一つです。生後1年以内に発症し、網膜電図(ERG)がほぼ完全に消失するほどの重篤な視覚障害を特徴とします。「先天」とついていますが、出生時から全盲というわけではなく、多くは生後数ヶ月〜1年以内に急速に視力が失われます。眼振(目がぶるぶると動く)や指で目を押す「オクロデジタルサイン」が特徴的な所見です。原因遺伝子は20種類以上が報告されており、その一部はABCA4遺伝子の両アレル性完全機能喪失変異によって引き起こされます。
EOSRDは大きく2つのカテゴリーに分けて理解するのが重要です。ひとつは「非症候群性EOSRD」——網膜のみに障害が現れ、全身の代謝や他臓器には異常を伴わないタイプです。もうひとつは「症候群性EOSRD」——全身性の遺伝性疾患の一部として網膜障害が現れるタイプです。この二つを正確に区別することが、適切な治療選択において決定的に重要です。
👁️ 非症候群性EOSRD
- 眼のみに症状が限局
- 全身の代謝異常を伴わない
- 主因遺伝子:ABCA4(最多)
- 治療:ビタミンAを避ける・遺伝子治療
⚠️ 症候群性EOSRD
- 全身疾患の一部として網膜障害が現れる
- 神経・代謝・血液障害を伴う
- 代表例:ABCD4変異(cblJ欠損症)
- 治療:高用量ビタミンB12の筋肉注射が必須
2. 原因遺伝子とメカニズム――ABCA4とABCD4の決定的な違い
EOSRDの遺伝的原因を理解するうえで、最も重要かつ混乱しやすいポイントが「ABCA4」と「ABCD4」の混同問題です。名前が似ているため学術文献やデータベース上での誤記が散見されますが、両者は細胞内の局在・分子機能・引き起こす疾患のすべてが根本的に異なります。この違いを正確に把握することが、正確な診断と適切な治療選択への第一歩です。
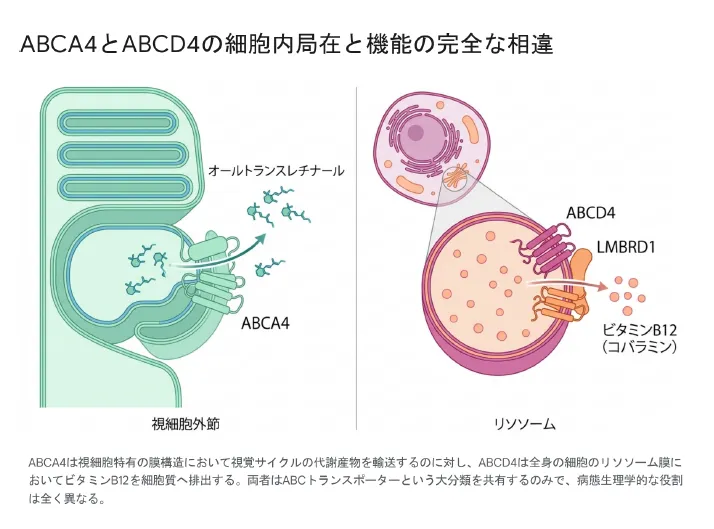
ABCA4は視細胞外節において視覚サイクルの代謝産物を輸送するのに対し、ABCD4は全身の細胞のリソソーム膜においてビタミンB12を細胞質へ排出する。両者はABCトランスポーターという大分類を共有するのみで、病態生理学的役割はまったく異なる。
非症候群性EOSRDの主役:ABCA4遺伝子と視覚サイクル障害
非症候群性EOSRDおよびスターガルト病・眼底白点症の主たる原因遺伝子は、第1染色体にマッピングされるABCA4(ABC1サブファミリー)です。ABCA4タンパク質は、網膜の光受容体細胞(主に杆体・錐体の外節円板膜)に極めて特異的に発現する大型の膜貫通タンパク質で、視覚サイクルにおいて不可欠な役割を担います。
💡 用語解説:視覚サイクルとABCA4の役割
私たちが「光を見る」たびに、視細胞の中では光の信号を受け取るための化学反応(視覚サイクル)が繰り返されます。光を受けると「11-シス-レチナール」という物質が「オールトランスレチナール」に変化し、このオールトランスレチナールを速やかに細胞の外へ排出することが次の光感知の準備になります。ABCA4は、このオールトランスレチナールをATPのエネルギーを使って円板膜の内側から外側へ能動的に輸送する「ポンプ」として機能します。ABCA4が壊れると、オールトランスレチナールが細胞内に蓄積し、毒性の高い物質「A2E」などのビスレチノイド化合物となって網膜色素上皮(RPE)細胞を傷つけ、最終的に視細胞が広範に死滅します。
ABCA4変異の重症度と表現型には強い相関があります。両アレル性の完全な機能喪失(ヌル変異)は、出生後最初の10年以内に発症する急速で重篤な進行性網膜ジストロフィ(EOSRD・重症錐体杆体ジストロフィ・網膜色素変性19型)を引き起こします。一方、部分的な機能が残存する軽度のミスセンス変異は遅発型のスターガルト病や加齢黄斑変性につながります。
早期発症型スターガルト病(STGD1)・重症錐体杆体ジストロフィ3型(CRD3)・網膜色素変性症19型(RP19)・眼底白点症(Fundus flavimaculatus)
真のABCD4遺伝子:リソソーム・コバラミン輸送体
一方、ABCD4(ALDサブファミリー)は、ABCA4とはまったく異なる遺伝子です。ABCA4が「網膜視細胞の外節円板膜」に局在するのに対し、ABCD4は「全身のあらゆる細胞のリソソーム膜」に存在します。その機能も視覚サイクルとは無関係で、リソソーム内に取り込まれたビタミンB12(コバラミン)を細胞質へ排出するポンプとして働きます。
💡 用語解説:リソソームとは
リソソームは細胞の中にある「ごみ処理施設」のような小器官です。食べ物や血液から取り込まれたビタミンB12は、まずリソソームの中で不要なタンパク質(トランスコバラミンII)から切り離されます。その後、遊離したビタミンB12はABCD4という「ポンプ」によって細胞質へ運び出されます。ABCD4が壊れると、ビタミンB12がリソソームに「閉じ込められた」状態になり、細胞質やミトコンドリアが極度のビタミンB12不足に陥ります。
ABCD4遺伝子に病的変異が生じると、cblJ型メチルマロン酸血症・ホモシスチン尿症(MAHCJ)という超希少な全身性代謝異常症を引き起こします。この疾患では、ビタミンB12不足によって「メチルマロン酸」と「ホモシステイン」という毒性物質が全身に蓄積し、脳・血液・腎臓・そして網膜に深刻なダメージを与えます。つまり、ABCD4変異による網膜障害は「全身性代謝異常症の一症状」であり、ABCA4変異による純粋な眼の疾患とは本質的に異なります。
| 比較項目 | ABCA4(ABC1サブファミリー) | ABCD4(ALDサブファミリー) |
|---|---|---|
| 細胞内局在 | 網膜光受容体細胞の外節円板膜 | 全身の細胞のリソソーム膜 |
| 主要な分子機能 | オールトランスレチナールの輸送(視覚サイクル) | ビタミンB12のリソソームから細胞質への排出 |
| 関連疾患 | スターガルト病1型・EOSRD・CRD3・RP19・眼底白点症 | cblJ型MAHCJ(全身性代謝異常症) |
| 疾患の性質 | 非症候群性(眼のみ) | 症候群性(全身性代謝異常+二次的網膜症) |
| 治療の方向性 | ビタミンA回避・遺伝子治療・薬物療法 | 高用量ヒドロキソコバラミン筋注・ベタイン・葉酸補充 |
ABCA4遺伝子のさらに詳しい分子機能については、ABCA4遺伝子ページをあわせてご覧ください。
3. 主な症状・眼科所見
EOSRDの主な眼科的症状は、病型(非症候群性か症候群性か)によって発症時期や進行速度に差があるものの、最終的な臨床像は非常に共通しています。いずれも視力の急速かつ不可逆的な低下が中心であり、子どもの場合は本人が症状を言葉で伝えられないため、保護者が異変に気づいた時点ですでに進行していることも少なくありません。
👁️ 視力・視野の異常
- 出生後〜1歳以内に始まる急速な視力低下
- 求心性視野狭窄(周辺視野から徐々に失われる)
- 夜盲(暗い場所での視力障害、杆体障害の初期症状)
- 羞明(明るい光への過敏)
👀 眼球運動の異常
- 感覚性眼振(眼球がぶるぶると動く):視力喪失に伴う代償性変化
- 斜視(目の向きが左右でそろわない)
- 迷走眼球運動(視線を一点に定められない)
🔬 眼底・網膜の所見
- 黄斑部の色素異常・ブルズアイ状黄斑
- 網膜周辺部への変性拡大・色素性網膜症
- 軽度〜高度の視神経乳頭蒼白・視神経萎縮
📊 検査所見(ERG・OCT)
- ERG暗視反応の消失(杆体視細胞の広範な機能不全)
- OCT:網膜全体の菲薄化・外顆粒層・RPEの消失
- 進行すると明所視ERGも消失(ERG完全平坦化)
💡 用語解説:網膜電図(ERG:Electroretinogram)
光を目に当てたときに網膜で発生する電気信号を記録する検査です。視細胞が正常に機能していれば大きな波形が記録されますが、視細胞が死滅・機能不全に陥ると波形が小さくなり、最終的には完全に平坦化(反応なし)になります。「暗視反応(scotopic response)」は杆体視細胞の機能を、「明所視反応(photopic response)」は錐体視細胞の機能を反映します。EOSRDでは生後まもない段階から暗視反応が著明に低下または消失しており、これが「早期発症型」診断の重要な根拠となります。
💡 用語解説:光干渉断層計(OCT:Optical Coherence Tomography)
赤外線レーザーを使って網膜の断面を高解像度で画像化する検査です。MRIが身体の断面を撮るように、OCTは網膜の各層構造(外顆粒層・網膜色素上皮など)の厚さや状態を詳しく評価できます。EOSRDでは、ERGが完全に平坦化するより早い段階から、OCTで網膜全体の菲薄化や光受容体外節の消失が確認されることがあります。進行すると最終的にすべての網膜層構造が消失した「萎縮性黄斑症」の状態になります。
症候群性EOSRD(cblJ欠損症)の治療生化学的応答:全身と網膜のパラドックス
ABCD4変異(cblJ欠損症)による網膜ジストロフィでは、高用量ヒドロキソコバラミンによる全身治療が開始されると、血液中の毒性物質は劇的に改善します。しかし、全身の生化学的改善が達成されているにもかかわらず、網膜変性は止まらないという深刻なパラドックスが存在します。
ABCD4遺伝子変異患者におけるビタミンB12強化治療の生化学的応答
総ホモシステイン(μmol/L)
メチルマロン酸(mmol/mol creatinine)
高用量ヒドロキソコバラミン筋肉内投与(週1〜3回)後、4ヶ月で血中総ホモシステインおよびメチルマロン酸レベルが劇的に減少し正常範囲に近づいた。生化学的パラメーターの正常化は達成されるが、並行して発生している網膜ジストロフィの進行抑制効果については限界が指摘されている。
4. 鑑別診断:似ている疾患との見分け方
EOSRDは表現型が多様であり、多くの遺伝性網膜疾患と症状が重なります。正確な診断のためには、臨床所見と遺伝子検査・生化学検査を組み合わせた段階的なアプローチが必要です。
スターガルト病1型(STGD1)との鑑別
共通点:ABCA4変異・黄斑変性・ERG異常
違い:スターガルト病は軽度のミスセンス変異で部分機能が残存し、発症が遅め(学童期〜成人)。EOSRDは両アレル性完全機能喪失で生後10年以内に発症・ERG早期消失。詳しくはスターガルト病1型ページへ。
錐体杆体ジストロフィ3型(CRD3)との鑑別
共通点:ABCA4変異・黄斑萎縮・視力低下・ERG異常
違い:CRD3では錐体(色と明るさを見る細胞)が先に障害を受け、明所視ERGの低下が先行。EOSRDは杆体・錐体双方が早期から急速に障害される。詳しくはCRD3ページへ。
網膜色素変性症19型(RP19)との鑑別
共通点:ABCA4変異・夜盲・視野狭窄・骨小体様色素沈着
違い:RP19では杆体優位の変性が周辺から中心に向かう。EOSRDは中心黄斑から早期に障害される傾向がある。詳しくはRP19ページへ。
cblJ欠損症(ABCD4変異)による症候群性EOSRD
注意点:眼科的所見のみではLCAや非症候群性EOSRDと区別が困難。
鑑別のポイント:全身症状(筋緊張低下・発達遅滞・巨赤芽球性貧血)の有無と「血漿ホモシステイン上昇+尿中MMA上昇+血清B12低値」の組み合わせが鑑別に直結。
5. 診断・遺伝子検査のアプローチ
EOSRDの確定診断には、眼科的評価・生化学的スクリーニング・分子遺伝学的検査の三本柱を組み合わせた段階的アプローチが必要です。特に症候群性(cblJ欠損症など)か非症候群性(ABCA4変異など)かを早期に見極めることが、治療方針を左右します。
眼科的評価:まず行うべき検査
💡 EOSRDが疑われる乳幼児への眼科的評価の流れ
- ➤眼底検査:黄斑色素異常・ブルズアイ黄斑・視神経蒼白・色素性網膜症の確認
- ➤網膜電図(ERG):暗視・明所視反応の評価。EOSRDでは生後まもない段階で暗視反応消失が特徴的
- ➤OCT(光干渉断層計):網膜全層の菲薄化・外顆粒層・RPE消失の程度評価
- ➤視力・眼振の評価:感覚性眼振の存在はすでに不可逆的な網膜障害が進行しているサイン
生化学的スクリーニング:症候群性EOSRDの鑑別に必須
眼科所見とあわせて、以下の生化学的マーカーを評価することで、ABCD4変異(cblJ欠損症)による症候群性EOSRDを速やかに鑑別できます。
| 検査項目 | cblJ型(ABCD4変異)での所見 | 鑑別上の意義 |
|---|---|---|
| 血漿総ホモシステイン(tHcy) | 著明な上昇(50 μmol/L以上) | MTR経路の障害を示す |
| 尿中・血中メチルマロン酸(MMA) | 著明な上昇 | MUT経路の障害を示す |
| 血清ビタミンB12 | 低値〜正常下限が多い | cblC型(正常〜高値)との重要な鑑別点 |
| 血液算定(MCV等) | 巨赤芽球性貧血・大球性貧血・汎血球減少 | 骨髄のDNA合成障害を反映 |
💡 用語解説:ホモシステインとメチルマロン酸
ホモシステイン(Homocysteine)は体内で生成されるアミノ酸の一種で、通常はメチオニンというアミノ酸に変換されて消費されます。ビタミンB12が細胞質に届かないと、この変換が止まりホモシステインが蓄積します。ホモシステインは血管・神経・網膜の細胞に対して強い毒性を持ちます。メチルマロン酸(MMA)はミトコンドリア内でのビタミンB12依存性の代謝が障害されると蓄積する物質で、代謝性アシドーシスや神経毒性を引き起こします。この2つが同時に上昇する「複合型」はcblJ欠損症・cblC欠損症などの細胞内コバラミン代謝異常症の特徴です。
次世代シーケンシング(NGS)による確定診断
💡 用語解説:次世代シーケンシング(NGS)とは
次世代シーケンシング(NGS:Next-Generation Sequencing)は、一度に多数の遺伝子を同時に解読できる最新の遺伝子解析技術です。従来のサンガー法(一遺伝子ずつ解読)とは異なり、EOSRDに関連する数百の遺伝子を一度に調べられる「網膜ジストロフィ遺伝子パネル検査」や、タンパク質をコードするすべての遺伝子領域を一気に解析する「全エクソームシーケンス(WES)」が実用化されています。EOSRDの原因遺伝子が多様なため、NGSによる網羅的解析は診断に不可欠なツールです。
NGSによりABCA4またはABCD4の両アレル性(常染色体潜性遺伝のため、父方・母方両方から変異を受け継ぐ必要がある)病的バリアントが同定されることで確定診断となります。ABCD4変異が同定された場合は、前述の生化学的マーカー測定と組み合わせることで、cblJ欠損症の確定診断と治療開始が可能になります。
💡 用語解説:常染色体潜性遺伝(劣性遺伝)とは
ABCA4・ABCD4変異はどちらも常染色体潜性遺伝(以前は「劣性遺伝」と呼ばれていました)の形式をとります。これは「父から受け継いだ遺伝子」と「母から受け継いだ遺伝子」の両方に変異がある場合に発症するという意味です。片方だけに変異があるご両親(キャリア)は症状が出ません。お子さんが発症する確率は理論上25%(4人に1人)です。ご両親はどちらも健康でありながらお子さんが発症するため、家族が大きな衝撃を受けることが多く、遺伝カウンセリングが非常に重要です。
6. 治療・長期管理
EOSRDの治療戦略は、原因遺伝子によって根本的に異なります。非症候群性(ABCA4変異など)と症候群性(ABCD4変異・cblJ欠損症)では治療法がまったく違うため、正確な診断が治療の出発点です。
非症候群性EOSRD(ABCA4変異)の治療
⚠️ ビタミンAサプリメントの回避
ABCA4機能不全下では、ビタミンAの過剰が有害なビスレチノイド(A2E)の蓄積を加速させる可能性があります。網膜色素変性症の他のタイプでは補充療法が有効な場合がありますが、ABCA4変異患者へのビタミンA補充は禁忌です。診断を知らずにビタミンAサプリを服用することは病状を悪化させるリスクがあります。
🔬 遺伝子治療(臨床試験中)
ABCA4遺伝子は大型すぎて従来のAAVベクターに乗らないという技術的課題がありましたが、二重AAVベクター法や最新のリポナノ粒子法が開発され、国際的な臨床試験が進行中です。将来的に根本治療となる可能性があります。
💊 薬物療法(エミクススタト等)
視覚サイクルを緩やかにし、有害なオールトランスレチナール産生を抑制する「エミクススタト塩酸塩」が研究・臨床試験段階にあります。光を避ける(強い光への暴露を減らす)という生活指導も補完的に推奨されます。
症候群性EOSRD(ABCD4変異・cblJ欠損症)の治療
💡 用語解説:ヒドロキソコバラミンとは
ヒドロキソコバラミン(Hydroxocobalamin / OHCbl)はビタミンB12の一形態です。一般的なビタミンB12サプリに含まれるシアノコバラミンとは異なり、細胞内でアデノシルコバラミン(AdoCbl)とメチルコバラミン(MeCbl)への変換効率が極めて高いため、ABCD4変異のように細胞内輸送に欠陥がある患者でも効果を発揮しやすいとされています。cblJ欠損症の治療では、高用量ヒドロキソコバラミンを筋肉内注射(IM)で生涯にわたって投与することが国際的なガイドラインで推奨されています。経口のビタミンB12では代替できません。
治療の初期導入段階では連日の筋肉内注射が行われ、急性期の代謝不全をコントロールします。その後、週3回→週1回の維持療法へと移行します。これにより、血中ホモシステインとMMAは数ヶ月以内に著明に改善し、巨赤芽球性貧血・筋緊張低下・脳症・反復性腹痛などの生命を脅かす全身症状は劇的に消失します。さらにベタイン(Betaine)・葉酸・ピリドキシン(ビタミンB6)の経口補充を組み合わせることで、神経予後と生存率の改善が期待されます。
複数の専門家が指摘しているように、網膜の不可逆的な構造変性や感覚性眼振が完全に定着する前に超早期に高用量治療を開始できれば、網膜変性の進行速度を決定的に遅延させ、感覚性眼振の発生を予防できる可能性があります。生化学的異常が疑われた時点で、確定診断を待たずに治療を開始することが視力予後を左右する最重要ポイントです。
7. 遺伝カウンセリング
EOSRDの確定診断後、当事者・ご家族への丁寧な遺伝カウンセリングが不可欠です。「なぜ我が子が?」という疑問、再発リスク、次の子どもへの影響、出生前診断の選択肢——これらすべてについて、臨床遺伝専門医が時間をかけて対話することが遺伝カウンセリングの役割です。
- ➤遺伝形式と再発リスク:ABCA4・ABCD4変異はどちらも常染色体潜性遺伝です。両親がそれぞれキャリアであれば、次子への遺伝確率は理論上25%。ご両親自身は通常、症状が出ません。
- ➤出生前診断の選択肢:次子を望む場合、絨毛検査・羊水検査による出生前遺伝子診断が可能です。既知の変異が同定されている場合は確実な診断ができます。
- ➤患者本人の将来:成長後に子どもを持つ場合、遺伝する確率は相手の遺伝子型によって変わります。パートナーがキャリアであれば50%、非キャリアであれば0%(ただしすべてキャリアになります)。
- ➤支援資源の案内:希少眼疾患の患者団体・難病指定申請・補助器具・教育的支援制度など、生活の質を支えるための社会的情報提供も遺伝カウンセリングの重要な柱です。
8. よくある誤解
誤解①「ABCD4変異=眼の病気」
ABCD4変異はcblJ欠損症という重篤な全身性代謝異常症を引き起こします。網膜障害は二次的な症状のひとつに過ぎず、貧血・神経障害・代謝性アシドーシスなど生命に関わる全身症状への対応が最優先です。
誤解②「ビタミンB12を飲めば網膜も治る」
高用量ヒドロキソコバラミン筋肉内注射は全身の生化学的正常化に劇的な効果を持ちますが、すでに壊れた網膜光受容体は再生しません。また経口のビタミンB12サプリでは代替できません。医師の処方による適切な治療が必要です。
誤解③「ABCA4変異にビタミンAは有効」
網膜色素変性症の一部にはビタミンA補充が有効ですが、ABCA4変異患者へのビタミンA補充は有害となる可能性があります。視覚サイクルの産物であるオールトランスレチナールが増加し、毒性ビスレチノイドの蓄積を加速させるリスクがあるためです。
誤解④「眼振が出てから治療を始めれば間に合う」
感覚性眼振が現れた時点で、すでに不可逆的な網膜ダメージが進行しています。特にcblJ欠損症では、眼振・視力障害が顕在化する前に生化学的異常が疑われた段階で治療を開始することが視力予後を大きく左右します。
9. 臨床遺伝専門医からのメッセージ
よくある質問(FAQ)
🏥 遺伝性網膜疾患・遺伝子検査のご相談
EOSRDをはじめとする遺伝性眼疾患・希少遺伝性疾患に関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
参考文献
- [1] NCBI MedGen. Severe early-childhood-onset retinal dystrophy (Concept Id: C1855465). [NCBI MedGen]
- [2] Gene Vision. ABCA4-retinopathy: for professionals. [Gene Vision]
- [3] NCBI Gene. ABCA4 gene entry (Gene ID: 24). [NCBI Gene]
- [4] Cornelis SS, et al. An Overview of the Genetics of ABCA4 Retinopathies, an Evolving Story. Genes (Basel). 2021;12(8):1241. [MDPI Genes]
- [5] Zernant J, et al. Expansion of the ABCA4-Associated Retinopathy Spectrum: Severe Variants Can be Associated With Early-Onset Severe Retinal Dystrophy. Invest Ophthalmol Vis Sci. 2023. [IOVS]
- [6] MedlinePlus Genetics. ABCA4 gene. [MedlinePlus]
- [7] Coelho D, et al. Clinical or ATPase domain mutations in ABCD4 disrupt the interaction with LMBRD1 and cause methylmalonic aciduria with homocystinuria, cblJ type. Nat Genet. 2012. PMC5512089. [PMC5512089]
- [8] Isgandarov K, et al. Cobalamin J Disorder in a Teenage Boy with Recurrent Abdominal Pain Attacks: A Case Report and Literature Review. PMC. 2025. PMC12688352. [PMC12688352]
- [9] Huemer M, et al. Guidelines for diagnosis and management of the cobalamin-related remethylation disorders cblC, cblD, cblE, cblF, cblG, cblJ and MTHFR deficiency. J Inherit Metab Dis. 2017;40(1):21-48. [PMC5203859]
- [10] Watkins D, Rosenblatt DS. Disorders of Intracellular Cobalamin Metabolism. GeneReviews® [Internet]. Seattle (WA): NCBI Bookshelf. [GeneReviews / NCBI]
- [11] Morel CF, et al. Ocular manifestations in patients with inborn errors of intracellular cobalamin metabolism: a systematic review. Orphanet J Rare Dis. 2021. [ResearchGate]
- [12] Retinal Changes in Early-Onset cblC Methylmalonic Acidemia Identified Through Expanded Newborn Screening. PMC12193327. [PMC12193327]
- [13] Ferrazzi F, et al. Vitamin B12 Deficiency and the Nervous System: Beyond Metabolic Decompensation. Int J Mol Sci. 2024;25(1):590. [MDPI IJMS]
- [14] tellmeGen. Methylmalonic Aciduria with Homocystinuria, cblJ type (MAHCJ). [tellmeGen]









