目次
ヌーナン症候群7型(Noonan Syndrome 7: NS7、OMIM #613706)は、第7染色体長腕(7q34)に位置するBRAF遺伝子の機能獲得型ミスセンス変異によって引き起こされる常染色体顕性遺伝の先天性多発奇形症候群です。ヌーナン症候群全体の約2%未満を占める比較的稀なサブタイプですが、RAS-MAPKシグナル伝達経路の恒常的な過剰活性化を通じて、特異的顔貌・先天性心疾患・低身長・神経発達遅滞をもたらし、同じBRAF遺伝子を原因とするCFC症候群やLEOPARD症候群3型と連続的な表現型スペクトラムを形成する点で臨床上きわめて重要な疾患です。
Q. ヌーナン症候群7型(NS7)とはどのような疾患ですか?まず結論だけ知りたいです
A. BRAF遺伝子の機能獲得型変異によって引き起こされる常染色体顕性遺伝の先天性多発奇形症候群(OMIM #613706)です。特異的顔貌・先天性心疾患・低身長・神経発達遅滞を主徴とし、同じBRAF遺伝子を原因とするCFC症候群やLEOPARD症候群3型と臨床的に連続したスペクトラムを形成する点が他のヌーナン症候群サブタイプと大きく異なる特徴です。
- ➤疾患の定義 → OMIM #613706、ヌーナン症候群全体の約2%未満、RAS異常症スペクトラムに属する
- ➤分子メカニズム → BRAF遺伝子(7q34)の機能獲得型変異によるMEK/ERKの恒常的過剰リン酸化
- ➤主な症状 → 特異的顔貌・肺動脈弁狭窄・肥大型心筋症(重症化リスク高)・低身長・知的障害(一部)
- ➤鑑別診断 → CFC症候群・LEOPARD症候群3型・神経線維腫症との連続スペクトラムと鑑別のポイント
- ➤診断・精密医療 → van der Burgt基準・マルチ遺伝子パネル・MEK阻害薬による精密医療の最前線
1. ヌーナン症候群7型とは:疾患の定義と位置づけ
ヌーナン症候群(Noonan Syndrome: NS)は、特徴的な頭蓋顔面部の異常(特異的顔貌)・先天性心疾患・著明な低身長・骨格異常・多様な程度の精神運動発達遅滞を主徴とする、常染色体顕性遺伝の多発奇形症候群です。出生1,000人から2,500人に1人の割合で発症すると推定されており、先天性心疾患を伴う遺伝性疾患としてはダウン症候群に次いで発生頻度が高い疾患の一つとして広く認識されています。
ヌーナン症候群にはPTPN11・SOS1・RAF1・RIT1・KRASなど多数の原因遺伝子が知られており、なかでもBRAF遺伝子の病的バリアントによって引き起こされるサブタイプが「ヌーナン症候群7型(Noonan Syndrome 7: NS7、OMIM #613706)」です。全ヌーナン症候群の約2%未満を占める稀なサブタイプですが、臨床的に重要な特徴を持ちます。
💡 用語解説:RAS異常症(RASopathies)とは
細胞の増殖・分化・生存・アポトーシスを制御する「RAS-MAPKシグナル伝達経路」を構成する遺伝子群の生殖細胞系列変異によって引き起こされる疾患群の総称です。ヌーナン症候群を筆頭に、心臓・顔貌・皮膚症候群(CFC症候群)・コステロ症候群・神経線維腫症1型・LEOPARD症候群などが含まれます。これらは分子メカニズムを共有しているため、臨床症状に多くのオーバーラップが見られることが特徴です。NS7はこのRAS異常症スペクトラムの中に位置づけられます。
💡 用語解説:常染色体顕性遺伝(じょうせんしょくたいけんせいいでん)
「常染色体」とは性染色体(X・Y)以外の染色体のこと。「顕性(優性)」とは、2本の染色体のうちどちらか1本に変異があるだけで症状が現れることを意味します。NS7では、変異したBRAF遺伝子を1つ持つだけで発症します。変異を持つ親から子への遺伝確率は理論上50%です。ただし、ヌーナン症候群の多くのケースは両親からの遺伝ではなく、精子や卵子の形成過程で偶発的に生じた「de novo(新生)変異」によって引き起こされます。
ヌーナン症候群7型が他のサブタイプと特に異なる点は、原因遺伝子であるBRAFがCFC症候群(心臓・顔貌・皮膚症候群)の主要原因遺伝子でもあるという点です。つまり、同一のBRAF遺伝子に生じた変異であっても、その変異の種類や位置によって「ヌーナン症候群7型」と「CFC症候群」という異なる疾患ラベルが与えられ、両者の臨床的境界はしばしば曖昧で連続的なスペクトラムを形成します。このことが、NS7の診断を複雑にする最大の要因の一つとなっています。
2. 原因遺伝子BRAFとRAS-MAPKシグナル伝達経路
NS7の病態を理解するうえで核心となるのが、RAS-MAPKシグナル伝達経路とそこに位置するBRAF遺伝子の役割です。このシグナル経路の異常が、なぜ心臓・顔面・骨格・神経系など多臓器にわたる先天異常を一挙に引き起こすのか——そのメカニズムを順を追って解説します。
💡 用語解説:RAS-MAPKシグナル伝達経路とは
細胞の外から増殖因子・サイトカイン・ホルモンなどのシグナルが届くと、細胞膜上の受容体がそれを受け取り、細胞内に情報を伝えるリレー経路(カスケード)です。具体的には 受容体チロシンキナーゼ → RAS → RAF(BRAF含む)→ MEK → ERK という順に連鎖的なリン酸化反応が起こり、最終的にERKが核内に移行して細胞増殖・分化・生存を制御する転写因子を活性化します。胚発生期におけるこの経路の精密な制御は、正常な臓器形成に不可欠です。
BRAF遺伝子の機能獲得型変異がもたらすもの
💡 用語解説:機能獲得型変異(Gain-of-Function mutation)
変異によってタンパク質が本来の調節機構を超えた「余計な機能」または「強すぎる機能」を獲得してしまう変異です。NS7でのBRAF変異では、B-Rafタンパク質が上流からの制御シグナルを待たずに「常にオンの状態」に陥ります。これは電球のスイッチが壊れて消えなくなるようなイメージで、MEK・ERKを継続的に過剰に活性化し続けます。この状態が胚発生期に生じることで、心臓・顔面・骨格・神経系などの発達プログラムが乱されます。
第7染色体長腕(7q34)に位置するBRAF遺伝子は、セリン/スレオニンキナーゼであるB-Rafタンパク質をコードする原がん遺伝子です。正常な細胞では、B-Rafは上流のRASから活性化シグナルを受けて一時的にMEKをリン酸化し、役割を終えると速やかに不活性化されます。しかしNS7を引き起こすBRAFの病的バリアント(その多くはミスセンス変異)では、この自己抑制機能が破綻し、B-Rafが恒常的に活性化された状態を維持します。
このキナーゼ活性の持続的な亢進は、下流のMEKおよびERKを恒常的に過剰リン酸化し、RAS-MAPK経路全体の持続的な過剰シグナル伝達を招きます。胚発生期におけるこのシグナルの空間的・時間的な異常持続が、心臓の中隔や弁の形成過程・顔面頭蓋の骨組織の癒合プロセス・神経系のネットワーク形成に決定的な悪影響をもたらし、NS7に特徴的な多彩な表現型の根本的な病態生理学的要因となります。
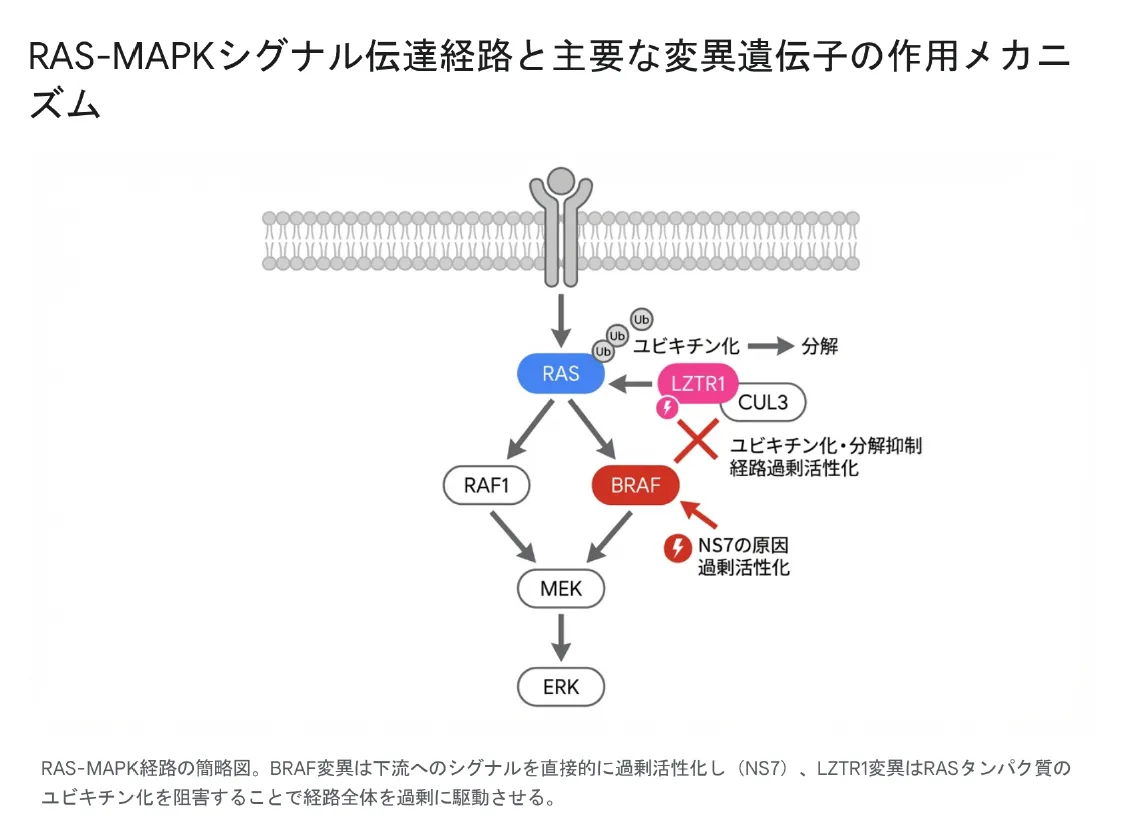
RAS-MAPK経路の概略図。BRAF変異(NS7)は下流のMEK/ERKへのシグナルを直接的に過剰活性化し(赤矢印)、LZTR1変異はRASタンパク質のユビキチン化・分解を阻害することで経路全体を過剰に駆動させる(異なる機序で同じ終点に至る)。
遺伝的異質性のパラダイムシフト:BRAFとLZTR1の機能的対比
RAS異常症の深い理解のために、BRAF変異とはまったく異なるメカニズムで同じ経路を過剰活性化する遺伝子との比較が重要です。それが近年ヌーナン症候群の新たな原因として同定されたLZTR1(Leucine-zipper-like transcriptional regulator 1)遺伝子です。
💡 用語解説:LZTR1遺伝子とユビキチン・プロテアソーム系
LZTR1は染色体22q11.2に位置し、CUL3ユビキチンリガーゼ複合体の基質特異的アダプターとして機能します。通常の細胞では、LZTR1は役割を終えたRASタンパク質を「ユビキチン化(廃棄タグを貼る)」してプロテアソームによる分解へと誘導するネガティブ・レギュレーター(負の制御因子)です。LZTR1が変異すると、RASタンパク質の分解が阻害されて細胞内に異常蓄積し、BRAF変異時と同様にMEK/ERKが過剰活性化されます。
つまり「BRAF変異=キナーゼが直接的に暴走」、「LZTR1変異=ブレーキ(分解機構)が壊れてRASが溢れる」という全く異なるルートで、最終的に同一のシグナル経路異常とヌーナン症候群の表現型に至るのです。この発見はRAS異常症の病態が単なるキナーゼ異常を超え、タンパク質の恒常性維持機構(プロテオスタシス)の破綻にも起因することを証明した画期的なパラダイムシフトをもたらしました。
3. 主な症状と臓器別表現型スペクトラム
ヌーナン症候群の臨床症状は極めて多岐にわたり、軽度なものから生命を脅かす重篤な合併症まで、その表現型は個々の患者や年齢によって大きく変化します。NS7(BRAF関連)の患者は全体として古典的なヌーナン症候群の症状を呈しますが、原因遺伝子の機能的特異性により、特定の症状の出現頻度や重症度に特徴的なパターンが見られます。
ヌーナン症候群における主要な臨床症状の推定有病率
各症状の発生頻度(%)
データはヌーナン症候群コホートに基づく推定値の中間値。BRAF変異(NS7)においては知的障害の発生率がグラフの平均値よりやや高くなる傾向がある点に留意が必要。データソース:GeneReviews (NCBI), ERN ITHACA Guidelines
頭蓋顔面部の特徴
ヌーナン症候群の顔貌は、乳児期・小児期中期に最も特徴的であり、成長とともにやや目立たなくなる(subtleになる)という特異な性質があります。NS7の患者においても、以下の顔貌特徴が高い浸透率で認められます。
眼部では著明な両眼開離(Hypertelorism)が頻発し、眼裂は斜下(Downslanting palpebral fissures)していることが多く、内眼角贅皮・上眼瞼下垂を伴います。虹彩の色素沈着異常により鮮やかな青色または青緑色の瞳を呈することも特徴的です。耳介は後方に大きく回転した低位耳介、肥厚した耳輪(fleshy helices)、突出した耳たぶが観察されます。口唇から下顎にかけては深い人中・高口蓋・小顎症が特徴的で、短頚・翼状頸(Webbed neck)も多くの患者に見られます。
心血管系の異常
先天性心疾患の合併はヌーナン症候群患者の約50〜80%に見られ、生命予後を決定づける最も重要な合併症です。
❤️ 肺動脈弁狭窄(PVS)
最多の心疾患形態。患者の20〜50%に確認され、肺動脈弁の肥厚・異形成を伴い右室流出路の血流障害を引き起こします。カテーテル介入(経皮的バルーン弁形成術)または外科的弁切開術が適応となります。
🫀 肥大型心筋症(HCM)
患者の20〜30%に見られます。NS7(BRAF変異)の患者では重篤な左室・右室流出路狭窄を引き起こし致死的経過をたどるリスクが報告されています。RAF1・RIT1変異ではさらに高頻度です。出生時から存在するか、乳幼児期以降に進行することもあります。
📊 心電図異常
構造的心奇形が明らかでない場合でも、約90%の患者に心電図上の異常が記録されます。極端な右軸偏位・左前枝ブロック・前胸部誘導における異常Q波はヌーナン症候群の強力な臨床マーカーです。
💡 用語解説:肥大型心筋症(HCM)とは
心筋(心臓の筋肉)が過剰に肥厚し、左室や右室の流出路を狭めてしまう疾患です。ヌーナン症候群では遺伝的なRAS-MAPK経路の過剰活性化が心筋細胞の異常な肥大を引き起こします。重症例では突然死や心不全のリスクがあるため、早期発見と定期的な心エコー評価が不可欠です。
成長障害・骨格系異常
低身長はヌーナン症候群の最も普遍的な特徴の一つで、患者の50〜70%に影響を及ぼします。出生時の身長は正常範囲内のことが多いですが、乳幼児期以降に成長曲線が低下し、思春期スパートの遅延または欠如とともに最終身長は健常者の下限かそれ以下にとどまるケースが大半です。胸郭は鳩胸(Pectus carinatum)と漏斗胸(Pectus excavatum)が混在する特異な形態を示し、幅広い乳首・脊柱側弯症・外反肘・全身の関節過伸展も頻繁に認められます。
精神運動発達と神経・認知機能
大半のヌーナン症候群患者は正常範囲の知能を維持しますが、約25%の患者に軽度の知的障害や学習障害が認められます。重要な遺伝型・表現型の相関として、PTPN11変異患者が比較的良好な認知機能を保つ傾向があるのに対し、BRAF(NS7)やKRASの病的バリアントを持つ患者は知的障害や認知機能低下の頻度がやや高くなる傾向が示唆されています。
言語発達の遅れは一般集団と比較して有意に高い割合で見られます。運動面では新生児期・乳児期からの全身性筋緊張低下(Generalized hypotonia)が広く見られ、首のすわり・寝返り・独歩などの粗大運動マイルストーンの遅延や、乳児期の重度な哺乳不良(Dysphagia)・体重増加不良(Failure to thrive)をもたらすことがあります。
血液・凝固異常・リンパ管異形成・その他
患者の30〜65%において、あざができやすい・頻繁な鼻出血・手術後の出血遷延などの出血傾向が報告されています。これは第XI・VIII・XII因子などの凝固因子の部分的欠乏や血小板機能異常が複合的に関与します。胎児期には頸部浮腫・後頸部透亮像(NT)の肥厚・嚢胞性ヒグローマとして現れ、出生後には末梢性リンパ浮腫として観察されることがあります。
💡 用語解説:停留精巣(Cryptorchidism)とは
精巣が出生後も陰嚢内に降下せず腹腔内や鼠径管内にとどまった状態です。ヌーナン症候群では男児の60〜80%という高頻度で発生し、適切な時期に外科的固定術(精巣固定術)を行わなければ精子形成機能が不可逆的に障害され、男性不妊の原因となります。また、腫瘍リスクの増加とも関連するため早期発見・治療が重要です。
また、RAS-MAPK経路は細胞増殖を司る中心的な経路であるため、ヌーナン症候群の小児患者は同年代と比較して白血病や固形腫瘍を発症するリスクが約8倍高いと推定されています。特に若年性骨髄単球性白血病(JMML)と神経芽腫のリスクが顕著であり、定期的なスクリーニングが推奨されます。
4. 鑑別診断:アレリック疾患と連続するスペクトラム
NS7の診断において専門的知識を要する最大の課題が「アレリズム(対立遺伝子疾患)」の概念です。全く同一のBRAF遺伝子に生じた変異であっても、その変異がタンパク質の三次元構造やキナーゼ活性にどのような機能的変化をもたらすかによって、異なる疾患ラベルが与えられます。
🔴 CFC症候群(同一遺伝子のアレリック疾患)
BRAF遺伝子のアレリック疾患として最重要。心血管奇形や頭蓋顔面部の特徴はNS7と非常に類似しますが、CFC症候群はヌーナン症候群よりもはるかに重度な知的障害・精神運動発達遅滞を伴います。
特徴的な外胚葉系の異常(疎で脆い巻き毛・乏しい眉毛・睫毛・魚鱗癬様の皮膚病変)を有する点で区別されますが、NS7とCFC症候群の境界はしばしば連続的で臨床的に曖昧です。
🟣 LEOPARD症候群3型(同一遺伝子のアレリック疾患)
BRAF変異はLEOPARD症候群(多発黒子を伴うヌーナン症候群)の一因ともなります。
NSの特徴的顔貌・心奇形に加えて、全身に多発する黒子(Lentigines)・感音性難聴・心電図異常の組み合わせによって鑑別されます。
🟡 神経線維腫症1型・NF-NSとの鑑別
NF1遺伝子はRAS-MAPKのネガティブレギュレーターをコードし、NF1変異でもNS様の顔貌や肺動脈狭窄が合併する「Neurofibromatosis-Noonan syndrome」が存在します。
カフェ・オ・レ斑や神経線維腫の有無、ならびに遺伝子検査によって区別されます。
🔵 他のヌーナン症候群サブタイプとの比較
NS全体の約50%を占めるPTPN11変異(NS1)は比較的良好な認知機能を保ちます。RAF1変異・RIT1変異例はHCMのリスクが特に顕著です。
BRAF変異(NS7)は知的障害リスクがやや高く、かつCFC症候群と連続したスペクトラムを形成する点で固有の特徴を持ちます。
💡 用語解説:アレリズム(対立遺伝子疾患)とは
同一の遺伝子に生じた変異であっても、その変異が引き起こすタンパク質の機能変化の「質と量」の違いによって、臨床的に異なる名前の疾患が生じる現象です。BRAF遺伝子はその典型例で、変異の種類によってヌーナン症候群7型・CFC症候群・LEOPARD症候群3型のいずれもが生じ得ます。したがって「BRAF変異が見つかった」というだけでは診断は確定せず、変異の機能的影響と患者の臨床像を総合して判断する専門的な遺伝子解釈が不可欠です。
5. 臨床診断基準と分子遺伝学的検査
van der Burgt診断基準(臨床診断のゴールドスタンダード)
💡 用語解説:van der Burgt(ファン・デル・ブルフト)診断基準とは
1994年に提唱され2007年に改訂された、ヌーナン症候群の臨床診断のためのスコアリングシステムです。遺伝子検査以前から世界中で使用されてきたゴールドスタンダードで、現在も分子診断と併用されています。特徴的な症状をその特異性に応じて「大基準(A)」と「小基準(B)」に分類し、組み合わせによって確定診断を行います。
以下の表が、van der Burgt診断基準のスコアリングシステムです。
📋 確定診断の要件(Scoring Rules)
シナリオ1(顔貌が典型的な場合):「1A(典型的な顔貌)」を満たし、さらにカテゴリー2〜6から「大基準を1つ」または「小基準を2つ」満たす場合。
シナリオ2(顔貌が非典型的な場合):「1B(示唆する程度の顔貌)」を満たし、さらにカテゴリー2〜6から「大基準を2つ」または「小基準を3つ」満たす場合。
マルチ遺伝子パネル検査:分子診断の第一選択
💡 用語解説:マルチ遺伝子パネル検査(Multigene Panel Sequencing)とは
次世代シーケンシング(NGS)を用いて、疾患に関連する複数の遺伝子を一度に網羅的に解析する検査です。ヌーナン症候群は極めて高い遺伝的異質性を持つため、PTPN11・SOS1・RAF1・RIT1・KRAS・NRAS・BRAF(NS7)・LZTR1・MAP2K1・SHOC2・CBLなど10〜20以上の遺伝子を同時に調べます。単一遺伝子の検査を逐次的に行うよりも時間・コストの両面で効率的であり、国際的なガイドラインで第一選択として推奨されています。包括的なパネル検査によって約80%以上の患者で原因バリアントを特定できます。
マルチ遺伝子パネル検査でも原因遺伝子が特定されない場合(全体の10〜20%)は、臨床診断が覆るわけではありませんが、未知の原因遺伝子を探索するために全エクソームシーケンス(WES)や全ゲノムシーケンス(WGS)へのステップアップが考慮されます。
特定の原因遺伝子(BRAFやLZTR1など)を分子レベルで同定することは、単なる診断名の確定にとどまりません。それは重篤な合併症(肥大型心筋症・若年性骨髄単球性白血病など)の発症リスクを層別化し、患者ごとにパーソナライズされた長期管理計画を策定するための基盤となります。また、次子への出生前診断(羊水検査・絨毛検査)や着床前診断(PGT-M)の選択肢を提供するうえでも不可欠です。
6. 治療・長期管理と精密医療の展望
現在のところ、BRAF遺伝子変異そのものを根本的に修復する遺伝子治療は臨床応用されていません。したがってNS7の管理は、小児科医・循環器科医・内分泌科医・臨床遺伝専門医・眼科医などによる多学際的チーム(Multidisciplinary team)による対症療法と、各年齢段階に応じた定期的スクリーニングが主体となります。
心血管系の生涯管理
診断時における心エコー検査と心電図検査は全患者で必須であり、その後も生涯にわたる定期的モニタリングが必要です。肺動脈弁狭窄(PVS)に対しては、右室圧が著しく上昇した場合に経皮的肺動脈弁形成術(バルーンカテーテルによる弁拡張)や外科的弁切開術が適応となります。日本の専門施設のコホートデータでは、肺動脈血流速度3.0 m/s超のPVS患者へのカテーテル介入が血流速度の長期的な有意な低下をもたらし、良好な臨床予後を示すことが実証されています。
BRAF変異患者でリスクが高まる肥大型心筋症(HCM)に対しては、β遮断薬やカルシウム拮抗薬による内科的薬物療法が行われます。薬物療法に抵抗性を示す重度の心筋肥厚・流出路狭窄が進行した場合には、中隔心筋切除術や植え込み型除細動器(ICD)の留置が必要となるケースも存在します。
内分泌・成長・凝固異常への対応
📏 低身長への介入
顕著な低身長に対しては成長ホルモン(GH)補充療法が広く行われています。GH療法は短期的には成長速度を有意に改善し、長期的には最終的な成人身長の増加に寄与することが確認されており、患者のQOL向上に重要です。成長ホルモン分泌試験などによる精密な評価が前提となります。
🩸 凝固異常への備え
外科的手術・歯科抜歯・侵襲的検査の前には致命的な大出血を防ぐための厳重な事前評価が不可欠です。PT・APTT・特定の凝固因子(第XI因子など)の定量・血小板凝集能の検査を行い、必要に応じて因子補充や止血剤の投与を計画します。
👁️ 眼科・発達・泌尿生殖器
斜視・弱視は早期発見・早期治療が視力予後を大きく左右します。男児の停留精巣は適切な時期の外科的固定術(精巣固定術)が将来的な不妊予防に不可欠です。発達面では言語療法・理学療法・特別支援教育などの包括的な支援体制が重要です。
標的治療(精密医療)の幕開け
近年、RAS-MAPK経路の分子メカニズムの解明が進み、本来はがん治療薬として開発された分子標的薬をRAS異常症治療に転用(Drug Repurposing)しようとする革新的なアプローチが始まっています。
💡 用語解説:MEK阻害薬(トラメチニブ)とRAS異常症への応用
MEK阻害薬とは、RAS-MAPKシグナル経路の中間分子MEKの活性を薬理学的にブロックする薬剤です。トラメチニブ(Trametinib)はFDA承認済みの抗がん剤ですが、LZTR1変異モデルマウスへの全身投与実験において、心筋細胞の異常な肥大やヌーナン症候群様の表現型が劇的に改善されたことが報告されました。NS7のようにBRAF変異でMEKが過剰活性化されているケースでも、理論上MEK阻害は効果的な標的となり得ます。これらは現時点では前臨床段階の知見ですが、対症療法から根本病態を直接標的とする精密医療への歴史的な転換点を示しています。
さらに、LZTR1変異による重度な出血傾向・血管透過性亢進の研究では、異常蓄積したVEGFR2のシグナルをブロックするVEGFR2阻害薬(セディラニブ)の投与によって血管内皮の細胞間接着が回復し、出血病態がレスキューされることが証明されています。これらの知見は、特定の遺伝子変異の種類に基づいて経路内の適切な分子標的を薬理学的にブロックすることで、これまで不可逆的と考えられていた心筋肥大や血管異常を可逆的に治療できる可能性を力強く示唆しています。
7. 遺伝カウンセリングの意義
NS7(BRAF関連ヌーナン症候群)の確定診断後、家族への丁寧な遺伝カウンセリングが不可欠です。以下の内容が主に扱われます。
- ➤遺伝形式と再発リスクの説明:NS7は常染色体顕性遺伝ですが、30〜75%のケースで臨床的に気づかれていなかった親からの遺伝が確認されます。残りの多くはde novo変異です。変異を持つ親から子への遺伝確率は理論上50%です。
- ➤LZTR1変異がもたらす遺伝的複雑性:LZTR1変異によるヌーナン症候群は常染色体顕性(NS10型)と常染色体潜性(NS2型)の両方が存在します。潜性遺伝の場合、両親はキャリアでありながら無症候性です。子どもが両親から変異遺伝子を受け継いだ場合(ホモ接合・複合ヘテロ接合体)は重篤な心筋症や致死的白血病を合併する極めて重症型となるため、LZTR1変異の正確な同定は遺伝カウンセリングにおいてとりわけ重要です。
- ➤出生前診断・着床前診断の選択肢:次子を望む場合、既知の変異が同定されていれば絨毛検査・羊水検査による出生前遺伝子診断が可能です。また着床前診断(PGT-M)によって特定の変異を持たない胚を選択する選択肢も存在します。
- ➤発がんリスクへの備え:RAS-MAPK経路の恒常的過剰活性化は発がんプロセスと密接に関連します。ヌーナン症候群患者は白血病・固形腫瘍リスクが約8倍高く、特にJMMLや神経芽腫の定期的スクリーニングが推奨されます。
- ➤LZTR1のSchwannomatosis素因について:LZTR1のヘテロ接合性変異は、末梢神経系に多発性の良性シュワン腫を形成する「神経鞘腫症(Schwannomatosis)」の強力な素因ともなります。一つの遺伝子が全く異なる疾患表現型を同時に引き起こし得るこの事実は、正確な遺伝子解析に基づく長期的フォローの重要性を示しています。
8. よくある誤解
誤解①「BRAF変異=がんのリスクが高い?」
がんで問題になるBRAF V600Eなどの変異は「体細胞性(ソマティック)変異」であり、NS7の原因は生殖細胞系列の機能獲得型変異です。腫瘍リスクはゼロではありませんが、BRAF変異があるからといって直接的にがんになりやすいわけではありません。定期スクリーニングは重要ですが過度な不安は不要です。
誤解②「BRAF変異ならCFC症候群では?」
同じBRAF遺伝子でも変異の種類・位置によってNS7とCFC症候群は区別されます。臨床像・変異の機能的影響・総合的な評価による診断が必要で、「BRAF変異=CFC症候群」とは言えません。スペクトラムの中にあり、専門家による評価が欠かせません。
誤解③「ヌーナン症候群は全員知的障害がある」
NS全体の約75%の患者は正常範囲の知能を維持しています。NS7(BRAF変異)はやや知的障害リスクが高い傾向がありますが、それでも多くの患者は通常教育を受け社会参加できます。個別の評価と支援体制が大切です。
誤解④「遺伝子検査が陰性なら診断は除外」
マルチ遺伝子パネル検査を行っても約10〜20%のケースは原因遺伝子が特定されません。しかしvan der Burgt臨床診断基準を満たすなら診断は有効です。WES/WGSへのステップアップや新規遺伝子の発見により、将来的に診断が確定するケースもあります。
9. 臨床遺伝専門医からのメッセージ
よくある質問(FAQ)
🏥 ヌーナン症候群・RAS異常症に関するご相談
ヌーナン症候群7型をはじめとするRAS異常症・希少遺伝性疾患に関するご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にご相談ください。
関連記事
参考文献
- [1] NCBI MedGen. Noonan syndrome 7 (Concept Id: C3150970). [NCBI MedGen]
- [2] Children’s Hospital of Philadelphia. Noonan Syndrome. [CHOP]
- [3] Tartaglia M, et al. Noonan Syndrome. GeneReviews® – NCBI Bookshelf. [GeneReviews]
- [4] MedlinePlus. Noonan syndrome – Genetics. [MedlinePlus]
- [5] Motta M, et al. LZTR1 molecular genetic overlap with clinical implications for Noonan syndrome and schwannomatosis. Genet Med. 2022. [PMC9288044]
- [6] Zenker M, et al. Noonan syndrome: improving recognition and diagnosis. Arch Dis Child. 2022;107(12):1073-1078. [ADC BMJ]
- [7] Nakamura Y, et al. Dysregulation of RAS proteostasis by autosomal-dominant LZTR1 mutation induces Noonan syndrome-like phenotypes in mice. JCI Insight. 2024. [JCI Insight]
- [8] Pagnamenta AT, et al. LZTR1-Related Hypertrophic Cardiomyopathy Without Typical Noonan Syndrome Features. Circ Genom Precis Med. 2019. [Circulation Genomic]
- [9] Monarch Initiative. Noonan syndrome 7 MONDO:0013379. [Monarch Initiative]
- [10] Romano AA, et al. Noonan Syndrome: Clinical Features, Diagnosis, and Management Guidelines. Pediatrics. 2010;126(4):746-759. [ERN ITHACA Guidelines]
- [11] Sawada H, et al. Cardiac features of Noonan syndrome in Japanese patients. Cardiol Young. 2018. [Cardiology in the Young]
- [12] Yamamoto GL, et al. The Noonan Syndrome Gene Lztr1 Controls Cardiovascular Function by Regulating Vesicular Trafficking. Circ Res. 2021. [Circulation Research]
- [13] OMIM #613706. Noonan Syndrome 7. Johns Hopkins University. [OMIM]
- [14] Medicover Genetics. Noonan Syndrome overview. [Medicover Genetics]