目次
📍 クイックナビゲーション
TPM2遺伝子はβ-トロポミオシンをコードし、筋肉の精密な収縮制御から細胞の形態維持、さらには癌の抑制まで、生命活動の根幹を担う多機能遺伝子です。この遺伝子のわずかな変異が、「筋肉が動かない」と「関節が固まる」という正反対の症状を引き起こすことがあります。その理由は、分子レベルの”働きすぎ”か”働かなさすぎ”にあります。
- ➤TPM2遺伝子の全体像 → β-トロポミオシンが担う多彩な機能とその発現組織
- ➤筋収縮の分子メカニズム → カルシウムと立体障害モデルのしくみ
- ➤関連疾患の種類と特徴 → ネマリンミオパチー・遠位型関節拘縮症など
- ➤Q93H変異とE97K変異の違い → 同じ遺伝子の隣接変異が正反対の表現型をもたらす理由
- ➤癌抑制遺伝子・最新治療 → 腫瘍学での新たな役割と遺伝子治療の展望
1. TPM2遺伝子とは?β-トロポミオシンの全体像
TPM2遺伝子は、β-トロポミオシン(β-tropomyosin)と呼ばれるタンパク質アイソフォーム群をコードする遺伝子です。染色体9番短腕(9p13.3)に位置し、骨格筋・心筋・平滑筋から皮膚線維芽細胞・血管内皮細胞に至るまで、体中のほぼあらゆる組織で発現しています。
トロポミオシン(TPM)ファミリーは哺乳類においてTPM1・TPM2・TPM3・TPM4の4つのパラログから構成されています。これらは全ゲノム重複などの進化的イベントを経て分岐したとされており、その基本的なコイルドコイル構造は哺乳類から両生類にわたって驚くほど高く保存されています。TPM2が担うβ-トロポミオシンは、骨格筋サルコメアの必須構成要素であると同時に、非筋細胞における細胞骨格の要でもあります。
細胞内に張り巡らされたタンパク質の繊維状構造物で、細胞の形態維持・運動・分裂など多岐にわたる機能を担います。骨格筋ではサルコメアの「細いフィラメント」として、ミオシン(太いフィラメント)と相互作用することで収縮力を生み出します。TPM2はこのアクチンフィラメントに沿って螺旋状に結合し、その機能を精密に制御する「調節因子」として働きます。
2本のαヘリックスが互いに絡み合った縄状の二次構造です。TPM2タンパク質はこの構造をとることで強い機械的安定性を持ち、アクチンフィラメントの溝に沿って頭部と尾部を11〜14残基ずつ重ね合わせながら重合し、連続した螺旋状のポリマーを形成します。この重合こそがアクチン全長にわたる「滑らかな制御ロッド」としての機能を可能にします。
2. 選択的スプライシングによるアイソフォームの多様性
TPM遺伝子群の最も際立った特徴は、1つの遺伝子から40種類以上もの機能的に異なるタンパク質を生み出す能力にあります。複数のプロモーターの切り替え、選択的スプライシング、代替ポリアデニル化部位の利用、そして翻訳後修飾を組み合わせることで、この驚異的な多様性が実現されています。
1つの遺伝子のDNAから転写されたmRNA前駆体(pre-mRNA)を、複数の異なるパターンで切り貼り(スプライシング)することで、異なるタンパク質を作り出す仕組みです。これにより同じ遺伝子から組織の種類・発生段階・細胞状態に応じた「特化型タンパク質」が生み出されます。TPM2では特にエクソン1・2・6・9などのバリアントエクソンが代替的に使用されることが、アイソフォームの多様性に大きく寄与しています。
TPM2遺伝子から生み出される主なアイソフォームは以下の通りです。Tpm2.2は骨格筋サルコメアに組み込まれる高分子量の主要アイソフォームであり、ブタ・ラット・ヒトの骨格筋でTpm1.1とともに共発現することが質量分析(トップダウンMS)によって確認されています。Tpm2.1は非筋細胞に広く発現し、細胞骨格の維持や癌抑制に中心的な役割を果たします。また平滑筋型のTPM2βも存在し、組織の種類や発生段階によって厳密に発現が切り替えられています。
| 遺伝子 | 主要アイソフォーム | 主な発現・役割 |
|---|---|---|
| TPM1 | Tpm1.1(α-トロポミオシン) | 心筋・速筋。心臓発生に必須。変異は心筋症を引き起こす |
| TPM2 ★ | Tpm2.2(筋)/ Tpm2.1(非筋) | 遅筋線維・非筋細胞。細胞骨格安定化・癌抑制 |
| TPM3 | Tpm3.12など多数 | 遅筋・神経系。神経軸索伸長・樹状突起分岐に関与 |
| TPM4 | Tpm4.3など | 心筋・骨格筋。シナプス後膜の構築などにも関与 |
3. 骨格筋における役割:カルシウムが動かす精密な収縮機械
骨格筋においてTPM2がコードするβ-トロポミオシン(主としてTpm2.2)は、筋収縮の基本単位であるサルコメア(筋節)の細いフィラメントを構成する必須要素です。トロポミオシン分子は7つの擬似リピートを持ち、アクチンフィラメントの溝に沿って頭部と尾部が重なり合いながら重合し、連続した螺旋状ポリマーを形成します。
筋収縮の最小反復単位で、アクチン(細いフィラメント)とミオシン(太いフィラメント)がZ線とZ線の間に規則的に配列した構造です。Z線からZ線の長さは安静時で約2.5μm。TPM2(β-トロポミオシン)はトロポニン複合体とともにこの細いフィラメントに沿って存在し、ミオシン頭部がアクチンに結合できるかどうかを”ゲート”として制御します。
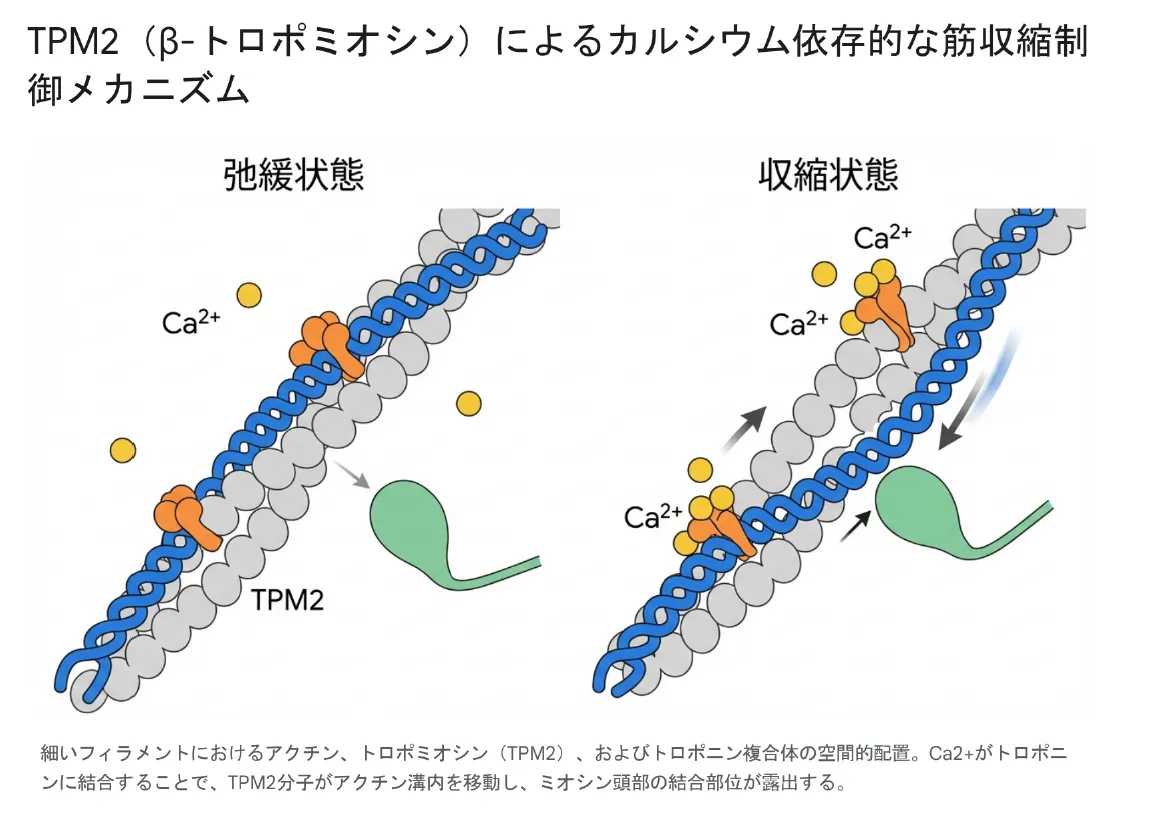
筋収縮制御の核心は「立体障害モデル(steric blocking model)」にあります。安静時(Ca²⁺濃度が低い状態)ではTPM2がアクチンフィラメントの溝を覆い、ミオシン頭部の結合部位を物理的に遮断しています。運動神経からの刺激で筋小胞体からCa²⁺が放出されると、Ca²⁺がトロポニンCに結合し、トロポニン複合体全体にアロステリックな構造変化が起こります。この変化がTPM2分子をアクチン溝のより深い位置へスライドさせ、ミオシン結合部位を露出させることで、強力なクロスブリッジ(架橋)形成とATP加水分解による張力発生が可能になります。
トロポニンC(TnC)・トロポニンI(TnI)・トロポニンT(TnT)の3サブユニットからなる複合体で、アクチンフィラメント上に一定間隔で配置されています。TnCがCa²⁺を感知するセンサーとして機能し、Ca²⁺が結合するとTnIを介してTPM2の位置が変化します。この「Ca²⁺→トロポニン→TPM2」という信号リレーが筋収縮のスイッチとなっています。
注目すべきは、TPM2の発現が骨格筋の中でも特に遅筋線維(type 1線維)に集中していることです。姿勢維持に使われる遅筋は疲労に強く持続的収縮に最適化されています。TPM2は自己同士のホモ二量体(Tpm2.2/Tpm2.2)だけでなく、TPM1産物とのヘテロ二量体(Tpm1.1/Tpm2.2)も形成し、ミオシン架橋のキネティクスを微調整することで、効率的かつリズミカルな収縮を可能にしています。
4. 非筋細胞での機能:細胞の形と動きを支配するメカノセンサー
TPM2の役割は骨格筋の収縮にとどまりません。非筋細胞に広く発現するTpm2.1は、細胞の形態・運動・生存を支配する「メカノセンサー」として機能しています。
細胞が外部の「物理的な力」(基質の硬さ・剪断応力・圧力など)を感知し、それを細胞内の生化学シグナルに変換するプロセスです。がん細胞が柔らかい組織に浸潤する際や、線維症で組織が硬化する際にも深く関わります。Tpm2.1はこのプロセスの中核を担うタンパク質として注目されており、「細胞が外の世界の硬さを測るセンサー」として機能しています。
非筋細胞においてTpm2.1は、まずアクチンフィラメントの保護という重要な役割を担います。細胞内のアクチン骨格は常に重合と脱重合を繰り返す動的な構造(トレッドミリング)をとっていますが、Tpm2.1はアクチンフィラメントに沿って結合することでコフィリンなどのアクチン切断タンパク質の作用からフィラメントを物理的に守り、安定した細胞形態を維持します。実験的にTPM2を過剰発現させると、線維状アクチン(F-アクチン)の比率が顕著に増加することが確認されています。
さらにTpm2.1は接着斑(focal adhesion)の制御と密接に関わっています。Tpm2.1は主に細胞の背側・腹側ストレスファイバーに局在し、ミオシンIIが生み出す収縮力を接着斑へ適切に伝達するプロセスを制御します。TPM2の発現が低下すると、細胞内のRho-GTPレベルが上昇してRho-ROCK経路を介したアクトミオシン収縮が過剰活性化し、集団的な細胞移動の遅延や細胞極性の喪失をもたらします。この機能は後述する癌の転移や組織の線維化とも深く結びついています。
5. TPM2変異が引き起こす疾患スペクトラム
TPM2遺伝子のコード領域に生じる病的バリアントは、サルコメアおよび細胞骨格の構造的・機能的破綻を引き起こし、常染色体優性(顕性)遺伝の形式をとる多様な先天性疾患の原因となります。これまでに約30の病的バリアントが報告されており、タンパク質配列に沿って比較的均等に分布しています。
2本ある常染色体のうち、1本に変異があるだけで発症する遺伝形式です。「優性(顕性)」とは症状が現れやすいという意味で、道徳的な「優劣」とは無関係です。TPM2変異による疾患のほとんどはこの形式をとるため、変異を持つ親から子どもへ50%の確率で遺伝する可能性があります。なお、新生突然変異(de novo変異)として初めて発症するケースも少なくありません。
関連する主な疾患
🔴 ネマリンミオパチー(NM)・キャップ病
筋生検でサルコメアZ線に由来する異常なタンパク質凝集体「ネマリン小体」や「キャップ構造」が観察されることを特徴とします。生後早期からの重度な呼吸筋・四肢近位筋・顔面筋の筋力低下と筋緊張低下(hypotonia)を引き起こします。
🟠 遠位型関節拘縮症(DA)
手足の関節が固定された状態(拘縮)で生まれてくる疾患群です。TPM2変異は主にDA1型(カンプトダクティリー・内反足)と、顔面奇形を伴うDA2B型(シェルドン・ホール症候群)を引き起こします。
🔵 孤立性先天性内反足
全身の筋力低下を伴わない、足部のみに限局した形態異常です。近年TPM2の病的バリアントがこの患者群からも同定されており、TPM2関連疾患の臨床的スペクトラムは想定以上に広いことが明らかになっています。
補足:TPM2変異による疾患の重症度は変異の種類・位置・ドミナントネガティブ効果の強さによって大きく異なります。軽症例では成人まで診断がつかないケースも報告されています。
6. Q93HとE97K:隣接する変異が生む正反対の表現型
TPM2変異が引き起こす筋機能障害のメカニズムは、単純な「機能喪失(loss-of-function)」ではありません。変異はタンパク質のコイルドコイル構造に微細な変化をもたらし、正常アイソフォームの機能をも阻害するドミナントネガティブ効果を発揮します。
変異を持つタンパク質(mutant)が正常タンパク質(wild-type)と複合体を形成し、その正常な機能を”邪魔”することで機能不全を起こす現象です。常染色体優性(顕性)遺伝の重要なメカニズムの1つです。TPM2変異の多くはこの効果を示すため、「正常な遺伝子コピーを補充するだけ」の遺伝子治療では効果が得られず、変異アレルの発現抑制と正常遺伝子の同時導入という戦略が必要になります。
特に興味深いのは、同じアクチン結合ドメイン内のごく隣接したアミノ酸の変異でありながら、生化学的な挙動が全く正反対になるQ93H変異とE97K変異の関係です。
| 変異 | アクトミオシンATPase活性 | Ca²⁺感受性 | 収縮表現型 | 主な関連疾患 |
|---|---|---|---|---|
| Q93H | ↓ 著しい低下 | ↓ 低下 | 低収縮性 | 先天性ミオパチー(ネマリンミオパチー) |
| E97K | ↑ 過剰活性化 | ↑ 上昇 | 高収縮性 | 遠位型関節拘縮症 |
同一アクチン結合ドメイン内のQ93H・E97K変異は、生化学的特性が全く逆の方向に変化し、それぞれ異なる疾患表現型をもたらす
Q93H変異はアクチンへの親和性を大きく低下させ、ATPaseの活性化を阻害します。筋線維が収縮しにくくなることで、「動かない」筋力低下型の表現型(ネマリンミオパチーなど)が生じます。一方、E97K変異はヘプタドリピートの「f」位のグルタミン酸からリジンへの置換によりATPaseを過剰活性化し、Ca²⁺感受性を著しく高めます。筋線維が常に「収縮しやすい状態」となることで、「縮んで固まる」関節拘縮型の表現型が生じます。
筋発生(Myogenesis)そのものへの影響
近年、ショウジョウバエやゼブラフィッシュを用いた先端的研究により、TPM2変異の病態は「成熟した筋の収縮不全」にとどまらないことが判明しています。K49Del・E122Kといった変異型TPM2を発現させたモデル生物では、筋管(myotubes)の伸長異常が観察されました。変異を発現する筋管は正しい伸長標的に到達できなかったり、不適切な部位に接着するなど、サルコメアが形成される以前の「筋発生の初期段階そのものを直接阻害する」ことが示されています。この発達段階での不可逆的なエラーが、成熟後の臨床的重症度の根本的な基盤となっている可能性があります。
7. 癌抑制遺伝子としてのTPM2:腫瘍学における新たなパラダイム
長らく筋骨格系疾患の文脈で語られてきたTPM2ですが、近年の腫瘍学の進展により、その認識は大きく変わっています。非筋細胞において細胞骨格の動態を制御するTpm2.1は、多くの悪性腫瘍において発現が著しく低下しており、強力な「癌抑制遺伝子」として機能することが複数の研究によって証明されています。
正常な細胞が細胞外マトリックス(足場)から剥離したときに起こるプログラム細胞死(アポトーシスの一形態)です。本来は細胞が不適切な場所に移動・定着することを防ぐ生体防御機構です。癌細胞はこのアノイキスを回避する能力を獲得することで、原発巣から離脱して転移できるようになります。Tpm2.1はアノイキスの重要なセンサー・実行制御因子として機能しており、その消失が癌の転移能力を高めます。
細胞増殖・アポトーシス・器官サイズを制御する主要なシグナル経路です。この経路が正常に機能している場合、転写共役因子YAP1は細胞質にとどまり核内への移行が抑制されます。しかしTPM2の発現が失われるとYAP1が核内に移行し、増殖関連遺伝子群の転写を異常活性化して腫瘍の増殖・浸潤・ホルモン療法耐性(去勢抵抗性)を促進することが前立腺癌の研究で実証されています。
各臓器でのTPM2の癌抑制メカニズム
乳癌
低酸素(Hypoxia)環境によるプロモーターのDNAメチル化が発現を抑制。パクリタキセルなどの化学療法抵抗性に直接寄与。リンパ節転移・高グレードと相関。
前立腺癌
PDLIM7を介したYAP1核内移行阻害機構が破綻しHippo経路が異常活性化。腫瘍の増殖・浸潤・去勢抵抗性(ホルモン療法耐性)の獲得と直結。
結腸直腸癌(CRC)
免疫関連予後予測モデルを構成する主要6遺伝子の1つ。発現低下はメモリーB細胞などの異常な免疫浸潤と相関し、免疫療法への応答性低下と全生存期間の短縮を示す。
グリオーマ(悪性神経膠腫)
脳の柔らかい3D環境でTpm2.1が欠損すると細胞の牽引力が低下し、細胞が周囲マトリックスに沿って広がりやすくなる。間葉系浸潤を強力に助長する機序が解明されている。
8. 最新の治療戦略:遺伝子治療・低分子化合物・今後の展望
TPM2関連疾患は長らく対症療法・支持療法に限られてきましたが、近年の分子生物学・遺伝子工学の急速な発展により、病態の根本原因に直接介入する次世代治療戦略の開発が大きく加速しています。
①「ノックダウン&プレイス」アプローチ
TPM2変異の多くはドミナントネガティブ効果を示すため、正常遺伝子の補充だけでは効果がありません。米国Nationwide Children’s Hospitalが先天性ミオパチー(ACTA1変異NEM3)で実証した「ノックダウン&プレイス(Knock-down and Replace)」戦略が、TPM2変異疾患の遺伝子治療の青写真となっています。まずRNA干渉技術を用いて変異型遺伝子の発現を特異的に抑制(サイレンシング)し、同時にAAV(アデノ随伴ウイルス)ベクターで正常な遺伝子コピーを筋細胞内に導入します。細胞モデルとマウスモデルの初期試験でネマリン小体の劇的な減少が確認されており、2025〜2026年にかけて多くの臨床的マイルストーンが予定されています。
また、NEBのような搭載容量を超える巨大遺伝子に対する「プロテイン・スティッチング(protein-stitching)」技術や、CRISPRベースの遺伝子編集、低用量で標的組織に到達できる次世代AAVベクターの開発も急ピッチで進んでいます。
②低分子化合物による線維症・癌浸潤の抑制
Tpm2.1の活性・発現を特異的に修飾する低分子化合物の探索も活発化しています。特発性肺線維症(IPF)において、炎症性サイトカインTGF-β1はTpm2.1の発現を強力に誘導します。増加したTpm2.1が引き起こす過剰なアクトミオシン収縮力がマトリックスを強く牽引・再編成し、組織の硬化という致命的な悪循環を生み出します。Tpm2.1の発現を特異的にノックダウンするとコラーゲンゲルの収縮が顕著に減少することが証明されており、Tpm2.1が「炎症」と「物理的硬化」を繋ぐ中核的なハブであることが示されています。
癌領域では、前立腺癌でのTPM2発現回復アプローチや、TPM2喪失によって異常活性化するROCK経路を薬理学的に阻害して集団的細胞移動を抑制する手法が、有望な転移抑制戦略として期待されています。
9. 臨床遺伝専門医からのメッセージ
TPM2遺伝子は、単一の構造タンパク質を供給する受動的な役割を遥かに超え、筋収縮の精緻な制御から非筋細胞の力学応答、そして細胞死の決定に至るまで、生命活動の根幹を担う多機能な中枢として働いています。その変異が筋力低下から関節拘縮、さらには悪性腫瘍の転移や組織の線維化まで、多様で重篤な病態を引き起こすことは、この遺伝子の生物学的な重要性を何よりも雄弁に示しています。
よくある質問(FAQ)
🏥 遺伝子検査・遺伝性疾患についてのご相談
TPM2関連疾患をはじめ、遺伝性筋疾患・関節拘縮症・出生前遺伝子診断について
臨床遺伝専門医が丁寧にお答えします。
参考文献・外部リンク
- [1] NCBI Gene: TPM2 tropomyosin 2 [Homo sapiens (human)] Gene ID: 7169 [NCBI Gene]
- [2] MedlinePlus Genetics: TPM2 gene [MedlinePlus]
- [3] OMIM: Tropomyosin 2 (Beta); TPM2 – #190990 [OMIM]
- [4] Marston S, et al. Mutations Q93H and E97K in TPM2 Disrupt Ca-Dependent Regulation of Actin Filaments. Front Physiol. 2021. [PMC]
- [5] Whittle M, et al. A pathogenic mechanism associated with myopathies and structural birth defects involves TPM2-directed myogenesis. JCI Insight. 2022. [PMC]
- [6] He Y, et al. TPM2 attenuates progression of prostate cancer by blocking YAP1 nuclear translocation via PDLIM7. Front Oncol. 2023. [PMC]
- [7] Research Advances in the Role of the Tropomyosin Family in Cancer. Int J Mol Sci. 2023. [PMC]
- [8] Hypoxia-Induced TPM2 Methylation is Associated with Chemoresistance and Poor Prognosis in Breast Cancer. PubMed. [PubMed]
- [9] Comprehensive Analysis of Tropomyosin Isoforms in Skeletal Muscles by Top-down Proteomics. PMC. [PMC]
- [10] Tropomyosin 2.1 collaborates with fibronectin to promote TGF-β1-induced contraction of human lung fibroblasts. PMC. [PMC]
- [11] Early clinical and pre-clinical therapy development in Nemaline myopathy. Expert Opinion on Therapeutic Targets. 2022. [Taylor & Francis]
- [12] Human Protein Atlas: TPM2 protein expression summary [Protein Atlas]