目次
- 1 1. NEB遺伝子のゲノム構造と巨大タンパク質「ネブリン」の分子アーキテクチャ
- 2 2. NEB遺伝子変異とネマリンミオパチー(NEM2)の病態生理
- 3 3. 分子病態メカニズム:なぜ筋力が低下するのか
- 4 4. 前臨床研究のブレイクスルー:ゼブラフィッシュと次世代マウスモデル
- 5 5. 巨大遺伝子の壁を越えるAAV遺伝子治療:「プロテイン・スティッチング」
- 6 6. 薬理学的介入と低分子化合物アプローチ:Omecamtiv mecarbil (OM)
- 7 7. RNA標的療法とゲノム編集(CRISPR/Cas9)の最前線
- 8 8. 臨床試験の基盤構築:自然史研究の推進(NatHis-NM-MDUK)
- 9 よくある質問(FAQ)
- 10 関連記事
- 11 参考文献
全ネマリンミオパチー症例の50%以上を占める「NEB遺伝子変異型(NEM2)」。本記事では、巨大タンパク質ネブリンの緻密な分子ネットワークから、プロテイン・スティッチング技術や新薬開発などの最新の前臨床・臨床動向まで、網羅的に深掘りして解説します。
1. NEB遺伝子のゲノム構造と巨大タンパク質「ネブリン」の分子アーキテクチャ
ヒトの生体運動や呼吸を根本から支える骨格筋の機能は、筋繊維内の基本収縮単位である「サルコメア(筋節)」の高度に組織化された分子アーキテクチャに依存しています。このサルコメア内で筋肉の収縮を構造的に支え、制御する極めて重要な要素が、NEB遺伝子からコードされる巨大タンパク質「ネブリン(nebulin)」です。
💡 用語解説:サルコメア(筋節)
筋肉の細胞内に規則正しく並んでいる「収縮の最小単位」のことです。ミオシンからなる太いフィラメントと、アクチンからなる細いフィラメントがスライドして重なり合うことで、筋肉に張力が発生します。
ヒトNEB遺伝子は染色体2番の長腕(2q22)に位置しており、183個のエクソンから構成される、ヒトゲノムにおいて最大級かつ最も複雑な遺伝子の一つです。生成されるネブリンの分子量はおおむね600 kDaから900 kDaの範囲に及びます。
ネブリンタンパク質の一次構造の約90%は、約35〜40アミノ酸残基からなる「シンプルリピート」の繰り返しで構成されています。さらに高次の構造として、7つのドメインを1つの単位とする「スーパーリピート(super-repeats)」として組織化されています。この7ドメインという単位は、アクチンフィラメントにおける7つのアクチンモノマーの反復単位と物理的・幾何学的に正確に一致しており、極めて緊密な物理的会合を可能にしています。
進化が示すネブリンの重要性(動物サイズとの相関)
比較生物学的解析によると、ネブリンタンパク質の長さ(スーパーリピートの数)は動物の体格と強い正の相関があります。ハチドリなどの小型鳥類は最小で21個のリピートしか持ちませんが、チンパンジーやラクダなどの大型動物は最大31個、ヒトは29個のスーパーリピートを持ちます。体が大きい動物ほど長い筋肉の収縮ストロークを確保し、エネルギー効率を最適化するための進化的メカニズムだと考えられています。
分子定規としての機能と最新技術による新発見
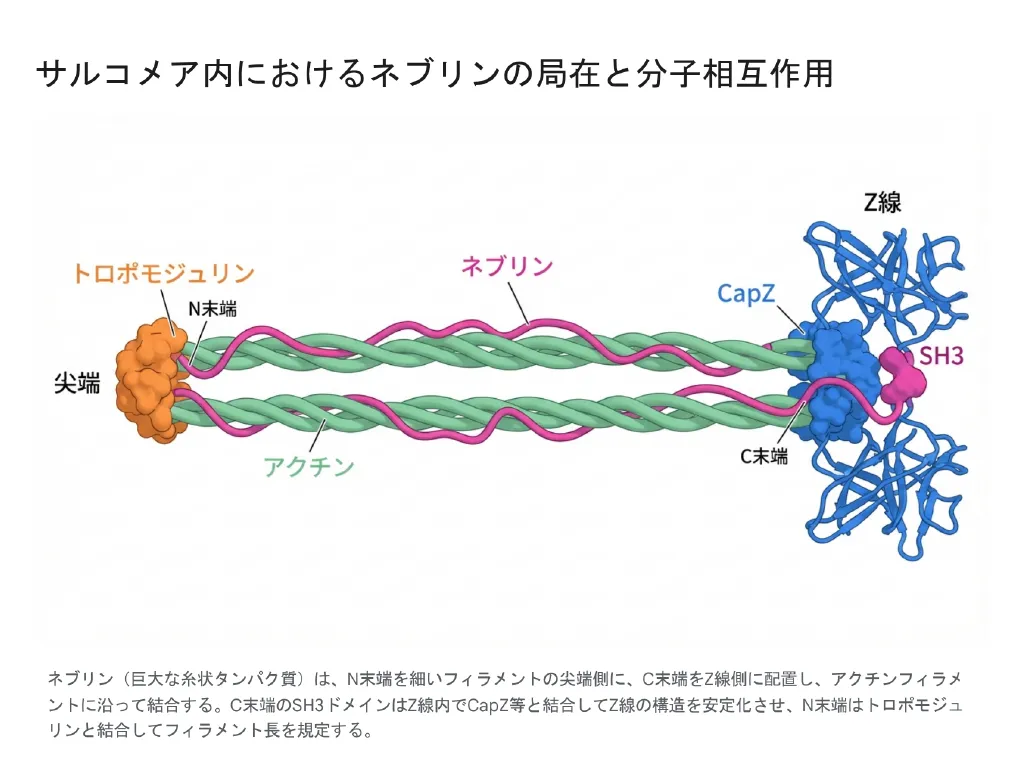
ネブリンは、筋肉の細胞内にバラバラに散らばっているわけではありません。決まった向き(極性)でピシッと配置され、筋肉の細い糸(アクチン)が「適切な長さ」になるように測って決める、いわば「分子定規(メジャー)」のような役割を果たしています。
💡 用語解説:画像に登場する筋肉のパーツ
- N末端(エヌまったん)・C末端(シーまったん):タンパク質は細長い「ヒモ」のような構造をしており、その「始まり」をN末端、「終わり」をC末端と呼びます。
- Z線(ゼットせん):筋肉のミクロの部屋(サルコメア)の「壁」や「仕切り」にあたる部分です。
- トロポモジュリン・CapZ(キャップゼット):伸びようとする筋肉の糸の端っこにパカッとはまり、「これ以上伸びないようにするフタ(キャップ)」の役割を持つタンパク質です。
ネブリンの始まり(N末端)は部屋の中央側にあり、「トロポモジュリン」というフタとくっついて糸の過剰な成長をピタリと止めます。一方、終わり(C末端)は部屋の壁(Z線)に約25nmという深さで突き刺さり、「CapZ」などと結合して壁をガッチリと安定させる「ハブ(留め具)」として働いています。
さらに2022年、「クライオ電子顕微鏡」というタンパク質の形をありのままに見ることができる最新技術を用いた研究で、驚くべき新事実が判明しました。これまでネブリンは、筋肉を動かす他の主要なタンパク質とは直接関わっていないと思われていましたが、実は「トロポニンT(TnT)」という部品の「リンカー領域」と直接つながっていることが初めて解明されたのです。
💡 用語解説:筋肉を動かすスイッチ
- トロポニンT(TnT):カルシウムに反応して、筋肉に「縮め・緩め」の指令を伝える、極めて重要な「スイッチ」の役割を果たすタンパク質です。
- リンカー領域:タンパク質の中で、部品と部品をつなぐ「柔軟なヒンジ(蝶番)」や「橋渡し」の役割をしている部分のことです。
この発見は非常に重要な意味を持ちます。ネブリンはただの「長さを測る定規(動かない骨組み)」ではなく、トロポニンTというスイッチと直接つながることで、筋肉が発揮する「力加減(活性化レベル)」まで間接的かつ精巧にコントロールしていることが、分子レベルで証明されたのです。
2. NEB遺伝子変異とネマリンミオパチー(NEM2)の病態生理
ネマリンミオパチーとは?原因遺伝子・症状から最新の遺伝子治療まで徹底解説
NEB以外の原因遺伝子や、6つのサブタイプ分類、疾患の全体像など、ネマリンミオパチーに関するさらに詳しい総合解説はこちらのページをご覧ください。
ネマリンミオパチーは、少なくとも12種類の異なる遺伝子の変異によって引き起こされる遺伝的異質性の高い疾患群ですが、その中でNEB遺伝子の変異に起因するタイプ(NEM2)が最も頻度が高く、全症例の50%以上を占めています。
💡 用語解説:ネマリン小体(nemaline rods)
患者の筋肉組織を染色して顕微鏡で観察した際に、Z線の周辺に見られる電子密度の高い異常なタンパク質の凝集体です。ネブリンが欠損することでZ線の結合ネットワークが崩壊し、Z線の異常な拡大(Z-disk widening)が起きることで形成されます。
NEM2の臨床表現型は、生後間もなく呼吸不全となる重篤なものから成人発症型まで広範なスペクトラムを呈しますが、典型的な症状群には以下が含まれます。
- 進行性筋力低下:初期症状として「フロッピーインファント(全身の筋緊張低下)」が現れ、近位筋群を中心に進行します。約35%の患者は補助なしで自立歩行することが困難です。
- 呼吸器および球麻痺の関与:横隔膜などの呼吸筋の低下により、患者の約55%が何らかの人工呼吸管理(BiPAPや気管切開など)を必要とします。また、嚥下障害により約32%が胃瘻(Gtube)チューブの造設を必要とします。
- 特異的な顔面異常:嚥下障害を有する患者の半数において、舌に3つの縦の溝が走る「三本溝パターン」が確認されています。また、筋肉からの刺激不足により「細長い顔」や「高口蓋」といった頭蓋顔面骨格の異常を高頻度で呈します。
- 二次的な骨格系の合併症:体幹を支持する筋力不足と人工呼吸器の使用期間に相関して、重度の脊柱側弯症(scoliosis)が極めて高い頻度で発症します。
3. 分子病態メカニズム:なぜ筋力が低下するのか
遺伝子の変異が、具体的にどのようにして筋肉の張力低下を引き起こすのかについて、2024年の最新コホート研究により詳細なメカニズムが解明されています。
💡 用語解説:ナンセンス変異依存的mRNA分解(NMD)
遺伝子に変異が起き「ここでタンパク質の合成を停止せよ」という間違ったストップ信号(早期終止コドン)が形成された際、細胞が異常なタンパク質を排除しようとして、設計図であるmRNAごと迅速に分解してしまう自己防衛システムです。
切断変異を持つNEM2患者では、このNMD経路が誘導されることで翻訳されるネブリンタンパク質の絶対量が「枯渇」します。その結果、細いフィラメントの長さが極端に短縮し、ミオシンとの相互作用面積が減少することで、筋収縮張力が劇的に低下します。実際、患者の筋肉中のネブリンタンパク質量と最大張力の低下の間には、明確な正の相関が観察されています。
また、スプライシング関連の変異では「クリプティックスプライスサイト(隠れたスプライシング部位)」が活性化し、アクチン結合サイトが破壊された異常なアイソフォームが生成されることが確認されています。
4. 前臨床研究のブレイクスルー:ゼブラフィッシュと次世代マウスモデル
NEB関連疾患の治療法開発における歴史的な最大の障壁は、「遺伝子が巨大すぎて従来の相同組換えなどの遺伝子操作が困難であり、適切な動物モデルを作れない」ことでした。しかし、近年のゲノム編集技術の飛躍的進歩がこの壁を打ち破りました。
ゼブラフィッシュにおける対立遺伝子シリーズ
2024年の研究で、ナンセンス変異やスプライス変異を持つ5つの新しいゼブラフィッシュモデル(neb15, neb11, neb21, neb34, neb30)が確立されました。これらのモデルは、細いフィラメントの短縮やネマリン小体の出現など、ヒトの臨床像を驚くほど忠実に再現しました。
NEB変異ゼブラフィッシュモデルにおける相対的筋収縮力の低下
(スプライス)
(スプライス)
(ナンセンス)
(ナンセンス)
(スプライス)
生体力学的な調査により、ナンセンス変異モデル(neb15, neb11)はタンパク質が完全に消失し、生後12〜13日で致死となる重篤な表現型を示した一方で、スプライス変異モデルは表現型にバリアビリティが生じ、生存期間が延長することが判明しました。
CRISPRゲノム編集による「偽エクソン」排除(次世代Hmzモデル)
哺乳類モデルにおいても長年の課題が解決されました。以前開発された「エクソン55欠失マウス」は、ヒトの臨床像とは異なり生後1週間以内に致死となるため、治療薬のスクリーニングに使用できませんでした。
2025年、その失敗の原因が「マウスゲノム内で意図せず形成された『偽エクソン』によるNMDの誘導」であることが特定されました。研究チームはCRISPR-Cas9を用いてこの偽エクソンを正確に切り出し、代わりにヒト・イントロン配列をノックインしました。この巧妙な改変により誕生した「Hmz-NebΔExon55モデル」は、安定した転写産物の発現を回復し、長期生存しながらヒトNEM2の病態を忠実に模倣する、新薬評価のための不可欠な基盤となりました。
5. 巨大遺伝子の壁を越えるAAV遺伝子治療:「プロテイン・スティッチング」
失われた正常な遺伝子を外部から補完する遺伝子補充療法は、SMA(脊髄性筋萎縮症)等ですでに臨床承認を得ていますが、NEB遺伝子を標的とする場合には決定的な物理的障害が存在しました。
💡 用語解説:AAVベクターの容量制限
治療用の遺伝子を細胞へ届ける「ウイルスの運び屋(AAV)」には、DNAを搭載できるサイズの上限(約4.7 kb)があります。NEB遺伝子はこの限界を遥かに超過しているため、1つのベクターに搭載することは絶対に不可能です。
過去には「ミニ・ネブリン断片(一部だけを切り取ったもの)」を入れる試みもありましたが、天然のネブリンと競合して逆に筋力を低下させるという有害な結果に終わりました。ネブリンが分子定規として機能するには、細いフィラメント全体を覆う完全長が必要不可欠なのです。
6. 薬理学的介入と低分子化合物アプローチ:Omecamtiv mecarbil (OM)
遺伝子治療の長期的な安全性が確立されるまでの間、並行して筋収縮の生化学的プロセスに直接介入し、低下した筋力を薬理学的に増強する「低分子化合物」の研究も実用化に向けた最終段階に入っています。
💡 用語解説:ドラッグ・リポジショニング
既存の承認薬や開発中の薬を、本来の目的とは別の疾患の治療薬として転用することです。安全性などのデータがすでにあるため、開発期間とコストを大幅に短縮できるメリットがあります。
ネマリンミオパチーの筋肉の最大の弱点は「カルシウム(Ca2+)に対する感受性が劇的に低下していること」です。この欠陥を補うため、心不全治療薬として開発されたOmecamtiv mecarbil(OM)の転用が注目を集めています。
インビトロおよび生体内実験において、OMの投与は低下したカルシウム感受性を正常レベルにまで回復させることが証明されました。特に、日常の活動や呼吸を維持するために筋肉が頻繁に使用する「最大下活性化レベル」において、OMは患者由来の筋線維の張力を87%から最大318%もの大幅な増加を示しました。
人工呼吸器からの離脱や運動機能の獲得を可能にする強力なポテンシャルを秘めており、現在臨床試験への移行が真剣に準備されています。
7. RNA標的療法とゲノム編集(CRISPR/Cas9)の最前線
遺伝子を外から補ったり、別の薬で筋力を底上げするアプローチに加え、患者さん自身の「変異した遺伝子(設計図)そのものを直接修理・調整する」究極のアプローチも活発に研究されています。
💡 用語解説:遺伝子を「直接いじる」最新治療のキーワード
- エクソン・スキッピング:遺伝子の設計図の中で、エラーがあるページ(エクソン)だけをあえて「読み飛ばす」技術です。
- ASO(アンチセンス・オリゴヌクレオチド):エラー部分を読み飛ばさせるために貼る「目隠しシール」のような役割を持つ、短い人工のお薬のことです。
- インフレーム:ページを一部読み飛ばしたあとも、前後の文章がズレずに「意味が通じる状態」で繋がっていること。
- in vivo(イン・ビボ):細胞を取り出して試験管で治療するのではなく、お薬を投与して「患者さんの体の中で直接」治療を行うことを指します。
- エクソン・スキッピングとASO:ネブリンは元々、形にある程度の柔軟性を持っています。そこで、エラーがある部分(エクソン32など)にASOというお薬を使ってフタをし、人為的にスキップ(読み飛ばし)させます。少し短くなっても、意味が通じる状態(インフレーム)で十分に機能するネブリンを作らせるこの療法が、現在有力視されています。
- CRISPR/Cas9によるin vivo(体内)ゲノム編集:最新の技術を利用し、患者さんの体の中で直接、失われた正常な遺伝子配列を正確な位置に組み込むゲノム編集の研究も進んでいます。動物モデル等で成功を収めており、長期的には「一度の治療で完治をもたらす(One-and-done)」究極の治療法となるポテンシャルを持っています。
8. 臨床試験の基盤構築:自然史研究の推進(NatHis-NM-MDUK)
プロテイン・スティッチングやOMなど、極めて強力な治療法が臨床試験へと移行する現在、実用化に向けた最大のボトルネックは「疾患の自然歴データの圧倒的な不足」です。
💡 用語解説:自然歴(Natural History)
治療介入を行わなかった場合に、病気が時間とともにどのように進行するか(筋肉の衰え方、呼吸機能の低下率など)を追跡したデータのこと。新薬の有効性を証明するための「比較対象(過去対照)」として絶対に欠かせない指標です。
この決定的な課題を克服するため、北米および欧州の複数施設からなる国際的な臨床研究ネットワークにおいて、小児患者を対象とした大規模な前向き縦断的自然史研究「NatHis-NM-MDUK」が開始されました。
ウェアラブルセンサーによる連続的運動分析、スパイロメトリーによる呼吸分析、分子バイオマーカーの探索などを包括的に行い、このデータの蓄積が2026年以降に本格化する臨床試験において極めて重要な役割を果たします。
よくある質問(FAQ)
🏥 不安を、ひとりで抱えないために
希少疾患に関する膨大な情報やご不安は、一人で抱え込まずに専門医にご相談ください。
私たちは正確性と心の安全を最優先に、次の一手を一緒に整理します。
関連記事
参考文献
- [1] NEB gene: MedlinePlus Genetics [MedlinePlus]
- [2] Nebulin: big protein with big responsibilities [PMC]
- [3] Split intein-mediated protein trans-splicing to express large dystrophins [PMC]
- [4] Omecamtiv mecarbil lowers the contractile deficit in a mouse model of nebulin-based nemaline myopathy [PMC]
- [5] Natural History Study for Patients With Nemaline Myopathy in the UK (NatHis-NM-MDUK) [ClinicalTrials.gov]