目次
抱合 conjugationとは?
抱合とは、生体内で異物や生体内物質の官能基に生体成分を結合させる反応のことです。この反応は、主に肝臓などで行われ、有害物質を無毒化する解毒作用の一つとして機能します。抱合反応を受けた物質は、多くの場合、尿中や胆汁中に排泄されますが、一部では活性化により毒性の原因となることもあります。
生体においては、いろんな化学物質を無毒化して排出しています。そのために必要なのがこの抱合といわれる化学反応になります。
抱合とは、外来性の化学物質(異物)や生体内で合成された化学物質の官能基に生体成分を結合させる反応をいいます。官能基については次の項目をご覧ください。
多くの場合、抱合反応を受けることにより尿中や胆汁中に排泄されるようになりますが、抱合により活性化されてしまい毒性を発揮する場合も一部あります。
生体内の主な抱合反応としては、グルクロン酸抱合(もっとも有名です)、グルタチオン抱合、硫酸抱合、アミノ酸抱合、メチル抱合、アセチル抱合、チオシアン合成があります。
官能基とは
官能基とは、有機化合物の中にある特定の構造(基)で、その化合物の特徴的な反応性を決定している原子(団)をいい、同じ官能基を持つ化合物は一般的に類似する性質を持ちます。有機化合物の名称も、官能基をもとに分類して命名されています。
代表的な官能基としては以下のようなものがあります。
- アルコール(R-OH)
- ケトン(R1-CO-R2)
- カルボン酸(R-COOH)
- アミン(アンモニアNH3の水素原子をR基で置き換えたもの)
- エーテル(R-O-R’)
関連記事:官能基
なぜ抱合が必要なのか?
抱合は生体内での解毒作用の一環として重要な役割を果たします。生物体は、外来物質(異物)や体内由来の一部物質を代謝する過程で、これらの物質を無毒化し、排泄しやすくするために抱合反応を行います[11]。
具体的には、抱合反応によって、有害物質が他の物質と結合し、水溶性が高まることで、体外への排泄が促進されます。例えば、肝臓などの臓器では、有害物質がグリシンなどと結合して無毒化されることがあります[9][10]。この過程は、薬物などの外来物質が体内に入った際に特に重要で、これらの物質が体内に蓄積することを防ぎ、潜在的な毒性や副作用を減少させるために必要です[7][14]。
また、抱合反応は、薬物代謝の第II相反応の一部であり、第I相代謝によって新たに形成された官能基や修飾された官能基に内因性物質(例えば、グルクロン酸、硫酸塩、グリシン)が結合することで行われます[7]。この反応によって生成された抱合体は、一般に元の物質よりも極性が高く、腎臓や胆汁を通じて体外に排泄されやすくなります[5][7]。
抱合反応は、薬物の安全性評価や治療効果の最適化においても重要であり、薬物の生体利用率や作用時間に影響を与えることがあります[2][7]。さらに、食品中の機能性成分における抱合・脱抱合過程は、これらの成分の効果発現機構の解明にも寄与しています[6]。
- 参考文献・出典
-
[5] www.chem-station.com/blog/2021/01/cooh.html
[7] www.msdmanuals.com/ja-jp/%E3%83%97%E3%83%AD%E3%83%95%E3%82%A7%E3%83%83%E3%82%B7%E3%83%A7%E3%83%8A%E3%83%AB/23-%E8%87%A8%E5%BA%8A%E8%96%AC%E7%90%86%E5%AD%A6/%E8%96%AC%E7%89%A9%E5%8B%95%E6%85%8B/%E8%96%AC%E7%89%A9%E4%BB%A3%E8%AC%9D
[9] dictionary.goo.ne.jp/word/%E6%8A%B1%E5%90%88/
[10] www.weblio.jp/content/%E6%8A%B1%E5%90%88
[11] ja.wikipedia.org/wiki/%E6%8A%B1%E5%90%88
[14] minerva-clinic.or.jp/academic/terminololgyofmedicalgenetics/hagyou/conjugation/
抱合反応が薬物代謝においてどのような役割を果たすか?
抱合反応は薬物代謝において重要な役割を果たします。具体的には、薬物や毒物などの生体外物質の代謝反応において、対象物質の親水性を高め、分解・排出しやすくすることがその主な目的です[10]。この過程は、薬物の効果や副作用、および薬物間の相互作用に密接に関連しています。
抱合反応は、第II相反応とも呼ばれ、シトクロムP450などの第I相反応によって生成した官能基に、硫酸やアミノ酸などの水溶性物質が結合する反応です。この反応によって水溶性が上昇し、薬物が体外に排泄されやすくなります[1]。抱合反応には、グルクロン酸抱合、硫酸抱合、グルタチオン抱合、アセチル抱合(アセチル化)、アミノ酸抱合(アミド化)などがあります[1]。
例えば、グルクロン酸抱合は小胞体(ミクロゾーム)で行われ、補酵素をUDP-GA(UDP-α-グルクロン酸)とし、グルクロン酸転移酵素(UGT)によってグルクロン酸が転移されます。これによってグルクロン酸抱合体が生成し、「-OH,-SH,-NH2,-COOH」などの官能基にグルクロン酸が転移されます[1]。
また、抱合反応は薬物の安全性評価や治療効果の最適化においても重要であり、薬物の生体利用率や作用時間に影響を与えることがあります。さらに、食品中の機能性成分における抱合・脱抱合過程は、これらの成分の効果発現機構の解明にも寄与しています[6]。
抱合反応の生成物は、分子量が増加し、基質より不活性になる傾向があります。これにより、薬物や毒物が無毒化され、体外への排泄が促進されます[11]。
肝臓における薬物代謝
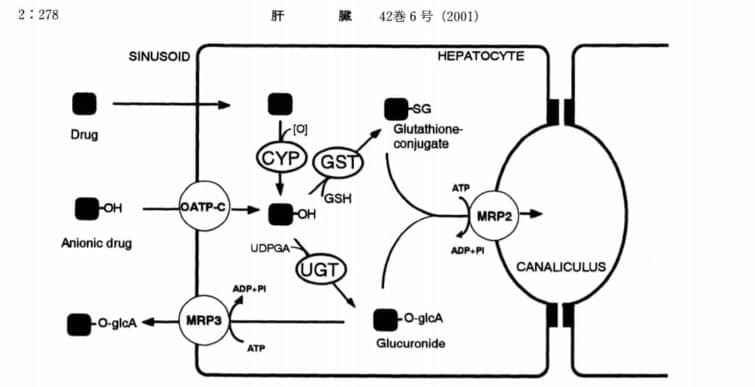
肝細胞に取り込まれる経路
1.単純拡散:脂溶性薬物が該当。
2.OATP-C(organic anion transporting polypeptide-C):アニオン性薬物、つまりマイナスに帯電した薬物の総称で、カルボン酸基(R-COOH)などの置換基を持つものが多いです:
肝細胞における抱合反応
第1相反応:脂溶性薬物はCYP(CYP: cytochrome P450)で酸化され、水酸基などの官能基を持つようになります。第1相反応を受けずに直接グルクロン酸抱合を受ける場合もあります。
第2相反応:水酸基などの官能基にグルクロン酸、硫酸、グルタチオンなどの抱合が行われ、水溶性となります。
抱合後の排泄経路
1.MRP2(multidrug resistance protein 2)により胆汁中に排泄。
2.MRP3(multidrug resistance protein 3)などのトランスポーターにより類洞側に戻る。
3.硫酸抱合体は未知の経路で胆汁中に排泄。
OATP-C: organic anion transporting polypeptide-C, UGT: UDP-glucuronosyltransferase (glycosyltransferase), GST: glutathione S-transferase, UDPGA:uridine diphospho-glucuronic acid, GSH: reduced glutathion
抱合の種類
グルクロン酸抱合
グルクロン酸化は、薬物、毒物、ビリルビン、アンドロゲン、エストロゲン、ミネラルコルチコイド、グルココルチコイド、脂肪酸誘導体、レチノイド、胆汁酸などの物質の薬物代謝に関与することが多く、肝臓で行われます。
グルクロン酸抱合は、生体内での重要な解毒機構の一つであり、特に肝臓において有害な物質を無害化するために行われる生化学的反応です。このプロセスでは、脂溶性の高い化合物に水溶性の高いグルクロン酸が結合され、水溶性の化合物に変換されます。これにより、体外への排泄が容易になります[1][4][6]。
グルクロン酸抱合は、肝臓の滑面小胞体に存在する酵素であるグルクロニルトランスフェラーゼによって触媒されます。この酵素は、グルクロン酸を薬物や他の化合物に転移させることで、グルクロン酸抱合体を形成します。形成されたグルクロン酸抱合体は、水溶性が増すため、胆汁中に分泌されたり、尿中に排泄されたりします[4][7]。
グルクロン酸抱合は、異物代謝において重要な役割を果たしており、薬物や環境汚染物質、食品添加物などの脂溶性化合物にグルクロン酸を転移させます。ヒトにおいては、食品成分(フラボノイドなど)もグルクロン酸抱合を受けることが知られています[3]。
グルクロン酸抱合の能力には個体差があり、新生児ではこの能力が低く、特定の薬物の毒性が増すことが知られています。また、遺伝子多型によるグルクロン酸抱合能の差が薬物の毒性に大きな影響を及ぼすことも明らかになっています[6]。
さらに、グルクロン酸抱合は、薬物代謝において補酵素UDP-グルクロン酸を使用し、小胞体で行われることが示されています。SLC35B1と呼ばれるタンパク質が、UDP-グルクロン酸を小胞体に取り込むトランスポーターとしての役割を果たしていることが研究によって明らかにされています[9]。
しかし、グルクロン酸抱合が必ずしも毒性を低下させるわけではなく、カルボン酸構造を有する有機化合物がグルクロン酸抱合を受けると、時に反応性代謝物を生じる場合があり、これが毒性を示すこともあります[5]。
グルクロン酸抱合は、肝臓の他の多くの機能とともに、体内の解毒プロセスの一部を形成しています。これには、グリコーゲンの貯蔵、タンパク質(アルブミン、フィブリノーゲン)の合成、コレステロール合成、ビタミンの貯蔵、血液貯蔵、免疫機能などが含まれます[14]。
- 参考文献・出典
-
[1] kotobank.jp/word/%E3%82%B0%E3%83%AB%E3%82%AF%E3%83%AD%E3%83%B3%E9%85%B8%E6%8A%B1%E5%90%88-1306933
[3] www.pu-toyama.ac.jp/BR/sakaki/research/research-ugt.html
[4] www.weblio.jp/content/%E3%82%B0%E3%83%AB%E3%82%AF%E3%83%AD%E3%83%B3%E9%85%B8%E6%8A%B1%E5%90%88
[5] www.chem-station.com/blog/2021/01/cooh.html
[6] www.weblio.jp/wkpja/content/%E3%82%B0%E3%83%AB%E3%82%AF%E3%83%AD%E3%83%B3%E9%85%B8_%E3%82%B0%E3%83%AB%E3%82%AF%E3%83%AD%E3%83%B3%E9%85%B8%E6%8A%B1%E5%90%88
[7] www.msdmanuals.com/ja-jp/%E3%83%97%E3%83%AD%E3%83%95%E3%82%A7%E3%83%83%E3%82%B7%E3%83%A7%E3%83%8A%E3%83%AB/23-%E8%87%A8%E5%BA%8A%E8%96%AC%E7%90%86%E5%AD%A6/%E8%96%AC%E7%89%A9%E5%8B%95%E6%85%8B/%E8%96%AC%E7%89%A9%E4%BB%A3%E8%AC%9D
[9] www.kanazawa-u.ac.jp/rd/80786
グルタチオン抱合
グルタチオンはグリシン、システイン、グルタミン酸からなるトリペプチドで、有機物質をグルタチオンと結合させてグルタチオン抱合をします。エポキシド、ハロゲン、ニトロ基などの電子吸引基を持つものが基質となります。グルタチオン抱合体からはグルタミン酸とグリシンがとれ、システイン抱合体となります。システイン抱合体さらにアセチル化を受けて、メルカプツール酸となり、尿中に排泄されます。
グルタチオン抱合は、生体内で発生する重要な代謝反応の一つであり、特に解毒過程において中心的な役割を果たします。この反応では、グルタチオン(GSH)が体内の有害物質や異物と結合し、それらを無害化することにより、体外への排泄を容易にします[2][6]。
グルタチオンは、グルタミン酸、システイン、グリシンという3つのアミノ酸から構成されるトリペプチドで、細胞内に広く存在し、抗酸化作用や酸化還元反応の調節、酵素の活性化など多様な生理的機能を持っています[6]。グルタチオン抱合反応は、グルタチオンS-転移酵素(GST)によって触媒され、この酵素は生物体に広く存在し、生合成や薬物の代謝に関与しています[8]。
この反応の過程では、グルタチオンが基質の求核性部位に結合し、グルタチオン抱合体を形成します。その後、この抱合体はさらなる代謝過程を経て、最終的には水溶性の物質に変換され、尿中や胆汁中に排泄されます[1][2][3]。この過程により、脂溶性の有害物質が水溶性化され、体外への排泄が促進されます[7]。
また、グルタチオン抱合反応は、特定の薬物や化学物質の代謝にも関与しており、アセトアミノフェンのような薬物の毒性発現にも影響を与えることが知られています[6]。この反応によって形成されるメルカプツール酸は、グルタチオン抱合体が加水分解を受けてシステイン抱合体となり、さらにアセチル抱合を受けることで生成されます[1]。
グルタチオン抱合反応は、生体の解毒機能を支える基本的なメカニズムの一つであり、生体内での有害物質の無害化や排泄を促進することにより、生物の生存と健康を守る重要な役割を担っています。
- 参考文献・出典
-
[1] e-rec123.jp/e-REC/contents/102/130.html
[2] kusuri-jouhou.com/creature1/conjugation.html
[3] www.pharm.or.jp/words/word00903.html
[4] opac.ll.chiba-u.jp/da/curator/900034438/Y2006-12.pdf
[5] www.jstage.jst.go.jp/article/fpj/134/6/134_6_334/_pdf
[6] www.hoku-iryo-u.ac.jp/~wadakg/keyword/gsh.html
[7] www.jstage.jst.go.jp/article/jscc1971b/36/3/36_181/_pdf/-char/ja
[8] agriknowledge.affrc.go.jp/RN/2030851517.pdf
硫酸抱合
スルホトランスフェラーゼがPAPS(活性硫酸)を補酵素として利用して抱合を行います。基質となるのは水酸基(ヒドロキシ基ともいいます)とアミノ基です。
R-OH → R-OSO3– R-NH2 → R-NHSO3–
硫酸抱合(Sulfate conjugation)は、生体内で発生する代謝反応の一つで、血中の物質を硫酸エステル化(-OSO3−)して分子の極性を高め、排出しやすい有機陰イオンに変換するプロセスです[17]。この反応は、主に肝臓で行われ、硫酸転移酵素(SULT)によって触媒されます。硫酸抱合は、内因性の代謝産物や外来物質(例えば薬物や毒素)の排泄を促進するために重要な役割を果たします。
硫酸抱合体は、脂溶性の高い薬物などが硫酸抱合されることによって水溶性が高まり、体外へ排泄しやすくなります[11]。この反応によって生成された硫酸抱合体は、尿や胆汁を通じて体外に排出されることが多いです。また、硫酸抱合は、薬物や農薬の開発や安全性評価を行う上で極めて重要とされています[16]。
硫酸抱合の具体的な例としては、ドーパミンやノルエピネフリンなどのモノアミン系化合物が硫酸抱合体として血中を循環していることが報告されています[2]。また、硫酸抱合は、薬物代謝においても重要であり、特定の薬物の硫酸抱合体が尿中に排泄されることが知られています[8]。
硫酸抱合に関わる酵素の一つであるSULT1A1は、肝臓に高発現しており、腎線維化形成においても重要な役割を果たしていることが示されています[11]。さらに、硫酸抱合は、腎障害形成・進展における硫酸抱合型尿毒素の役割を究明する研究においても注目されており、尿毒症抑制薬の探索において重要な機軸となっています[9]。
- 参考文献・出典
-
[2] www.dojindo.co.jp/letterj/129/review/01.html
[8] www.falco.co.jp/rinsyo/detail/061025.html
[9] kaken.nii.ac.jp/ja/grant/KAKENHI-PROJECT-17H04104/
[11] www.kumamoto-u.ac.jp/whatsnew/seimei/20230720
[16] www.jstage.jst.go.jp/article/jpestics/36/2/36_W11-03/_pdf
[17] ja.wikipedia.org/wiki/%E7%A1%AB%E9%85%B8%E6%8A%B1%E5%90%88
アセチル抱合
アセチル抱合の基質はアミノ基、水酸基です。細胞質で行われ、アセチルCoAトランスフェラーゼ(転移酵素)により行われます。イソニアジドのN-アセチル化など、遺伝的多型があることで有名です。
アセチル抱合は、薬物代謝の第II相反応の一つで、特定の薬物や化学物質が体内で無害化される過程です。この反応では、アセチルCoAが供与体として機能し、アセチルトランスフェラーゼ(NAT)という酵素によって、薬物や異物のアミノ基や水酸基にアセチル基が結合されます[3]。アセチル抱合は、水溶性が低下する反応であり、主にアミノ基や水酸基と反応します[3]。
アセチル抱合によって生成された代謝物は、一般的には尿中に排泄されますが、場合によっては毒性を持つこともあります[5]。アセチル抱合は、芳香族第一級アミンやヒドラジン基を有する薬物に対して特に起こりやすいとされています[11]。
日本人ではアセチル化能が高い人が多く、欧米人では逆に低い人が多いという遺伝的多型が存在します[3]。このため、アセチル抱合の速度は個人差が大きく、薬物の効果や副作用に影響を与える可能性があります。
アセチル抱合に関与する酵素の一つであるNATには、NAT1とNAT2という分子種が存在し、NAT2はイソニアジドのアセチル化に関与しています[3]。また、アセチル抱合による代謝物は、硫酸抱合体(解毒代謝物)の生成が抑制された場合に、毒性代謝物としての生成量が増えることがあります[4]。
アセチル抱合は、薬剤師国家試験などで問われることもあり、薬剤師を目指す学生にとって重要な知識の一つです[1][11]。
アミノ酸抱合
ミトコンドリアで行われます。基質はカルボキシ基、カルボキシ基がアシルCoAと結合して活性化した後にアミノ酸(グリシンとグルタミン)抱合を受けます。
アミノ酸抱合は、生体内での異物や薬物の代謝過程の一つであり、特にカルボキシル基を持つ外来性の化合物(薬物、農薬、殺虫剤など)や内因性物質(中鎖脂肪酸など)の解毒に重要な役割を果たしています[14]。この反応は、アミノ酸(主にグリシンまたはグルタミン)がカルボキシル基を持つ薬物に結合し、より水溶性が高く、尿中や胆汁中に排泄されやすい抱合体を生成することにより、体外への排泄を促進します[2][10]。
アミノ酸抱合反応は、特に肝臓で行われることが多く、アシル転移酵素によって進行します。CoAチオエステルは高エネルギー化合物であり、生理的条件下での加水分解時に重要な役割を果たします[13]。また、抱合型胆汁酸は脂質の消化と吸収を助ける乳化剤としても働き、グリシンは貝類に多く含まれることから、「貝類は肝臓に良い」と言われる理由の一つとなっています[12]。
アミノ酸抱合は、薬物代謝の第II相反応の一部であり、第I相反応によって生成された官能基に、硫酸やアミノ酸などの水溶性物質が結合する反応です[3]。この過程は、薬物や異物が体内でより速やかに排泄されるようにするために重要であり、特にアミノ酸抱合は、特定の薬物に対して重要な代謝経路となっています[16]。
総じて、アミノ酸抱合は生体内での薬物や異物の代謝において重要な役割を果たし、特に水溶性が低く排泄が困難な化合物の排泄を促進することにより、体内の解毒プロセスに貢献しています。
- 参考文献・出典
-
[2] e-rec123.jp/e-REC/contents/98/22.html
[10] www.msdmanuals.com/ja-jp/%E3%83%97%E3%83%AD%E3%83%95%E3%82%A7%E3%83%83%E3%82%B7%E3%83%A7%E3%83%8A%E3%83%AB/23-%E8%87%A8%E5%BA%8A%E8%96%AC%E7%90%86%E5%AD%A6/%E8%96%AC%E7%89%A9%E5%8B%95%E6%85%8B/%E8%96%AC%E7%89%A9%E4%BB%A3%E8%AC%9D
[11] www.med.teikyo-u.ac.jp/~lipo/lecture/ba/ba.html
[12] www.yuki-gosei.co.jp/glycine/page_6/
[13] www.jstage.jst.go.jp/article/jscc1971b/36/3/36_173/_pdf/-char/en
[16] onlinelibrary.wiley.com/doi/abs/10.1002/9780470921920.edm020
メチル抱合
S-アデノシルメチオニンにより行われます。
メチル抱合は、生体内で異物や生体内物質の官能基にメチル基(CH3)を結合させる反応の一つです。この反応は、主に第II相代謝反応の一部として行われ、薬物や毒素などの水溶性を高め、体外への排泄を容易にすることを目的としています[5][6][7]。
第II相代謝反応は、主にグルクロン酸抱合、硫酸抱合、グルタチオン抱合、アセチル抱合、アミノ酸抱合、そしてメチル抱合などが含まれます。これらの反応は、薬物や毒素が第I相代謝を経て、その官能基にさらに反応性の低い基を結合させることで、水溶性を高め、尿や胆汁を通じて体外に排泄しやすくすることが目的です[5][6][7]。
メチル抱合は、特に脂溶性が高く水溶性が低い化合物の排泄を促進するために重要です。メチル基の供与体としては、主にS-アデノシルメチオニンが用いられ、メチルトランスフェラーゼと呼ばれる酵素によって触媒されます[5][6][7]。
この反応は、薬剤師国家試験の範囲内でも重要な概念の一つであり、異物代謝の理解において基本的な知識となります[6][14][15]。また、メチル抱合は、薬物の効果を減少させたり、毒性を低減させるなど、薬物療法においても重要な役割を果たします。
- 参考文献・出典
-
[5] www.pharm.or.jp/words/word00903.html
[6] yakugaku-gokaku.com/%E7%AC%AC2%E7%9B%B8%E5%8F%8D%E5%BF%9C%E3%80%80%E6%8A%B1%E5%90%88%E5%8F%8D%E5%BF%9C/
[7] minerva-clinic.or.jp/academic/terminololgyofmedicalgenetics/hagyou/conjugation/
[14] yakuzero.com/range/hygiene/poison/drug-metabolism/699/
[15] www.youtube.com/watch?v=ZCsPGfm_2NE