目次
エーラス・ダンロス症候群関節弛緩型(aEDS)は、出生時から両側の股関節脱臼が生じる超希少な遺伝性結合組織疾患です。世界で約30〜42例しか報告されていないほど稀ですが、患者の生涯にわたる運動機能と生活の質に深刻な影響を及ぼします。
Q. aEDS(関節弛緩型EDS)とはどのような病気ですか?
A. COL1A1またはCOL1A2遺伝子の異常によりI型コラーゲンの形成が障害される、常染色体顕性遺伝の超希少疾患です。出生時の両側股関節脱臼が最大の特徴で、全身性の著しい関節弛緩・皮膚の過伸展性・筋緊張低下を伴います。根治療法はなく、多職種連携による長期的な対症療法が治療の中心となります。
- ➤原因 → COL1A1/COL1A2遺伝子のエクソン6スキッピングによるI型コラーゲン形成不全
- ➤頻度 → 100万人あたり1人未満の超希少疾患。世界報告症例は約30〜42例
- ➤症状 → 出生時両側股関節脱臼・全身性関節弛緩・筋緊張低下・皮膚の過伸展性
- ➤診断 → 2017年国際臨床診断基準+COL1A1/COL1A2遺伝子検査による確定診断
- ➤治療 → 骨切り術・MAGECロッド・理学療法を中心とした多職種チームアプローチ
1. aEDSとは何か:疾患の概要と疫学
エーラス・ダンロス症候群(EDS)は、コラーゲンをはじめとする結合組織の生合成・構造・修飾プロセスに関わる遺伝的欠陥によって生じる、臨床的・遺伝的に多様な遺伝性疾患群です。2017年の国際EDSコンソーシアムによる再分類では、臨床的特徴と分子遺伝学的基盤に基づいて13の独立した病型に分けられています。
その中でも、関節弛緩型EDS(Arthrochalasia EDS:aEDS)は最も稀有でありながら極めて重篤な身体障害をもたらす病型の一つです。歴史的には「EDS VII型(VIIAおよびVIIB)」または「多発性先天性関節弛緩症」と呼ばれてきました。
有病率:aEDSは100万人あたり1人未満とされる「超希少疾患(ultra-rare disorder)」です。世界の学術文献で詳細が報告されている症例数は約30〜42例にとどまります。EDS全体の有病率が3,100〜5,000人に1人であることと比較すると、その稀少さが際立ちます。
結合組織とは、骨・皮膚・腱・靭帯・血管壁など、体のあらゆる部位で「構造的な足場」を担う組織の総称です。その主要な構成タンパク質がコラーゲンです。結合組織が正常に機能しないと、関節・皮膚・内臓など多系統にわたる症状が現れます。aEDSではこのコラーゲンの形成そのものが遺伝子レベルで障害されています。
日本国内では、EDS全体が指定難病168として認定されており、医療費助成の対象となっています。aEDSはICD-10コード「Q79.6(エーラス・ダンロス症候群)」に分類され、稀少かつ重篤な病型として高度な専門的介入が必要な疾患に位置づけられています。
2. 原因遺伝子と遺伝形式
aEDSは常染色体顕性遺伝(常染色体優性遺伝)の形式をとります。つまり、両親のいずれかから変異を持つアレルを1つ受け継ぐだけで発症します。患者が子どもをもうける場合、その変異が次世代に伝わる確率は各妊娠において50%です。また、家族歴がない孤発例(de novo変異)として生じるケースも報告されています。
23対ある染色体のうち、性染色体(X・Y染色体)以外の「常染色体」上の遺伝子に変異があり、1つのアレル(対になる遺伝子の片方)だけに変異があっても発症する遺伝形式です。「顕性(優性)」とは「1コピーで効果が現れる」という意味であり、「強い・弱い」の意味ではありません。両親のどちらかが患者であれば、子への遺伝確率は50%です。
原因となる遺伝子は、I型コラーゲンをコードする以下の2つのいずれかです。
COL1A1遺伝子(染色体17q21.33)
I型コラーゲンのプロα1(I)鎖をコードします。この遺伝子の変異によるものは歴史的に「EDS VIIA型」と呼ばれていました。特定の変異(c.472-1G>AおよびC.472-2A>T)では、歯の象牙質形成不全(dentinogenesis imperfecta)が合併することが知られています。
COL1A2遺伝子(染色体7q21.3)
I型コラーゲンのプロα2(I)鎖をコードします。「EDS VIIB型」と呼ばれていました。COL1A2変異の患者では、歯の象牙質形成不全が見られない傾向があり、遺伝子座による微細な表現型の違いが存在します。
変異の浸透率(penetrance)は男女ともにほぼ100%と推定されており、変異を持っていれば必ず何らかの臨床症状が現れます。ただし、重症度には個体差や家族間でのばらつきが存在します。
3. 分子病態メカニズム:エクソン6スキッピングが引き起こすもの
aEDSの根底にある分子異常は、単なるタンパク質量の低下ではなく、RNAのスプライシング過程における特異的な欠失(エクソン6スキッピング)と、それに続くコラーゲン分子の立体的な構造異常です。
DNAからタンパク質が作られる過程では、まず「プレmRNA」が作られ、その後「スプライシング」という編集作業でイントロン(不要部分)が取り除かれ、エクソン(必要部分)だけがつなぎ合わされます。「エクソン6スキッピング」とは、スプライス部位の変異によりエクソン6(必要な情報部分)が誤って丸ごと除去されてしまう現象です。これにより、コラーゲン前駆体(プロコラーゲン)の切断部位が失われます。
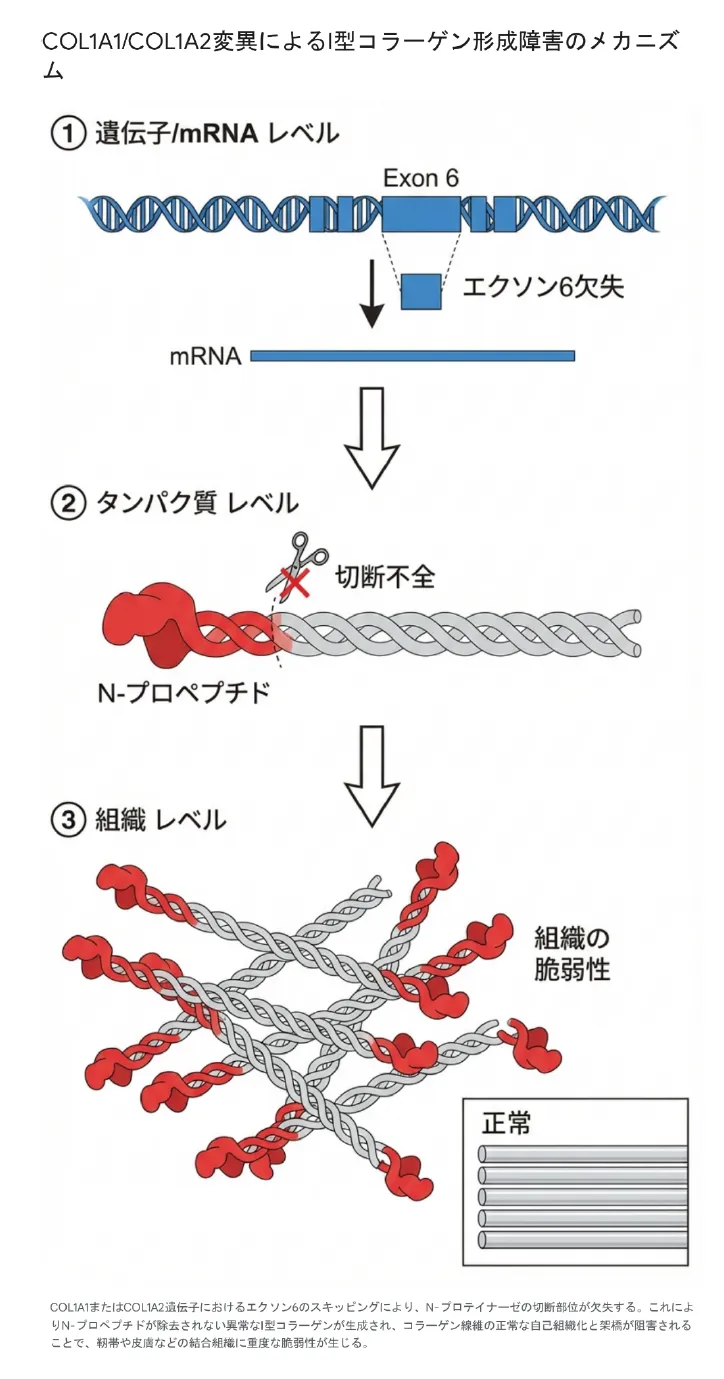
正常なI型コラーゲンが完成するには、前駆体であるプロコラーゲンのN末端(アミノ末端)にある「N-プロペプチド」を、ADAMTS-2などの酵素(N-プロテイナーゼ)が特異的に切断する必要があります。エクソン6がスキッピングされると、この酵素の切断部位がコードされなくなり、N-プロペプチドが残ったままの異常なコラーゲン分子(pN-コラーゲン)が細胞外に分泌・蓄積されます。
この切り離されなかった巨大なN-プロペプチドが立体障害(steric hindrance)を引き起こし、コラーゲン分子間の規則正しい架橋形成と平行配列を著しく阻害します。その結果、皮膚・靭帯・関節包・骨などにおけるコラーゲン線維の強度が根本的に失われ、aEDSの臨床症状として表れます。
変異によって生じた異常タンパク質が、正常なタンパク質とも結合して三量体(3本のらせん構造)を形成し、正常な機能まで阻害してしまう現象です。aEDSでは、変異アレルから産生された短縮型α1(I)鎖が正常なコラーゲン分子に取り込まれることで、ハプロ不全(タンパク質が半減するだけ)よりもはるかに深刻な結合組織の破壊をもたらします。これがaEDSが骨形成不全症軽症型と異なり、多系統に重篤な症状を示す分子生化学的な理由です。
4. 多系統にわたる臨床症状
aEDSの患者は出生直後から成人まで、多くの臓器・組織にわたる症状を呈します。I型コラーゲンが体のあらゆる部位に存在するため、症状は筋骨格系だけにとどまりません。
① 筋骨格系・整形外科的異常
aEDSで最も顕著かつ生活に直結する症状が筋骨格系に集中しています。
先天性両側股関節脱臼
aEDSの決定的ホールマーク(指標)です。事実上すべての患者が出生時にこの所見を持ちます。胎児期からの関節包の異常弛緩と寛骨臼(ソケット)の浅い形成が複合して生じます。この有無が診断の出発点となります。
重度の全身性関節過可動性
肩・膝・肘などの大関節から、手指・足趾・手首などの小関節まで、正常な解剖学的可動域をはるかに超えた過可動性があります。乳児期には日常のおむつ替えや着替えでさえ脱臼を来すほど関節が不安定です。
反復性脱臼・変形性関節症
四肢のあらゆる関節において日常的な反復性脱臼・亜脱臼が生じます。慢性的な微小外傷が蓄積し、関節軟骨の早期摩耗から若年性変形性関節症を招きます。
重度の脊椎変形
小児期早期から後側彎症(後彎+側彎の合併)や腰椎過前彎が進行します。重度の後側彎症は胸腔を圧迫し、致死的な呼吸機能障害をもたらすリスクがあります。
その他、先天性の内反尖足・重度の扁平足・外反膝なども高頻度で見られます。放射線学的には軽度の骨減少症や、頭蓋骨縫合線に沿ったウォーム骨(縫合間骨)が観察されることもあります。
② 神経・筋機能への影響
出生時からの重度の筋緊張低下(ヒポトニア)が認められます。筋肉が「フロッピー(ぐにゃぐにゃ)」な状態となり、首のすわり・寝返り・座位・歩行などの運動発達マイルストーンが著しく遅れます。この極端な筋力低下から、乳幼児期には脊髄性筋萎縮症(SMA)などの神経筋疾患と誤診されるリスクがあります。
重要ポイント:aEDSのヒポトニアは神経・筋疾患によるものではなく、結合組織の欠陥に由来する二次的なものです。年齢を重ねるにつれて徐々に改善する傾向があり、SMAなどとは異なります。神経学的反射は保たれており、関節の過可動性・皮膚の特徴との組み合わせで鑑別します。
また、頸椎の不安定性からキアリ奇形(小脳扁桃の下垂)が合併することがあります。硬膜のコラーゲン異常による脳脊髄液(CSF)漏出は頭蓋内圧低下を引き起こし、体位性頭痛・羞明・複視などの症状の原因となります。輻輳不全などの眼球運動障害が読字困難や学習障害に繋がるケースもあります。
③ 皮膚・結合組織の異常
皮膚は異常に伸びやすく、引っ張ると正常範囲を大きく超えて伸展しますが、放すと即座に元の位置に戻ります(皮膚弛緩症とは異なります)。触感は非常に柔らかく、ビロードやパン生地のように表現されます。手掌・足底に特徴的な十字の折り目パターン(criss-cross creases)が見られることもあります。
軽微な外傷で容易に挫傷(内出血・血腫)が生じ、創傷治癒が遅延します。治癒後には陥凹したシワ状の萎縮性瘢痕(cigarette-paper scars)が形成されます。ただし皮膚症状の重症度は、古典型EDS(cEDS)と比べて一般的に軽度です。
④ 頭蓋顔面の特徴
小児期には、小顎症・両眼開離(目の間隔が広い)・内眼角贅皮・前頭部突出・鼻梁の陥凹・青色強膜・中顔面低形成・大きな泉門などの特徴的な顔貌が見られます。これらの顔貌的特徴はヒポトニアと同様、年齢とともに目立たなくなる傾向があります。
5. 診断基準:2017年国際分類と分子遺伝学的確定診断
aEDSの診断は、①臨床的評価と②分子遺伝学的検査の二段階で行われます。2017年の国際EDSコンソーシアムにより、aEDSの大基準・小基準が初めて明確に定義され、診断の標準化が実現しました。
▍大基準(Major Criteria)
- 大基準1(必須)先天性両側股関節脱臼 ── 出生時のX線または超音波検査で確認。aEDS診断のゲートウェイ
- 大基準2重度の全身性関節過可動性(複数関節での脱臼または亜脱臼を伴う)
- 大基準3皮膚の過伸展性(引っ張ると正常範囲を超えて伸び、放すと速やかに戻る)
▍小基準(Minor Criteria)
- ●筋緊張低下(ヒポトニア)
- ●後側彎症(小児期早期から進行する後彎と側彎の合併)
- ●軽度の骨減少症(放射線学的に確認される骨密度低下)
- ●組織の脆弱性(萎縮性瘢痕形成を含む)
- ●挫傷を生じやすい皮膚(軽微な接触による内出血・血腫)
遺伝学的検査への適応条件:「大基準1+大基準3」を満たすか、「大基準1+大基準2+小基準2項目以上」を満たす場合。いずれのパスでも大基準1(先天性両側股関節脱臼)が必須要件です。
上記の臨床基準を満たした場合、確定診断のためには分子遺伝学的検査が必須です。血液・唾液などからDNAを抽出し、次世代シーケンサー(NGS)やサンガー法でCOL1A1またはCOL1A2遺伝子のエクソン6スキッピングを引き起こす病原性バリアントを特定します。
関節過可動性を数値化するための国際的な評価指標です。小指の背屈・親指の手首への接触・肘の過伸展・膝の過伸展・立位前屈時の手掌の床接触という9点満点のスクリーニングスコアです。aEDSでは全身性の高度な関節弛緩が存在するため、通常はスコアが高値を示します。ただし乳幼児期は標準基準値の適用に注意が必要です。
6. 鑑別診断:他のEDS病型・類縁疾患との見分け方
aEDSの症状は他のEDS病型や結合組織疾患と部分的に重複するため、精緻な鑑別が不可欠です。
| 疾患名 | 関連遺伝子 | 遺伝形式 | aEDSとの決定的な相違点 |
|---|---|---|---|
| 古典型EDS (cEDS) | COL5A1, COL5A2 | 常染色体顕性 | 非常に脆弱な皮膚と重度の萎縮性瘢痕が顕著。先天性股関節脱臼は必須ではない |
| 血管型EDS (vEDS) | COL3A1 | 常染色体顕性 | 大動脈解離・腸管破裂のリスクが極めて高く致死的。皮膚の過伸展性は乏しい |
| 過可動型EDS (hEDS) | 未確定 | 常染色体顕性 | EDSの90%を占める最も一般的な病型。両側股関節脱臼や皮膚の極端な脆弱性は伴わない |
| 後側彎型EDS (kEDS) | PLOD1, FKBP14 | 常染色体潜性 | 後側彎症・筋緊張低下は共通するが、強膜破裂・難聴を伴う点と潜性遺伝である点が異なる |
| 皮膚脆弱型EDS (dEDS) | ADAMTS2 | 常染色体潜性 | N-プロテイナーゼ酵素自体の欠損。過剰なたるんだ皮膚と重度の皮膚裂傷が特徴。股関節脱臼は主徴ではない |
| ラーセン症候群 | FLNB | 顕性/潜性 | 多発性関節脱臼を伴うが、特有の平坦な顔貌と頸椎の異常が際立つ。コラーゲン異常による皮膚の過伸展性は見られない |
7. 治療・管理:多職種チームによる対症療法
aEDSに対する根治療法は現在のところ存在せず、治療はすべて対症療法です。患者の身体的安定性・歩行能力・生活の質の最大化を目指し、整形外科医・理学療法士・臨床遺伝専門医・皮膚科医・疼痛管理専門医・心理士などによる学際的チームアプローチが不可欠です。
① 股関節脱臼への外科的介入
出生直後の両側股関節脱臼の管理は、患者が将来歩行能力を獲得できるかどうかを決する最重要課題です。
一般的な発達性股関節形成不全(DDH)に用いるパブリック・ハーネスや股関節ギプスなどの保存的整復術はaEDS患者にはほとんど効果がなく、成功例は皆無に等しいとされます。また、関節包のみを縫縮する軟部組織手術も術後短期間での再脱臼率が極めて高く、失敗に終わるケースが大多数です。
医学文献が示す唯一の有効な手段は、腸骨骨切り術(Salter法・Pemberton法など)です。骨格の形状そのものを物理的に改変し、寛骨臼を深くすることで弛緩した関節包に依存せずに大腿骨頭を安定して保持します。必要に応じて大腿骨骨切り術と併用されます。
人工股関節置換術(THA)のリスク:EDS患者はTHA後の不安定性・再脱臼リスクが対照群の約3.2倍、インプラントの無菌的ゆるみのリスクは約3.8倍、全原因による再手術リスクは約2.4倍に達するとの研究データがあります。手術適応は極めて慎重に判断する必要があります。
② 脊椎変形の外科的管理:MAGECロッドという革新
早期発症型の重度後側彎症に対しては脊椎の矯正・固定が必要ですが、従来の成長ロッドは半年ごとの皮膚切開が必要で、aEDS患者の極度に脆弱な皮膚では深刻な創傷離開・感染症のリスクがありました。
MAGnetic Expansion Controlロッドの略称です。一度体内に埋め込んだ後、体外から磁力を当てるだけで非侵襲的にロッドを伸長できる脊椎固定デバイスです。消毒シートで皮膚が崩壊するほど脆弱なaEDS患者において、繰り返しの切開手術を回避しつつ17年間にわたり重度の脊椎変形の矯正に成功した長期追跡症例が報告されており、aEDSの脊椎管理における新たなパラダイムとして評価されています。
③ 理学療法とリハビリテーション
筋肉のサポートによって不安定な関節を動的に安定させるため、理学療法は管理戦略の中核です。基本方針は「start low and go slow」(関節への負荷を極めて少なくした等尺性エクササイズから始め、ゆっくり進む)です。
- ➤固有受容感覚の再訓練:関節の位置感覚が鈍麻しているため、鏡を使ったフィードバックやバランス訓練でニュートラルな関節位置の保持を学習させます
- ➤装具(AFO等)の活用:皮膚が極度に脆弱なため、装具のフィッティング調整と毎日の皮膚状態の監視がセットで必要です
- ➤避けるべき運動:ランニング・ジャンプ・コンタクトスポーツ・関節の過伸展を強調するヨガや体操は脱臼と軟骨損傷を誘発するため厳格に避けます
- ➤水中運動(アクアセラピー):関節への衝撃が少なく、aEDS患者に適した運動形態として推奨されることがあります
④ 心血管モニタリング・創傷管理・疼痛マネジメント
I型コラーゲンは血管壁にも存在するため、大動脈基部拡張や僧帽弁逸脱の有無を評価するベースラインの心エコー検査をすべての患者に実施します。創傷縫合の際は通常より深く縫合糸をかけ、抜糸まで通常の2倍程度の期間を確保します。Steri-Stripsや組織接着剤の併用が強く推奨されます。疼痛管理にはNSAIDs・トリガーポイント注射・TENSなどが用いられます。
8. 長期予後と生活支援・合理的配慮
aEDSは生命予後そのものを直ちに脅かす疾患ではありませんが、生涯にわたる重度の身体障害と慢性疼痛をもたらします。乳幼児期に最も顕著だった筋緊張低下と関節過可動性は、筋肉の発達とともに年齢を重ねるにつれてある程度改善する傾向があります。適切な整形外科的介入と理学療法を受けた患者の中には、小児期後期に自力歩行が可能になるケースも報告されています。
成人期でも関節の根本的な不安定性は残存し、若年期からの変形性関節症は避けられません。骨減少症・骨粗鬆症のリスクも生涯継続するため、成人以降も1〜2年ごとのDEXAスキャン(骨密度測定)が推奨されます。
教育現場・職場における合理的配慮
学校・職場においては、物理的ストレスを軽減し能力を最大限発揮させるための合理的配慮が必要です。主な例を以下に示します。
物理的・環境的配慮
エルゴノミクスチェアの導入、定期的な横臥休息時間の確保、重いカバンの免除、教科書デジタル化、エレベーター利用、車椅子使用の許可など
学習・書字への配慮
試験時間の延長、音声入力ソフトやPCの使用許可、太いグリップの筆記具の提供、代筆者の配置など
視覚・体育への配慮
教室照明の調整、文字の拡大・コントラスト強調、体育は医師・理学療法士の指導に基づく適応型プログラムへの変更
超希少疾患を抱えながら生きることは、身体的苦痛だけでなく、周囲の無理解による孤立感や不確実な未来への不安など深刻な精神的負担を伴います。認知行動療法(CBT)などの心理的ケアや患者支援団体を通じたピアサポートへのアクセスが強く推奨されます。
9. 最新研究動向と将来の展望(2024–2026年)
aEDS研究は2024年から2026年にかけて、歴史的な転換点を迎えています。
「The Road to 2026」イニシアチブ
国際EDSコンソーシアムが2017年基準のアップデートを推進中です。大規模なゲノム解析・コミュニティ体験調査のデータを統合し、2026年後半に新たな分類基準と管理ガイドラインを公式発表予定。aEDSを含む希少病型の診断アルゴリズムがさらに洗練されます。
EDS/HSDグローバル・バイオバンク
2025年秋、The Ehlers-Danlos Societyが250万ドルの資金提供を受けて世界初のEDS/HSDグローバル・バイオバンクを設立予定。世界で数十人しかいないaEDS患者の生体サンプルを一元管理し、新規バイオマーカー発見・個別化医療の基盤整備を加速します。
分子標的治療の研究
COL1A1/COL1A2のエクソン6スキッピングをインビトロのミニ遺伝子アッセイで再現・解析する手法が確立されています。将来的にはアンチセンス・オリゴヌクレオチド(ASO)などのRNAモジュレーション技術で異常なスプライシングを補正する根本的な分子標的薬の開発が期待されています。
よくある質問(FAQ)
関連記事
参考文献
- [1] GARD(NIH希少疾患情報センター). Ehlers-Danlos syndrome, arthrochalasia type. [NIH GARD]
- [2] The Ehlers-Danlos Society. aEDS(関節弛緩型EDS)疾患情報. [Ehlers-Danlos Society]
- [3] Sobey G, et al. Ehlers–Danlos Syndrome Type Arthrochalasia: A Systematic Review. PMC 2022. [PMC]
- [4] Malfait F, et al. The 2017 international classification of the Ehlers–Danlos syndromes. Am J Med Genet C Semin Med Genet. 2017. [EDS Society]
- [5] Orphanet. Arthrochalasia Ehlers-Danlos syndrome(疾患詳細情報). [Orphanet]
- [6] Giunta C, et al. Ehlers-Danlos Arthrochalasia type (VIIA-B) – expanding the phenotype. PMC 2014. [PMC]
- [7] Baban A, et al. Seventeen-year outcome of surgical management of severe early onset kyphoscoliosis in a patient with arthrochalasia-type Ehlers–Danlos. PMC 2025. [PMC]
- [8] MedlinePlus(NIH). Ehlers-Danlos syndrome – Genetics. [MedlinePlus]
- [9] The Ehlers-Danlos Society. The Road to 2026: A Path Toward Progress. [EDS Society]
- [10] 厚生労働省難病情報センター. エーラス・ダンロス症候群(指定難病168). [難病情報センター]
- [11] GeneSkin. Ehlers-Danlos Syndrome, Arthrochalasis Type(専門医向け情報). [GeneSkin]
- [12] Zhang M, et al. A novel splice-altering frameshift variant in the COL1A1 gene: molecular characterization and literature review. PMC 2025. [PMC]









