目次
- 1 EXT2遺伝子の新たな二面性骨腫瘍の抑制から癌バイオマーカー・自己免疫性腎症への関与まで徹底解説
- 1.1 1. 生命の足場を作るEXT2遺伝子と「ヘパラン硫酸」
- 1.2 2. EXT1との緻密な連携プレー:9ナノメートルの奇跡
- 1.3 3. 遺伝性多発性外骨腫(HMO)の発症メカニズムと遺伝学
- 1.4 4. HMOの全身に及ぶ合併症と「悪性転化」の恐怖
- 1.5 5. 画像診断のフレームワークと外科治療の限界
- 1.6 6. 疾患修飾薬(新薬)開発:パロバロテンの挫折と次世代への希望
- 1.7 7. 隣接遺伝子欠失:ポトキ・シャッファー症候群との関連
- 1.8 8. 腫瘍学への応用:癌を促進する「EXT2のもう一つの顔」
- 1.9 9. 腎臓病学における新発見:EXT1/EXT2関連自己免疫性膜性腎症
- 1.10 よくある質問(FAQ)
- 1.11 関連記事
- 1.12 参考文献
EXT2遺伝子の新たな二面性
骨腫瘍の抑制から癌バイオマーカー・自己免疫性腎症への関与まで徹底解説
📍 クイックナビゲーション
「EXT2遺伝子」という名前を耳にしたとき、整形外科の領域に詳しい方や、ご自身あるいはご家族が骨の疾患と向き合っている方であれば、「遺伝性多発性外骨腫(HMO)」という、全身の骨に多数のコブ(良性腫瘍)ができる病気を思い浮かべることでしょう。歴史的に見ても、この遺伝子は長い間、その機能が失われることで腫瘍が発生する「古典的な腫瘍抑制遺伝子」として、主に骨の成長と形状を司るものだと考えられてきました。
しかし、近年の最先端の分子生物学や大規模なゲノム・トランスクリプトーム解析技術の飛躍的な進歩により、私たちのEXT2遺伝子に対する理解は根本から覆されようとしています。EXT2遺伝子は、単に骨の形を整えるだけの局所的なプレーヤーではありませんでした。実は、私たちの体を構成するあらゆる細胞の隙間を満たし、細胞同士の複雑な会話(シグナル伝達)を仕切る「生命のマスターコントローラー」とも呼べる極めて重要な役割を担っていたのです。
さらに驚くべきことに、骨においては腫瘍を「抑える」はずのこの遺伝子が、特定の悪性腫瘍(頭頸部がんや膠芽腫など)においては、全く逆に癌細胞の増殖や転移を「強力に促進する」バイオマーカーとして機能するという、恐ろしいほどの「二面性」を持っていることが明らかになりました。そればかりか、腎臓内科の領域においては、難病に指定されるような重篤な全身性自己免疫疾患(SLEやTAFRO症候群など)に合併する「膜性腎症」の標的抗原として同定され、免疫学の常識にも一石を投じています。
本記事では、このEXT2遺伝子が体内で果たしている驚くべき生化学的な基礎メカニズムから、患者さんの人生に多大な影響を与える遺伝性多発性外骨腫(HMO)の深い病態と最新治療の動向、そして腫瘍学や腎臓病学における最新のパラダイムシフトまで、一般の方にも直感的にわかりやすく、かつ専門的な深さを一切損なうことなく徹底的に網羅して解説していきます。
Q. EXT2遺伝子に変異があると、具体的にどのようなことが起こるのですか?
A. 最も代表的なのは「遺伝性多発性外骨腫(HMO)」という小児期から進行する骨の疾患の発症です。
全身の長管骨(腕や脚の骨)などに良性のコブ(腫瘍)が多数形成され、正常な骨の成長が物理的に阻害されることで、腕の著しい弯曲や脚の長さの違い、神経や血管の圧迫による激しい痛みが生じます。また、成人後にはこの良性腫瘍の一部が「悪性の軟骨肉腫(がん)」に転化するリスクも伴います。さらに近年では、この遺伝子が骨以外の病気(特定のがんの悪性度や、重篤な自己免疫性の腎機能障害)の進行度を測る重要なバイオマーカーとしても機能していることが判明し、世界中の医療界で大きな注目を集めています。
1. 生命の足場を作るEXT2遺伝子と「ヘパラン硫酸」
私たちの体は、約37兆個とも言われる膨大な数の細胞からできています。しかし、細胞たちはただ無秩序に集まっているわけではありません。細胞と細胞の間には「細胞外マトリックス」と呼ばれる、建物の鉄骨や足場のような空間が緻密に広がっており、そこで細胞同士が情報をやり取りして、整然と組織や臓器を作り上げています。
この「細胞の足場作り」において、極めて中心的な役割を果たすのがEXT2(Exostosin Glycosyltransferase 2)遺伝子です。ヒトのゲノムにおいて、EXT2遺伝子は11番染色体の短腕上、具体的には細胞遺伝学的バンド「11p11.2領域」にマッピングされています。NCBIの公式データベース(Gene ID: 2132)によれば、この遺伝子は「エキソストーシン-2」というタンパク質(糖転移酵素)の設計図を持っています。
📌 専門用語解説:ヘパラン硫酸(Heparan Sulfate: HS)
EXT2遺伝子が作り出す酵素によって合成される、長く連なった「糖の鎖(グリコサミノグリカン)」の一種です。細胞の表面にアンテナのように生えていたり、細胞の周りの空間を満たしていたりします。血管の形成(血管新生)や血液凝固の制御、細胞の分化や増殖、さらには癌細胞の転移(メタスタシス)の制御など、生体内における多岐にわたる生理的・病理的プロセスを根本から調節する「魔法の鎖」とも言える重要な物質です。
エキソストーシン-2タンパク質は、細胞の中にある「ゴルジ体」という膜構造の小器官に局在します。ゴルジ体はいわば、細胞内で作られたタンパク質に糖の飾り付け(修飾)を行って完成させ、目的の場所へと正確に出荷する「巨大な配送センター」のような場所です。EXT2はここで、ヘパラン硫酸という長大な糖の鎖を「延長する(chain elongation)」という、生合成プロセスの中核を担う非常に精巧な作業を行っています。現在までに、EXT2遺伝子には約220種類以上の突然変異が同定されており、これらの変異が広範な細胞機能の破綻を招くことが明らかになっています。
2. EXT1との緻密な連携プレー:9ナノメートルの奇跡
生化学的および最先端の構造生物学的な解析から、驚くべき事実が判明しています。それは、EXT2タンパク質は、自分一人(単独)では生理的に十分な糖転移酵素活性を発揮することができないという点です。単独の状態では、糖をくっつける力が極めて微弱なのです。
そこでEXT2は、同じゴルジ体の中にいるパラログ(進化的に関連した遺伝子)である「EXT1」という別の酵素と物理的に強固に結合し、安定な「ヘテロオリゴマー複合体(hetero-oligomeric complex)」という強力なタッグを形成します。酵母や哺乳類細胞を用いた遺伝子発現実験によれば、この2つを別々に作って後から混合しても複合体は形成されず、細胞内で「共発現(coexpression)」させた場合にのみ、飛躍的に増強された糖転移酵素活性を持つ複合体が生まれることが実証されています。生体内においては、このヘテロ複合体こそが真に生物学的に関連性のある形態(biologically relevant form)なのです。
解離的重合:シャトルバスのように行き交う糖の鎖
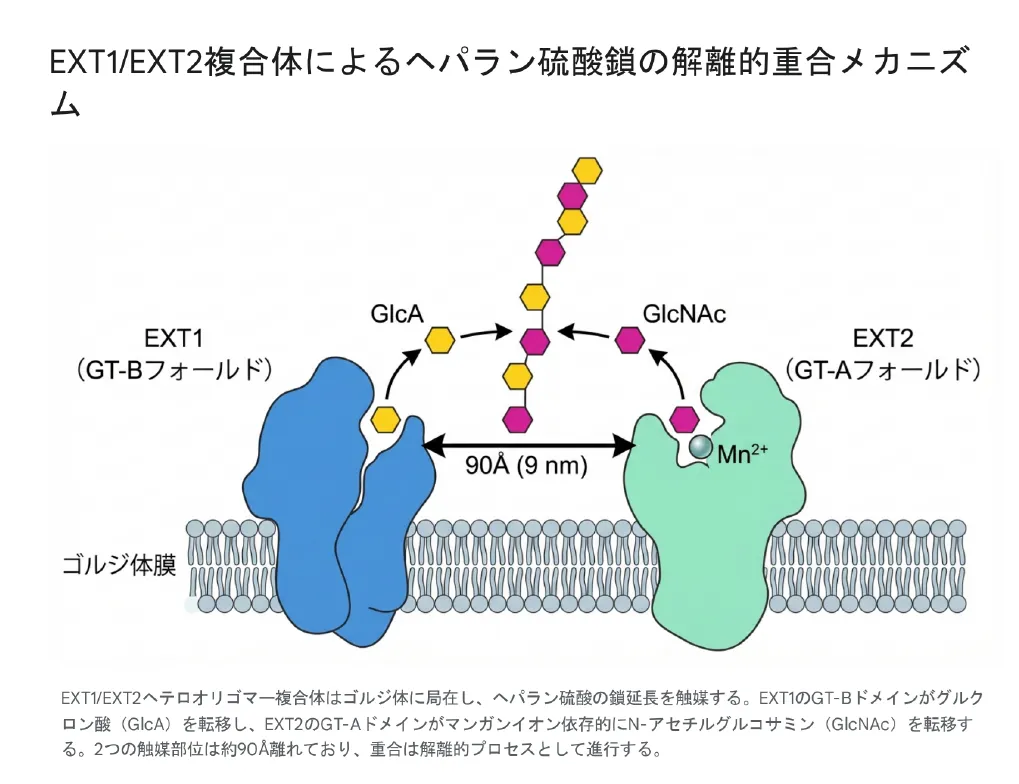
近年の画期的な分子構造解析により、このEXT1/EXT2複合体の詳細な触媒メカニズムが原子レベルで解明されました。
複合体内には全体で4つのドメインがありますが、ポリマー合成に直接寄与するのは主に2つの「作業台(触媒部位)」に限定されます。
- EXT1の作業台(GT47 GT-Bフォールド): N末端側に位置し、β1,4-グルクロン酸(GlcA)という糖分子を転移します。この反応は金属イオンに依存しません。
- EXT2の作業台(GT64 GT-Aフォールド): C末端側に位置し、α1,4-N-アセチルグルコサミン(GlcNAc)という糖分子を転移します。この反応にはマンガン(Mn²⁺)などの2価金属イオンの存在が絶対的に必要です。
さらに驚愕すべきは、これら2つの主要な触媒部位の空間的配置です。構造データによると、EXT1のGlcA転移部位とEXT2のGlcNAc転移部位は、複合体内において90オングストローム(9ナノメートル)以上という、ミクロの世界では「極端に大きな物理的距離」を隔てて存在しています。通常、工場でベルトコンベア作業をするなら、作業台は隣同士にあるべきです。しかし彼らは離れています。
ではどうやって鎖を長くしているのでしょうか?それは、糖鎖が酵素に結合したまま連続的に処理されるのではなく、一方の作業台で部品をもらったら、一旦離れてもう一方の作業台へと移動し、そこで別の部品をもらい、また戻る……という、シャトルバスのように2つの離れた作業台の間を往復しながら交互に部品を付加していくという方法です。これを専門用語で「解離的重合プロセス(dissociative process)」と呼びます。
また、体内にはNDST1などの他の修飾酵素群も存在し、EXT1/EXT2はこれらと物理的に相互作用して「GAGosome(グリコサミノグリカン合成酵素の超分子複合体)」を形成していると考えられており、EXT2は単なる触媒以上の構造的足場を提供していると推測されています。
3. 遺伝性多発性外骨腫(HMO)の発症メカニズムと遺伝学
もし、このEXT2遺伝子に変異が生じ、機能が失われる「機能喪失型(loss-of-function)」変異が起こるとどうなるでしょうか? 相棒であるEXT1は単独では十分な働きができないため、前述のEXT1/EXT2複合体形成が阻害され、細胞レベルでのヘパラン硫酸の生合成が著しく低下(ヘパラン硫酸欠乏状態)してしまいます。
この欠乏が引き起こす最も顕著な臨床的・病理学的帰結が、遺伝性多発性外骨腫(HMO:Hereditary Multiple Osteochondromas)です(別称としてMultiple Hereditary Exostoses: MHE などとも呼ばれます)。この疾患は世界中で50,000人から100,000人に1人の割合で発生する稀な先天性小児疾患であり、男女比は3:1で男性に多く見られます。
📌 専門用語解説:常染色体顕性(優性)遺伝
HMOは「常染色体顕性(優性)遺伝」の形式をとります。人間は両親から1つずつ、合計2つの同じ遺伝子のセットを受け継ぎますが、そのうち「片方」の遺伝子にヘテロ接合性の病的バリアント(変異)があるだけで発症するのが顕性遺伝です。HMOの症例の約90%は罹患した親からの遺伝であり、その場合、子どもへは50%の確率で遺伝します。残りの約10%は、生殖細胞系列における新規の突然変異(de novo変異)によって発症します。
遺伝学的な観点から見ると、HMO患者全体の約94%において、EXT1またはEXT2遺伝子のいずれかに変異が同定されています。具体的には、EXT1遺伝子の変異が全症例の約65%〜70%を占め、EXT2遺伝子の変異が約30%〜35%を占めます。歴史的にはEXT3という第3の遺伝子の関与も議論されましたが、現在の臨床診断においてはEXT1とEXT2が主要な責任遺伝子として扱われています。一般的に、EXT2変異に起因するHMOは、EXT1変異例と比較して病変数が少なく症状が相対的に軽度であることが多いとされています。
なぜ「ヘパラン硫酸」が減ると「骨腫瘍」ができるのか?
長年、「糖鎖が欠乏することが、なぜ異常な骨腫瘍の形成を導くのか」は大きな謎でした。近年の分子生物学がそのメカニズムを解明しました。キーワードは「シグナル伝達の暴走と強制的な再プログラミング」です。
通常、ヘパラン硫酸は細胞外マトリックスにおいて、骨形成タンパク質(BMP)や線維芽細胞増殖因子(FGF)、Wntシグナルといった形態形成シグナルの濃度勾配を緻密に調節し、細胞の正常な分化をガイドしています。しかし、EXT2変異によりヘパラン硫酸が欠乏すると、特にカノニカルBMPシグナルの異所性活性化(異常な暴走)が引き起こされます。
これにより、本来は骨形成を支持する裏方であるはずの「軟骨膜細胞(perichondrial cells)」が、自己増殖能を持つ腫瘍形成性の軟骨細胞へと強制的に再プログラミングされてしまいます。同時に、抗軟骨形成性として機能するはずの「FGF/ERK/MEK経路のシグナル伝達」が極端に低下することも、骨軟骨腫の発生を強力に後押ししていることが判明しています。
4. HMOの全身に及ぶ合併症と「悪性転化」の恐怖
HMOの臨床症状は多岐にわたり、生涯を通じて患者さんのQOLに不可逆的な影響を及ぼします。新生児期には無症状であることが一般的ですが、疾患の進行は早く、患者さんの50%は5歳までに、80%は10歳までに視認可能な腫瘍(多くの場合6つ以上、重症例では50個以上)を発症し、平均診断年齢は約3歳となっています。
深刻な骨格変形と圧迫障害の連鎖
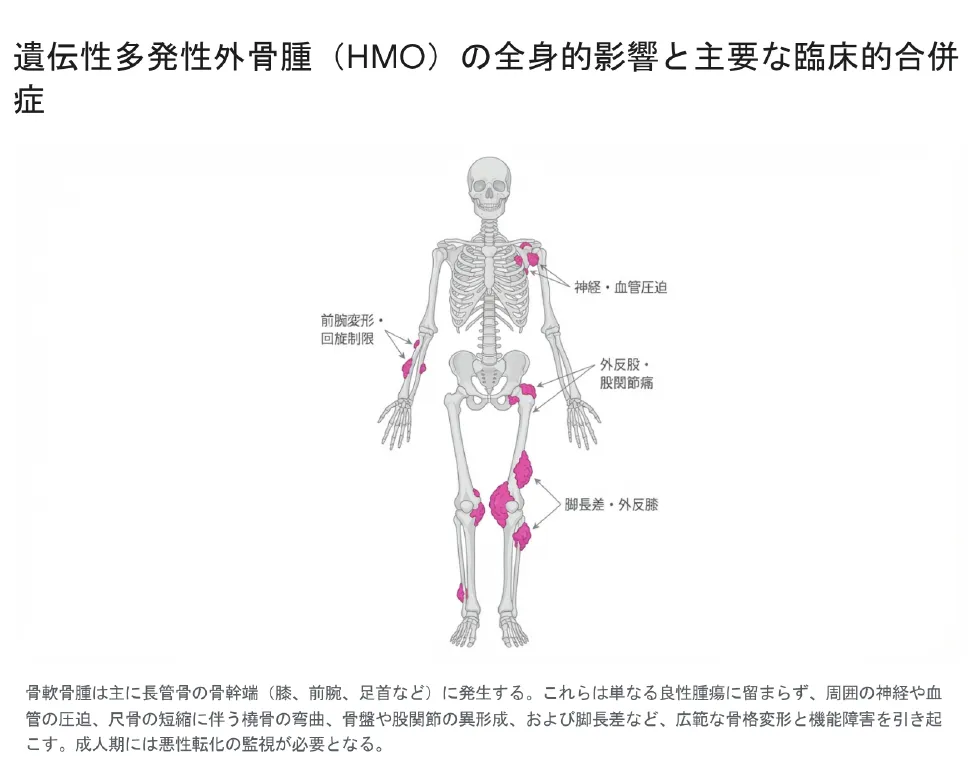
長管骨の骨幹端に発生した骨軟骨腫は「良性」ですが、その不規則な成長が成長板へ物理的に干渉し、広範な解剖学的障害(マスエフェクト)を引き起こします。
- 前腕の変形(約39%〜74%で発生): 尺骨が不釣り合いに短縮し、それに伴い橈骨が代償的に弯曲(radial bowing)して脱臼を引き起こします。これにより、ドアノブを回すような前腕の回旋機能が著しく制限されます。
- 下肢の変形と脚長差: 大腿骨や脛骨の短縮による脚長差(Limb length discrepancy)が患者の10%〜50%に見られ、しばしば2cm以上の深刻な差異が生じます。また、大腿骨頸部の角度異常である外反股(Coxa valga、最大25%)や、膝の外反変形(Genu valgus、8〜33%)、足首の外反変形(Ankle valgus、45〜73%)が歩行時の激痛を招き、早期の二次性変形性関節症の原因となります。
- 神経・血管への圧迫と滑液包炎: 末梢神経が圧迫されて知覚麻痺が生じたり、血管への圧迫や鋭利な骨片による摩擦が静脈血栓症や致死的な動脈破裂、偽動脈瘤の形成を引き起こすことがあります。また、筋肉との摩擦による滑液包炎や、翼状肩甲(scapular winging)も頻発します。
最大の脅威「悪性転化(二次性軟骨肉腫への変異)」
HMOにおいて最も警戒すべき致死的な合併症は、長年安定していた良性の骨軟骨腫が、悪性のがん細胞である「二次性軟骨肉腫(secondary chondrosarcoma)」へと悪性転化することです。単発の骨軟骨腫の悪性化リスクが約1%であるのに対し、HMO患者さんにおける生涯リスクは2%から最大10%に達すると推定されており、年齢とともにそのリスクは着実に増加します。
⚠️ 見逃してはならない悪性転化の臨床的サイン
腫瘍の成長は通常、骨格が成熟し成長板が閉鎖する時期と同期して停止します。したがって、骨格の成熟(成人)後に腫瘍が急激に増大し始めた場合や、安静時にそれまでになかった新たな痛みが生じた場合は、直ちに悪性化を疑い、迅速な画像診断と病理学的評価を行う必要があります。
5. 画像診断のフレームワークと外科治療の限界
HMOの診断は、主に臨床所見と放射線学的所見に基づいて確立されます。WHOの厳密な診断基準によれば、「長管骨の骨端線近傍領域に、画像上で確認できる2つ以上の骨軟骨腫が存在すること」が必須要件です。
X線撮影における極めて特徴的な所見は、腫瘍の皮質骨および髄腔が、母床となる元の骨と途切れることなく連続している「髄腔の連続性(medullary continuity)」です。非典型例や家族内リスク評価のためには、EXT1/EXT2遺伝子の変異解析が用いられます。
とりわけMRI検査は、悪性転化を疑う際に決定的な役割を果たします。腫瘍の先端を覆う「軟骨帽(cartilage cap)」の厚さを測定し、成人においてこれが1.5cm〜2cm以上に肥厚している場合、軟骨肉腫への悪性転化の強力な客観的指標となります。小児の被曝低減のための超音波検査や、全身モニタリングのための全身MRIの導入も進んでいます。
外科的介入の原則と医原性合併症の課題
現在までのところ、遺伝的異常を非侵襲的に修正する標準治療薬は存在せず、治療の主体は整形外科的な外科的切除です。痛みや機能障害、神経血管圧迫がある病変が絶対的な手術適応となります。
再発を防ぐための外科的原則として、腫瘍本体だけでなく、表面を覆う軟骨帽と周囲の軟骨膜をマージンを確保して完全に切除することが極めて重要です。また、進行する骨格変形に対しては、Masada-Jo分類に基づいた橈骨の骨切り術(osteotomy)や、Ahn分類に基づく下肢の骨端線成長停止術(epiphysiodesis)、外反股への内反骨切り術など、複雑な再建手術が必要となります。
手術に伴う医原性の合併症も深刻です。腫瘍切除部位に残存した鋭利な骨片が術後に大腿動脈を物理的に損傷し、術後出血や偽動脈瘤を形成した致死的事例も報告されており、術後の骨表面の入念な平滑化(スムージング)が不可欠です。
6. 疾患修飾薬(新薬)開発:パロバロテンの挫折と次世代への希望
外科手術はあくまで対症療法に過ぎず、生涯にわたり腫瘍が形成され続けるHMOの根本的な解決には至りません。そのため、遺伝的変異によるシグナル異常を標的とし、疾患の進行を根本から食い止める「疾患修飾薬(Disease-Modifying Drugs)」の開発が近年急速に進められてきました。
医療界最大の関心を集めたのが、レチノイドシグナル伝達経路を標的とする低分子化合物「パロバロテン(Palovarotene)」の第2相臨床試験(MO-Ped試験)でした。この薬は別の稀な骨疾患(進行性骨化性線維異形成症:FOP)で劇的な効果を示し、マウスのHMOモデルでも腫瘍形成を著しく抑制したため、2歳から14歳の小児患者193名を対象とした世界初の薬物治療の試みとして実施されました。
しかし2020年に完了した試験結果は、研究者と患者コミュニティの期待に反するものでした。全身MRIによる評価で、プラセボ群とパロバロテン投与群との間に、新たな腫瘍の発生率や体積変化において統計学的に有意な差が全く認められなかったのです。一方で全身性レチノイド特有の副作用が観察されたため、開発は実質的に中止されました。
シグナルの複雑さと次なる標的「BMP阻害薬」
この治験の失敗は、EXT2変異によるヘパラン硫酸欠乏がもたらす「BMP、FGF、Wntなどの同時多発的なシグナルの暴走」が、単一の経路修飾(レチノイド)では制御しきれないほど複雑であることを浮き彫りにしました。
現在、研究のパラダイムはより直接的かつ上流の制御へとシフトしています。特に有望視されているのが、過剰活性化したBMPシグナルを直接抑制する「カノニカルBMPシグナル阻害薬(LDN-193189など)」です。動物モデルの実験では、この阻害薬が腫瘍の体積を60%以上減少させる強力なデータを示しており、ヒトへの応用が急務とされています。さらに将来的な究極の根治治療として、CRISPR/Cas9を用いたゲノム編集技術による遺伝子修復も理論的なアプローチとして期待されています。
7. 隣接遺伝子欠失:ポトキ・シャッファー症候群との関連
EXT2遺伝子の喪失は、単一のHMOだけでなく、ゲノムのより広範な構造異常の一部としても発現します。その代表的かつ臨床的に極めて重要な例が11p11.2欠失症候群(Potocki-Shaffer症候群:ポトキ・シャッファー症候群)です。
📌 専門用語解説:ハプロ不全と隣接遺伝子欠失症候群
染色体上の特定の領域にある「複数の隣接する遺伝子群」がゴッソリと欠失することで引き起こされる疾患群です。一対ある遺伝子の片方が失われることで正常な機能維持に必要なタンパク質が不足する状態を「ハプロ不全」と呼びます。
Potocki-Shaffer症候群の複雑な臨床像は、欠失した領域(11p11.2)に含まれる複数の遺伝子不全がモザイク状に組み合わさった結果です。
- EXT2遺伝子の喪失: ハプロ不全により、HMOと同様の多発性外骨腫の直接的な原因となります。
- ALX4遺伝子の喪失: 頭蓋骨の発達不全により、異常な開口部が生じる「頭頂骨孔拡大(enlarged parietal foramina)」を引き起こします。
- PHF21A遺伝子の喪失: 特徴的な重度の知的障害、発達遅滞、および特異な顔貌異常(craniofacial abnormalities)の主要因となります。
これら3つの遺伝子の同時欠失が本症候群の「最小責任領域」を構成しており、マイクロアレイ解析等においてEXT2の欠失を確認することは、複雑な症候群を紐解くための決定的な診断マーカーとなります(なお、同じ11番染色体短腕上の11p13領域欠失によるWAGR症候群とは独立した疾患概念です)。
8. 腫瘍学への応用:癌を促進する「EXT2のもう一つの顔」
ここからが、現代の腫瘍学における最大のパラダイムシフトです。
歴史的に、EXT2は機能が失われることで良性腫瘍ができる「古典的な腫瘍抑制遺伝子」として認識されてきました。ところが近年、Cancer Genome Atlas(TCGA)などの大規模な癌ゲノム・トランスクリプトーム解析から、骨格系以外の多様な組織、とりわけ上皮系や神経系の特定の悪性腫瘍においては、EXT2が全く逆に「癌を促進する」新規バイオマーカーとして機能しているという驚くべき知見が次々と報告されています。
頭頸部扁平上皮癌(HNSCC)や膠芽腫における悪性化のドライバー
最も顕著な例が頭頸部扁平上皮癌(HNSCC)です。HNSCC患者の腫瘍組織において、EXT2は正常組織と比較して極めて有意に「過剰発現(アップレギュレート)」しています。細胞株を用いた実験でEXT2を人工的に抑制すると、癌細胞の異常な増殖、遊走(migration)、浸潤(invasion)が劇的に阻害され、細胞死(アポトーシス)が誘導されることが証明されました。このメカニズムの中心には、発癌性因子であるWNT2やWNT3を介したWntシグナル伝達経路との強力な相互作用が存在します。
📌 専門用語解説:エクソソームを介した免疫抑制
癌細胞は「エクソソーム」という細胞外小胞を通じて周囲の免疫細胞を無力化し、自分たちに有利な微小環境を作ります。最新のプロテオミクスと機械学習を用いた研究で、EXT2はHNSCCにおける免疫抑制的微小環境と生存予後不良を高精度に予測する「7つの高リスク遺伝子シグネチャー(ERGs)」のコアメンバーとして特定されています。
さらに、中枢神経系で最も悪性度の高い「膠芽腫(Glioblastoma)」においても、腫瘍が周囲の脳組織へ浸潤していく「腫瘍周辺脳ゾーン(PBZ)」において、EXT2がCDK4と並んで悪性化を推進する潜在的なドライバー遺伝子として機能していることが確認されています。
つまり、EXT2が合成するヘパラン硫酸は、骨組織では秩序を守るための通信網ですが、癌の微小環境においては癌の増殖と転移を助ける最悪のネットワークモジュレーターとして悪用されてしまうのです。高レベルのEXT2発現は患者の全生存率の低さと明確にリンクしており、独立した予後予測バイオマーカーとしての医療応用が強く期待されています。
💡 がん治療と遺伝子検査の選択肢
EXT2遺伝子のように、特定のがんの悪性度や進行に関わる遺伝子は多数存在します。ご自身のがんの性質(遺伝子変異の状況)を深く知り、より適した治療法や治験を探すための手段として、がんの遺伝子を網羅的に調べる「がんゲノムプロファイリング検査」なども重要な選択肢となります。
9. 腎臓病学における新発見:EXT1/EXT2関連自己免疫性膜性腎症
EXT2遺伝子とその産物が関与する病理学のフロンティアは、ついに腎臓病学(Nephrology)の領域にも到達しました。
腎臓の濾過フィルターである「糸球体」に免疫複合体が沈着し、大量のタンパク尿とネフローゼ症候群を引き起こす「膜性腎症」において、ごく最近になって「EXT1/EXT2を標的抗原とする新たなサブタイプ(EXT1/EXT2関連膜性腎症)」が提唱され、国際的な注目を集めています。
SLE(ループス)やTAFRO症候群との深い関わりと「保護的役割」
このサブタイプの最大の特徴は、原発性ではなく、全身性エリテマトーデス(SLE)や混合性結合組織病(MCTD)、さらには重篤な全身性炎症疾患であるTAFRO症候群(血小板減少、全身浮腫、発熱、細網線維化、腎障害、臓器腫大を伴う)といった、自己免疫疾患の背景を持って発症するケース(二次性膜性腎症)に極めて多く見られる点です。
腎生検においてSLE特有の「フルハウス免疫沈着」を示すループス様膜性腎症の患者において、糸球体にEXT1/EXT2に対する著明な染色性の増強が認められます。これは、本格的なSLE(ループス腎炎)を発症するための強力な予測バイオマーカーとなる可能性を示唆しています。
さらに逆説的なパラダイムとして、糸球体に沈着したEXT1/EXT2複合体が、過剰な炎症反応や補体の活性化をマスキングし、組織破壊から保護して治癒プロセス(healing process)を促進している可能性も推測されています。実際のコホート研究では、EXT1の陽性所見がループス腎炎患者における完全寛解(Complete Remission)を予測する強力かつ独立した良好な因子(ハザード比5.647)であることが報告されています。
総じて、EXT2遺伝子は「骨の成長を司る遺伝子」という狭い枠組みを完全に脱却しました。細胞微小環境のシグナルハブとして、癌の精密予後予測マーカーとして、そして難治性自己免疫疾患の診断ツールとして、その多面的な生物学的意義は今後の医療の未来を切り拓く極めて重要な鍵となるでしょう。
よくある質問(FAQ)
🏥 遺伝子に関する不安を、ひとりで抱えないために
遺伝性疾患の診断や、ご自身の遺伝子変異に関する疑問と向き合うのは非常に勇気がいることです。
私たちは最新の医学的知見に基づいた正確な診断と、患者様・ご家族の心の安全を最優先に、次の一手を共に考えます。
関連記事
参考文献
- NCBI: EXT2 exostosin glycosyltransferase 2 [Homo sapiens (human)] – Gene [NCBI Gene]
- The EXT1/EXT2 tumor suppressors: catalytic activities and role in heparan sulfate biosynthesis [PubMed Central]
- Hereditary Multiple Osteochondromas – GeneReviews® [NCBI Bookshelf]
- EXT2: a novel prognostic and predictive biomarker for head and neck squamous cell carcinoma [PubMed]
- Primary Membranous Nephropathy With Enhanced Staining of Exostosin 1/Exostosin 2 in the Glomeruli [PubMed]
- A Diagnostic and Therapeutic Dilemma Concerning Exostosin 1/Exostosin 2-associated Lupus-like Membranous Nephropathy [PubMed Central]