目次
- 1 EXT1遺伝子とは?遺伝性多発性外骨腫(HMO)のメカニズムと最新治療を徹底解説
EXT1遺伝子とは?
遺伝性多発性外骨腫(HMO)のメカニズムと最新治療を徹底解説
📍 クイックナビゲーション
EXT1遺伝子は、骨格形成や細胞のシグナル伝達に不可欠な役割を果たすマスター遺伝子です。この遺伝子の変異は、全身の骨に腫瘍が多発する「遺伝性多発性外骨腫(HMO/HME)」の最も主要な原因となります。本記事では、発症の分子メカニズムから、長年外科手術に頼ってきた治療の歴史を根本から変える可能性を秘めた新薬候補(パロバロテン)まで、2025年時点の最新情報を網羅的に解説します。
Q. EXT1遺伝子に変異があると、必ず子どもに遺伝しますか?
A. 50%の確率で遺伝します。
遺伝性多発性外骨腫(HMO)は「常染色体顕性(優性)遺伝」という形式をとるため、男女の性別に関わらず、親から子へ1/2の確率で病的バリアントが受け継がれます。ただし、患者の約10%は親に異常がない「突然変異(de novo変異)」によって発症します。
- ➤結論: EXT1は多発性外骨腫(HMO)の最も主要かつ重症化しやすい原因遺伝子です。
- ➤分子メカニズム: 糖鎖(ヘパラン硫酸)の生合成が低下し、細胞のシグナル伝達が狂うことで発生します。
- ➤LOH仮説: 腫瘍が局所的に発生する真の理由(後天的なツーヒットモデル)が近年証明されました。
- ➤治療の最前線: ついに外科手術から、内科的治療薬(パロバロテン)へパラダイムシフトが起きています。
- ➤遺伝子検査: 確定診断や将来の家族計画において、NGSパネル検査が極めて重要な役割を果たします。
1. 【結論】EXT1遺伝子と遺伝性多発性外骨腫(HMO)の関係
ヒトの第8染色体の長腕(8q24.1)に位置するEXT1遺伝子(Exostosin Glycosyltransferase 1)は、細胞表面や細胞外マトリックスに存在する「ヘパラン硫酸」という糖鎖を合成するための重要な酵素(糖転移酵素)の設計図です。
この遺伝子の機能が失われると、骨端線(成長板)での局所的なシグナル伝達が破綻し、良性の軟骨性腫瘍が多発する遺伝性多発性外骨腫(HMO:Hereditary Multiple Osteochondromas) [cite: 4] を引き起こします。
【重要ポイント】HMO患者の約90%において、EXT1またはEXT2遺伝子のいずれかに病的バリアントが同定されます。特にEXT1遺伝子変異は全体の約65〜78%を占め [cite: 1]、EXT2変異と比較して骨格変形や低身長などの臨床的表現型が重症化しやすい傾向があります。
📝 補足:遺伝の形式は「常染色体顕性遺伝」です(かつては「常染色体優性遺伝」と呼ばれていました)。対義語である劣性遺伝は「常染色体潜性遺伝」と呼称が変更されています。HMOは、約50,000人から100,000人に1人の割合で発症する稀少な遺伝性骨格疾患です。
2. ヘパラン硫酸生合成の分子基盤と「GAGosome」
EXT1がなぜ骨格形成にそれほど重要なのでしょうか。その答えは、細胞のアンテナ役である「ヘパラン硫酸」の合成メカニズムにあります。
🧬 専門用語解説:ヘパラン硫酸 (Heparan Sulfate) とは?
細胞表面や細胞外マトリックスに豊富に存在するグリコサミノグリカンの一種です。単なる構造的な足場ではなく、多様な成長因子やモルフォゲンの共受容体(コ・レセプター)として機能し、細胞のシグナル伝達を精密に制御する生体分子です。
EXT1とEXT2の強固なパートナーシップ
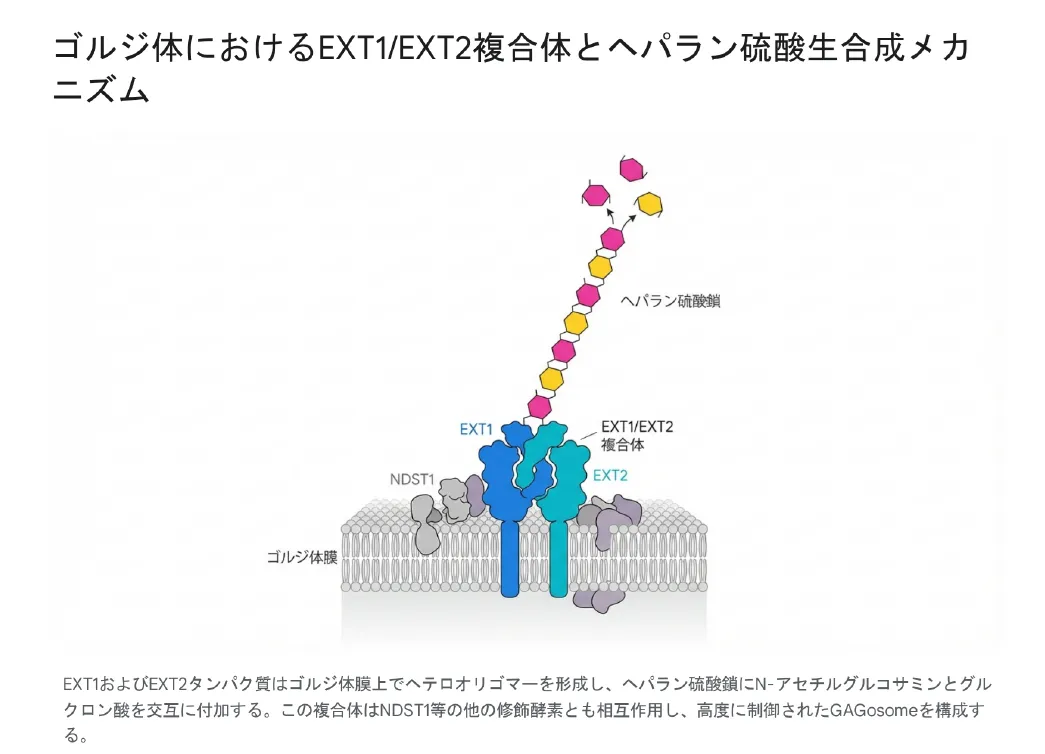
細胞内のゴルジ体において、EXT1タンパク質は単独で働くのではなく、EXT2タンパク質と強固なヘテロオリゴマー複合体を形成します。この複合体は、NDST1等の他の修飾酵素とも物理的に近接して相互作用し、「GAGosome(ガグオソーム)」と呼ばれる巨大な多酵素超複合体を形成します [cite: 2]。
細胞シグナル(Hedgehog, FGF, BMP)の深刻な破綻
EXT1の変異により、図に示されたようなヘパラン硫酸の合成プロセスが阻害されると、成長板における主要なシグナル伝達経路が大混乱に陥ります。
- Indian Hedgehog (Ihh) シグナル: ヘパラン硫酸が枯渇するとIhhタンパク質の細胞間拡散が阻害され、適切な分化のブレーキが効かなくなり、軟骨細胞が過剰増殖して腫瘍の芽となります。
- FGFシグナル: FGFと受容体(FGFR)の相互作用もヘパラン硫酸によって媒介されるため、合成阻害によりFGFシグナルが低下し、軟骨細胞の正常な分化プロセスに重大な欠陥をもたらします。
- BMP / Wntシグナル: BMPシグナルがFGFに過剰に拮抗して軟骨形成を異常促進するなど、発生に関わるネットワーク全体のバランスが崩壊します。
3. なぜ腫瘍が多発するのか?「LOH仮説」へのパラダイムシフト
HMO患者は、全身の細胞にEXT1遺伝子のヘテロ接合性変異(一方のアレルのみ変異)を持っています。しかし、腫瘍は全身の至る所にできるわけではなく、長管骨の骨幹端などの特定の部位にのみ局所的に形成されます。この長年の謎が、2024年〜2025年の最新研究でついに解明されました。
🔬 専門用語解説:LOH(ヘテロ接合性の消失)
Loss of Heterozygosityの略。もともと一方の遺伝子(アレル)に変異を持つ人が、後天的な体細胞変異によってもう一方の正常な遺伝子も失う「セカンドヒット」現象です。古典的ながん抑制遺伝子モデルである「ツーヒット仮説」に基づいています。
かつては、正常なアレルが1つだけでは必要なヘパラン硫酸を作れないとする「ハプロ不全モデル」が議論されてきました。しかし、最新の動物実験やヒト患者からの組織解析により、ヘパラン硫酸を合成できる正常な細胞と、合成できない細胞(EXT機能を完全に喪失した細胞)がモザイク状に混在していることが確認されました [cite: 4]。
詳細な解析では、分析された骨軟骨腫の実に63%において腫瘍細胞内に「セカンドヒット」が検出されており、骨軟骨腫は「LOH(ツーヒット)」を起点とするクローン性の細胞増殖疾患であることが結論づけられています [cite: 4]。
4. 悪性化(軟骨肉腫)と全身への合併症リスク
良性の骨軟骨腫であっても、多発し、かつ物理的に突出することで多岐にわたる合併症を引き起こします [cite: 6]。
- 骨格の変形と成長障害: 前腕や下腿の骨の正常な伸長を妨げ、肢の長短の不一致(脚長差)や湾曲変形をもたらします。患者の半数以上が身長50パーセンタイルを下回る低身長を示すとの報告もあります。
- 運動機能の喪失と疼痛: 関節近傍の腫瘍が可動域を制限し、慢性的な短期的・長期的疼痛症候群や滑液包炎を引き起こします。
- 神経・血管の圧迫と損傷: 末梢神経を圧迫してしびれや運動麻痺を引き起こすほか、鋭利な骨表面が隣接する血管(特に膝窩動脈や大腿動脈)を継続的に摩擦し、致死的な仮性動脈瘤などの重篤な血管合併症を引き起こす事例も報告されています。
最大の脅威:二次性末梢性軟骨肉腫への悪性転化
HMOにおける最大の医学的脅威は、既存の良性腫瘍が成人期(主に成長が完了した後)に悪性の「二次性末梢性軟骨肉腫」へと転化(がん化)することです。
孤立性の外骨腫では悪性転化リスクが約1%であるのに対し、HMO患者全体では0.5%〜5%(一部の研究では最大10%)と有意に高くなります。特にEXT1変異キャリアでの発症例が多く報告されており、ここでもEXT1変異の重症化リスクが示唆されています。
悪性化には、単純なLOHだけでなく、IDH1/2変異やTP53(代表的ながん抑制遺伝子)の不活化といった、他の肉腫と共通する発がん経路の破綻が追加で必要となります。
⚠️ 注意(早期発見のサイン):成人後、既存の腫瘍部位に「新たな持続する疼痛」が生じたり、MRI等の画像検査で腫瘍を覆う「軟骨キャップの持続的な成長・肥厚(通常2cm以上)」が確認された場合は、悪性転化を強く疑い、速やかな外科的切除を検討する必要があります。
5. 骨格を超えた機能:血液がん・糖尿病との新たな関連
近年の研究により、EXT1遺伝子の役割は単なる「骨の形を整える遺伝子」にとどまらず、臓器の形態形成(肺の分岐形成など)や、腫瘍学、血管内分泌代謝学へと急速に拡大しています。
小児期における血液がん発症との議論
2024年〜2025年に発表された文献レビューにおいて、HMO患者に併発した非骨格系悪性腫瘍のうち、実に18歳未満の小児の67%が急性骨髄性白血病や急性リンパ芽球性白血病などの血液悪性腫瘍であったという報告が大きな学術的関心を集めました。
しかし研究者らは、このデータから直ちに因果関係を結論づけることには強く警鐘を鳴らしています。これは「稀な遺伝性骨疾患を持つ小児が白血病を発症する」という特異な事象が、一般のがん併発例よりも医学論文になりやすい「報告バイアス(Reporting Bias)」の可能性が高いためです。現時点では明確な生物学的素因とは未確定ですが、臨床医はHMOの小児患者が原因不明の全身症状を呈した場合、血液疾患も鑑別診断に含めるべきと提言されています。
糖尿病性微小血管合併症への画期的な治療応用
ヘパラン硫酸は、血管内皮細胞の管腔表面にある「内皮グリコカリックス」というバリア機能の最も主要な構成要素です。
2025年に発表された最先端の研究では、高血糖等によって破壊されるこのグリコカリックスを保護するため、ヘパラン硫酸を分解する酵素(ヘパラナーゼ)の作用を阻害する新規化合物「OVZ/HS-1638」が2型糖尿病マウスモデルに投与されました。結果として、この治療はグリコカリックスの構造を保護し、糖尿病性網膜症や腎症に関連する有害な微小血管透過性の異常を見事に予防しました。
この画期的な研究は、EXT1が関与するヘパラン硫酸ネットワークを薬理学的に安定化させることが、複数の臓器にまたがる糖尿病合併症を同時に防ぐ新たな全身的治療(Systemic therapeutic approach)となる可能性を強力に提示しています。
6. 染色体レベルの欠失:8q23q24欠失症候群(ランガー・ギデオン症候群)
EXT1遺伝子の異常は、単一の点突然変異(シーケンス異常)だけでなく、染色体の広範な「微小欠失(Microdeletion)」の一部として発生することもあります。
🧬 隣接遺伝子欠失症候群とは
染色体の8q23.2-q24.1領域が欠失することによって引き起こされる「8q23q24欠失症候群(ランガー・ギデオン症候群:LGS)」がその代表例です。
微小欠失は単一の遺伝子だけでなく、隣接する複数の遺伝子を同時に失うため、複合的な病態を形成します。LGSの原因となる欠失領域には、EXT1遺伝子に加えて、TRPS1遺伝子およびRAD21遺伝子などが含まれています。
臨床現場において、小児が多発性骨軟骨腫の症状(EXT1欠失由来)に加えて、以下のような非典型的な所見を伴う場合は、単なるEXT1の点突然変異ではなく、LGSなどの広範な染色体異常を疑う必要があります。
- 特異な顔貌・外胚葉異常(TRPS1欠失由来): 洋ナシ型の球根状の鼻、長い人中、薄い上唇、大きく突出した耳、細くまばらな頭髪、異栄養性の爪など。
- その他: 軽度から中等度の知的発達障害(精神遅滞)、骨密度低下に伴う頻繁な骨折など。
7. 遺伝子検査(NGSパネル)と遺伝カウンセリング
HMOの確定診断と正確なリスク評価には、臨床的・放射線学的な骨格評価(WHO基準:長管骨に2つ以上の骨軟骨腫)に加えて、分子遺伝学的検査によってEXT1またはEXT2遺伝子の病的バリアントを同定することが確立されています [cite: 3]。
📝 用語解説:トランケーション変異
遺伝子の塩基配列の変化により、途中で「翻訳終了(ストップ)」のサインが出てしまい、本来よりも短い、機能を持たない異常なタンパク質が作られてしまう変異の総称です。
📝 用語解説:ナンセンス変異とフレームシフト変異
ナンセンス変異:塩基が1つ置き換わることで終止コドン(ストップサイン)ができる変異です。
フレームシフト変異:塩基の挿入や欠失により、暗号の読み枠(フレーム)がズレてしまい、全く異なるアミノ酸が繋がった後に途中でストップしてしまう変異です。
【重要ポイント】EXT1およびEXT2変異の約80%〜90%は、上記のような「トランケーション変異(ナンセンス変異、フレームシフト変異等)」であり、機能を完全に喪失させます。
最適な遺伝子診断は以下の段階的かつコスト効率の高いアプローチで実施されます。
- 1. 単一遺伝子シーケンシング: EXT1変異が多数を占めるため第一選択となります。コーディング領域全体をスキャンし、病的バリアントの約88%〜93%が特定されます。
- 2. 欠失/重複解析(MLPA等): シーケンスで異常がない場合、単一エクソンから遺伝子全体に及ぶ大規模な欠失や重複(約7%〜12%を占める)を調べます。
- 3. 包括的ゲノム解析(NGSパネル等): 複数の関連遺伝子を同時に解析するパネル検査や、非典型的な症状(前述のランガー・ギデオン症候群など)を伴う場合は、全エクソーム解析やマイクロアレイ染色体検査が適用されます。
🔍 当院の検査詳細:
HMO NGS遺伝子検査パネル|次世代シーケンサーによる網羅的解析
8. 待望の新薬候補「パロバロテン」がもたらす希望
HMOに対する伝統的な医療アプローチは、長年にわたり完全に「外科的」かつ「対症療法的」なものに限定されてきました。骨の変形に対しては、骨延長術や骨切り術など、患者様にとって肉体的・精神的負担の大きい手術が幾度となく繰り返されるのが常でした。
しかし、ヘパラン硫酸生合成の欠如が引き起こすシグナル伝達の異常(FGF低下やBMP亢進)に関する分子メカニズムの解明により、HMOの治療は劇的なパラダイムシフトを迎えつつあります。
そのブレイクスルーの中心にあるのが、「パロバロテン(Palovarotene)」という化合物です。パロバロテンは、細胞の核内受容体である「レチノイン酸受容体ガンマ(RARγ)」に対する選択的アゴニスト(作動薬)であり、前軟骨間葉系幹細胞の細胞運命決定を強制的に書き換え、骨・軟骨形成系統から非骨系系統へとシフトさせることで、過剰な軟骨生成(腫瘍の発生)を元から断ちます。
💡 パロバロテンの臨床効果と乗り越えるべき課題
- ➤前臨床試験の驚異的結果: SBP医学研究所などのマウスモデル実験において、異常なBMPシグナル伝達が減衰し、骨軟骨腫の発生数が用量依存的に最大91%減少することが完全立証されました [cite: 5]。
- ➤臨床試験(MO-Ped Trial): 世界初の小児HMO患者を対象としたパロバロテンの第2相無作為化二重盲検臨床試験が実施され、骨軟骨腫の進行予防、骨格の成長、QOL、疼痛への有効性が総合評価されています。
- ➤副作用(骨格毒性): 軟骨形成を強力に抑制する薬理作用は諸刃の剣であり、年少者で「正常な成長板の早期閉鎖(骨格成長の阻害)」という重大なリスクが浮き彫りになっています。現在、この副作用を回避しつつ腫瘍を抑える「投与の最適なタイミング(治療ウィンドウ)」の探索が全世界で注視されています。
よくある質問(FAQ)
🏥 遺伝に関するご不安は、専門医へご相談ください
ご自身やご家族の診断、遺伝子検査、これからの治療方針について。
ミネルバクリニックでは臨床遺伝専門医が最新の知見とエビデンスに基づき、しっかりと伴走いたします。
関連記事
参考文献
- [1] Genotype and phenotype correlation analysis in 27 families with multiple osteochondroma [PMC]
- [2] Heparan sulfate biosynthesis enzymes EXT1 and EXT2 affect NDST1 expression [PNAS]
- [3] Hereditary Multiple Osteochondromas – GeneReviews® [NCBI Bookshelf]
- [4] No Haploinsufficiency but Loss of Heterozygosity for EXT in Multiple Osteochondromas [ResearchGate]
- [5] Palovarotene Inhibits Osteochondroma Formation in a Mouse Model of Multiple Hereditary Exostoses [PubMed]
- [6] Hereditary multiple exostoses: an educational review [PMC]