目次
この記事では、ミスマッチリペア(MMR)の基本概念、その遺伝的重要性、および癌などの疾患との関連性について詳しく解説します。DNA修復プロセスの詳細なメカニズムから、MMR欠損による疾患のリスク、最新の治療戦略まで、幅広くカバーしています。
ミスマッチリペアとは何か
ミスマッチリペア(MMR)は、DNAの複製中に偶発的に生じる塩基の誤配(ミスマッチ)を修正する細胞の修復メカニズムです。このプロセスは、遺伝情報の正確な伝達を保証し、遺伝的安定性を維持するために不可欠です。DNAミスマッチリペア(DNA mismatch repair; dMMR)は、DNAが複製される際や遺伝情報が組み替えられる際に生じる塩基の挿入ミスや欠損を修復するシステムです。この修復は特定のDNA鎖に対して行われ、一部のDNA損傷も修復します。
このシステムは、バクテリアから人間に至るまで多くの生物で見られるDNA修復の経路の一つで、主にDNA複製時にDNAポリメラーゼが犯すエラーを修正します。このエラーには、塩基の挿入や欠損が含まれます。
MMR遺伝子に変異が生じると、ミスマッチ修復機能が失われ、結果として多数の突然変異がゲノムに蓄積されます。これにより、マイクロサテライト不安定性(MSI)と呼ばれる現象が引き起こされます。例えば、胃がんの約15%から30%の症例でMSIが観察されます。
● ミスマッチリペアの基本概念
1. 検出と修復の開始:
– ミスマッチリペアは、DNAが複製された後に生じる塩基対の誤りを検出します。複製中にDNAポリメラーゼが誤ったヌクレオチドを組み込むことがあります。このようなミスは、DNAの二重らせんの形状に異常を引き起こし、修復機構のトリガーとなります。
2. 修復プロセス:
– 特定のタンパク質複合体がミスマッチを認識し、その周辺のDNAを切断します。続いて、エキソヌクレアーゼが誤ったヌクレオチドを含む一部のDNA鎖を除去し、DNAポリメラーゼが新しい正しいヌクレオチドで穴を埋め、最後にDNAリガーゼが繋ぎ合わせます。
3. 重要性:
– ミスマッチリペアシステムが機能しない場合、DNAの誤りが蓄積され、突然変異率が高まります。これは、がんを含む多くの遺伝性疾患のリスクを増加させる原因となります。例えば、ミスマッチリペアの不具合は、リンチ症候群と呼ばれる遺伝性非ポリポーシス性大腸癌の一因となります。
ミスマッチリペアは、生物の生存と遺伝的健康を守るための基本的な防御機構の一つであり、細胞が遺伝的な誤りから自身を保護するための重要な手段です。この修復メカニズムの研究は、がんやその他の遺伝病の理解と治療に貢献しています。
ミスマッチリペアの基本メカニズム
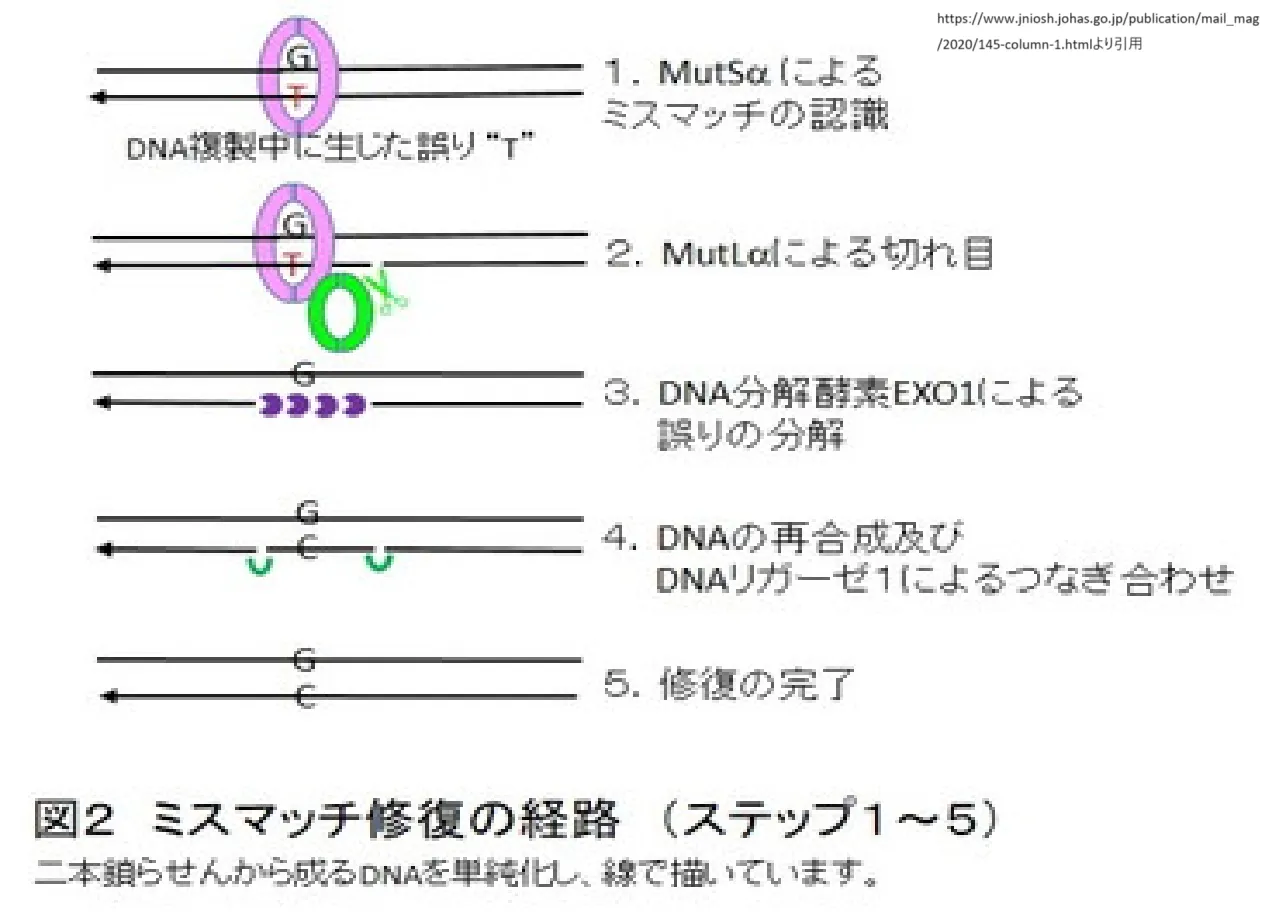
ミスマッチ修復(Mismatch Repair、MMR)の基本メカニズムは以下のステップで構成されています。
1. 誤りの識別: DNA複製中に生じたミスマッチ(誤った塩基対合)を、MMRタンパク質複合体が検出します[1][3][7].
2. 新生鎖の識別: 新生鎖とテンプレート鎖を区別します。原核生物ではDNAのメチル化パターンを利用し、真核生物ではまだ完全には解明されていない他のメカニズムが存在すると考えられています[7].
3. 切断と除去: 誤った塩基を含むDNA領域が識別されると、MMR機構は新生鎖に切れ目を入れ、ミスマッチ塩基を含む領域を除去します[1][7].
4. DNAの再合成と連結: 除去された領域は、残された一本鎖のDNAを鋳型として、DNAポリメラーゼによって再合成されます。最後に、DNAリガーゼが新たに合成されたDNA鎖のギャップを埋め、連結します[1][7].
MMRシステムの主要な成分と機能
MMR(ミスマッチ修復)システムは、DNA複製中に生じた塩基対の誤りや小さな塩基の挿入・欠失(1~4塩基対)を修復する役割を担っています。このシステムは少なくとも以下の7つのタンパク質から構成されています。
1. h-MLH1
2. h-MLH3
3. h-MSH2
4. h-MSH3
5. h-MSH6
6. h-PMS1
7. h-PMS2
これらのタンパク質は、特定のパートナーと結合して機能的なヘテロダイマーを形成します。中でも、h-MLH1とh-MSH2はMMRシステムの中心的な役割を果たし、5つの主要なヘテロダイマー複合体を形成します。
● MutS複合体
1. h-MSH2/h-MSH3(hMutSβ) – ミスマッチや小さな挿入・欠失を認識します。
2. h-MSH2/h-MSH6(hMutSα) – ミスマッチや小さな挿入・欠失を認識する主要な複合体です。
● MutL複合体
3. h-MLH1/h-PMS2(hMutLα) – 修復プロセスの中心的な複合体です。
4. h-MLH1/h-PMS1(hMutLβ)
5. h-MLH1/h-MLH3(hMutLγ)
これらの複合体は、ミスマッチを正確に認識し、修復することで、DNAの安定性を保ち、突然変異の蓄積を防ぐ重要な役割を果たします。
1.DNAミスマッチ修復の開始
DNAミスマッチ修復(MMR)過程は、hMutS複合体がDNAに集まることから始まります。このプロセスで形成されるMutSヘテロ二量体の種類は、修正が必要なDNAの変化の種類によって決まります。
1. h-MSH2/h-MSH6ヘテロ二量体 – この複合体は、塩基のミスペアだけでなく、小さな挿入や欠失ループも修正します。これは一般的なミスマッチや簡単な挿入・欠失に対応するため、より一般的に活動する主要なヘテロ二量体です。
2. h-MSH2/h-MSH3ヘテロ二量体 – この複合体は主に、より大きな挿入や欠失ループを修復します。このヘテロ二量体は特定の大きなループ構造に特化しており、h-MSH2/h-MSH6よりも特定のケースに適応しています。
これらの複合体が適切に機能することにより、DNAのコピー時に生じたエラーが修正され、細胞の遺伝情報の正確性が保たれます。これにより、がんなどの疾患のリスクが減少します。
2.MutLヘテロ二量体のリクルートとミスマッチ部位の切断
MutS複合体によるDNAミスマッチ修復(MMR)の開始の後、MutLヘテロ二量体がリクルートされる過程が重要です。このステップでは、MutLタンパクが活動を開始し、DNA修復のための様々な要素との接続を担います。
● MutLタンパクの役割
MutLタンパクは、DNAミスマッチを認識した後の重要なリンクとして機能します。これには以下のような要素が含まれます:
– 増殖細胞核抗原(PCNA):DNA複製と修復に不可欠です。
– DNAポリメラーゼδおよびε:新しいDNA鎖の合成を助けます。
– 一本鎖DNA結合タンパク質:修復中のDNA鎖を安定させます。
– DNAヘリカーゼ:二重鎖を解くことで修復過程を容易にします。
特に、h-MLH1/PMS2(MutLα)ヘテロ二量体は、がんの原因となる主要なMMR関連タンパクとして知られています。MutLαはエンドヌクレアーゼ活性を持ち、この活性はC末端ドメインの特定のモチーフに依存しています。このモチーフは「DQHA(X)2E(X)4E」という配列で、DNAミスマッチ修復で重要な役割を果たします。
他のhMutL複合体、例えばh-MLH1/h-MLH3(MutLγ)は、塩基のミスマッチや小さな挿入・欠失ループの修復に関与していますが、その生体内での機能性についてはまだ十分には解明されていません。
これらの複合体の活動により、DNAの整合性が保たれ、遺伝子の突然変異が防がれることで、がんを含む様々な病状のリスクが低減されます。
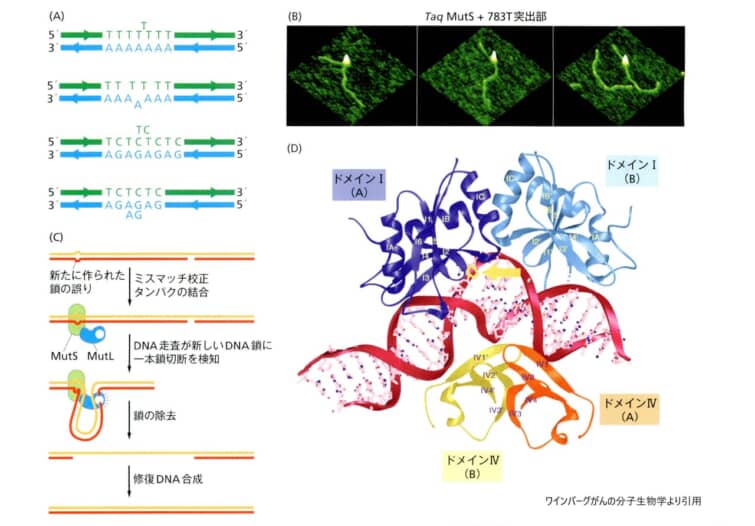
説明している図は、DNAミスマッチ修復(MMR)システムの様々な段階を描いています。以下、各段階を簡潔に解説します:
● (A) DNAポリメラーゼの動作
– ポリメラーゼδの役割:DNA複製中、特にpol-δは微小衛星配列などのDNA反復配列で時々「どもる」(stutter)ことがあり、この結果として、新規に合成された鎖(緑色で示されている)は、反復配列の数を誤って1つ多く取り込むか、または1つ欠損することがある。この現象は、より複雑な反復配列でも同様に起こる。
● (B) ミスマッチ修復の初期段階
– MutSの役割:細菌Thamus aquaticsのMutSが、特定のヌクレオチド部位でのミスマッチを含むDNA断片に結合している様子が可視化されています。MutSはミスマッチ領域を探索し、見つけるとDNAの二重らせんを折り曲げて安定に結合します。
● (C) MMRシステムの協調作業
– MutSとMutLの協力:真核細胞では、MutSがミスマッチDNAを探索し(緑色で示されている)、その後MutLがDNAの一本鎖切断(nick)を探し、最近合成された鎖(赤色で示されている)を特定します。この鎖はメチル化が少ないため、識別に役立ちます。その後、MutLは検出されたミスマッチ部を含むDNAを分解し、修復合成を促進します。
● (D) MutSの構造的詳細
– X線結晶解析:好熱菌Thamus aquaticsのMMRタンパクMutSの機能がX線結晶解析により詳細に示されています。この解析では、MutSのホモダイマーがミスマッチを含むDNAらせん(赤色で示されている)との複合体を形成しており、各サブユニットのドメインが色分けされています。特定の残基がミスマッチした塩基とどのように相互作用しているかが示されています。
この説明は、MMRシステムがDNAのコピーエラーをどのように検出し、修正するかを示すものであり、このプロセスの異常がリンチ症候群のような遺伝性非ポリポーシス大腸がん(HNPCC)を引き起こす原因となることを示しています。
ミスマッチリペアとマイクロサテライト不安定性
DNAミスマッチ修復(MMR)システムの不全は、マイクロサテライト不安定性(MSI)という現象を引き起こします。ここでは、MMRとMSIの関連について詳しく説明します。
● DNAミスマッチ修復(MMR)
MMRは、DNA複製中に発生する塩基のミスペアや小さな挿入・欠損を修復するための主要なメカニズムです。このプロセスは、遺伝情報の正確性を保持し、突然変異の蓄積を防ぐ役割を果たします。MMRシステムが機能しない場合、これらの小さなエラーが修復されず、細胞の遺伝子に永続的な変更が残ることになります。
● マイクロサテライト不安定性(MSI)
マイクロサテライトは、繰り返し配列を含むDNAの領域で、特に複製時のエラーが生じやすい場所です。MSIは、これらのマイクロサテライト領域における繰り返し配列の長さが、細胞内で不均一になる現象を指します。MMRシステムの不全は、これらの繰り返し配列のエラーを修復できないため、MSIを引き起こします。
● MMRとMSIの関連性
– がんの発生:MSIは特に色々な種類のがん、特にリンチ症候群に関連する大腸がんなどでよく見られます。MSI高頻度(MSI-H)のがんは、MMR遺伝子の機能不全によって特徴づけられます。
– 診断と治療:MSIの存在はがん診断における重要なマーカーとなります。また、MSIの状態は、特定の化学療法や免疫療法に対するがんの感受性に影響を与えることが示されています。例えば、MMR欠損があるがんは、免疫チェックポイント阻害剤による治療により良い反応を示すことがあります。
● まとめ
MMRの欠陥は、DNAの複製エラーを修復できず、これが蓄積されるとMSIを引き起こし、結果としてがんなどの疾患のリスクが増大します。これらの理解は、がんの診断や治療戦略の向上に寄与しています。
ミスマッチリペアの生物学的重要性
遺伝的安定性の維持
ミスマッチリペア(MMR)システムは、DNA複製中に生じる塩基のミスマッチや小さな挿入・欠失を修復することで、遺伝的安定性を維持します。このシステムが機能することにより、DNA複製時のエラーが修正され、突然変異の発生が抑制されます。遺伝的安定性の維持は、細胞の正常な機能と生物の健康を保つために不可欠です。
DNAポリメラーゼは10万回に1回の割合で複製の誤りを引き起こすとされています。(参考文献)
DNAポリメラーゼは非常に高い精度でDNAを複製しますが、人間のゲノムが約30億塩基対という膨大な長さを持つため、複製過程で稀に(105回に一度)誤った塩基が挿入されることがあります。興味深いことに、DNAポリメラーゼには「校正機構」が備わっており、誤った塩基が挿入された際には、これを削除して正しい塩基を再び合成することで、エラー率を大幅に低減させています。具体的には、この校正機能によってエラー率は100万回に1回程度(107)まで下がるとされています。
しかし、この校正機構だけではすべての誤りを防ぐことはできません。そのため、細胞はミスマッチ修復(Mismatch Repair, MMR)と呼ばれるさらなるバックアップシステムを持っており、100万回に一度の複製エラーをさらに1/1000にまで減らすことができます。これによってゲノムの安定性が強化されています。ミスマッチ修復は、DNAが複製された後に残った誤りを修正するシステムで、誤った塩基対を認識し、修復する過程を経てDNAの正確性を保ちます。このシステムのおかげで、生物は遺伝情報の正確な伝達と安定した遺伝的特性を維持することができるのです。
これらの機構により、DNA複製の際の微細なエラーも見逃されることなく、確実に修正されます。これによって細胞は突然変異のリスクを抑え、がんをはじめとする多くの疾患から身を守ることが可能となっています。
突然変異率への影響
ミスマッチリペア(MMR)システムは、DNA複製中に発生する塩基対のミスマッチを修正することで、突然変異率を大幅に低下させる重要な役割を果たします。このシステムがどのようにして突然変異率に影響を与えるのか、以下に詳細を説明します。
1. 突然変異の防止
– ミスマッチリペアシステムは、DNA複製時にポリメラーゼによって誤って組み込まれたヌクレオチドを検出し、修正します。このプロセスにより、誤った塩基対が固定される前に除去されるため、遺伝情報の誤伝達が防がれます。この機構がない場合、DNAの複製エラーがそのまま細胞に蓄積され、高い突然変異率を引き起こす可能性があります。
2. 突然変異率の低下
– ミスマッチリペアシステムが効果的に機能することで、DNA複製中に発生するエラーの大部分が修正され、細胞の突然変異率は大幅に低下します。研究によると、ミスマッチリペア機能の欠如は突然変異率を100倍以上に増加させることが示されています。これは、遺伝的不安定性を招き、がんをはじめとする多くの疾患の発生リスクを高めることにつながります。
3. がんとの関連
– 特に注目すべきは、ミスマッチリペアシステムの不具合ががんの発生に深く関与していることです。例えば、ミスマッチリペア遺伝子(MSH2、MLH1など)の変異は、リンチ症候群と密接に関連しており、この症候群の患者は大腸がんや他の種類のがんのリスクが非常に高くなります。これは、ミスマッチリペアシステムの欠損が突然変異の蓄積を許し、細胞の異常増殖を促進するためです。
4. 遺伝子疾患への影響
– ミスマッチリペアシステムの不全は、がんだけでなく、その他の遺伝子疾患の原因にもなり得ます。遺伝情報の伝達エラーが蓄積されることで、さまざまな代謝異常や発達障害が引き起こされることがあります。
ミスマッチリペアシステムの正確な機能は、生物の遺伝的健康と安定性を維持するために極めて重要です。このシステムの理解を深めることで、遺伝的疾患やがんのより効果的な予防と治療戦略が開発されることが期待されます。
ミスマッチリペアと疾患
MMR欠損と癌の関係
ミスマッチリペア(MMR)システムの不具合は、遺伝子の突然変異を増加させ、多くの遺伝性および非遺伝性疾患、特に癌の発生に深く関与しています。以下では、MMR欠損が癌とどのように関連しているかについて詳しく解説します。
● MMR欠損と癌の関係
1. 癌の発生とMMRの役割:
– ミスマッチリペアシステムは、DNA複製中に生じた誤ったヌクレオチドの挿入や欠落といったエラーを修正することで、DNAの整合性を保ちます。このシステムの機能不全は、細胞の遺伝的安定性の損失を引き起こし、結果的にがんを含む多くの疾患のリスクが高まります。
2. 遺伝性非ポリポーシス性大腸がん(リンチ症候群):
– MMR遺伝子の変異は、リンチ症候群と密接に関連しています。この遺伝症は、大腸がん、子宮がん、卵巣がんなど、複数のがん種の発生リスクを高めるものです。MLH1、MSH2、MSH6、PMS2といったMMR遺伝子のうちの一つまたは複数に変異があると、DNAのミスマッチが修復されず、がんへの進行が加速されることが知られています。
3. MMR欠損と微小衛星不安定性(MSI):
– MMRシステムの欠損は、微小衛星不安定性(MSI)と呼ばれる現象を引き起こすことがあります。MSIは、DNAの短い繰り返し配列(微小衛星)が複製の際に異常に繰り返されるか、逆に失われることを指し、これががん細胞の遺伝子に影響を与えることがあります。MSIは特に大腸がんやその他の消化器がんにおいてよく見られます。
4. 治療への影響:
– MMRの欠損は、がんの治療選択にも重要な影響を与えます。例えば、MSIが高いがんは、免疫チェックポイント阻害薬に対してより敏感であることが示されています。これは、MSIが高いがん細胞が異常なタンパク質を多く表現するため、免疫系により認識されやすいためです。
MMRシステムの欠損による癌の発症は、遺伝的機構の理解を深めることで、未来のがん予防や治療法の向上に寄与する重要な知見です。この知識は、がんのリスクを評価し、適切な治療戦略を立てる上で不可欠です。
ミスマッチリペア欠損に関連する遺伝病
ミスマッチリペア(Mismatch Repair, MMR)は、DNA複製中に生じた誤りを修正する重要なメカニズムです。この修復プロセスがうまく機能しないと、DNAの誤りが蓄積され、細胞の遺伝情報が変異することにつながります。これにより、がんを含む様々な疾患が引き起こされる可能性があります。
● 主なミスマッチリペア欠損に関連する遺伝病
1. リンチ症候群(Lynch syndrome)
リンチ症候群は、最もよく知られるMMR欠損症の一つで、大腸がんや子宮がんなどのリスクを高めます。この症候群は、MMR遺伝子(例えばMLH1、MSH2、MSH6、PMS2)の変異によって引き起こされます。
2. 消化器がん
MMR欠損は、胃や小腸などの消化管がんの発生にも関連しています。これらのがんでは、修復メカニズムの不全ががん細胞の成長を助けることがあります。
3. 子宮内膜がん
MMR欠損は、子宮内膜がんのリスクも高めることが知られています。特に、リンチ症候群に関連する遺伝子変異は、この種のがんにおいて重要な役割を果たします。
これらの病状を理解することは、適切な診断や予防策、治療法の開発に役立つため、遺伝学およびがん研究の分野で注目されています。
ミスマッチリペアと癌治療
MMR欠損が癌治療に与える影響
ミスマッチリペア(MMR)システムの欠損は、癌の発生だけでなく治療にも大きな影響を与えます。特に、MMR欠損が癌治療に与える影響について詳しく掘り下げます。
● MMR欠損が癌治療に与える影響
1. 治療感受性の変化:
– MMRシステムの欠損は、がん細胞の治療に対する感受性に大きな影響を与えることが知られています。特に、化学療法薬に対する感受性が変わることがあります。例えば、MMR欠損がある場合、特定のアルキル化剤に対して耐性を示すことがあります。これは、MMRシステムが通常、薬剤によって誘発されるDNA損傷を修復する役割を持つためです。
2. 免疫チェックポイント阻害剤との相関:
– MMR欠損がある癌は、微小衛星不安定性(MSI)が高い傾向にあり、これが免疫チェックポイント阻害剤に対する反応性を高める可能性があります。MSIが高いがんは異常なペプチドを生成し、それが免疫システムによって異物として認識されやすくなります。このため、PD-1やPD-L1などの免疫チェックポイントをターゲットとした治療が効果的であることが報告されています。
3. 個別化医療への応用:
– MMRの状態を評価することで、個々の患者に最適な治療法を選択するための重要な指標となります。例えば、MMR欠損を持つ患者には、伝統的な化学療法よりも免疫療法が推奨される場合があります。また、MMR状態に基づいた予後の評価も可能になり、治療計画において重要な情報を提供します。
4. 研究と臨床試験への影響:
– MMR欠損を特定することは、新しい癌治療薬の開発や臨床試験の設計においても重要です。MMR欠損を有する患者群を対象とした臨床試験は、より精密な治療法の開発や、新薬の効果を正確に評価するために不可欠です。
MMR欠損が癌治療に与える影響は多岐にわたり、この分野の深い理解が、より効果的で副作用の少ない癌治療の実現に繋がります。これらの知見は、がんの診断、治療、予後判定において、今後ますますその価値を増していくでしょう。
新たな治療戦略:ミスマッチリペアをターゲットとしたアプローチ
ミスマッチリペア(MMR)システムの異常は、がんの発生と進行に深く関与しています。このため、MMRをターゲットとした治療アプローチは、がん治療の新たな戦略として注目されています。以下では、MMRを利用した革新的な治療戦略について詳述します。
● 新たな治療戦略:ミスマッチリペアをターゲットとしたアプローチ
1. 免疫チェックポイント阻害剤との組み合わせ:
– MMR欠損が原因で微小衛星不安定性(MSI)が高まるがんは、異常なタンパク質を多く産生し、結果として免疫システムによる認識が容易になります。この特性を利用し、PD-1やPD-L1といった免疫チェックポイントを阻害する薬剤を用いることで、免疫応答を強化し、がん細胞を攻撃させる戦略が有効です。
2. 合成致死性を利用した治療:
– MMR欠損細胞はDNA修復機能に障害があるため、特定の修復経路に依存して生存しています。PARP(ポリADPリボースポリメラーゼ)阻害剤を使用することで、これらの代替修復経路を阻害し、がん細胞のみを選択的に死滅させる「合成致死」のアプローチが研究されています。
3. MMR欠損のスクリーニングと個別化治療:
– がん治療において、患者のMMR状態を評価することは、治療法の選択に直結します。MMR欠損を持つ患者には、従来の化学療法よりも免疫療法が適している可能性が高いため、事前の遺伝子検査によるスクリーニングが推奨されます。
4. ターゲット療法の開発:
– MMR関連タンパク質を直接ターゲットにする小分子薬剤の開発が進行中です。これらの薬剤はMMR経路の特定の機能を修正または調節し、がん細胞の成長を抑制することを目指しています。
5. 臨床試験と研究の進展:
– MMRをターゲットとした新薬の効果と安全性を評価する臨床試験が数多く行われています。これらの試験は、がん治療におけるMMRの役割をさらに明らかにし、新たな治療オプションの提供を目指しています。
MMRをターゲットとしたがん治療戦略は、特に遺伝的背景に基づく個別化医療の進展に貢献しており、将来的には多くのがん患者にとって新しい希望となる可能性があります。
ミスマッチリペアの研究動向
● 最近の進歩と技術的革新
ミスマッチリペア(MMR)の研究は、がん治療における新たな治療法の開発や、遺伝性がん症候群の理解を深めるために重要な進展を遂げています。以下は、最近の進歩と技術的革新のいくつかです。
1. 免疫チェックポイント阻害薬の使用:
– ミスマッチ修復機構欠損(dMMR)がある直腸癌において、PD-1阻害薬であるdostarlimabが有望な結果を示しています。この治療法は、標準的な化学療法や手術を行う前にdostarlimabを投与し、完全寛解を目指すものです[11].
2. 遺伝子変異の詳細な解析:
– Lynch症候群に関連するMSH2遺伝子の大規模欠失を特定する研究が行われています。これは、ミスマッチ修復遺伝子の変異が遺伝性がん易罹患性症候群の原因となることを示しています[12].
3. 新たな治療薬の開発:
– オプジーボとヤーボイの併用療法が、高頻度マイクロサテライト不安定性(MSI-H)またはミスマッチ修復機構欠損(dMMR)の進行大腸がんにおいて、化学療法と比較して無増悪生存期間で統計学的に有意かつ臨床的に意義のある改善を示しています[1].
4. 診断技術の進化:
– MSI検査やMMRタンパク質に対する免疫染色(IHC)検査など、dMMRの判定に使用される診断技術が進化しています。これにより、適切な患者に対して効果的な治療を迅速に提供