目次
Fish法を用いた染色体検査は、導入から現在に至るまで、臨床診断と病理学的研究に革命をもたらしました。この記事では、Fish法の基本原理、技術の進歩、および臨床現場での有効性について解説します。
第1章 Fish法の基礎と歴史
Fish法とは
FISH法(Fluorescence in situ Hybridization)は、蛍光物質や酵素などで標識したオリゴヌクレオチドプローブを用いて、特定の遺伝子や染色体領域とハイブリダイゼーション(結合)させ、蛍光顕微鏡でその結合部位を検出する分子生物学的手法です[1][4][5]. この技術は、細胞の状態を保持したままで遺伝子異常を検出することが可能であり、PCR法やSouthern blot法では見ることのできない細胞毎の遺伝子異常を観察することができます[1].
FISH法は、悪性腫瘍の治療・診断において重要な役割を果たしており、遺伝子異常に基づく病型分類、治療選択、治療効果判定に利用されています[1]. また、FISH法は血液腫瘍の病型に特異的な遺伝子再構成を検出するためにも用いられ、特にB細胞腫瘍で認められるIGH転座のようなキメラ遺伝子を形成しない場合には欠かせない手法です[2].
FISH法は、染色体の数的異常や構造異常の解析にも利用されており、特定遺伝子の増減(欠失や増幅)や染色対中の位置(マッピング)を調べることができます[6]. さらに、ホルマリン固定パラフィン包埋切片上でFISHを行う方法が確立されており、日常の病理診断に用いる組織標本を用いることが可能になっています[2].
FISH法は、染色体上にハイブリダイゼーションさせた蛍光プローブの発色の有無で、特定領域の微細な欠失等を判定することができ、染色体の形態も合わせて評価できるため、染色体構造異常の確認に用いられます[7]. この方法による転座の検出は従来の方法と比べて迅速で精度も高いとされています[5].
- 参考文献・出典
-
[1] kir159440.kir.jp/giringi3/shiryou/33.pdf
[2] kotobank.jp/word/FISH%E6%B3%95%E3%81%A8SKY%E6%B3%95-2099015
[3] ameblo.jp/kenikukai-shonan/entry-12821496082.html
[4] www.weblio.jp/content/FISH%E6%B3%95
[5] sirabe.nirs.qst.go.jp/sirabe/FISH%E6%B3%95
[6] www.yodosha.co.jp/jikkenigaku/keyword/234.html
[7] www.saitama-pho.jp/scm-c/shokai/naikashinryo/idenka/senshokutaikensa.html
[8] digioka.libnet.pref.okayama.jp/detail-jp/id/ref/M2021032017174211890
染色体検査におけるFish法の革新的役割
染色体検査におけるFISH法(Fluorescence In Situ Hybridization、蛍光in situハイブリダイゼーション)の革新的役割は、その高い特異性と感度により、特定のDNA配列を染色体上で直接観察し、遺伝子の増減や位置の異常を明確に検出できる点にあります。この技術は、遺伝性疾患、がん、およびその他の染色体異常の診断と研究において重要な役割を果たしています。
FISH法は、特定のDNA領域に相補的な標識された核酸配列(プローブ)を用いて、固定された細胞内や組織中の特定のゲノムDNAの状態を調べる方法です。この技術により、細胞内の特定のDNA領域の位置や数の変化を観察することが可能になります。例えば、がん関連線維芽細胞の染色体構造の特徴を解明する研究では、サテライトII DNA領域に相補的なプローブを反応させて、ヒト線維芽細胞や乳がん患者組織中のサテライトII領域の形をDNA-FISH法を用いて解析しました[1]。
また、FISH法は、血液がんに対する包括的ゲノムプロファイリングのための遺伝子パネル検査においても使用され、融合遺伝子関連の構造異常の検出において100%の感度と特異度を示しました[3]。これは、FISH法が遺伝子異常の検出において非常に正確であることを示しています。
さらに、FISH法は小児急性リンパ芽球性白血病の治療においても重要な役割を果たしています。21番染色体の染色体内増幅(iAMP21)の検出にFISH法が用いられ、これはALL患児の生存率の増大に貢献しています[8]。
これらの例から、FISH法は染色体検査において革新的な役割を果たしており、特定の遺伝子異常の高精度な検出を可能にし、遺伝性疾患やがんの診断、治療選択において重要な情報を提供しています。
Fish法の導入前と導入後の比較
FISH法(Fluorescence In Situ Hybridization)は、特定のDNA配列を蛍光標識したプローブを用いて、染色体上の特定の遺伝子やDNA領域を可視化する技術です。この方法は、遺伝子の異常を検出するための強力なツールとして、臨床診断や研究に広く利用されています。
● 導入前の状況
FISH法が導入される前は、染色体の異常を検出するためには主にGバンディングと呼ばれる染色体バンドパターンを利用した方法が用いられていました。この方法では、染色体を特定の染色技術で染めて、顕微鏡で観察することにより、大きな染色体の異常を検出することができました。しかし、Gバンディングでは微細な遺伝子の変化や低レベルのモザイク状態は検出が困難であり、また解析には専門的なスキルと時間が必要でした[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
● 導入後の状況
FISH法の導入により、以下のような利点がもたらされました:
– 高感度・高特異性: FISH法は非常に高い感度と特異性を持ち、微細な遺伝子の変化や低レベルのモザイク状態も検出可能になりました[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
– 迅速な結果の提供: FISH法は培養を必要としないため、Gバンディングに比べて迅速に結果を提供できるようになりました[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
– 定量的な分析: FISH法により、染色体異常を有する細胞の割合を定量的に分析できるようになり、治療効果の判定や移植後の経過観察に有用な情報を提供します[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
– 多色染色の可能性: 複数のプローブを同時に使用することで、一度に複数の遺伝子領域を検出することが可能になり、より複雑な遺伝子異常の解析が行えるようになりました[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
● 問題点と課題
導入後もFISH法にはいくつかの問題点が存在します。例えば、FISH法は比較的高価な検査であり、専門的な訓練を受けた技術者が必要です。また、解析には専用の蛍光顕微鏡が必要であり、機器の導入と維持管理にはコストがかかります[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20]。
● 結論
FISH法の導入は、遺伝子異常の検出において大きな進歩をもたらしましたが、コストや技術的な要求が高いため、その利用は一部の専門施設に限られることがあります。今後は、よりコスト効率の良い方法や、FISH法を補完する他の技術の開発が期待されています。
- 参考文献・出典
-
[1] www.jstage.jst.go.jp/article/tct/12/1/12_22-013/_pdf/-char/ja
[2] www.shizuoka-med.jrc.or.jp/section/department/inspection/03/file/611/blood22.pdf
[3] www.cytogen.jp/index/pdf/09-a.pdf
[4] www.agilent.com/cs/library/articlereprints/public/106_1101_connection15_p34-39_0210.pdf
[5] www.jmedj.co.jp/journal/paper/detail.php?id=3409
[6] katosei.jsbba.or.jp/view_html.php?aid=1365
[7] www.jstage.jst.go.jp/article/kagakutoseibutsu/58/11/58_581102/_pdf
[8] congress.jamt.or.jp/chubu55/pdf/join.php?f%5B%5D=special%2F9016.pdf&f%5B%5D=special%2F9017.pdf
[9] plaza.umin.ac.jp/~patho-genetics/NGS%E5%8B%89%E5%BC%B7%E4%BC%9A%E3%83%86%E3%82%AD%E3%82%B9%E3%83%88.pdf
[10] medicaleducation.co.jp/cancer_training/article03-03/
[11] sph.med.kyoto-u.ac.jp/gccrc/pdf/090918_a1_cyakusyoumae.pdf
[12] www.mhlw.go.jp/content/11908000/000696770.pdf
[13] huhp-hokudai-lab.com/%E9%81%BA%E4%BC%9D%E5%AD%90%E6%9F%93%E8%89%B2%E4%BD%93%E6%A4%9C%E6%9F%BB%E5%AE%A4/
[14] www.jstage.jst.go.jp/article/haigan/62/Supplement/62_931/_pdf
[15] www.jstage.jst.go.jp/article/tenrikiyo/18/2/18_18-013/_pdf
[16] www.jstage.jst.go.jp/article/faruawpsj/38/5/38_KJ00009722235/_pdf/-char/ja
[17] pathos223.com/for_student/onepoint_histopathologic_technology/14.pdf
[18] congress.jamt.or.jp/chubu55/pdf/special/9017.pdf
[19] redcross.repo.nii.ac.jp/record/12081/files/jrcsh2401_14-22.pdf
[20] www.merckmillipore.com/INTERSHOP/web/WFS/Merck-JP-Site/ja_JP/-/JPY/ShowDocument-Pronet?id=201711.074
第2章 Fish法の技術的側面
in situハイブリダイゼーションの原理
In situハイブリダイゼーション(ISH)は、特定の核酸配列を固定された細胞や組織内で特定し、局在を明らかにする技術です。この方法は、遺伝子の発現や遺伝子座の位置情報を時間的、空間的に解析することを可能にします。ISHの基本的な原理は、相補的な塩基配列を持つ一本鎖核酸分子間の特異的な結合を利用することにあります。この技術で検出に用いられる核酸分子をプローブと呼びます[7]。
プローブは、目的の核酸配列に特異的に結合するように設計された、ラベル付きの核酸分子です。プローブのラベルには、放射性同位体(RI)や非放射性の標識(例:DIGシステム)が用いられます。プローブが目的の核酸配列にハイブリダイズ(結合)した後、何らかの方法で可視化されます[8]。
ISH法には、主に二つの検出方法があります。一つは蛍光in situハイブリダイゼーション(FISH)で、複数のターゲットを同時に検出し、単一の標本内での共局在を視覚化することが可能です。FISHでは、異なるハイブリダイゼーションプローブに対してスペクトル的に異なる蛍光ラベルを使用します[6]。もう一つはクロモジェンin situハイブリダイゼーション(CISH)で、CISH信号と組織形態を同時に観察することができます[6]。
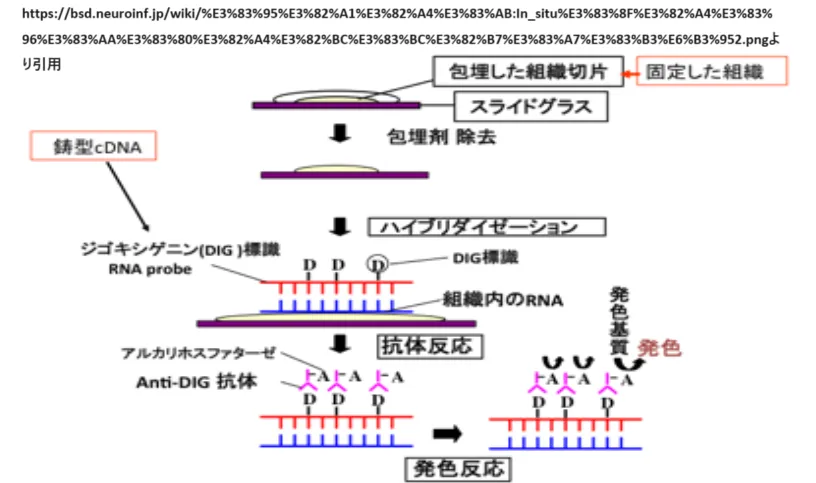
プローブの検出には、DIGシステムのような酵素免疫法による方法があります。この方法では、プローブとターゲットの結合を検出するために、dUTPにジゴキシゲニン(DIG)と呼ばれるステロイド化合物を標識し、その後、DIGを特異的に認識するアルカリホスファターゼ(AP)標識抗体を反応させます。APによる加水分解により化学発光が生じ、ターゲットの存在する場所を検出することができます[4]。
総じて、in situハイブリダイゼーションは、特定の核酸配列の細胞内または組織内での正確な位置を特定するための強力な技術であり、遺伝子発現の解析や遺伝子座のマッピングに広く利用されています。
蛍光標識技術の発展
蛍光標識技術は、生物学や医学研究において重要な役割を果たしています。この技術は、特定のタンパク質や細胞器官、DNA配列などを蛍光物質で標識し、蛍光顕微鏡を用いて可視化することを可能にします。FISH法(Fluorescence In Situ Hybridization、蛍光 in situ ハイブリダイゼーション法)は、この蛍光標識技術の一つであり、特に遺伝子や染色体の研究において広く用いられています。
● FISH法の概要
FISH法は、特定のDNA配列に対応する蛍光物質で標識したプローブを用いて、染色体や核DNAとハイブリダイズ(結合)させることで、その遺伝子の位置やコピー数の変化(増減、欠失や増幅)を観察する方法です[2][3][9]。この技術は、遺伝子マッピング、染色体異常の同定、特定の遺伝子や染色体領域のコピー数の変化の検出などに利用されます[5]。
● FISH法の応用
FISH法は、血液腫瘍の病型に特異的な遺伝子再構成の検出、B細胞腫瘍で特異的に認められるIGH転座の検出、不均一な腫瘍クローンの解析などに有用です[2]。また、ホルマリン固定パラフィン包埋切片上でFISHを行う方法が確立され、日常の病理診断にも応用されています[2]。さらに、羊水検査などの産前診断においても、特定の染色体異常を迅速に検出するためにFISH法が用いられます[6]。
● FISH法の発展
FISH法の発展は、遺伝学や細胞生物学の研究において重要な進歩をもたらしました。この技術により、細胞内の遺伝的変化を直接可視化できるようになり、遺伝子型と表現型の相関関係を特徴づける研究が進展しています[6]。また、FISH法は染色体の分類に用いられるだけでなく、医療や生物学の分野で幅広く応用されており、遺伝性疾患や腫瘍性疾患に関連する遺伝子異常の同定、ウイルスゲノムの検出などにも利用されています[6]。
● 結論
FISH法は、蛍光標識技術の中でも特に遺伝子や染色体の研究において重要な役割を果たしています。この技術の発展により、遺伝学的な研究や病理診断の精度が向上し、遺伝性疾患や腫瘍の診断において重要な情報を提供しています。FISH法のさらなる発展と応用は、未来の医学研究や臨床診断において大きな可能性を秘めています。
- 参考文献・出典
-
[2] kotobank.jp/word/FISH%E6%B3%95%E3%81%A8SKY%E6%B3%95-2099015
[3] institute.yakult.co.jp/dictionary/word_6653.php
[4] www.nagoya-u.ac.jp/researchinfo/result/2024/02/post-632.html
[5] digioka.libnet.pref.okayama.jp/detail-jp/id/ref/M2021032017174211890
[6] minerva-clinic.or.jp/about-human-genom-index/cytogenetics/fluorescence-in-situ-hybridization/
[7] labchem-wako.fujifilm.com/jp/siyaku-blog/018850.html
[8] www.saitama-pho.jp/scm-c/shokai/naikashinryo/idenka/senshokutaikensa.html
[9] www.yodosha.co.jp/jikkenigaku/keyword/234.html
染色体と組織切片での応用
Fluorescence in situ hybridization (FISH)法は、特定のDNAまたはRNA配列を標的として、その存在や位置を蛍光標識プローブを用いて細胞内で直接観察する技術です。この方法は、染色体上の特定遺伝子の位置のマッピング、遺伝子のコピー数の変化、特定のRNA分子の細胞内局在、染色体異常の検出など、多岐にわたる分野で応用されています。
● 染色体での応用
染色体でのFISH法の応用は主に、遺伝子マッピング、染色体異常の同定、テロメア短縮の検出などに利用されます。特定の染色体異常、例えば転座、欠失、増幅などが関与する遺伝性疾患やがんなどの診断に有効です。FISH法により、特定の染色体領域や遺伝子の異常を直接視覚化し、数的、構造的異常を検出することが可能です[3][6][7][12]。
● 組織切片での応用
組織切片でのFISH法の応用は、特にがん研究や診断において重要です。がん細胞特有の遺伝子再配列や遺伝子のコピー数の変化を検出することで、がんの種類の特定や予後の評価、治療法の選択に役立ちます。また、組織切片上でのFISH法は、細胞の形態学的特徴を保持しながら遺伝子レベルの情報を得ることができるため、病理診断においても有用です[5][15][17][18]。
● 技術の特徴と課題
FISH法の特徴は、特定のDNAやRNA配列を高感度かつ高特異性で検出できる点にあります。また、複数のプローブを異なる蛍光色素で標識することにより、同一細胞内で複数の遺伝子や染色体領域を同時に観察するマルチプレックスFISHも可能です[4][9]。しかし、FISH法は比較的高価であり、また、プローブの設計やハイブリダイゼーション条件の最適化が必要なため、技術的な専門知識を要します。さらに、組織切片での応用においては、標本の前処理や固定方法が結果に影響を与えることがあります[5][15]。
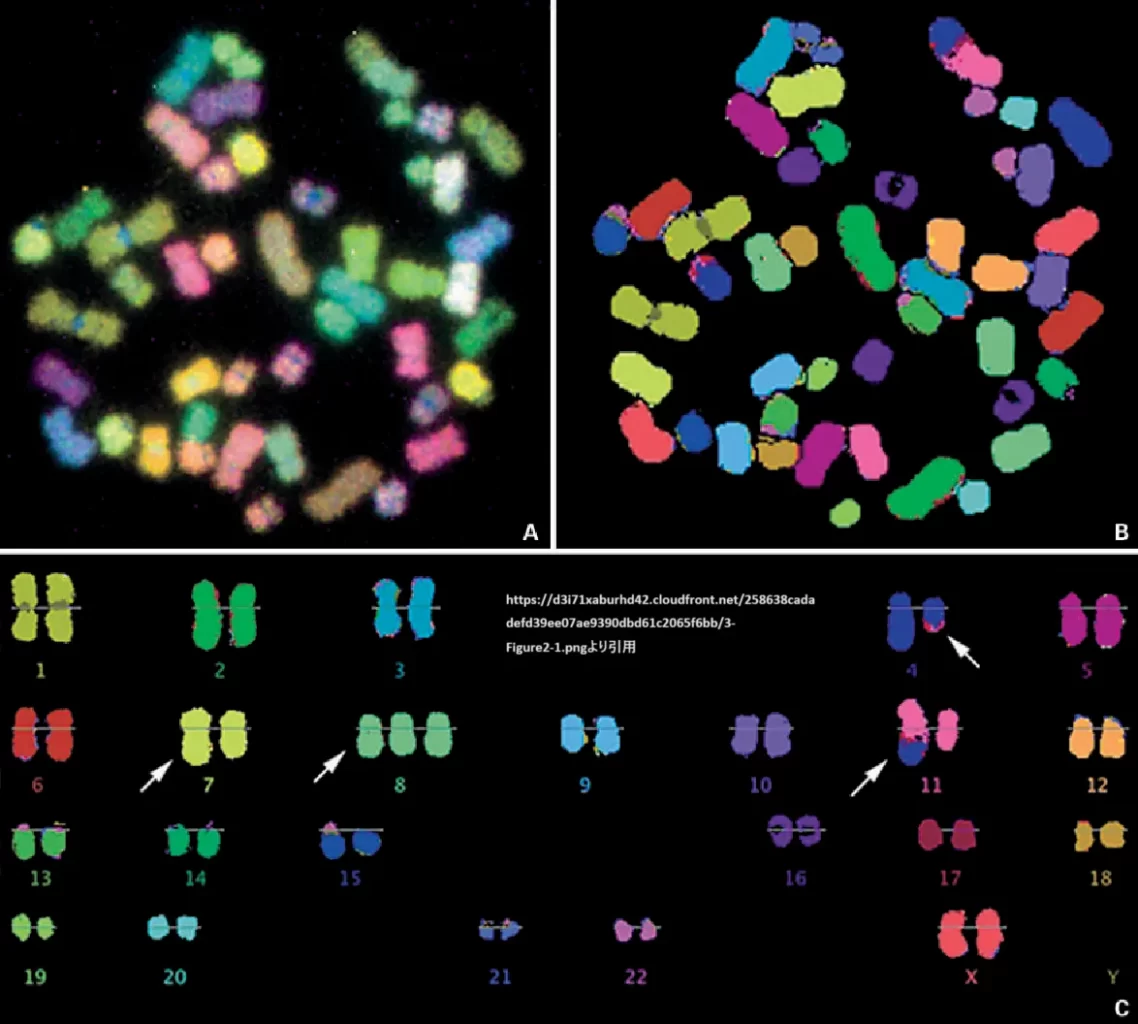
上図の説明:プレB ALL由来細胞株RS4; 11のM-FISHで、( A )別々の蛍光色素画像を統合して作成したブレンドカラー、( B )図1のカラースキームを用いて作成した擬似カラー、( C )t(4;11)(q21;q23)、i(7q)、トリソミー8を示すカラー核型。
● まとめ
FISH法は、染色体研究や病理診断、特にがん診断において重要な役割を果たしています。その高い感度と特異性により、遺伝子レベルでの疾患の理解を深め、個別化医療への応用が期待されています。
- 参考文献・出典
-
[3] kotobank.jp/word/FISH%E6%B3%95%E3%81%A8SKY%E6%B3%95-2099015
[4] institute.yakult.co.jp/dictionary/word_6653.php
[5] www.saitama-med.ac.jp/jsms/vol28/03/p143_149.html
[9] www.thermofisher.com/jp/ja/home/life-science/cell-analysis/cellular-imaging/in-situ-hybridization-ish/fluorescence-in-situ-hybridization-fish.html
[15] www.jst.go.jp/pr/announce/20160706/index.html
[17] www.kyoto-u.ac.jp/ja/research-news/2016-07-06-1
[18] www.saitama-pho.jp/scm-c/shokai/naikashinryo/idenka/senshokutaikensa.html
第3章 Fish法の臨床診断への応用
中皮腫の診断におけるFish法の利用
中皮腫の診断において、FISH法(Fluorescence In Situ Hybridization)は重要な役割を果たしています。FISH法は、特定のDNAシーケンスに対して蛍光標識されたプローブを使用し、細胞内の遺伝子の存在や異常を直接観察する技術です。中皮腫の診断におけるFISH法の応用は、特にCDKN2A(p16)遺伝子の欠失を検出することに焦点を当てています。
CDKN2A遺伝子は、細胞周期の調節に関与する重要な遺伝子であり、その欠失は中皮腫の発生に関連しています。FISH法によるCDKN2A遺伝子のホモ欠失の検出は、中皮腫と他の胸膜疾患との鑑別診断に有用であるとされています。この方法は、中皮腫の診断において高い感度と特異度を持つと報告されており、中皮腫の確定診断に寄与しています[2][10][12][14][15]。
また、FISH法は他の免疫染色法と組み合わせて使用されることもあります。例えば、BAP1タンパク質の喪失やMTAPタンパク質の喪失を検出する免疫染色と組み合わせることで、中皮腫の診断精度をさらに向上させることができます[2][6][8]。
FISH法は、中皮腫診断における標準的なアプローチとして広く受け入れられており、診断の精度を高めるために不可欠なツールとなっています。この技術は、中皮腫の診断だけでなく、他のがん種の診断や遺伝子異常の検出にも応用されています[7][9][11][13]。
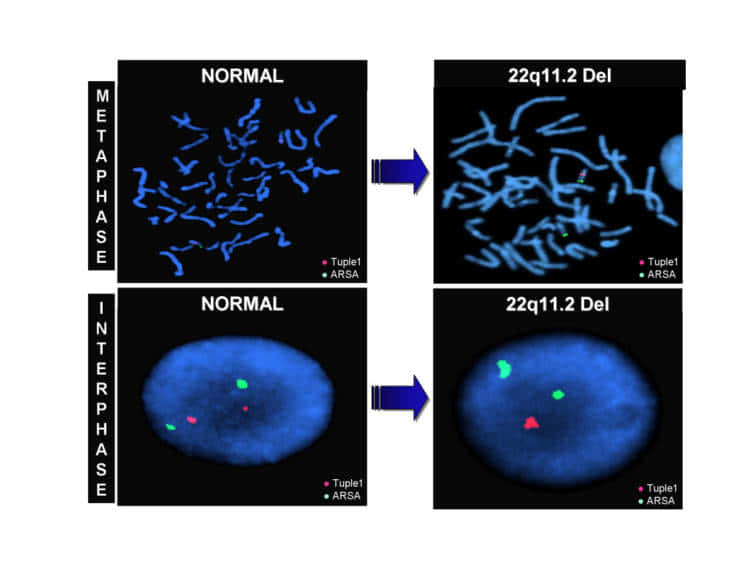
上図の説明:a,b正常コピー数の中皮細胞(赤色シグナル2本、緑色シグナル2本)。c,dヘミ接合性NF2欠損中皮細胞(赤色シグナル1本、緑色シグナル1本)(22番染色体モノソミーパターン)。
- 参考文献・出典
-
[2] www.haigan.gr.jp/guideline/2022/2/1/220201030100.html
[6] kaken.nii.ac.jp/ja/grant/KAKENHI-PROJECT-16K08678/
[7] www.jmedj.co.jp/files/item/books%20PDF/978-4-7849-4082-0.pdf
[8] www.jsomt.jp/journal/pdf/067060473.pdf
[9] www.m-book.co.jp/product/4755
[10] byouri.tokushukai.or.jp/effort/cdkn2afish
[11] www.yodosha.co.jp/yodobook/book/9784758120623/
[12] www.medience.co.jp/clinical/information/parts/pdf/19-05.pdf
[13] www.shinryobunko.co.jp/item-detail/703684
[14] fukuoka-u.repo.nii.ac.jp/record/3849/files/R2102_0007.pdf
[15] dr.tokushukai.or.jp/news/news20230308.php
染色体異常の確定診断への寄与
FISH法(Fluorescence in situ Hybridization)は、特定のDNA配列を標的として、その配列が存在する染色体上の位置を蛍光マーカーを用いて可視化する技術です。この方法は、染色体異常の確定診断において重要な役割を果たしています。FISH法による臨床診断への応用は多岐にわたり、特にがんや遺伝性疾患の診断、染色体異常の同定においてその価値が認められています。
● がんの診断と治療選択
がん細胞はしばしば特定の染色体異常を持ち、これらの異常はがんの種類や進行度、治療反応性を示すバイオマーカーとなり得ます。FISH法を用いることで、これらの染色体異常を正確に同定し、がんの診断や予後の評価、さらには標的治療薬の選択に役立てることができます。例えば、慢性骨髄性白血病(CML)では、BCR-ABL遺伝子の融合が特徴的な染色体異常であり、FISH法による検出が治療選択の重要な指標となります。
● 遺伝性疾患の診断
遺伝性疾患においても、FISH法は特定の遺伝子変異や染色体異常の検出に有効です。ダウン症候群やターナー症候群などの染色体数異常症や、特定の遺伝子欠失が原因で起こる疾患の診断にFISH法が用いられます。これにより、早期に正確な診断を下し、適切な医療支援やカウンセリングを提供することが可能になります。
● 染色体異常の同定
FISH法は、染色体異常の詳細な解析にも利用されます。例えば、不明瞭な染色体構造異常や、微細な欠失・増幅など、従来の染色体分析では検出が困難だった異常を明らかにすることができます。これにより、疾患の原因解明や新たな遺伝子異常の同定に貢献しています。
FISH法の臨床診断への応用は、その高い感度と特異性により、染色体異常に関連する多くの疾患の診断と治療において不可欠な技術となっています。今後も、新たなバイオマーカーの発見や治療法の開発において、FISH法の役割はさらに拡大していくことが期待されます。
臨床検査としての有効性
Fluorescence in situ hybridization(FISH)法は、特定のDNAまたはRNA配列を標的として、その存在や位置を蛍光プローブを用いて直接観察する技術です。この方法は、特に染色体異常の検出や遺伝子の発現状態の解析において、臨床検査として広く利用されています。FISH法の臨床診断への応用は多岐にわたり、がん診断、遺伝性疾患の検査、感染症の診断など、様々な分野でその有効性が認められています。
● がん診断におけるFISH法の応用
がん細胞はしばしば特定の染色体異常を示します。FISH法は、これらの異常を検出するために有効な手段として用いられます。例えば、慢性骨髄性白血病(CML)では、BCR-ABL遺伝子の融合が特徴的な染色体異常として知られており、FISH法による検出が治療選択や予後判定に重要な役割を果たします[18]。また、乳がんにおいては、HER2遺伝子の増幅をFISH法で検出することで、患者に対する適切な治療法の選択に貢献します[14]。
● 遺伝性疾患の検査への応用
遺伝性疾患の多くは、特定の遺伝子変異や染色体異常によって引き起こされます。FISH法は、これらの異常を検出するために有効なツールです。例えば、ダウン症候群やターナー症候群などの染色体数の異常や、特定の遺伝子の欠失や重複が原因で発症する疾患の診断にFISH法が利用されます[11]。
● 感染症の診断への応用
FISH法は、特定の病原体のDNAやRNAを標的として、感染症の診断にも応用されます。細菌やウイルスの特定の遺伝子配列を標的とすることで、感染症の原因となる病原体を迅速に同定することが可能です[3]。この方法は、従来の培養法に比べて迅速であり、感染症の早期診断に貢献します。
● 結論
FISH法は、その高い感度と特異性により、がん診断、遺伝性疾患の検査、感染症の診断など、多岐にわたる臨床検査において有効なツールとして認められています。特定の染色体異常や遺伝子の発現状態を直接観察できることから、診断、治療選択、予後判定において重要な情報を提供します。今後もFISH法の技術的進歩と応用範囲の拡大が期待されます。
第4章 Fish法の最新動向と未来
最新の技術革新と臨床研究
FISH(Fluorescence In Situ Hybridization、蛍光 in situ ハイブリダイゼーション)法は、特定のDNA配列を染色体上で検出し、その位置を特定するために使用される分子細胞遺伝学技術です。この技術は、遺伝性疾患の診断、遺伝子マッピング、がんなどの疾患に寄与する新規がん遺伝子の同定に広く利用されています[17][18]。
近年の技術革新により、FISH法はさらに快速化、自動化、そして智能化が進んでいます。これらの進化は、FISH法の操作を簡素化し、分析時間を短縮するとともに、より高い精度と再現性を実現しています。特に、自動化されたFISH解析システムの開発は、病理診断や研究における効率性と正確性を大幅に向上させています[16]。
● 臨床研究における応用
FISH法は、がんの診断と治療選択において重要な役割を果たしています。特定のがん遺伝子の異常を検出することで、患者に最適な治療法を選択するための重要な情報を提供します。また、FISH法は、がん細胞の遺伝的特徴を詳細に解析することで、新しい治療標的の同定や、個別化医療の実現に貢献しています[17][18]。
● 未来への展望
FISH法の未来は、さらなる技術革新と臨床応用の拡大によって形作られていきます。新しい探索技術や自動化技術の開発により、FISH法はより高速で正確な遺伝子解析を可能にし、がんだけでなく、遺伝性疾患や希少疾患の診断においてもその価値を高めていくでしょう。また、デジタルイメージング技術との組み合わせにより、FISH法による解析結果の解釈がより容易になり、遺伝子異常に基づく疾患の理解が深まることが期待されます。
さらに、FISH法の応用範囲は、がん研究や遺伝学の領域に留まらず、神経科学や発生生物学など、新たな研究分野へと広がっていく可能性があります。これにより、生命科学のさまざまな分野における基礎研究や臨床研究において、FISH法が中心的な役割を果たすようになることが予想されます。
技術革新と臨床研究におけるFISH法の進化は、医学と生命科学の未来を形作る重要な要素となります。これらの進展は、疾患の早期発見、正確な診断、効果的な治療法の開発に貢献し、人々の健康と福祉の向上に寄与することでしょう。
Fish法による新たな診断可能性
FISH (Fluorescence In Situ Hybridization) 法は、特定のDNA配列を標的とする蛍光色素をつけたプローブを使用して、細胞内の遺伝子や染色体の位置や数を可視化する技術です。この技術は、がんや遺伝性疾患の診断、遺伝子の発現状態の解析、染色体異常の検出など、多岐にわたる分野で利用されています。最新の動向としては、FISH法の解像度と感度の向上、自動化技術の発展、および多色FISH法の進化が挙げられます。
● 解像度と感度の向上
FISH法の解像度と感度の向上は、より詳細な遺伝子や染色体の解析を可能にしています。これにより、微細な遺伝子の変異や低頻度の染色体異常も検出できるようになり、疾患の早期診断や個別化医療への応用が期待されています。例えば、高感度FISH法は、がん細胞内の特定の遺伝子変異を検出するために用いられ、治療選択や予後判定に役立てられています。
● 自動化技術の発展
FISH法の自動化は、検査の効率化と再現性の向上に寄与しています。自動化されたFISHシステムは、プローブのハイブリダイゼーションから画像の取得、解析までのプロセスを自動で行うことができ、大量のサンプルを迅速に処理することが可能です。これにより、臨床検査のワークフローが改善され、診断までの時間が短縮されます。
● 多色FISH法の進化
多色FISH法は、複数の異なる蛍光色素を用いて、一度に複数の遺伝子や染色体領域を標的とする技術です。この進化により、単一の細胞内での遺伝子間の相互作用や染色体の構造的変化を同時に解析することが可能になりました。特にがん研究において、複数の遺伝子変異や染色体再編を同時に検出することで、がんの発生メカニズムの解明や新たな治療標的の同定に貢献しています。
● 未来への展望
FISH法の未来は、さらなる技術革新により、より高精度で包括的な遺伝子・染色体解析が可能になることが期待されています。また、デジタルイメージング技術との組み合わせによるデータ解析の高度化や、AI (人工知能) 技術を活用した解析アルゴリズムの開発により、診断精度の向上と解析時間の短縮が進むことでしょう。これらの進展は、遺伝性疾患やがんなどの疾患診断におけるFISH法の応用範囲をさらに広げ、個別化医療の実現に貢献することが期待されます。
未来への展望と技術の進化
FISH法(Fluorescence in situ Hybridization、蛍光in situハイブリダイゼーション)は、特定のDNAまたはRNA配列を細胞内で直接観察するための強力な分子生物学的技術です。この技術は、遺伝子の局在や数の変化、染色体異常の検出、がん診断、遺伝性疾患の研究など、多岐にわたる分野で応用されています。近年のFISH法の進化と未来の展望について、以下にまとめます。
♦ 最新動向
● マルチカラーFISH
マルチカラーFISHは、複数の蛍光プローブを同時に使用し、異なる色で標識することで、一つの細胞内で複数の遺伝子や染色体領域を同時に観察できる技術です。この技術により、複雑な遺伝子間の相互作用や染色体の再構成を詳細に解析することが可能になります。
● 高解像度FISH
従来のFISH法では、数百キロベース以上の大きなDNA領域を検出するのが一般的でしたが、高解像度FISH技術の開発により、数キロベース単位の小さなDNA領域や特定の遺伝子配列を検出できるようになりました。これにより、より精密な遺伝子の解析が可能になります。
● in situシーケンシング
in situシーケンシングは、細胞内で直接RNAやDNAの配列を読み取る技術です。FISH法と組み合わせることで、特定の遺伝子の発現パターンや変異を細胞の正確な位置で特定できます。この技術は、単一細胞レベルでの遺伝子発現の解析に革命をもたらす可能性があります。
♦ 未来への展望
● AIとの統合
人工知能(AI)技術とFISH法の統合により、膨大な量の画像データから迅速に情報を抽出し、解析することが可能になります。AIは、複雑なパターンの認識や異常の検出を自動化し、診断の精度を向上させることが期待されています。
● ナノテクノロジーの応用
ナノテクノロジーを利用した新しいプローブの開発により、FISH法の感度と特異性がさらに向上することが期待されます。ナノスケールのプローブは、細胞内の特定の分子や構造に高い親和性を持ち、未知の遺伝子や病態の解明に貢献する可能性があります。
● 臨床応用の拡大
FISH法の技術進化により、がんや遺伝性疾患の早期診断、個別化医療への応用がさらに進むことが期待されます。特に、非侵襲的な検査方法としての開発や、治療効果のモニタリング、予後予測など、臨床現場での利用が拡大することでしょう。
FISH法は、分子生物学と臨床医学の架け橋として、今後も多くの革新をもたらす技術です。技術の進化とともに、生命科学の未知の領域を解明し、医療の質を向上させるための重要なツールとなるでしょう。