目次
CD96(別名:TACTILE)は、1992年にT細胞の後期活性化マーカーとして発見されながら、長らく機能解明が進まなかった遺伝子です。しかし近年、CTLA-4・PD-1に続く「次世代の免疫チェックポイント」として急速に注目を集めています。CD96はNK細胞やCD8+T細胞に発現し、共通リガンドCD155(PVR)をめぐってTIGITやCD226と競合することで、腫瘍微小環境における免疫細胞の疲弊を誘導します。一方で急性骨髄性白血病(AML)においては、正常造血幹細胞には発現しない白血病幹細胞(LSC)特異的マーカーとしても注目される、二重の臨床的意義を持つ分子です。
Q. CD96遺伝子とはどのような遺伝子ですか?まず結論だけ知りたいです
A. CD96(別名:TACTILE)は、NK細胞・CD8+T細胞の表面に発現する免疫グロブリンスーパーファミリーの膜受容体をコードする遺伝子です。CD155(PVR)を主要リガンドとしてTIGITやCD226と競合し、腫瘍微小環境でエフェクター細胞の疲弊を誘導する免疫チェックポイントとして機能します。一方で急性骨髄性白血病(AML)では白血病幹細胞(LSC)に特異的に高発現し、正常造血幹細胞との劇的な発現差異が確認されているため、診断マーカーおよびCAR-T療法の標的としても有望視されています。
- ➤CD96の発見と特性 → 1992年「TACTILE」として同定、IgSF1型膜貫通糖タンパク質、5種類のアイソフォーム
- ➤CD226/TIGIT/CD96軸 → CD155への親和性階層(TIGIT>CD96>CD226)と競合によるシグナル制御
- ➤免疫細胞での多面的役割 → NK細胞(活性化と抑制の二面性)、CD8+T細胞(疲弊誘導)、Th9細胞(サブセット分類)
- ➤AML白血病幹細胞マーカー → LSC特異的高発現・予後不良との相関・CAR-T療法の最前線
- ➤自己免疫疾患との関連 → 強直性脊椎炎でのCD96機能低下とシーソーモデルの概念
- ➤臨床開発動向 → GSK nelistotug開発中止・BMS-986442(TIGIT×CD96二重特異性抗体)第1b/2相進行中
1. CD96遺伝子の発見と基礎特性
CD96遺伝子は、1992年にT細胞の活性化に伴って後期に発現が上昇する抗原として同定され、「TACTILE(T cell activation, increased late expression)」と命名されました。当初から急性白血病のサブセットを区別するマーカーとして注目されていたものの、その後10年以上にわたり詳細な機能的研究の対象となることはほとんどありませんでした。
状況が一変したのは、ポリオウイルス受容体(PVR)として知られていたCD155がCD96の相互作用パートナーとして同定されたことがきっかけです。これにより、CD96が細胞接着および免疫応答の制御において重要な役割を担うことが再評価され、「次世代の免疫チェックポイント」としての研究が加速しました。
💡 用語解説:免疫グロブリンスーパーファミリー(IgSF)
抗体(免疫グロブリン)に類似した「Igドメイン」という構造をもつタンパク質の大家族です。細胞の表面に存在し、細胞どうしの認識・接着・シグナル伝達に関わるものが多く含まれます。CD96のほか、CTLA-4・PD-1・TIGIT・CD28など、よく知られた免疫チェックポイント分子の多くがこのファミリーに属しています。
💡 用語解説:NK(ナチュラルキラー)細胞とは
NK細胞は全循環リンパ球の約15%を占める自然免疫の担い手です。「自然」=生まれつき備わった免疫で、抗原提示なしに腫瘍細胞やウイルス感染細胞を認識・殺傷できます。CD56brightCD16−(サイトカイン産生型)とCD56dimCD16+(細胞傷害型)の2つの主要サブセットに分類され、CD96はどちらのサブセットにも発現しています。
健常状態におけるCD96の発現は主に造血器由来の細胞群に限定されており、特にNK細胞・CD8+T細胞・CD4+T細胞の表面に恒常的または活性化依存的に発現しています。活性化されたT細胞およびNK細胞がインテグリンやセレクチンを用いて血管内皮を通過し、炎症部位や病変組織へ移動して標的細胞と接着する際の相互作用にも関与することが確認されています。
2. 分子構造とアイソフォームの多様性
CD96遺伝子がコードするタンパク質は、免疫グロブリンスーパーファミリーに分類される1型膜貫通型糖タンパク質です。ゲノムレベルでの選択的スプライシングにより、長さやアミノ酸配列が異なる複数の転写バリアントが生成されます。UniProtデータベースの解析によれば、CD96には少なくとも5つの潜在的なアイソフォームが確認されています。
💡 用語解説:アイソフォームとは
同じ遺伝子からつくられるが、スプライシング(mRNAの切り貼り)の違いによって生まれる、構造が少し異なる複数のタンパク質バリアントのことです。アイソフォームが異なると、リガンド(結合相手)への結合能力や細胞内シグナルの強度が変化することがあります。CD96の場合、アイソフォームの違いがヒトとマウスで異なる機能特性を示す一因と考えられています。
| エントリー名 | アイソフォーム長(aa) | 備考 |
|---|---|---|
| TACT_HUMAN(P40200) | 585 aa | 主要な長鎖アイソフォーム |
| Q8WUE2_HUMAN | 402 aa | スプライシングバリアント |
| F8WDV3_HUMAN | 118 aa(13,675 Da) | 短鎖マッピング配列 |
| H7C4F0_HUMAN | 146 aa | 潜在的アイソフォーム |
| E9PEJ1_HUMAN | 568 aa | 潜在的アイソフォーム |
出典:UniProtKB(ヒトCD96)
💡 用語解説:ITIM(免疫受容体チロシンベース抑制モチーフ)
ITIMとは、受容体の細胞内ドメインに存在する特定のアミノ酸配列で、この配列を介してリン酸化が起こると抑制シグナルが伝達されます。CTLA-4やTIGITなど多くの共抑制性受容体はこのモチーフを持ちます。興味深いことに、CD96の細胞内ドメインには古典的なITIMが完全な形では存在しないにもかかわらず、機能的には強力な抑制シグナルを免疫細胞に伝達します。このユニークな抑制メカニズムの解明は現在も進行中の研究領域です。
構造解析によれば、CD96の第1(膜遠位)Ig様ドメインが主要なリガンド結合部位として機能し、第3ドメインの変異(T280Mなど)はCD155への結合親和性を著しく低下させることが報告されています。また、リガンド結合は単純な1対1の相互作用にとどまらず、シス-トランス受容体クラスター形成(cis-trans receptor clustering)という動的な空間配置を要求するシグナル伝達メカニズムを介して機能しています。
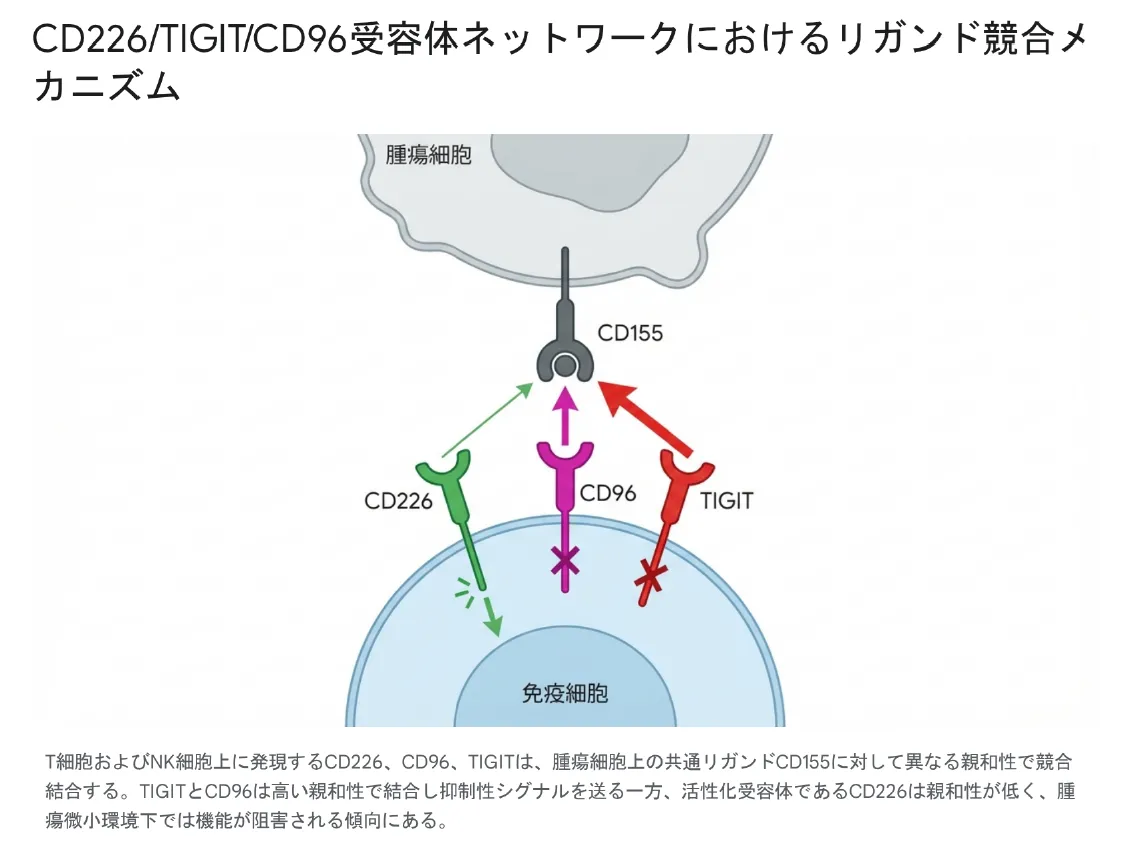
3. CD226/TIGIT/CD96 競合的受容体ネットワークの分子基盤
CD96の生物学的機能を理解する上で不可欠なのが、共通リガンドCD155(PVR)をめぐる競合的な受容体ネットワークです。CD96は、共刺激性受容体のCD226(DNAM-1)、および共抑制性受容体のTIGIT、さらにはCD112R(PVRIG)とともに、「CD226軸」と呼ばれるシグナル伝達経路を形成しています。このCD226軸は、T細胞の活性化を微調整する古典的な「CD28/CTLA-4経路」と機能的・構造的に酷似したリガンド競合モデルを形成しています。
💡 用語解説:CD155(PVR:ポリオウイルス受容体)とは
もともとポリオウイルスが細胞に侵入する際の受容体として発見されたタンパク質です(正式名称:CD155)。樹状細胞・内皮細胞・マクロファージなどの抗原提示細胞(APC)に広く発現しているほか、頭頸部扁平上皮癌・メラノーマ・結腸直腸癌・非小細胞肺癌・神経膠腫など多種多様な固形腫瘍の細胞表面で顕著に発現が亢進しています。腫瘍細胞がCD155を過剰発現することで、CD96やTIGITへのシグナルを強め、免疫細胞を「疲弊」させる免疫逃避の主要メカニズムとなっています。
T細胞およびNK細胞上に発現するCD226・CD96・TIGITは、腫瘍細胞上の共通リガンドCD155に対して異なる親和性で競合結合する。TIGITとCD96は高い親和性で結合し抑制性シグナルを送る一方、活性化受容体であるCD226は親和性が低く、腫瘍微小環境では機能が阻害される傾向にある。
CD155への結合親和性の階層構造
このネットワークの最も重要な特徴は、各受容体のCD155への結合親和性に明確な階層が存在する点です。TIGITが最も高い親和性を示し、次いでCD96が中程度、共刺激受容体のCD226が最も低い親和性を持ちます。
CD155への結合親和性の比較(高 → 低)
腫瘍微小環境でCD155が高発現すると、TIGITとCD96がCD155を占有し、活性化受容体のCD226の結合を物理的・機能的に阻害。免疫細胞への入力は活性化から抑制へと傾く。
💡 用語解説:TIGITとは
TIGIT(T cell immunoglobulin and ITIM domain)は、NK細胞・CD8+T細胞・制御性T細胞(Treg)に発現する共抑制性受容体です。CD155・CD112に結合し、細胞内のITIMおよびITT様モチーフを介して強力な抑制シグナルを伝達します。CD96と同じくCD155を主要リガンドとして共有するため、腫瘍微小環境では両者が連携して免疫細胞の疲弊を誘導します。TIGITはCD96よりも高い親和性でCD155に結合し、また制御性T細胞(Treg)にも強く発現する点がCD96との機能的な違いです。
| 受容体 | 主な発現細胞 | 結合リガンド | CD155親和性 | 機能 |
|---|---|---|---|---|
| TIGIT | NK細胞・CD8+T・Treg | CD155・CD112 | 最も高い | 抑制性(ITIM・ITT様モチーフ) |
| CD96 | NK細胞・CD8+T・Th9 | CD155(主要) | 中程度 | 抑制性(固有メカニズム) |
| CD226(DNAM-1) | NK細胞・T細胞・骨髄系 | CD155・CD112 | 最も低い | 活性化(Y322/S329リン酸化) |
腫瘍微小環境(TME)においてCD155が高発現すると、より親和性の高いTIGITやCD96がCD155を空間的に占有し、活性化受容体であるCD226の結合を物理的・機能的に阻害します。細胞内シグナル統合においても、CD226がチロシン(Y322)およびセリン(S329)残基をリン酸化して活性化シグナルを送るのに対し、TIGITはITIMおよびITT様モチーフを通じて抑制シグナルを伝達します。CD96を通じたシグナルも最終的に抑制をもたらすため、CD226の活性化シグナルは多重に遮断され、T細胞やNK細胞は活性化から疲弊へと傾いていきます。
4. 各免疫細胞サブセットにおける多面的機能
CD96は、発現する免疫細胞のサブセットによって、また動物モデルとヒトの系とで異なる機能的役割を担う可能性があり、その生理学的機能は極めて多面的です。
4-1. NK細胞における機能:活性化と抑制の二面性
NK細胞におけるCD96の役割は、歴史的に議論の的となってきました。ヒトCD96に関する初期研究では、CD96がCD155を介して標的細胞への接着を促進し、活性化NK細胞の細胞傷害性を刺激する「活性化」受容体として報告されていました。
しかし、その後のマウスモデルを用いた多くの生体内実験により、CD96が強力な「共抑制性(阻害的)」チェックポイントとして働くことが実証されました。具体的には、CD96を特異的抗体でブロックするか遺伝子ノックアウトしたマウスでは、NK細胞によるIFN-γの産生が著しく亢進し、メラノーマ肺転移モデルにおいて腫瘍の転移拡散が顕著に抑制されることが確認されました。
💡 用語解説:IFN-γ(インターフェロンガンマ)とは
T細胞やNK細胞が産生する重要なサイトカイン(細胞間シグナル物質)で、抗腫瘍免疫において中心的な役割を担います。IFN-γが産生されると、マクロファージの活性化・抗原提示の増強・腫瘍細胞への直接攻撃が促進されます。腫瘍微小環境でCD96シグナルが活性化されIFN-γ産生が低下すると、抗腫瘍免疫応答全体が弱体化します。IFN-γ産生量の増減は免疫チェックポイント阻害薬の効果指標としても広く用いられています。
ヒトにおける活性化シグナルの報告とマウスモデルにおける強力な抑制シグナルの間のこの不一致は、CD96のアイソフォームの違い、実験モデルの限界、あるいはCD226とのクロストークの状況に依存している可能性があります。肝細胞癌(HCC)患者の腫瘍内NK細胞を用いた近年の臨床研究では、CD96の高発現が機能的疲弊とIFN-γ・TNF-α産生の低下に関連し、無病生存期間の悪化と強く相関することが示されており、ヒトの腫瘍微小環境下でも抑制的に働くことが強く支持されています。
4-2. CD8+T細胞:免疫チェックポイントとしての確立
腫瘍微小環境(TME)において、腫瘍抗原特異的なCD8+T細胞は慢性的な抗原刺激に曝され、エフェクター機能(サイトカイン産生や細胞傷害能)を喪失する「疲弊(Exhaustion)」という状態に陥ります。CD96は、マウスおよびヒトの腫瘍浸潤リンパ球(TILs)において、PD-1やTIGITといった既知の強力な抑制性受容体と高い頻度で共発現していることが確認されています。
💡 用語解説:T細胞疲弊(Exhaustion)とは
T細胞疲弊とは、腫瘍内や慢性感染部位で長期間にわたって抗原刺激を受け続けたT細胞が、増殖能・サイトカイン産生能・細胞傷害能などのエフェクター機能を段階的に喪失していく状態です。PD-1・TIM-3・LAG-3・TIGITなどの抑制性受容体が高発現し、「疲弊マーカー」として機能不全の指標となります。CD96もこれらと共発現することで疲弊プログラムに加担することが近年明らかになっています。疲弊T細胞の再活性化が現代のがん免疫療法の中心的な課題です。
前臨床の腫瘍モデルにおいて、CD96阻害抗体を単独または抗PD-1抗体と併用投与すると、CD8+T細胞におけるIFN-γ産生細胞の割合が有意に増加し、T細胞依存的に原発巣の腫瘍増殖が強く抑制されることが確認されています。重要なことに、同じCD226軸のTIGITが制御性T細胞(Treg)にも強く発現してTreg機能を亢進させるのに対し、CD96は主に機能不全に陥ったエフェクターCD8+T細胞上に存在し、Tregを介さない非冗長的な(固有の)抑制経路を制御している点に大きな機能的特長があります。
また、PD-1療法に非感受性の患者由来のCD96+PD-1+CD8+TILsは、末期的な疲弊エフェクター表現型を示すことが分かっており、CD96の発現はPD-1阻害に対する抵抗性のバイオマーカーとしても機能し得ます。
4-3. Th9細胞サブセットにおける役割
エフェクターCD8+T細胞のみならず、ヘルパーT細胞の一種であるTh9細胞におけるCD96の役割も特筆すべきです。最新の単一細胞レベルの遺伝子発現解析から、Th9細胞はCD96の発現レベルに基づいて「CD96高発現(CD96high)」と「CD96低発現(CD96low)」の2つの明確なサブセットに分類されることが判明しました。
💡 用語解説:Th9細胞とは
CD4+T細胞がIL-4とTGF-βの刺激を受けて分化するサブセットで、IL-9(インターロイキン9)を主に産生します。転写因子PU.1やIRF4によって制御され、アレルギー・自己免疫疾患・抗腫瘍免疫の両方に関与することが知られています。CD96lowのTh9細胞はIL-9産生が高く強力な炎症惹起能をもつ一方、CD96highのTh9細胞はその炎症惹起能が抑制されていることが近年明らかになり、IBD(炎症性腸疾患)などの自己免疫疾患における新たな治療標的として注目されています。
解析の結果、CD96low Th9細胞はIL-9産生が極めて高く、マウスに移植すると重度の大腸炎(Colitis)などの強力な組織炎症を引き起こすことが示されました。一方、CD96high Th9細胞はこのような炎症惹起能を持たず、組織への集積能力も低いことが分かっています。CD96を抗体で阻害するとCD96high Th9細胞の増殖が促され、炎症性の表現型が完全に回復することも確認されており、CD96がCD4+T細胞においても「ブレーキ」として機能し、サイトカイン産生とエフェクター機能を制御していることが強く裏付けられています。
5. 腫瘍免疫における臨床的意義と多重チェックポイント遮断
CD96は前述のNK細胞およびCD8+T細胞の機能制御を通じて、抗腫瘍免疫応答において極めて重要な鍵を握っています。多種多様な固形腫瘍において、CD155の発現亢進とそれに伴うCD96シグナルの過剰入力がT細胞の疲弊を誘発していることが明らかになっています。
💡 用語解説:腫瘍微小環境(TME)とは
腫瘍を取り囲む免疫細胞・線維芽細胞・血管・細胞外基質・サイトカインなどの複合的な環境のことです。腫瘍細胞はTMEを積極的に「免疫抑制的」な状態へ操作し、免疫細胞による排除を回避しようとします。TME内ではCD155の高発現・TGF-β・IL-10などの免疫抑制性サイトカインが充満し、浸潤したT細胞やNK細胞をすみやかに疲弊させます。CD96・TIGIT・PD-1の複合的な発現がTMEにおける免疫細胞の機能不全を決定づける主要な要因です。
CD96による免疫抑制が確認されているがん種には、頭頸部扁平上皮癌(HNSCC/OSCC)・悪性黒色腫(メラノーマ)・結腸直腸癌・非小細胞肺癌(NSCLC)・神経膠腫(グリオーマ)・子宮頸癌・肝細胞癌(HCC)などが含まれます。頭頸部扁平上皮癌(OSCC)の組織解析では、腫瘍細胞におけるMHCクラスI分子のダウンレギュレーションという古典的な免疫逃避機構に加え、CD96経路が独立した抑制経路として機能していることがmRNAレベルの解析で特定されています。
前臨床における併用療法の有効性
マウスモデルを用いた前臨床研究は、CD96を標的とした併用療法の有効性を強力に支持しています。CT26大腸癌モデルやMCA(メチルコラントレン)誘発線維肉腫モデルにおける主な結果を以下に示します。
MCA誘発線維肉腫モデルにおける腫瘍拒絶率(概念図)
Triple ICB:抗CD96+抗TIGIT+抗PD-1の三剤併用。マウスの50%で腫瘍完全拒絶が観察された。数値は文献報告からの概念的表示。
ヒト臨床の観点からも、子宮頸癌患者を対象とした研究において、PD-1抗体のインビトロブロック後にCD8+TILs上のCD96の発現が代償的に顕著に上昇する現象が確認されており、これがPD-1治療に対する適応耐性(Adaptive resistance)のメカニズムの一つであると推測されています。
💡 用語解説:適応耐性(Adaptive resistance)とは
治療薬に対して腫瘍または免疫細胞が動的に応答し、代替の抑制経路を上方調節することで治療効果を回避するメカニズムです。PD-1阻害薬による治療でPD-1シグナルが遮断されると、腫瘍微小環境はCD96など別の免疫チェックポイント受容体を代償的に発現させることがあります。これが「PD-1阻害薬が効いたのに途中から効かなくなる(獲得耐性)」原因の一つと考えられており、CD96をはじめとする次世代チェックポイント分子の遮断が解決策として期待されています。
6. 急性骨髄性白血病(AML)における白血病幹細胞マーカーとしての意義
固形腫瘍における免疫チェックポイントとしての機能とはまったく独立した文脈で、CD96は急性骨髄性白血病(AML)において白血病細胞自身の表面マーカーとして極めて重大な病理学的意義を持ちます。
AMLは骨髄中の骨髄系芽球がクローン性に増殖する予後不良の血液悪性腫瘍であり、高い再発率が臨床上の最大の障壁となっています。この再発と化学療法抵抗性の主要な原因は、自己複製能と増殖能を有する白血病幹細胞(LSC)の存在にあります。
💡 用語解説:白血病幹細胞(LSC)とは
LSC(Leukemic Stem Cell)とは、白血病の階層構造の頂点に位置し、自己複製能・増殖能・化学療法抵抗性を持つ細胞集団です。通常の寛解後療法でも根絶されずに骨髄内に潜伏し、再発の「種」となります。正常な造血幹細胞(HSC)と同じくCD34+CD38−という表現型を持つため、正常細胞を傷つけずLSCのみを標的とする特異的マーカーの同定が、AML根治の鍵とされてきました。
画期的な発見は、CD96が正常なHSC(CD34+CD38−)にはほとんど発現していないにもかかわらず、AML患者のLSC画分(Lin−CD34+CD38−CD90−)の大多数において高頻度かつ高レベルに発現していることです。
| 細胞表面マーカー | AML白血病幹細胞(LSC) | 正常造血幹細胞(HSC) | 臨床的意義 |
|---|---|---|---|
| CD34+/CD38−(基本骨格) | 陽性 | 陽性 | 特異性に欠ける共通マーカー |
| CD96(TACTILE)★ | 高発現(多数患者で陽性) | 陰性〜極低発現 | 高発現→導入化学療法への低反応性・予後不良と相関 |
| CD123(IL-3Rα) | 陽性 | 低発現 | 治療後骨髄での細胞数減少に関与 |
| CD33 | 陽性 | 骨髄系前駆細胞で陽性 | 複数マーカー発現でOS・PFS悪化と相関 |
★印:正常HSCとLSCの間に劇的な発現差異が確認されている理想的な治療標的マーカー
💡 用語解説:異種移植モデル(Xenograft)とは
ヒトのがん細胞または患者由来の細胞を、免疫機能が低下した(免疫不全の)マウスに移植してヒトのがんを再現する動物実験モデルです。AML研究ではRag2−/−γc−/−新生児マウスが用いられることが多く、ヒトAML細胞をCD96+画分とCD96−画分に分離して移植したところ、CD96+画分の細胞のみがレシピエントマウスの骨髄で強力な生着・白血病発症能力を示したことが、CD96をLSCマーカーとして確立する決定的な根拠となりました。
臨床的にも、診断時のCD34+CD38−細胞群におけるCD96発現率の高さは、導入化学療法に対する完全寛解(CR)率の低下や治療抵抗性と強い統計的相関を持つことが複数のコホート研究で実証されており、強力な予後不良予測因子として機能します。この正常幹細胞と白血病幹細胞間での劇的な発現差異により、CD96はAMLにおける理想的な治療標的分子と見なされています。
7. 自己免疫疾患との関連:CD96シグナルのシーソーモデル
免疫チェックポイントは、がんに対する過剰な免疫抑制を解除するための優れた標的となる一方で、自己免疫疾患においてはその機能低下(ブレーキの故障)が病態の引き金となります。CD96も例外ではなく、複数の自己免疫疾患との関連が報告されています。
強直性脊椎炎(AS)とIBDにおけるCD96機能不全
強直性脊椎炎(AS)は、HLA-B27などの遺伝的要因が関与する慢性炎症性疾患です。AS患者由来の末梢血を用いたトランスクリプトームおよびフローサイトメトリー解析において、健常者と比較してCD96(およびCD112R)の発現がCD4+T細胞上で有意に低下していることが明らかになりました。
CD96の発現低下は、細胞内シグナル伝達においてERKのリン酸化を異常に亢進させ、TNF-α・IL-23・IL-17A・IFN-γなどの炎症性サイトカインの過剰な分泌を引き起こします。これは、CD96のダウンレギュレーションが直接的に自己反応性T細胞の活性化を促し、ASの病因に寄与していることを明白に示しています。また、Th9細胞によるIL-9産生制御においても、CD96機能の低下(CD96lowサブセットの優位性)が潰瘍性大腸炎(UC)やクローン病などの炎症性腸疾患(IBD)における重篤な組織破壊と粘膜炎症の主要なドライバーであることが前臨床モデルで証明されています。
GWASメタ解析が示す相反するリスクパターン
💡 用語解説:GWAS(ゲノムワイド関連解析)とは
ゲノム全体にわたって何十万〜何百万ものSNP(一塩基多型)を同時にスキャンし、疾患リスクと関連する遺伝子多型を網羅的に同定する統計解析手法です。大規模なコホート(数万〜数十万人規模)が必要で、多因子疾患の遺伝的背景を理解するための最も強力なツールの一つです。複数の疾患にわたるクロスディスオーダーGWASメタ解析により、CD96近傍の遺伝子多型ががんリスクと自己免疫疾患リスクに「反対方向」の効果を持つことが確認されました。
乳癌・前立腺癌・卵巣癌などの癌(約24万症例)と7つの自己免疫/自己炎症性疾患(約11万症例)のGWASデータを統合した大規模なクロスディスオーダーメタ解析において、自己免疫疾患の発症リスクを高めるアレルは、同時に特定のがんに対しては防御的に働く(リスクを下げる)という「相反するリスクパターン」が確認されました。
⚖️ CD96シグナルのシーソーモデル
CD96シグナル低下・阻害
- NK/CD8+T細胞 過剰活性化
- IFN-γ・TNF-α・IL-9・IL-17産生↑
- 強力な抗腫瘍免疫・転移抑制
- 強直性脊椎炎・IBDリスク↑
CD96
CD96シグナル過剰・作動
- エフェクター細胞の機能不全(疲弊)
- 炎症性サイトカイン産生↓
- 腫瘍の免疫逃避・増殖の許容
- 自己免疫応答の抑制(リスク↓)
CD96の機能低下→抗腫瘍免疫は強化されるが自己免疫リスクも上昇。CD96の過剰活性化→腫瘍の免疫逃避を許すが自己免疫は抑制される。治療設計の際にこのトレードオフを意識することが重要。
💡 用語解説:irAE(免疫関連有害事象)とは
irAE(immune-related Adverse Events)とは、免疫チェックポイント阻害薬の投与によって免疫系が過剰に活性化した結果、正常な自己組織を攻撃することで生じる副作用の総称です。大腸炎・肺臓炎・肝炎・皮膚炎・内分泌障害など多彩な臓器に発症し得ます。CD96阻害薬(アンタゴニスト)をがん免疫療法として投与する際には、シーソーモデルが示すように自己免疫疾患の誘発(irAE)に特に留意が必要です。逆に、CD96作動薬(アゴニスト)が自己免疫疾患の治療アプローチとなり得ることも示唆されています。
8. 臨床開発の最前線
CD96の生物学的有望性を背景に、製薬業界はCD96を標的とするモノクローナル抗体および二重特異性抗体の開発に莫大な投資を行ってきました。しかし最新の臨床試験の動向は、創薬の難しさと新たな技術的パラダイムの台頭の両方を浮き彫りにしています。
8-1. Nelistotug(GSK6097608)の軌跡と戦略的撤退
GlaxoSmithKline(GSK)社はCD226/TIGIT/CD96軸を「次世代の免疫腫瘍療法の極めて有望な領域」と位置づけ、完全ヒトIgG1κモノクローナル抗体であるnelistotug(開発コード:GSK6097608)を開発しました。この抗体はCD96とCD155の相互作用を強力に阻害し、機能的活性のために完全なFc-FcγRの共エンゲージメントを必要とするよう設計されていました。
進行固形癌に対する単剤療法および抗PD-1抗体(dostarlimab)や抗TIGIT抗体(belrestotug)との併用療法を評価する第1/2相臨床試験が進められ、再発・転移性HNSCC(GALAXIES H&N-202試験)や非小細胞肺癌を対象としたプラットフォーム試験において多剤併用による相乗効果が期待されていました。
しかし、2025年第3四半期の決算報告においてGSK社はnelistotugの臨床開発を中止することを決定しました。これはnelistotug自体の安全性懸念というよりも、同社が共同開発していた抗TIGIT抗体(belrestotug)・抗TIM-3抗体(cobolimab)・抗PVRIG抗体(GSK4381562)といった関連免疫チェックポイント阻害薬の後期臨床試験での相次ぐ失敗に伴う、CD226関連軸全体からの戦略的撤退であると業界アナリストは分析しています。
8-2. 次世代アプローチ:BMS-986442(AGEN1777)の躍進
GSK社の撤退により、現在臨床開発の先頭を走るCD96標的薬は、Bristol Myers Squibb(BMS)社がAgenus社から最大13億2000万ドル(約1.32B USD)に及ぶマイルストーンを含む大型契約でライセンスを取得して開発中の「BMS-986442(旧名:AGEN1777)」です。
💡 用語解説:二重特異性抗体(Bispecific Antibody)とは
通常の抗体が1種類の標的にしか結合しないのに対し、二重特異性抗体は2つの異なる標的を1つの分子で同時に認識・遮断できるよう設計された次世代抗体です。BMS-986442はTIGITとCD96を同時に標的とすることで、両受容体が形成する協調的な抑制回路を一分子で断ち切ります。さらにFc領域が増強(Fc-enhanced)されており、腫瘍反応性T細胞の応答性向上とADCC(抗体依存性細胞傷害)活性を付加的に誘導する設計になっています。
AACR(米国がん研究会議)2024における前臨床データの発表では、BMS-986442が従来の抗TIGIT単一抗体と比較して、単剤療法および抗PD-1抗体との併用において優れた免疫活性化と抗腫瘍効果を実証したことが報告されました。現在、進行固形癌・非小細胞肺癌・胃癌などを対象として、ニボルマブ(Opdivo)および化学療法との併用を評価する第1b/2相臨床試験(NCT05543629)が進行中です。
8-3. AMLに対するCD96標的CAR-T細胞療法
固形腫瘍における免疫チェックポイント阻害とは全く異なるアプローチとして、AMLにおけるCD96のLSC特異的発現を利用したCAR-T細胞療法の開発が急速に進展しています。
💡 用語解説:CAR-T細胞療法とは
患者自身のT細胞を体外に取り出し、特定の腫瘍抗原を認識するよう遺伝子改変(キメラ抗原受容体:CARを搭載)した後、体内に戻す細胞療法です。CD19を標的としたCAR-T療法はB細胞性白血病・リンパ腫で革命的な治療成果を挙げています。AMLではCAR-T標的となる理想的な抗原が乏しかったですが、CD96がLSC特異的に高発現し正常HSCには発現しないため、オフターゲット毒性(骨髄抑制)を回避しながらLSCを選択的に根絶できる可能性が注目されています。
最新の前臨床研究では、CD96を標的とするCAR-T細胞が正常な造血系コロニー形成(HSPC機能)を阻害することなくAML細胞を特異的に排除することが示されています。さらに、単一抗原を標的とした際の抗原エスケープ(腫瘍が標的抗原を失い治療を回避する現象)を防ぐため、CD33やCLL-1などの他の骨髄系抗原とCD96を同時に標的とするデュアルターゲットCAR-T(Logic-gated systemsやアダプターCAR技術)の開発も盛んに行われています。
| 薬剤名 | 企業 | モダリティ | 対象疾患 | ステータス |
|---|---|---|---|---|
| Nelistotug (GSK6097608) |
GSK | 抗CD96モノクローナル抗体 | 固形がん・HNSCC | 開発中止 |
| BMS-986442 (AGEN1777) |
BMS(導出:Agenus) | TIGIT/CD96二重特異性抗体(Fc増強型) | 固形がん・NSCLC・胃がん等 | 第1b/2相 進行中 |
| CD96-CAR-T (CD33/CLL-1併用含む) |
学術研究機関 | 細胞療法(CAR-T) | 急性骨髄性白血病(AML) | 前臨床段階 |
データソース:OncologyPipeline・Agenus・Fierce Biotech・PubMed・BMS Study Connect
9. 臨床遺伝専門医からのメッセージ
よくある質問(FAQ)
🏥 遺伝子・がん免疫学について専門医に相談したい方へ
CD96をはじめとする免疫チェックポイント・遺伝子関連のご相談は、
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にどうぞ。
関連記事
参考文献
- [1] Chan CJ, et al. Coming of Age: CD96 Emerges as Modulator of Immune Responses. Front Immunol. 2018;9:1072. [Frontiers in Immunology]
- [2] Blake SJ, et al. TIGIT and CD96: New Checkpoint Receptor Targets for Cancer Immunotherapy. Immunol Rev. 2016;276(1):112-120. [Immunological Reviews]
- [3] Mittal D, et al. CD96 Is an Immune Checkpoint That Regulates CD8+ T-cell Antitumor Function. Cancer Immunol Res. 2019;7(4):559-571. [Cancer Immunology Research]
- [4] Jin L, et al. CD96 is a leukemic stem cell-specific marker in human acute myeloid leukemia. Proc Natl Acad Sci USA. 2006;103(9):3224-3229. [PNAS]
- [5] Lucca LE, et al. TIGIT/CD226 Axis Regulates Anti-Tumor Immunity. Pharmaceuticals (Basel). 2021;14(3):200. [MDPI Pharmaceuticals]
- [6] Hu Y, et al. Targeting CD96 overcomes PD-1 blockade resistance by enhancing CD8+ TIL function in cervical cancer. J Immunother Cancer. 2022;10(3):e003667. [Journal for ImmunoTherapy of Cancer]
- [7] Peng H, et al. CD96 expression determines the inflammatory potential of IL-9–producing Th9 cells. Proc Natl Acad Sci USA. 2018;115(13):E2969-E2978. [PNAS]
- [8] Gao S, et al. CD96 Downregulation Promotes the Immune Response of CD4 T Cells and Associates with Ankylosing Spondylitis. Front Immunol. 2022;13:901899. [PMC9234051]
- [9] Camargo A, et al. Mapping Inherited Genetic Variation with Opposite Effects on Autoimmune Disease and Four Cancer Types Identifies Candidate Drug Targets. Genes (Basel). 2025;16(5):575. [MDPI Genes]
- [10] Fierce Biotech. GSK abandons hopes for CD226 cancer therapies, dropping remaining phase 2 assets. 2025. [Fierce Biotech]
- [11] Agenus Inc. Agenus Announces Preclinical Data on BMS-986442 (AGEN1777) at AACR 2024. 2024. [Agenus Press Release]
- [12] Sallman DA, et al. CD96 as a therapeutic target for CAR T cell therapy in acute myeloid leukemia. PubMed. 2024. [PubMed]
- [13] Hosen N, et al. Cluster of differentiation 96 as a leukemia stem cell-specific marker and a factor for prognosis evaluation in leukemia. Oncol Lett. 2015. [PMC4487019]
- [14] Evaluation of CD96 Expression in Acute Myeloid Leukemia Patients: Relation to Prognosis and Induction Chemotherapy. QJM. 2024;117(Supplement 2). [Oxford Academic QJM]
- [15] Nguyen A, et al. The Immune Checkpoint Receptor CD96: A Local and Systemic Immune Modulator in Oral Cancer? Cancers (Basel). 2023;15(7):2126. [MDPI Cancers]
- [16] Sun J, et al. CD96 as a Potential Immune Regulator in Cancers. Front Oncol. 2022. [PMC9866520]
- [17] Wang F, et al. An Inhibitory Role for Human CD96 Endodomain in T Cell Anti-Tumor Responses. Cells. 2023;12(2):309. [MDPI Cells]
- [18] NCBI Gene. CD96 CD96 molecule [Homo sapiens (human)]. Gene ID: 10225. [NCBI Gene]
- [19] UniProt. CD96 molecule – Homo sapiens (Human). Entry: P40200 (TACT_HUMAN). [UniProtKB]
- [20] BMS Study Connect. A Study of BMS-986442 With Nivolumab With or Without Chemotherapy in Solid Tumors and Non-small Cell Lung Cancer (NCT05543629). [BMS Study Connect]