目次
サザンブロット Southern blot
サザンブロット Southern blotとは
サザンブロッティングは、1975年にエドウィン・サザンによって、DNAサンプル中の特定のDNA配列を検出する方法として紹介されました。この方法から生まれた他のブロッティング技術は、Northern(RNA用)、Western(タンパク質用)、Eastern(タンパク質の翻訳後修飾用)、South-Western(DNAとタンパク質の相互作用用)と呼ばれている。
ブロッティングとは?
ブロッティングは、分子生物学においてタンパク質や核酸の同定に用いられ、診断目的で広く利用されている。この技術は、ニトロセルロース膜やナイロンなどの支持体上に目的の分子を固定化する。また、ハイブリダイゼーション技術を用いて、特定の核酸や遺伝子を同定する。ブロッティング技術は、遺伝子発現のさまざまな段階におけるDNA、mRNA、タンパク質などの生体分子の同定に用いられるツールである。タンパク質合成には、DNAセグメントの発現が含まれ、それがmRNAに変換されてそれぞれのタンパク質が生成される。DNA、RNA、タンパク質などの分子は、生化学的分析の対象となり、ブロッティング技術を用いて分離される。細胞の場合、これらの分子は完全に存在しているので、ブロッティングの助けを借りて、他のすべての分子から特定の分子を認識することができる。ブロッティングは、目的の分子の混合物を、分子の大きさに基づいて分子を分離するゲルのブロックに通過させることで行われる。このようにして処理された分子は、適切な膜に強く押し付けられ、毛細管現象によってゲルから適切な膜(ナイロン、ニトロセルロース、PVDF)に分子が移される。膜に転写された分子の位置は変わることはない。
ブロッティングのサブタイプ
Northern、Western、Southernなどのブロッティングのサブタイプは、対象となる分子によって異なる。
サザンブロットはDNA分子を対象とする技法である。DNA配列がタンパク質分子の基礎またはコードである場合、サザンブロッティング技術を用いて目的の特定のDNA分子をブロッティングすることができる。遺伝子発現において、DNAがタンパク質生成のためのmRNAとして発現する場合、このプロセスはノーザンブロッティングによって特定することができる。最後に、コード化されたmRNAが関連するタンパク質を産生しますが、このタンパク質の同定はウェスタンブロッティングで行うことができます。
ブロッティングの理論的背景
ブロッティングのアプローチは、DNA/RNA/タンパク質の分離に一般的に用いられるゲル電気泳動の補助的なものと考えられ、その優れた分解力により再現性のある結果が得られる。これにより、分離の対象となった分子の組み合わせの中から特定の分子を検出することが可能である。多くの方法では、分離した分子をゲルから固い膜に移すステップがあるが、これはゲルと膜の間に溶液を浸透させることで実現している。
エレクトロブロッティングは、多孔質のアガロースゲルに比べ、多孔質でないポリアクリルアミドゲルからの転写に適しており、多くのメーカーから多面的な装置が提供されている。DNAやRNAの場合は、核酸標識プローブとのハイブリダイゼーションによって膜内の特異的な配列を検出するが、タンパク質の場合は標識抗体プローブを使用する。当初開発されたプロトコルでは、放射性同位元素で標識された放射性プローブをオートラジオグラフィーの手順で検出することができた。このプロセスでは、放射性物質から放射される崩壊のパターンを利用して、X線フィルム上に画像を生成する。この画像は、シンチレーションを利用したガス検出器や、リンイメージングを利用したシステムを利用することで、デジタル画像としても利用できる。放射能の影響を考慮して、蛍光試薬や化学発光試薬を用いた標識システムも開発されている。発光・蛍光を利用した方法は、感度が高く、バックグラウンドがないため、より正確な結果が得られると考えられている。また、RNAよりもDNAプローブを使用したり、従来のニトロセルロースに代わってナイロン膜を使用したり、転写時のDNA配列の再飽和を避けるために、本来は中性溶液であるはずの転写をアルカリ性溶液で行うなど、オリジナルの方法とは異なる変更が加えられている。また、大きな断片の転写率を上げるために、DNAを酸処理してサイズを小さくしている。当初のプロトコールで使用されていたゲルストリップやチューブゲルは使用されなくなり、代わりにゲルフォーマットが適用されている。オリジナルのプロトコルには多くの変更が加えられているが、現代のプロトコルはオリジナルのプロトコルの基本的な特徴のほとんどを保持しているため名称は変更されていない。
サザンブロッティングは、制限断片長多型のブロッティングによる検出に基づいたヒトゲノムの遺伝子マッピングのような多くの重要な研究に応用された。また、ヒトDNAの制限消化産物とミニサテライトプローブとのハイブリダイゼーションによるDNAフィンガープリントも初めて開発された。しかし、この方法の主な用途のほとんどは、より広範な事実やデータを提供し、しかも実施が容易なDNAシーケンスやポリメラーゼ連鎖反応(PCR)に変わっていった。しかし、それらが不得意とするコピー数の測定、PCRやDNAシーケンシングでは増幅や配列決定が困難な長鎖DNAの解析、二次元ゲル電気泳動でDNAの物理的形態を分離した後、特定の成分をブロッティングして検出するDNAの構造解析など、多くの分野でブロッティングがいまでも応用されている。
ブロッティングの一般的な手順
1. 試料をホモジナイズし、細胞や組織など様々なものから抽出したDNA/RNA/タンパク質を精製する。
2. 制限酵素を用いてDNAを断片化する。これはRNA(ノーザンブロット)では必要ない。
3. 電気泳動膜で目的の分子を分離する(DNA断片の場合はアガロースゲル)。RNAの場合は、ホルムアルデヒドを変性剤として使用したアガロースゲルで分離することができる。これは、ホルムアルデヒドがRNA分子の二次構造を拘束するために必要なことです。
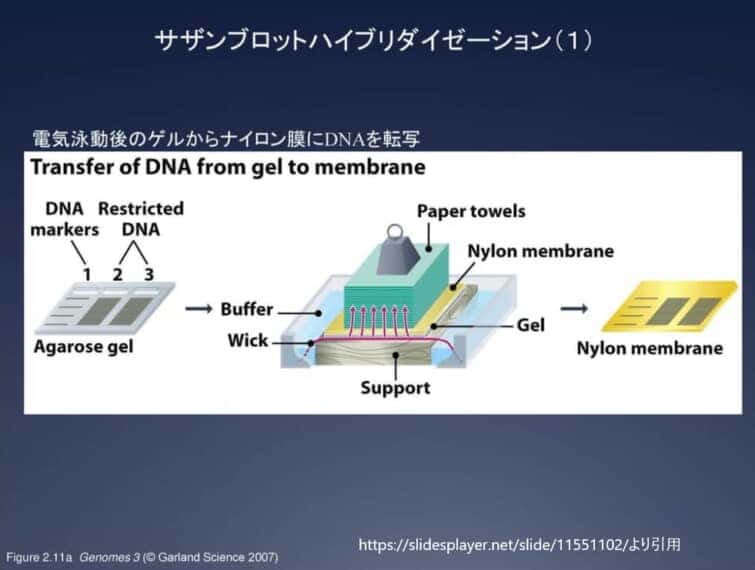
4. ゲルから分子(DNA/RNAフラグメント)をニトロセルロース膜/ナイロン膜に移す。
5. プレハイブリダイゼーション(ブロッキング)を行う。ナイロンメンブレンをブロッキング溶液である市販のブロッキングバッファー(PerfectHyb™ Plusバッファー)では、洗浄することは、非特異的なDNA相互作用をブロックするために必要であり、またバックグラウンドノイズを低減するのにも有効である。
プローブの調製には、32Pα標識dCTPで標識された新鮮なプローブDNAが用いられる。
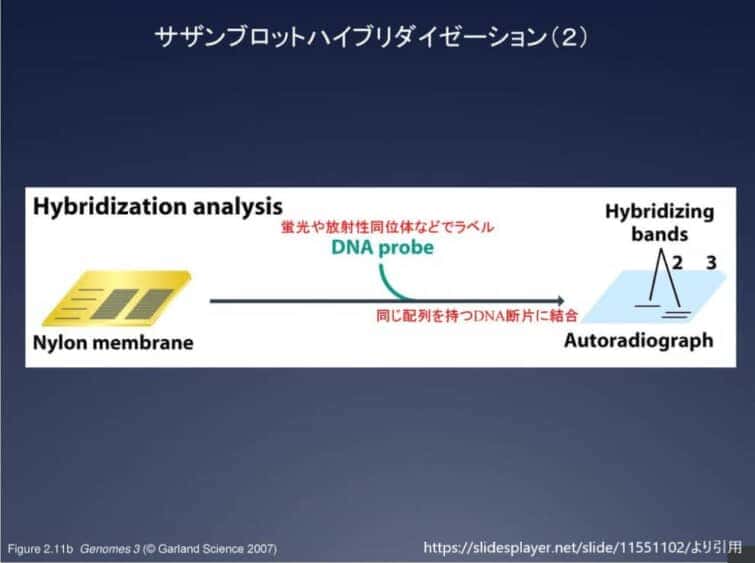
6. ブロットを特異的な標識プローブとインキュベートすることで、分子のハイブリダイゼーションまたは同定を行う。
7. プローブと目的のDNA/RNAの配列を検出。
この記事の著者:仲田洋美医師
医籍登録番号 第371210号
日本内科学会 総合内科専門医 第7900号
日本臨床腫瘍学会 がん薬物療法専門医 第1000001号
臨床遺伝専門医制度委員会認定 臨床遺伝専門医 第755号






