SHANKタンパク
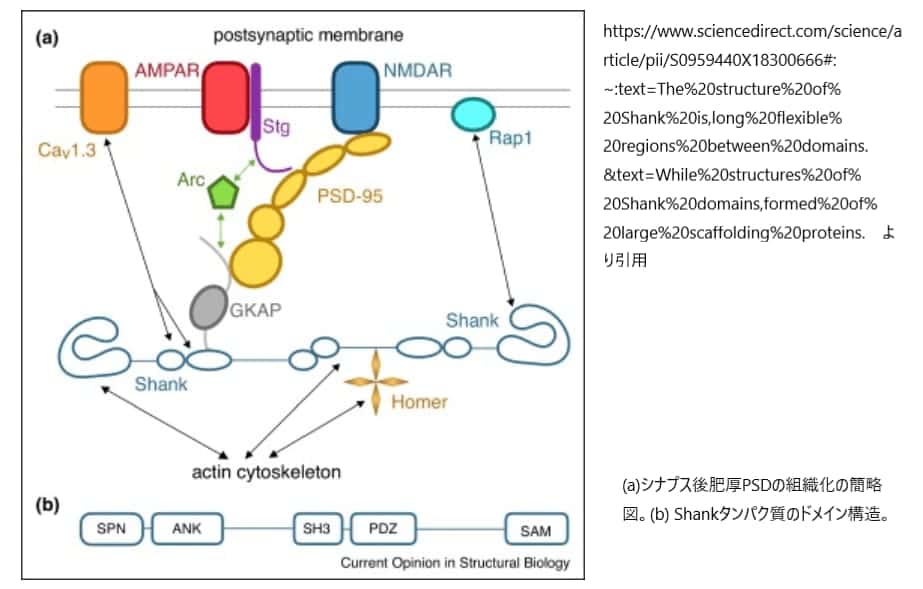
SHANK(SH3 and multiple ankyrin repeat domain protein)ファミリータンパク質は、興奮性シナプスのシナプス後肥厚(PSD)に見られる足場タンパク質である。PSDは樹状突起のシナプス後膜にある構造体で、神経伝達物質の受容体と制御因子を組織化するタンパク質の複雑な会合をする場所である。SHANKタンパク質は、シナプス後膜の受容体、シグナル伝達分子、細胞骨格タンパク質(AMPA、Neuroligin、NMDAグルタミン酸受容体など)と多量体を形成し、シナプス後肥厚PSDのマスターオーガナイザーとして機能している(文献)。シナプス後肥厚PSD内には300以上のシャンク分子が存在し、シナプス後肥厚内のタンパク分子全体の約5%を占める(文献)。シャンクは、作用制御タンパク質との結合に用いられるアンキリンリピートドメイン、AMPA受容体との結合に用いられるSrc homology 3(Sh3)ドメイン、Gタンパク質結合受容体との結合に用いられるPDZドメイン、複数のプロリン豊富なドメイン、シャンクの多量化を仲介するC末端のSAMドメインなどのタンパク質-タンパク質相互作用の5つのドメインを含んでいる(文献)。Shankは神経細胞の樹状突起スパインの成熟も媒介する(文献)。
Shank-3タンパク質の全長欠損は、AMPA受容体のシグナル伝達とスパインのリモデリングを減少させる。 Shank-3のハプロイン欠損マウスは、発情期の雌マウスとの交流において超音波発声が少なく、これは自閉症患者に見られる行動を連想させる。さらに、シャンクノックアウトマウスでは、樹状突起の発達が少なく、シナプス後肥厚PSDのサイズが小さくなり、GKAPタンパクとHormerタンパクのレベルが低下し、シナプスのシグナル伝達が大きく損なわれていることが判明した。
しかし、驚くべきことにShank-3の過剰発現も自閉症スペクトラム障害ASDを引き起こす可能性があり、自閉症は脳内の興奮性/抑制性神経細胞の不適切な比率によって引き起こされるという仮説を裏付ける(文献)可能性がある。
また、自閉症患者の幅広いmiRNA発現レベルを測定した論文では、レット症候群の原因であるMeCP2、ASDに関与する遺伝子NRXN-1、シャンク-3などASDに関わる遺伝子に対する異常なレベルのmiRNAが見つかり、自閉症におけるShank-3の役割に支持が集まった(文献)。Shank-3変異体ではAMPA受容体のシグナル伝達が著しく低下しているため、AMPA伝達を増強する化合物(AMPAkins)は、一部のASDの治療アプローチとして期待されている。






