プレニル化とは
プレニル化とは、疎水性のプレニル基を他の分子に付加する化学反応のことです。プレニル基は、炭素数5のイソプレン単位で構成される構造単位の総称であり、この基をタンパク質や他の有機分子に結合させることによって、その物質の物理化学的性質や生物学的機能を変化させることができます[3][4][7]。
プレニル化は、生体内での天然物の合成において重要な役割を果たしています。例えば、プレニル化はフラボノイドやテルペンインドールアルカロイドなどの生理活性物質の生合成に関与しており、これらの化合物は多様な生理活性を持つことが特徴です[2][5]。プレニル化によって、これらの化合物は組織への蓄積が高まり、体内滞留時間が延長されることが知られています[1]。
また、プレニル化は創薬においても重要であり、生体触媒によるドラッグデザインへの応用が期待されています。東京大学の研究グループは、インドール化合物にプレニル鎖を付加する酵素のメカニズムと立体構造を明らかにし、これにより有機合成では困難な反応を酵素を用いて行うことが可能になるとしています[2]。
プレニル化反応は、グリコシルホスファチジルイノシトールのようなタンパク質の修飾にも関与しており、タンパク質の局在や機能の調節に寄与しています[3][4]。プレニル化酵素は、特定のプレニル基を特定の受容体分子に結合させることで、生体内での精密な化学反応を可能にしています[8]。
- 参考文献・出典
-
[1] www.jstage.jst.go.jp/article/kagakutoseibutsu/53/2/53_71/_pdf
[2] www.u-tokyo.ac.jp/focus/ja/articles/a_00467.html
[3] ja.wikipedia.org/wiki/%E3%83%97%E3%83%AC%E3%83%8B%E3%83%AB%E5%8C%96
[4] www.weblio.jp/content/%E3%83%97%E3%83%AC%E3%83%8B%E3%83%AB%E5%8C%96
[5] kaken.nii.ac.jp/file/KAKENHI-PROJECT-24310156/24310156seika.pdf
[6] www.jstage.jst.go.jp/article/yukigoseikyokaishi1943/46/1/46_1_12/_pdf
[7] www.weblio.jp/wkpja/content/%E3%83%97%E3%83%AC%E3%83%8B%E3%83%AB%E5%8C%96_%E3%83%97%E3%83%AC%E3%83%8B%E3%83%AB%E5%8C%96%E3%81%AE%E6%A6%82%E8%A6%81
[8] www.rish.kyoto-u.ac.jp/lpge/research/research4.html
プレニル基とは
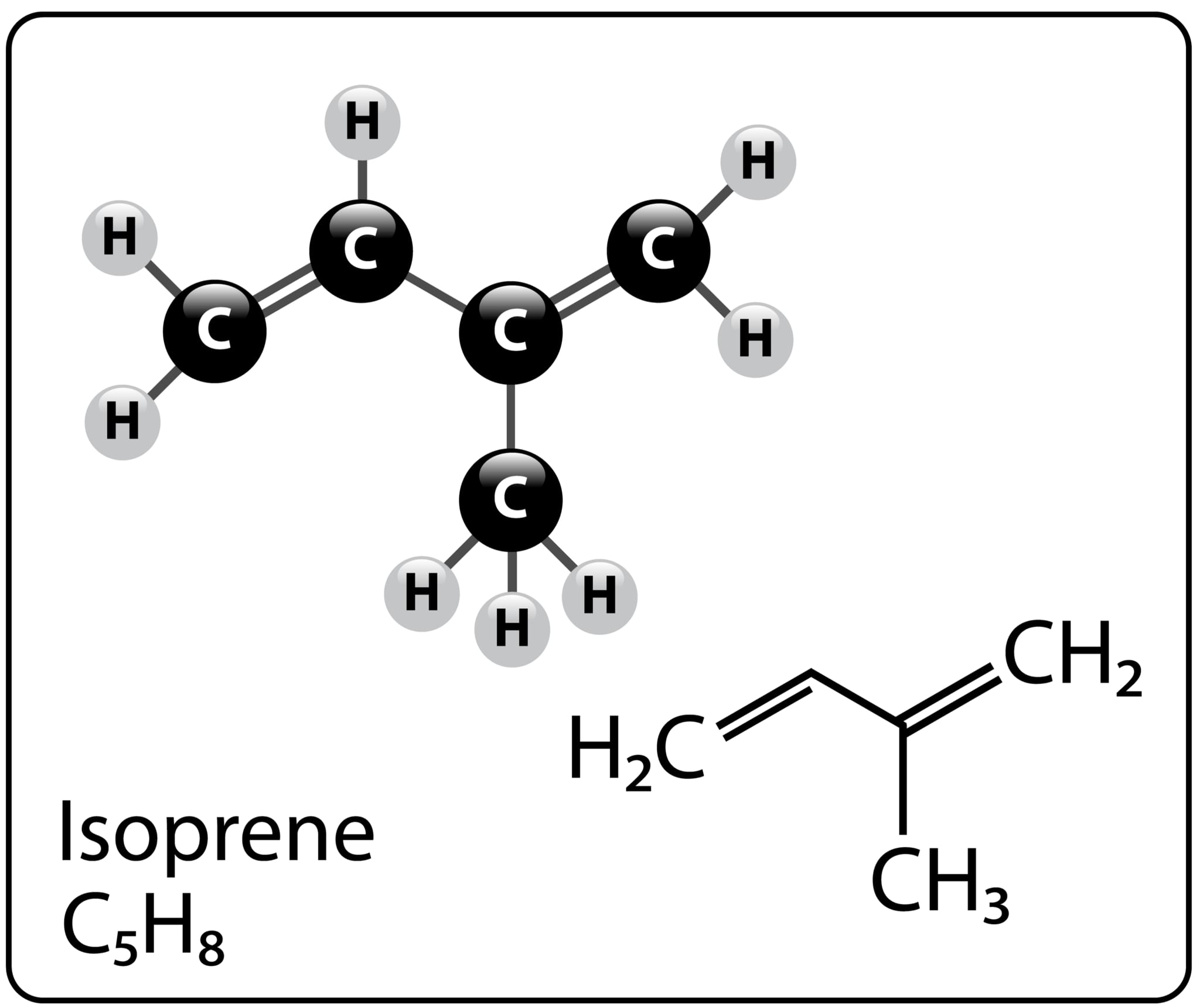
プレニル基は、イソプレン単位から構成される非常に重要な生化学的エンティティです。イソプレンは炭素数5のビルディングブロックであり、この基本的な単位が連結してさまざまな長さのプレニル基を形成します。それぞれのプレニル基は、連結されたイソプレン単位の数によって異なる名称が付けられます。これらのプレニル基は、タンパク質の修飾、細胞膜の構成、エネルギー代謝など、生物学的プロセスにおいて多岐にわたる役割を果たします。
以下はイソプレン単位の数に応じたプレニル基の一覧です:
– イソプレン数1 (C5): ジメチルアリル基 – この基は最も短いプレニル基で、特定の生合成経路で初期段階の修飾として見られます。
– イソプレン数2 (C10): ゲラニル基 – モノテルペンの合成に関与し、芳香性を持つ多くの植物のエッセンシャルオイルの主成分です。
– イソプレン数3 (C15): ファルネシル基 – セスキテルペンの合成やタンパク質のプレニル化に使われ、細胞膜のアンカーとして機能します。
– イソプレン数4 (C20): ゲラニルゲラニル基 – ダイテルペンの合成に用いられ、クロロフィルやカロテノイドなどの生合成に重要です。
– イソプレン数5 (C25): ゲラニルファルネシル基 – この長さのプレニル基は特定の生物学的役割に特化していますが、研究が進む必要があります。
– イソプレン数6 (C30): ヘキサプレニル基 – この基はトリテルペンの合成に関与し、ステロイドなどの生合成にも使用されます。
これらのプレニル基は、生物学的多様性と複雑性を示す素晴らしい例であり、生物がどのようにして様々な化学物質を合成し、利用しているかを理解するのに役立ちます。
タンパク質のプレニル化
タンパク質のプレニル化は細胞生物学において非常に重要な修飾の一つで、特に細胞膜への局在やタンパク質の機能調節に対して中心的な役割を果たします。ここでは、プレニル化のメカニズムとその生物学的目的についてさらに詳しく説明します。
● プレニル化のメカニズム
プレニル化は、特定のタンパク質のC末端にあるシステイン残基に、炭素数15のファルネシル基または炭素数20のゲラニルゲラニル基が結合する生化学的プロセスです。この結合はチオエーテル結合を介して行われ、タンパク質のC末端にある「CAAX」モチーフ(Cはシステイン、Aは脂肪族アミノ酸、Xは任意のアミノ酸)が認識シグナルとして機能します。
プレニル基を添加する酵素には大きく分けて二つあります:
– ファルネシルトランスフェラーゼ (FTase): X位置のアミノ酸がメチオニンやセリンの場合に活性化され、ファルネシル基を添加します。
– ゲラニルゲラニルトランスフェラーゼ I (GGTase I): X位置のアミノ酸がロイシンの場合に活性化され、ゲラニルゲラニル基を添加します。
● プレニル化の目的
プレニル化は以下のような複数の生物学的機能を担います:
1. 膜結合: プレニル基は高度に疎水性であり、タンパク質が細胞膜に結合しやすくなるため、細胞のシグナリングや物質輸送などの過程で局在性が重要になります。
2. タンパク質間相互作用の調節: プレニル化されたタンパク質は特定のドメインや膜結合部位において他の分子との結合が促進されることがあり、シグナル伝達経路の調節や細胞の応答性の変化に寄与します。
3. 機能的調節: タンパク質の活性やその他の生化学的プロパティがプレニル化によって修正されることがあり、細胞の成長、分化、アポトーシスなどのプロセスに影響を与えます。
プレニル化は細胞内でのタンパク質の正確な位置や機能を決定するための重要な修飾であり、多くの生理的および病理的プロセスにおいて中心的な役割を果たしています。このような理由から、特にがんや代謝疾患の研究において、プレニル化阻害剤が潜在的な治療薬として注目されています。
プレニル化後のタンパク質の修飾
プレニル化が完了した後に行われるさらなる修飾は、タンパク質がその機能を正しく果たすために不可欠です。これらの追加的な修飾ステップは、タンパク質の最終的な活性化、局在、およびタンパク質間相互作用に影響を及ぼします。
● プレニル化後の修飾の詳細
1. エンドプロテアーゼによる切断:
– タンパク質のプレニル化が完了すると、C末端の3つのアミノ酸は特定のエンドプロテアーゼ、特にhRce1によって切断されます。この切断は、プレニル化されたシステインがタンパク質の末端に露出するようにするために行われます。この過程はタンパク質が正しい構造と機能を獲得するのを助けます。
2. カルボキシメチル化:
– エンドプロテアーゼによる切断の後、プレニル化されたシステインは、pcCMTまたはIcmt(カルボキシメチルトランスフェラーゼ)という酵素によってカルボキシメチル化されます。この修飾は、タンパク質の疎水性をさらに高め、細胞膜への結合を強化します。これにより、タンパク質は細胞膜の特定の領域に効率的に局在することが可能になります。
3. Rab GGTase (GGTase II) によるプレニル化:
– 第3のプレニルトランスフェラーゼであるRab GGTase、またはGGTase IIは、特にRabタンパク質に対して作用し、これらのタンパク質が-CC、CXC、CCX、またはCCXXの配列で終わる場合にゲラニルゲラニルを結合させます。このプロセスのためには、Rabタンパク質がRabエスコートタンパク質(REP)と結合している必要があります。REPはRabタンパク質の正しい局在と機能を保証するために必要で、その遺伝子変異はコロイデレミアと呼ばれる網膜変性疾患を引き起こすことが知られています。
これらのプロセスを通じて、プレニル化されたタンパク質は細胞内で正しい位置に配置され、必要な機能を効果的に果たすことができます。これは、シグナル伝達、細胞成長、そして病気の進行など、多くの生物学的プロセスにおいて中心的な役割を果たします。








