目次
エピトープマッピングがいかにしてワクチンと抗体医薬の開発に革命をもたらすかを解説します。この入門記事は、科学者だけでなく一般の人々にも理解しやすい形で、エピトープマッピングの基本からその重要性までを網羅しています。
序章:エピトープとは?
エピトープ(抗原決定基とも呼ばれる)は、抗原の特定の部位であり、抗体やT細胞受容体などの免疫系の分子によって認識されます。エピトープはタンパク質、多糖類、核酸、リピドなど、様々な種類の抗原に存在することができますが、最も一般的にはタンパク質抗原のアミノ酸配列の一部分に見られます。
エピトープの特定は、ワクチン設計、診断ツールの開発、自己免疫疾患やアレルギーの研究において重要です。免疫反応の対象となるエピトープを特定することにより、より効果的なワクチンの開発や、特定の病原体を検出するための抗体ベースの診断試薬の開発が可能になります。また、エピトープの知識は、特定の抗体がクロスリアクティブであるかどうかを理解するのにも役立ち、異なる抗原に対する抗体の特異性を調べる際に重要です。
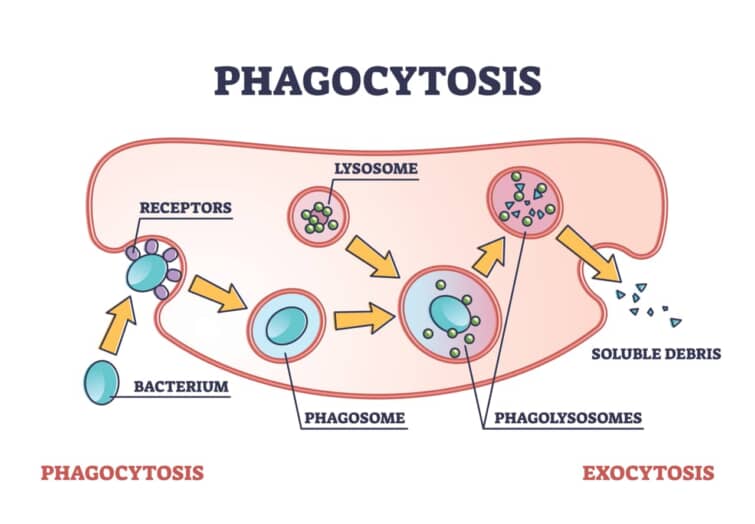
エピトープができるまで
抗原の一部を抗原提示細胞が細胞表面に提示するため、「エピ(外側)トープ(場所、位置)」と呼びます。
実際には、「エピトープ」の語源を直接「外側の場所」または「位置」と解釈するのは少し誤解があります。エピトープという用語は、抗原の一部である特定の部位を指し、免疫系が認識できる部分、つまり抗体やT細胞受容体が特異的に結合する部位を意味します。この結合は免疫応答を引き起こすきっかけとなります。
説明にあるプロセスは、免疫応答の中で抗原提示という重要なステップを説明しています。病原体は、宿主の免疫系によって異物と認識され、様々なメカニズムで処理されます。ウイルスのような小さな病原体はエンドサイトーシスによって細胞内に取り込まれます。一方、細菌やカビ、寄生虫などの比較的大きな病原体は、マクロファージや好中球などの食細胞によるファゴサイトーシスによって取り込まれ、消化されます。
消化された病原体の断片(エピトープを含む)は、MHC(主要組織適合性複合体)分子によって細胞表面に提示されます。これにより、T細胞はこれらのエピトープを認識し、適切な免疫応答を引き起こすことができます。抗原提示細胞が抗原の一部を細胞表面に提示することによって、免疫系は病原体に対する特異的な反応を開始することができるのです。
したがって、「エピトープ」という用語は、抗原の認識可能な部位を指しますが、その名前は直接的に抗原提示細胞による抗原の提示プロセスや位置から来ているわけではありません。それでも、この説明はエピトープが免疫系においてどのように機能するかについての理解を深めるのに役立ちます。
エピトープが受容体に結合すると
エピトープによるT細胞の活性化とその後の免疫応答についての説明には、いくつか修正すべき点があります。T細胞、B細胞、および液性免疫応答の役割と機能に関して、より正確な情報を提供します。
● T細胞とB細胞の相互作用
エピトープがT細胞によって認識されると、特にCD4+ ヘルパーT細胞は、免疫応答を調節し、強化する重要な役割を果たします。これらのヘルパーT細胞は、B細胞と相互作用し、B細胞が抗体を産生する形質細胞へと分化する過程を促進します。また、特定の抗原に対する記憶を持つメモリーB細胞の形成を支援します。これにより、将来同じ抗原に再び曝露された場合に、迅速な免疫応答が可能になります。
● 液性免疫応答
液性免疫応答は、主に抗体によって仲介される免疫応答です。B細胞が産生した抗体は、血液やその他の体液を介して病原体を中和したり、病原体を食細胞に認識させるマーキング(オプソニン化)を行うことで、免疫系が病原体をより効率的に除去できるようにします。
● CD4+ T細胞とCD8+ キラーT細胞
CD4+ T細胞は主にヘルパーT細胞として知られており、免疫応答の調節に関わります。これらは直接細胞を殺す機能は持ちません。一方で、キラーT細胞は正確にはCD8+ サイトトキシックT細胞と呼ばれ、病原体に感染した細胞を直接攻撃して破壊する機能を持っています。CD8+ T細胞は、病原体に感染した細胞の表面に提示されたエピトープを認識し、その細胞を殺すことにより、感染の拡散を防ぎます。
● 結論
したがって、CD4+ T細胞は「キラーT細胞」として機能するわけではなく、その役割は主に免疫応答の調節とB細胞の活性化にあります。CD8+ T細胞が実際の「キラー」または「サイトトキシック」機能を持つT細胞です。免疫系は非常に複雑で、細胞間相互作用が免疫応答の質と速度を決定する重要な要素です。
T細胞のうんちく
T細胞の分化とその教育過程は、胸腺で行われる複雑なプロセスです。T細胞が成熟する過程で、それらはMHC(主要組織適合性複合体)分子に対する特異性を獲得し、CD4+ T細胞またはCD8+ T細胞へと分化します。この分化プロセスは、T細胞が効率的に免疫応答を行えるようにするための「教育」の一環です。
● CD4+ T細胞とCD8+ T細胞の分化
– CD4+ T細胞: 主にヘルパーT細胞として機能し、免疫応答を調節します。CD4+ T細胞はMHCクラスII分子を提示する抗原提示細胞と相互作用します。MHCクラスII分子は通常、専門の抗原提示細胞(例えば、樹状細胞、マクロファージ、B細胞)の表面に発現しています。CD4+ T細胞は、これらの抗原提示細胞から提示される抗原を認識し、B細胞の抗体産生を促進したり、他の免疫細胞を活性化するシグナルを送ることで、免疫応答を強化します。
– CD8+ T細胞: サイトトキシックT細胞またはキラーT細胞として知られ、感染細胞やがん細胞を直接殺す機能を持ちます。CD8+ T細胞はMHCクラスI分子に結合します。MHCクラスI分子はほとんどの核を持つ細胞の表面に発現しており、細胞内で生成された抗原(例えば、ウイルスのペプチド)を提示します。CD8+ T細胞は、これらの細胞が提示する異常なペプチドを認識し、感染細胞や異常細胞を排除します。
● 胸腺におけるT細胞の教育
T細胞は、胸腺内で二つの主要な選抜過程を経ます:正の選抜と負の選抜です。これらの過程を通じて、自己反応性を持たず、かつMHC分子に適切に反応するT細胞のみが成熟し、末梢組織へと放出されます。
– 正の選抜: T細胞が自己のMHC分子に適度に結合できる能力を獲得します。これに失敗したT細胞はアポトーシスを起こします。
– 負の選抜: 自己抗原に対して過剰に反応するT細胞が排除されます。これにより、自己免疫反応のリスクが減少します。
CD4とCD8の補助受容体は、T細胞がMHC分子と効果的に相互作用するのを助け、T細胞受容体(TCR)のシグナル伝達を強化する役割を果たします。これにより、T細胞は特定の抗原に対して特異的な免疫応答を行うことができます。CD4とCD8の受容体は、T細胞がMHCクラスIIまたはMHCクラスI分子を持つ細胞との相互作用を最適化することにより、免疫系の精度と効率を高めます。
● T細胞受容体(TCR)との相互作用
T細胞受容体(TCR)は、特定の抗原エピトープとMHC分子の複合体に対して高度に特異的です。CD4+ T細胞やCD8+ T細胞が適切に分化し、成熟することで、これらの細胞は免疫応答中に特定のターゲットを認識し、適切な行動を取ることが可能になります。TCRと補助受容体(CD4またはCD8)の協調作用により、T細胞は抗原を認識し、活性化されると、サイトカインの放出、細胞増殖、または感染細胞の殺傷などの免疫応答を引き起こします。
● 免疫応答の調節
CD4+ T細胞は、異なるサブセット(Th1、Th2、Th17、Tregなど)に分化することができ、これにより様々な種類の免疫応答が調節されます。例えば、Th1細胞は細胞性免疫応答を促進し、病原体に感染した細胞の排除を助けるのに対し、Th2細胞は液性免疫応答を促進し、寄生虫の感染に対抗したり、アレルギー反応に関与します。Treg(調節性T細胞)は、免疫応答を抑制し、自己耐性を維持することで自己免疫疾患の発症を防ぎます。
※覚え方 2×4=8 1×8=8 つまりMHCクラスIIはCD4と、MHCクラスIはCD8と対応します。
正確に説明されています。T細胞の成熟と機能には複数の段階があり、胸腺を離れた後のナイーブT細胞の行動と活性化は免疫応答の効率性と特異性を確保するために重要です。ここでのポイントをさらに明確にします。
● ナイーブT細胞の移動と活性化
胸腺を離れたナイーブCD4+T細胞とCD8+T細胞は、血液とリンパ系を介して体を巡ります。彼らがリンパ節、脾臓、および粘膜関連リンパ組織(MALT)などの二次リンパ組織に到達すると、そこで樹状細胞などの抗原提示細胞(APC)によって提示される特異的抗原(エピトープ)と遭遇します。ナイーブT細胞がその特異的抗原を認識すると、それに応じてエフェクターT細胞に分化し、免疫応答を展開します。
● エフェクターT細胞の役割
– CD8+ T細胞(細胞傷害性T細胞): これらのT細胞は、感染細胞やがん細胞が提示するエピトープをMHCクラスI分子を介して認識します。活性化された細胞傷害性T細胞は、感染した細胞を直接殺すことにより、感染の拡大を防ぎます。
– CD4+ T細胞(ヘルパーT細胞): CD4+ T細胞は、MHCクラスII分子を持つ抗原提示細胞から抗原を提示されることで活性化されます。活性化されたヘルパーT細胞は、サイトカインの放出により他の免疫細胞の活動を促進したり、B細胞に抗体産生を指示するなど、免疫応答を調節します。
● 抗原提示の特異性
– MHCクラスI分子は、ほぼ全ての核を持つ細胞表面に存在し、細胞性免疫応答を担うCD8+ T細胞への抗原提示に関与します。
– MHCクラスII分子は、樹状細胞、マクロファージ、B細胞など限られたプロフェッショナル抗原提示細胞の表面に発現し、液性免疫応答と細胞性免疫応答の両方を調節するCD4+ T細胞への抗原提示に重要です。
これらのプロセスにより、免疫系は非常に多様な抗原に対して迅速かつ効果的に反応することができ、感染の拡大を防ぎながら、体を保護することができます。
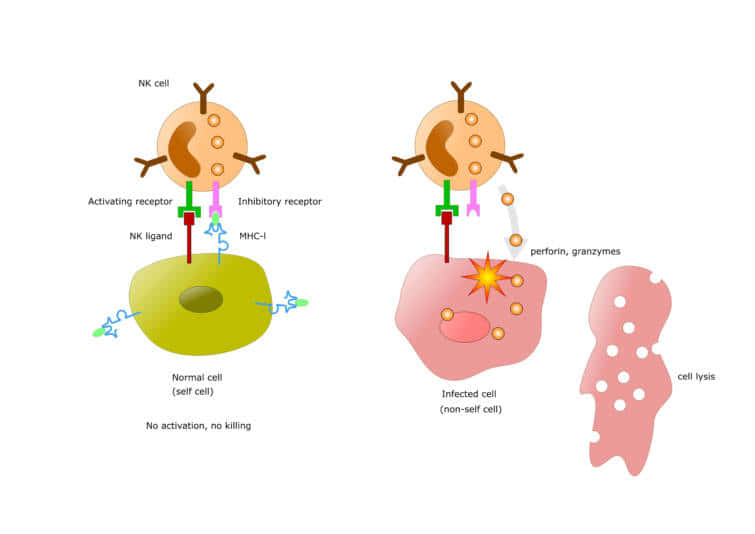
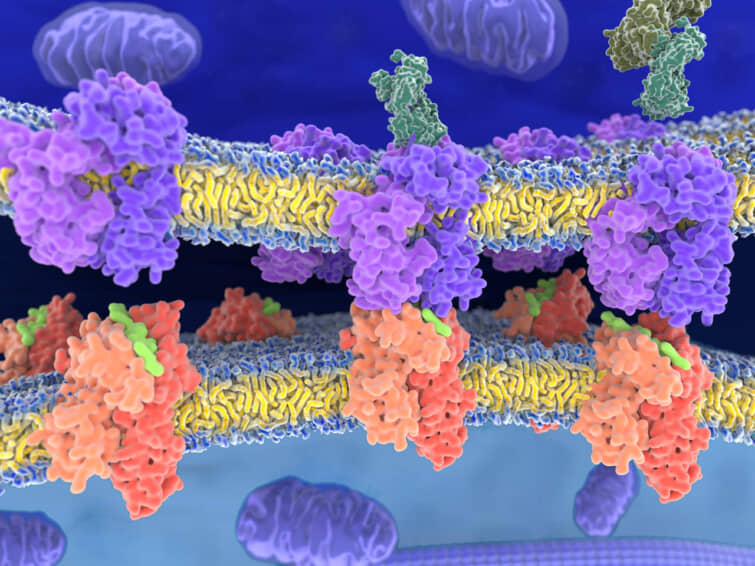
エピトープとT細胞受容体の結合はMHCクラスIIと呼ばれる分子を通じて行なわれます。
エピトープと呼ばれる部分はこの図では黄緑であらわされています。
エピトープと受容体がこのパズル(鍵と鍵穴)のような組み合わせで結合すると、最終的には抗体の産生が促進されます。こうして作られる抗体は、抗原受容体に結合したエピトープに特異的に結合するように産生されます。
つまり、エピトープは、特異的な抗体によって認識される抗原の領域でもあり、抗体は抗原のエピトープと同じアミノ酸配列(パラトープ)に結合した後、宿主生物から抗原を除去します。エピトープに結合する抗体上の領域はパラトープと呼ばれます。
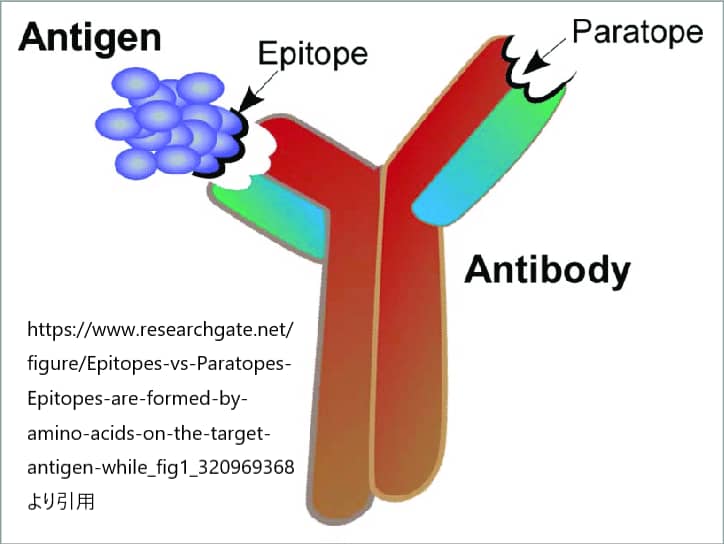
多くの抗原は、その表面にいくつもの異なるエピトープを持っている
多くの抗原は、その表面にいくつもの異なるエピトープを持っているのですが、これらのエピトープはそれぞれ、免疫細胞の異なる抗原受容体と相互作用することができます。特定病原体に対する免疫を獲得したヒトの血清には、通常、抗原表面の異なるエピトープに結合することができる抗体が混在しています。
また、同じエピトープを標的とする抗体でも、立体構造が違えばエピトープと結合する能力(親和性)は異なります。
エピトープは、抗原決定基とも呼ばれています。エピトープは通常、非自己のペプチドです。しかし、自己免疫疾患の場合には、宿主の配列が免疫系によってエピトープとして認識されることがあります。
エピトープの長さは一般的に5~6アミノ酸程度です。
エピトープの種類
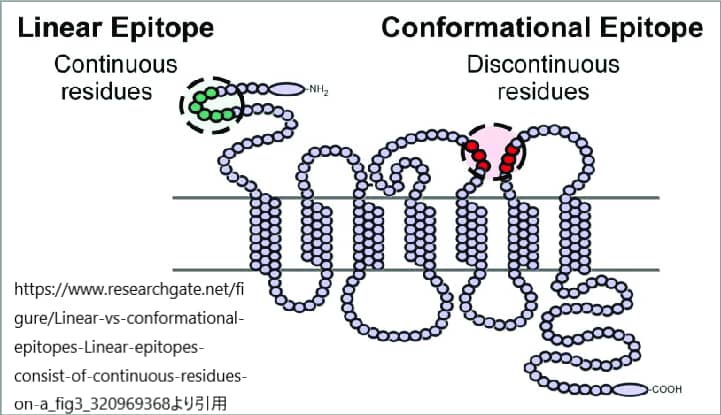
エピトープには、コンフォメーション型、線形型、不連続型の3種類があります。この分類は、エピトープの構造と抗体のパラトープとの相互作用に基づいています。
立体構造エピトープ(conformational epitope)
コンフォーマルエピトープは、互いに離れたアミノ酸残基の相互作用によって形成される。コンフォーメーションエピトープの数は分からないくらい多いものです。
線状エピトープ
線状エピトープは、その一次構造(アミノ酸の配列)だけではなく、存在する他の残基によっても決定されます。抗原のより遠くにあるアミノ酸残基や、一次構造の脇にあるアミノ酸残基が、線状エピトープの三次元的なコンフォメーションに影響を与えます。
不連続エピトープ
不連続エピトープは、構造上互いに近接しているのではなく、タンパク質の折り畳みの折りたたみ部分に集合したタンパク質の一部分からなります。このクラスのエピトープは、コンフォメーション部分と線状部分の両方を含むことができる。これまでのいろいろな研究から得られたデータによると、ほとんどの抗原抗体結合は不連続なエピトープ部位で起こるとされています。感染防御抗体(ワクチンに誘導される抗体はこれに当たります)は特に不連続エピトープに対する抗体であると考えられています。
病原体特異的な記憶に基づく免疫反応
T細胞もB細胞も病原体に特異的な記憶に基づいて免疫学的反応を行います。
B細胞のエピトープは、抗体や免疫グロブリンが結合する抗原の部分です。
T細胞エピトープは、抗原提示細胞の表面に存在し、主要組織適合性複合体分子に結合しています。
似たようなエピトープに別の病原体に対する抗体のパラトープやT細胞受容体のエピトープ結合部位が反応してしまうことがあり、これを交差反応といいます。たとえば、SARS-CoV-2(新型コロナウイルス)は従来のコロナウイルスに対する免疫の記憶がある人では交叉反応することがあります。
第1章 エピトープマッピングとは?
エピトープマッピングの基本概念
エピトープマッピングは、抗体が特定の抗原のどの部分に結合するかを特定する技術です。このプロセスは、ワクチンや抗体医薬の開発において重要な役割を果たします。エピトープは、抗原の表面に存在する小さな領域であり、特定の抗体によって認識されます。エピトープマッピングにより、科学者は抗体がどのエピトープに反応するかを正確に識別でき、これによって病原体に対するより効果的なワクチンや治療法の開発が可能になります。この技術は、免疫応答の理解を深め、疾患に対する新しい治療戦略の設計に不可欠です。エピトープマッピングは、分子レベルでの疾患と免疫系の相互作用の理解を助けるため、生物医学研究において中心的な技術となっています。
ワクチンと抗体医薬開発における役割
エピトープマッピングは、ワクチンと抗体医薬の開発において中核的な技術です。この技術により、病原体に対する特定の免疫応答を引き起こすエピトープを特定し、効果的なワクチンや治療薬を設計することが可能になります。ワクチン開発においては、エピトープマッピングによって最も免疫原性が高く、安全なエピトープを同定し、これらを基にワクチンを設計することで、体が特定の病原体を識別し、効果的に防御することを学ぶよう促します。一方、抗体医薬の開発においては、エピトープマッピングを通じて病原体または疾患関連分子の特定部位に結合する抗体を同定または設計することができ、これにより疾患の進行を遅らせたり、抑制する効果的な治療法を生み出すことができます。したがって、エピトープマッピングは、病気の予防と治療の両方において、より精密で個別化されたアプローチを可能にする革新的な技術として位置づけられています。
第2章 エピトープマッピングの方法と技術
主な技術手法:ペプチドアレイ、T細胞エピトープマッピング
エピトープマッピングには、ペプチドアレイとT細胞エピトープマッピングという二つの主要な技術手法があります。
ペプチドアレイは、数千から数万の異なるペプチド配列を固定化したチップやスライド上で、特定の抗体との相互作用を一度にスクリーニングする技術です。この方法により、大規模なライブラリから特定の抗体に対するエピトープを効率的に同定することが可能になります。ペプチドアレイは、抗体の特異性を詳細にマッピングすることができるため、抗体医薬の開発や疾患の診断マーカーの同定に広く利用されています。
T細胞エピトープマッピングは、T細胞の免疫反応を誘発するエピトープを同定する方法です。この技術は、細胞性免疫応答に関与するT細胞エピトープの特定に焦点を当てています。T細胞エピトープマッピングにより、ワクチンの設計において、強力な細胞性免疫反応を引き起こす可能性のあるエピトープを特定できます。この手法は、特に細胞媒介型免疫応答が重要な役割を果たす感染症やがんのワクチン開発において、極めて有用です。
これらの技術手法により、エピトープマッピングは抗体の特異性を理解し、ワクチンや治療薬の開発を加速するための強力なツールとなっています。
技術の進化:array based、Biacore、RayBiotechなど
エピトープマッピング技術の進化は、研究者が抗原と抗体の相互作用をより精密に分析できるようにしました。array based技術、Biacore、RayBiotechなどの先進的な手法は、この分野の進歩に大きく貢献しています。
Array based(アレイベース)技術は、固定化された数千から数万の異なるバイオモレキュール(例えば、ペプチドやタンパク質)を利用して、同時に多数の相互作用を解析できる高スループットなプラットフォームを提供します。この技術は、特にエピトープの広範なスクリーニングとマッピングに有用であり、効率的に大量のデータを生成することができます。
Biacoreは、表面プラズモン共鳴(SPR)技術を利用した分析装置であり、リアルタイムでの分子間相互作用の分析を可能にします。Biacoreシステムは、特定の抗体と抗原の結合親和性と動力学を精密に測定することができ、エピトープの特定に加えて、抗体の機能的特性を評価するのにも用いられます。
RayBiotechは、特にサイトカイン、増殖因子、アドヘション分子などの生物学的に重要なタンパク質の分析に焦点を当てた製品とサービスを提供しています。RayBiotechのアレイ技術は、これらの分子の相互作用を包括的に解析し、疾患のメカニズムの理解やバイオマーカーの同定に貢献します。
これらの技術は、エピトープマッピングの精度と効率を飛躍的に向上させ、研究者が新しいワクチンや治療薬の開発を加速できるようにしています。技術の進化は、より複雑な生物学的相互作用の理解を深め、将来の医療に革命をもたらす可能性を秘めています。
第3章 エピトープマッピングの応用事例
新型コロナウイルスワクチン開発の事例
新型コロナウイルス(COVID-19)ワクチン開発は、エピトープマッピング技術の応用が急速に進んだ顕著な事例です。この病原体に対するワクチンの迅速な開発と展開は、世界的なパンデミックに対する科学界の迅速な対応を示しています。
エピトープマッピングは、COVID-19ワクチン開発の初期段階で重要な役割を果たしました。研究者たちは、SARS-CoV-2(新型コロナウイルスの原因ウイルス)のスパイクタンパク質に焦点を当て、このタンパク質に含まれるエピトープが人間の免疫系によってどのように認識されるかを詳細に分析しました。スパイクタンパク質は、ウイルスがヒト細胞に侵入する際に重要な役割を果たすため、このタンパク質に結合し中和する能力を持つ抗体を誘導できるエピトープの同定は、有効なワクチン候補の設計に不可欠でした。
ペプチドアレイやT細胞エピトープマッピングなどの技術を用いて、研究者たちは数多くの潜在的なエピトープを迅速にスクリーニングし、特定のエピトープが免疫応答を効果的に引き起こすかどうかを評価しました。これにより、免疫系が強力に反応する特定のエピトープを含むワクチン設計の指針が得られました。
さらに、エピトープマッピングはワクチンの安全性と有効性の評価にも寄与しました。特定のエピトープが免疫系によってどのように認識されるかを理解することで、不要な免疫反応や副作用のリスクを最小限に抑えることが可能になりました。
COVID-19ワクチンの開発と展開は、エピトープマッピングが現代のワクチン科学においていかに不可欠かを明確に示す事例となりました。この成功は、将来の感染症対策におけるエピトープマッピングの価値を強調し、新たなワクチンや治療薬の開発におけるその応用可能性を広げています。
抗体医薬におけるエピトープマッピングの利用
エピトープマッピングは抗体医薬の開発において、疾患治療の効果を最大化し副作用を最小限に抑えるための重要な技術です。このプロセスを通じて、特定の病原体や疾患関連タンパク質に対する抗体の結合部位、すなわちエピトープを正確に特定します。これにより、高い特異性と親和性を持つ抗体を設計し、疾患の治療における標的としてのポテンシャルを高めることができます。
抗体医薬は、特定の疾患標的に対して高度に特異的な抗体を使用して、病気を治療する薬剤です。エピトープマッピングを利用することで、研究者は疾患標的上のどの部位が抗体によって認識されるべきかを決定し、その情報をもとに、疾患標的に対する強力な結合能力を持ち、治療効果を最大限に発揮する抗体を設計することができます。
この技術は、特にがんや自己免疫疾患、感染症といった病態に対して、治療薬の開発に革命をもたらしました。たとえば、特定のがん細胞の表面タンパク質に特異的に結合するエピトープを識別することで、そのがん細胞を標的とする抗体医薬を開発することが可能になります。これにより、正常な細胞に対する影響を最小限に抑えつつ、がん細胞を効果的に攻撃できる治療法を提供します。
また、エピトープマッピングは抗体医薬の安全性の評価にも貢献します。特定のエピトープに対する抗体の結合が予期せぬ免疫反応や副作用を引き起こさないよう、綿密な検討が可能になります。これにより、開発初期段階でのリスク評価が改善され、より安全な抗体医薬の開発が促進されます。
エピトープマッピングの進化は、抗体医薬の特異性、効果、安全性を高めることに直結しており、この技術は今後も疾患治療の新たな道を切り開いていくことでしょう。
第4章 エピトープマッピングの利点と課題
ワクチン・医薬品開発におけるメリット
エピトープマッピングは、ワクチンと医薬品開発において数多くのメリットを提供します。この技術を活用することで、疾患に対するより効果的かつ安全な治療法の開発が可能になります。
1. 効果的なワクチン設計: エピトープマッピングによって、免疫系が強く反応する特定のエピトープを同定できます。これにより、特定の病原体に対する高い保護効果を持つワクチンを設計することが可能になり、疾患の予防効果を最大化します。
2. 高特異性抗体医薬の開発: 疾患関連タンパク質の特定のエピトープに結合する抗体を開発することで、高い特異性を持つ治療薬を生み出すことができます。これは、正常な細胞に対する副作用を最小限に抑えながら、病気を効果的に治療するために不可欠です。
3. 迅速な開発プロセス: エピトープマッピング技術の進歩により、ワクチンや医薬品の標的となるエピトープの同定が以前に比べて迅速に行えるようになりました。これにより、研究開発の時間とコストを大幅に削減することが可能になります。
4. 安全性の向上: エピトープマッピングを通じて、ワクチンや治療薬が引き起こす可能性のある免疫反応を事前に評価することができます。これにより、予期せぬ副作用のリスクを早期に特定し、安全な医薬品の開発を促進します。
5. 個別化医療への応用: 個々の患者の免疫反応の差を考慮したワクチンや治療薬の開発が可能になります。エピトープマッピングにより、特定の個人に対して最も効果的な免疫反応を引き起こすエピトープを同定し、個別化された治療戦略を設計することができます。
エピトープマッピングは、これらのメリットにより、ワクチンと医薬品開発の分野で革新的な進歩を促進しています。この技術の活用は、疾患の予防と治療の新たなパラダイムを切り開くことでしょう。
現在の課題と解決への取り組み
エピトープマッピング技術はワクチンや抗体医薬の開発に革命をもたらしているものの、いくつかの課題が存在します。これらの課題に対する解決策の探求は、技術のさらなる発展と応用範囲の拡大を促進しています。
### 現在の課題
1. 複雑なエピトープの同定: 線形エピトープは比較的同定しやすいですが、立体的な構造を持つコンホメーショナル(立体構造)エピトープの同定は技術的に困難です。これらは免疫反応において重要な役割を果たすことが多く、その同定は精密な分析を要求します。
2. 高スループット分析の限界: 大規模なエピトープスクリーニングには高いコストと複雑なデータ解析が伴います。効率的なスクリーニング方法の開発とデータ解析ツールの改善が求められています。
3. 個体差への対応: 人々の免疫系は多様であり、同一のエピトープに対しても異なる反応を示すことがあります。この個体差に対応するためのエピトープマッピングは、特に個別化医療の文脈で重要です。
### 解決への取り組み
1. 先進的な分析技術の開発: コンホメーショナルエピトープの同定には、高度な技術が必要です。最新の分子イメージング技術や高解像度質量分析法などが、これらのエピトープの同定に対する解決策として開発されています。
2. AIと機械学習の活用: 大規模なデータセットの解析とエピトープ予測には、人工知能(AI)と機械学習が有効です。これらの技術を用いることで、エピトープの同定と予測を高速かつ正確に行うことが可能になります。
3. 個別化されたエピトープマッピングの推進: 個々の患者の免疫応答の差異を考慮したエピトープマッピングの手法が開発されています。これには、個人の免疫細胞を用いたin vitro(試験管内)での試験や、遺伝子情報を基にしたエピトープの予測が含まれます。
4. 国際的なコラボレーション: 複雑な課題に対処するため、世界中の研究機関や企業が協力し、共有データベースの構築や研究成果の共有を進めています。これにより、エピトープマッピング技術の発展が加速されています。
第5章 今後のエピトープマッピングの展望
技術革新の可能性
エピトープマッピングの分野は、技術革新によって大きな可能性を秘めています。これらの革新は、ワクチンや治療薬の開発を加速し、より効率的で個別化された医療へと道を開くことが期待されます。
1. ナノテクノロジーの応用: ナノテクノロジーを活用することで、より精密なエピトープマッピングが可能になります。ナノスケールでの操作と分析により、従来の方法では捉えきれなかったエピトープの特性や、微細な抗原-抗体相互作用を解明することができるようになります。
2. 高度なイメージング技術: 単分子イメージング技術や高度な顕微鏡技術の発展により、エピトープと抗体の相互作用を実時間で観察し、これまでにない詳細レベルでの分析が可能になります。これにより、エピトープの特定とその機能的特性の理解が深まります。
3. AIと機械学習の進化: AIと機械学習のアルゴリズムは、エピトープの予測と解析を効率化します。これらの技術は、膨大なデータセットから有意義な情報を抽出し、新たなエピトープの発見や、ワクチンおよび治療薬候補の迅速なスクリーニングを可能にします。
4. 多様な疾患への応用拡大: 技術革新は、がんや自己免疫疾患、感染症だけでなく、アレルギーや神経変性疾患など、さまざまな疾患に対するエピトープマッピングの応用範囲を広げます。これにより、これまで難治とされてきた疾患に対する新たな治療戦略が開発される可能性があります。
5. パーソナライズドメディシンへの貢献: 個々の患者の遺伝的背景や免疫反応の特性を考慮したエピトープマッピングにより、パーソナライズドメディシンがさらに進展します。個人に最適化されたワクチンや治療薬の開発が現実のものとなり、治療成績の向上が期待されます。
これらの技術革新は、エピトープマッピングの精度を高め、新しい治療薬やワクチンの開発サイクルを短縮することで、医療の未来を形作っていきます。エピトープマッピングの進化は、より安全で効果的な医療の提供を可能にし、患者の生活の質を向上させることに貢献するでしょう。
エピトープマッピングが開く新たな治療法
エピトープマッピングの進展は、新たな治療法の開発において画期的な可能性を開きます。この技術を通じて得られる知見は、特定の疾患を標的とする精密な治療戦略の設計を可能にします。
1. がん治療のパーソナライズ: エピトープマッピングは、がん細胞特有のエピトープを同定し、それを標的とする個別化されたがんワクチンの開発を促進します。これにより、患者特有のがんの特性に合わせた治療が可能になり、効果を最大化しつつ副作用を最小限に抑えることができます。
2. 自己免疫疾患の治療: 自己免疫疾患においては、エピトープマッピングにより、誤って免疫系が攻撃する自己抗原の特定部位を特定することが可能です。これらの情報を基に、免疫系の反応を特定のエピトープに対して「トレーニング」し直すことで、自己攻撃を防ぐ新しい治療法が開発されています。
3. 抗体医薬の進化: エピトープマッピングにより、疾患関連タンパク質の特定部位に結合し、その機能を阻害する抗体を設計することが可能になります。このアプローチにより、従来の治療法では対処が困難だった疾患に対しても、より効果的な治療オプションを提供することができます。
4. 感染症への応用: エピトープマッピングは、病原体の免疫回避戦略を理解し、それを無効化するワクチンや治療薬の開発に役立ちます。特に、変異が頻繁に起こるウイルスに対して、広範囲にわたる保護を提供するワクチンの設計が可能になることが期待されます。
5. アレルギー治療の新規性: アレルギー反応を引き起こす特定のエピトープを同定することで、アレルゲン特異的免疫療法(AIT)の精度を高めることができます。これにより、より安全で効果的なアレルギー治療法の開発が進んでいます。
6. 神経変性疾患の治療法: エピトープマッピングにより、アルツハイマー病やパーキンソン病などの神経変性疾患に関連するタンパク質の異常な蓄積を特定し、これをターゲットとした治療法の開発が進められています。
エピトープマッピングは、これらの新しい治療法の開発において中心的な役割を果たしており、疾患のより深い理解と治療の革新をもたらしています。この技術の進化は、未来の医療において個別化されたアプローチを可能にし、患者ごとに最適化された治療を提供するための鍵となります。また、エピトープマッピングにより得られる洞察は、予防医学においても重要な役割を果たす可能性があります。例えば、特定の疾患に対する個人の感受性や免疫応答の強さを予測し、カスタマイズされた予防策や早期介入戦略を立てることができるようになるかもしれません。
さらに、エピトープマッピングは、治療薬の開発だけでなく、疾患診断における新たなバイオマーカーの同定にも貢献することが期待されます。疾患特異的なエピトープを利用して、より精密で迅速な診断ツールを開発することが可能になり、早期診断とターゲット治療の選択に大きく寄与します。
技術革新とともに、エピトープマッピングは治療法だけでなく、疾患の予防、診断、治療管理の各段階にわたって、医療の質を向上させることに貢献しています。これにより、より効果的な治療成果の実現、副作用の削減、治療コストの最適化が期待されます。
しかし、これらの可能性を最大限に活かすためには、エピトープマッピング技術のさらなる発展と、それを支える研究基盤の強化が不可欠です。国際的な協力と資金の確保、さらには倫理的な考慮も含めた包括的なアプローチが求められます。未来の医療を形作るためには、これらの新しい技術の開発と応用に向けた積極的な投資と研究が不可欠であり、エピトープマッピングが開く新たな治療法の探求は、医学の新たな地平を開くことでしょう。








