目次
エフェクターT細胞は免疫系の中核をなす細胞であり、がん治療から感染症防御まで、多岐にわたる医学分野での研究が進められています。この記事では、エフェクターT細胞の機能、分化過程、そしてがん治療への応用について解説します。
第1章:エフェクターT細胞とは
エフェクターT細胞の基本概念
エフェクターT細胞は、免疫系の主要な細胞の一つであり、体を感染症やがんなどの異常から守るために活動します。これらの細胞は、特定の抗原に対する応答として活性化され、分化するT細胞から成ります。活性化されたエフェクターT細胞は、異物や感染した細胞を直接攻撃するサイトトキシックT細胞(CD8+ T細胞)と、他の免疫細胞を誘導して病原体と戦うヘルパーT細胞(CD4+ T細胞)に大きく分けられます。これらの細胞は、病原体の特定と排除、免疫記憶の形成に不可欠であり、免疫応答の効率化と長期的な保護に貢献します。エフェクターT細胞の理解は、特にがん治療において新たな免疫療法の開発への道を開く可能性があります。
エフェクターT細胞の分類と特性
エフェクターT細胞は、その機能と分泌するサイトカインに基づいていくつかのサブタイプに分類されます。主要なサブタイプには、サイトトキシックT細胞(CTLs)、ヘルパーT細胞(Th細胞)、および記憶T細胞が含まれます。これらの細胞は、体内の異物や感染に対する免疫応答において異なる役割を果たします。
1. サイトトキシックT細胞(CTLs、CD8+ T細胞): サイトトキシックT細胞は、主にウイルスに感染した細胞やがん細胞を標的とし、これらを直接殺傷する役割を持ちます。これらの細胞は、細胞死を引き起こすためにペルフォリンやグランザイムなどの毒性分子を含む小胞を標的細胞に放出します。
2. ヘルパーT細胞(Th細胞、CD4+ T細胞): ヘルパーT細胞は、免疫応答の調節と増強に重要な役割を果たします。これらはさらに、分泌するサイトカインの種類に基づいて、Th1細胞、Th2細胞、Th17細胞などのサブセットに分類されます。Th1細胞は細胞性免疫を、Th2細胞は体液性免疫をそれぞれ促進し、Th17細胞は炎症と自己免疫疾患に関与します。
3. 記憶T細胞: 一度特定の抗原に曝露された後、長期間にわたって抗原を記憶する能力を持ち、再び同じ抗原に遭遇した際に迅速な免疫応答を提供します。記憶T細胞は、その機能に応じて、中心記憶T細胞と効果記憶T細胞に分類されることがあります。
これらのエフェクターT細胞の特性と機能の理解は、特にがんや感染症に対する免疫療法の設計と改善に不可欠です。例えば、がん治療においては、サイトトキシックT細胞の活性化や増加を促進する戦略が研究されています。また、特定の疾患コンテキストにおけるヘルパーT細胞のサブセットの調節は、より効果的な免疫応答を引き出すための鍵となります。
第2章:エフェクターT細胞の活性化と機能
T細胞受容体と免疫応答の活性化
T細胞受容体(TCR)は、T細胞の表面に存在する特異的な分子で、体の免疫応答の活性化に中心的な役割を果たします。TCRは、メジャーヒストコンパチビリティコンプレックス(MHC)に提示される特定の抗原ペプチドを認識することにより、T細胞の活性化を引き起こします。この認識過程は、T細胞の機能を決定し、体内の異物や感染症、がん細胞に対する免疫反応の指令を出します。
●T細胞受容体の構造と機能
TCRは、αチェーンとβチェーンから成るヘテロダイマーで構成されており、それぞれが変数領域と定数領域を持ちます。変数領域は、異なる抗原ペプチドに対する特異性を持ち、定数領域はT細胞内のシグナル伝達に関与します。TCRは、MHC分子に結合して提示される抗原ペプチドを認識することで、T細胞の活性化シグナルを開始します。
●免疫応答の活性化
1. 抗原認識: T細胞は、抗原提示細胞(APC)によってMHC分子に提示される特定の抗原ペプチドをTCRを介して認識します。この認識は、免疫応答の第一段階であり、T細胞の活性化への信号を提供します。
2. コストィミュラトリーシグナル: 抗原認識だけでは不十分で、T細胞の完全な活性化には第二の信号が必要です。この第二の信号は、APC上のB7分子とT細胞上のCD28との相互作用によって提供されます。このコストィミュラトリーシグナルがない場合、T細胞は無反応状態(アネルギー)になります。
3. シグナル伝達とエフェクター機能の活性化: T細胞の活性化後、シグナル伝達経路が活性化され、サイトカインの産生、細胞増殖、およびエフェクター機能の発現が促進されます。これにより、サイトトキシックT細胞は標的細胞を殺傷し、ヘルパーT細胞は免疫応答を増強します。
T細胞受容体と免疫応答の活性化の理解は、特にがんや自己免疫疾患、感染症の治療において重要です。T細胞の特異的な活性化を促すことにより、疾患に対するより効果的な免疫応答を引き出すことが可能になります。
エフェクターT細胞の細胞傷害性機能
エフェクターT細胞、特にサイトトキシックTリンパ球(CTLs、CD8+ T細胞)は、その細胞傷害性機能を通じて、感染症やがんなどの異常細胞を排除する重要な役割を果たします。この機能は、体内で異常細胞が認識された際に、これらを直接攻撃して死滅させることにより、健康な組織の保護と病状の回復を促進します。
●細胞傷害性機能のメカニズム
1. ペルフォリンとグランザイム経路: CTLは、感染した細胞やがん細胞と密接に接触した後、ペルフォリンとグランザイムというタンパク質を含む小胞を標的細胞に放出します。ペルフォリンは標的細胞の膜に穴を開け、グランザイムが細胞内に侵入して細胞死を引き起こすための道を作ります。グランザイムは標的細胞内でカスパーゼを活性化し、アポトーシス(プログラムされた細胞死)を誘導します。
2. Fas/Fasリガンド経路: CTLは、Fasリガンド(FasL)を表面に発現しており、これが標的細胞のFas受容体と結合することで、細胞死シグナルを送ります。この相互作用もまた、カスパーゼのカスケードを活性化し、アポトーシスを誘導します。
3. 細胞障害性サイトカイン: CTLは、IFN-γ(インターフェロンガンマ)やTNF-α(腫瘍壊死因子アルファ)などのサイトカインも分泌します。これらのサイトカインは、直接的に標的細胞の死を促進したり、感染の拡大を防ぐために免疫応答を増強したりする効果があります。
●細胞傷害性機能の意義
エフェクターT細胞の細胞傷害性機能は、体を保護する上で非常に重要です。特に、がん治療においては、CTLの活性化と増殖を促進することで、がん細胞を効果的に排除し、疾患の進行を抑制する新たな治療法が開発されています。また、ワクチンの開発においても、強力なCTL応答を誘導することが目標の一つとされています。エフェクターT細胞の細胞傷害性機能に対する深い理解は、感染症やがんなどの疾患治療において新たな治療戦略を導き出す鍵となります。
第3章:エフェクターT細胞の分化と発達
ナイーブT細胞からエフェクターT細胞への分化過程
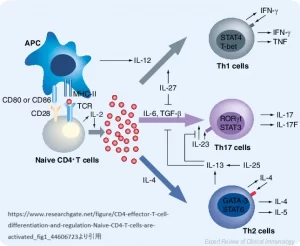
CD4+エフェクターT細胞の分化と制御。ナイーブなCD4+ T細胞は、抗原を提示するAPCとコスティミュレーションによって活性化される。特定のサイトカインの影響下で、T細胞はCD4 +エフェクターT細胞の3つの異なる系譜に分化することができる: Th1細胞、Th2細胞、Th17細胞である。Th17細胞の分化はIL-6とTGF-βによって促進され、IFN-γ、IL-4、IL-13、IL-27によって抑制される。IL-23は分化したTh17細胞を維持する。矢印はサイトカインの作用を示す。APC:抗原提示細胞;IL:インターロイキン;MHC:主要組織適合性複合体;ROR:レチノイン酸関連オーファン受容体: レチノイン酸関連オーファン受容体;STAT:Signal transducers and activators of transcription;TCR:T細胞受容体;TGF:トランスフォーミング増殖因子;Th: Tヘルパー;TNF:腫瘍壊死因子。
ナイーブT細胞からエフェクターT細胞への分化は、免疫応答の核心的な過程であり、体が病原体やがん細胞に効果的に対処するために不可欠です。この過程は、特定のシグナルと環境要因の影響を受け、高度に調節されています。
●ナイーブT細胞の活性化
1. 抗原認識: ナイーブT細胞は、初めて抗原を経験する際に、その抗原を提示するメジャーヒストコンパチビリティコンプレックス(MHC)分子に結合することで活性化されます。この過程は主に抗原提示細胞(APC)によって行われます。
2. コストィミュラトリー信号: 抗原とMHCの複合体に加え、ナイーブT細胞の完全な活性化には、APCからの追加のコストィミュラトリー信号(例:CD28とB7分子間の相互作用)が必要です。
3. サイトカインの役割: APCや他の免疫細胞から分泌されるサイトカインは、ナイーブT細胞の分化方向を決定する重要な要因です。例えば、インターフェロンガンマ(IFN-γ)はTh1型の応答を、インターロイキン4(IL-4)はTh2型の応答をそれぞれ促進します。
●エフェクターT細胞への分化
ナイーブT細胞が活性化されると、特定のエフェクターT細胞サブタイプに分化します。この過程では、T細胞の増殖と特定の遺伝子発現プログラムの活性化が伴います。
– サイトトキシックTリンパ球(CTL、CD8+ T細胞): CTLは、主にウイルス感染細胞やがん細胞を標的とし、細胞傷害性機能を持ちます。
– ヘルパーT細胞(Th細胞、CD4+ T細胞): Th細胞はさらに複数のサブタイプ(Th1、Th2、Th17、Tregなど)に分化し、異なる種類の免疫応答を調節します。それぞれが特定の病原体への対応や、免疫調節、炎症反応に関与します。
●分化の結果
この分化過程を通じて、エフェクターT細胞は、抗原特異的な応答を提供し、病原体の排除やがん細胞の抑制に寄与します。また、一部のT細胞は記憶T細胞に分化し、将来同じ抗原に再び遭遇した際に迅速な免疫応答を提供します。
ナイーブT細胞からエフェクターT細胞への分化は、免疫系の適応性と特異性を支える基盤であり、疾患治療やワクチン開発における重要な標的となります。
サイトカインとその他の因子による分化調節
サイトカインは、T細胞の分化と機能を調節する上で極めて重要な役割を果たします。これらの分子は、免疫細胞から分泌され、細胞間でのコミュニケーションを促進し、特定の免疫応答の方向性を決定します。ナイーブT細胞がエフェクターT細胞や記憶T細胞へと分化する過程では、サイトカインだけでなく、細胞外の他のシグナルや環境因子も重要な役割を果たします。
●サイトカインによる分化の調節
– Th1細胞: インターフェロン-γ(IFN-γ)やイリノイシン12(IL-12)のようなサイトカインは、ナイーブT細胞をTh1細胞へと分化させます。Th1細胞は細胞性免疫応答を強化し、主に細菌やウイルスに対抗します。
– Th2細胞: イリノイシン4(IL-4)は、ナイーブT細胞をTh2細胞へと分化させる主要なサイトカインです。Th2細胞は体液性免疫応答、特にアレルゲンや寄生虫に対する反応を促進します。
– Th17細胞: イリノイシン6(IL-6)、トランスフォーミング成長因子β(TGF-β)、およびイリノイシン23(IL-23)は、ナイーブT細胞をTh17細胞へと分化させます。Th17細胞は、特に真菌感染に対する防御と炎症反応に関与します。
– 調節性T細胞(Treg): TGF-βは、調節性T細胞の分化も促進します。Treg細胞は免疫系の調節に重要で、自己免疫反応の抑制や過剰な免疫応答の調節に貢献します。
●その他の分化調節因子
– 細胞間相互作用: 免疫細胞間、特に抗原提示細胞(APC)とT細胞間の物理的な接触は、コストィミュラトリーシグナルを介してT細胞の分化を促進します。
– 代謝因子: T細胞の代謝状態も、その分化と機能を調節する上で重要です。例えば、特定の栄養素や酸素レベルが低い環境は、T細胞の活性化や分化に影響を与えます。
– 組織特異的な環境: T細胞は、リンパ節、脾臓、腸管など、体内の異なる組織で異なる反応を示すことがあります。これは、組織固有のサイトカインや化学誘引因子の影響を受けるためです。
サイトカインとこれらの因子による分化の調節は、免疫系が多様な病原体や異常細胞に適切に対応できるようにするための、複雑で微妙なバランスを維持する上で重要です。この理解は、特定の疾患に対する治療戦略の開発や、免疫応答の調節を目的とした治療介入に役立ちます。
第4章:エフェクターT細胞とがん治療
がん免疫療法におけるエフェクターT細胞の役割
がん免疫療法は、体の自然な免疫システムを活用してがん細胞を攻撃し、排除する治療法です。この分野において、エフェクターT細胞、特にサイトトキシックTリンパ球(CTL)と特定のヘルパーT細胞(Th細胞)は、がん細胞の識別と排除に中心的な役割を果たします。
●エフェクターT細胞の役割
1. がん細胞の識別と攻撃: CTLは、がん細胞が表面に提示する特異的な抗原を認識し、これを標的として攻撃します。CTLは、ペルフォリンやグランザイムといった分子を用いてがん細胞を直接殺傷することができます。また、Fasリガンド経路を介してがん細胞にアポトーシスを誘導することもあります。
2. 免疫応答の増強: 特定のヘルパーT細胞(例えばTh1細胞)は、IFN-γなどのサイトカインを分泌し、CTLの活性化と増殖を促進します。これにより、より多くのエフェクターT細胞ががん細胞を攻撃するために利用可能になります。
3. 免疫記憶の形成: がん免疫療法において、記憶T細胞の形成も重要な役割を果たします。これらの細胞は、同じがん抗原に再び遭遇した際に迅速な免疫応答を提供し、がんの再発を防ぐことができます。
●がん免疫療法の戦略
– チェックポイント阻害剤: CTLA-4やPD-1/PD-L1といった免疫チェックポイントは、T細胞の活性化を制御する重要な分子です。チェックポイント阻害剤は、これらの分子の機能を阻害し、エフェクターT細胞の抗がん活性を増強します。
– CAR-T細胞療法: 患者自身のT細胞を遺伝子工学で改変し、がん細胞特異的な抗原を認識するキメラ抗原受容体(CAR)を発現させます。これらの改変T細胞は体内に戻されると、がん細胞を効果的に標的として攻撃します。
– がんワクチン: がん抗原を含むワクチンを使用して、体内でがん特異的なエフェクターT細胞の応答を誘導し、がん細胞を攻撃します。
がん免疫療法におけるエフェクターT細胞の役割は、がん治療の新たな地平を開くものです。これらの細胞を活性化し、調節することにより、従来の治療法では難しかったがんの種類に対しても効果的な治療オプションを提供する可能性があります。研究の進展により、より多くの患者にとって安全で効果的な治療法が開発されることが期待されます。
エフェクターT細胞を利用した治療法の最新進展
最新のエフェクターT細胞を利用した治療法の進展には、特にがん治療における革新的なアプローチが含まれます。これらの治療法は、がん細胞を特異的に標的とすることに焦点を当て、免疫システムの能力を最大限に活用することを目指しています。
aAVCワクチンとIL-2の併用療法: 理化学研究所による研究では、aAVCワクチンとインターロイキン-2(IL-2)の併用療法が開発されました。この療法では、特にIL-2Cx(S4B6)を併用することで、高腫瘍量を持つマウスモデルにおいて、エフェクター細胞(NK細胞、NKT細胞、CD8陽性T細胞)が有意に増幅され、強力な抗腫瘍効果を誘導できることが示されました。
抗CCR4モノクローナル抗体(モガムリズマブ)を用いた新規免疫療法: 国立がん研究センターによると、血液がん治療薬であるモガムリズマブを固形がん患者に投与することで、抗腫瘍効果を抑制する制御性T細胞を効率的に除去できることが分かりました。さらに、モガムリズマブの投与量を適正化することで、セントラルメモリーCD8陽性T細胞を温存しながら制御性T細胞を選択的に除去し、治療効果を得られる可能性が示唆されました。
次世代CAR-T療法: CAR-T細胞療法は、患者自身のT細胞に遺伝子操作を施し、がん細胞表面のタンパク質と結合できるキメラ抗原受容体(CAR)を組み込むことで、がん細胞を破壊します。MIT Technology Reviewによると、このアプローチは固形腫瘍の治療においても新たな成果を示しており、がん治療における大きな課題の一つである適切な標的抗原の選定に焦点を当てています。
これらの進展は、エフェクターT細胞を利用したがん治療において、個別化医療への道をさらに拓くものです。これらの治療法は、免疫システムの特定のコンポーネントを標的とすることで、がんに対するより効果的で精密なアプローチを可能にしています。
第5章:エフェクターT細胞の研究と未来
エフェクターT細胞研究の現状と課題
エフェクターT細胞研究の現状に関する直接的な情報を新たに見つけることができませんでしたが、既存の知識と最近の進展に基づいて現状と課題を概説することは可能です。
### 現状
エフェクターT細胞、特にサイトトキシックT細胞(CTL)とヘルパーT細胞(Th細胞)は、がんや感染症などの疾患に対する体の免疫応答に不可欠な役割を果たしています。最近の研究では、これらの細胞を活性化し、特定の疾患に対してより効果的に作用させる方法に焦点を当てています。例えば、CAR-T細胞療法は、特定のがん細胞に対する強力な治療効果を示しており、特に血液がんの分野で顕著な成功を収めています。
### 課題
1. 固形がんへの応用: CAR-T細胞療法は血液がんには有効ですが、固形がんへの応用は依然として大きな課題です。固形がんの微小環境は、T細胞の浸潤や活性化を妨げる要因が多く、治療効果を制限しています。
2. 耐性の発生: 長期間の治療によって、疾患が治療に対して耐性を持つ場合があります。特に、がん細胞は変異によってその特性を変化させ、T細胞の認識を逃れることがあります。
3. 副作用の管理: エフェクターT細胞を活性化する治療法は、時に重篤な副作用を引き起こす可能性があります。例えば、免疫細胞の過剰活性化によるサイトカイン放出症候群(CRS)などが挙げられます。
4. 適切な標的の同定: 特にCAR-T細胞療法において、適切な標的抗原を同定することは重要です。がん細胞だけに特異的に存在する抗原を見つけることは困難であり、健康な細胞を攻撃するリスクを最小限に抑える必要があります。
5. 治療へのアクセス: 高度な治療法は、高価であり、すべての患者がこれらの治療を受けられるわけではありません。治療のコスト削減と広範なアクセスの提供は、今後の研究と開発の主要な課題です。
エフェクターT細胞研究は、がん治療をはじめとする免疫療法の分野で顕著な進展を遂げていますが、上記の課題を克服するためのさらなる研究と革新が求められています。これらの課題に対処することで、より多くの患者に安全で効果的な治療を提供することができるようになるでしょう。
がん治療を超えるエフェクターT細胞の可能性
エフェクターT細胞の可能性はがん治療にとどまらず、多岐にわたる疾患への応用が期待されています。これらの細胞は、体の自然な防御メカニズムの一部として、感染症や自己免疫疾患、さらには移植片対宿主病(GVHD)などの治療に貢献することができます。
1.感染症への応用
エフェクターT細胞は、特にウイルス感染症に対する強力な免疫応答を提供します。HIVやインフルエンザ、新型コロナウイルス(SARS-CoV-2)など、生命を脅かすウイルス感染症に対して、特異的なエフェクターT細胞応答を誘導するワクチンや治療法の開発が進んでいます。これらの細胞は、感染をコントロールし、感染症の重症化を防ぐことができます。
2.自己免疫疾患の治療
自己免疫疾患では、誤って自身の組織を攻撃する免疫反応が起こります。特定のエフェクターT細胞サブセット(例えば、Th17細胞)は、多くの自己免疫疾患の発症に関与しています。これらの細胞の活動を抑制することにより、リウマチ性関節炎や多発性硬化症(MS)、炎症性腸疾患(IBD)などの疾患の治療が可能になります。
3.移植片対宿主病(GVHD)の予防と治療
骨髄移植や臓器移植後に発生するGVHDは、ドナー由来の免疫細胞が受け手の組織を攻撃することで起こります。エフェクターT細胞、特に調節性T細胞(Treg細胞)の操作により、この反応を抑制し、移植片の拒絶反応を減少させることができます。
4.アレルギー疾患への応用
アレルギー反応も、不適切な免疫応答の一形態です。エフェクターT細胞のバランスを調節することで、アレルギー性疾患(例えば、アトピー性皮膚炎や喘息)の症状を軽減する治療法が開発されています。
5.精密医療への応用
エフェクターT細胞の研究は、個々の患者の免疫系の特性に基づいた精密医療への道を開く可能性があります。個々の患者の免疫応答の遺伝的および分子生物学的プロファイルを理解することにより、より効果的で副作用の少ない治療法の開発が可能になります。
エフェクターT細胞の研究は、これらの分野で有望な進展を遂げており、今後さらに多くの治療法が開発されることが期待されています。免疫系の深い理解に基づくこれらの治療法は、多くの疾患に対して新たな治療オプションを提供することでしょう。
第6章:エフェクターT細胞と患者ケア
エフェクターT細胞治療の副作用と管理
エフェクターT細胞治療、特にCAR-T細胞療法は、がん治療において顕著な効果を示していますが、副作用の管理も非常に重要です。治療によって引き起こされる可能性のある副作用は、軽度のものから生命を脅かすものまで様々です。効果的な管理戦略により、これらの副作用を最小限に抑え、患者の安全と快適性を確保することが可能です。
●主な副作用
1. サイトカイン放出症候群(CRS): CAR-T細胞療法で最も一般的な副作用で、T細胞が大量のサイトカインを放出することによって起こります。症状は発熱、倦怠感、筋肉痛から、低血圧、多臓器不全に至るまで様々です。
2. 神経毒性: 頭痛、混乱、けいれん、意識障害など、中枢神経系に影響を与える副作用が報告されています。これはCRSと同時期またはそれに続いて発生することがあります。
3. B細胞枯渇: 特定のCAR-T細胞療法は、正常なB細胞も標的とすることがあり、長期的な免疫不全や低ガンマグロブリン血症を引き起こすことがあります。
4. 感染症: 免疫細胞の一部が標的とされることにより、患者の感染症に対する抵抗力が低下することがあります。
●副作用の管理
1. CRSの管理: 軽度から中等度のCRSは、解熱剤や抗炎症薬によって管理できます。重症の場合は、トシリズマブ(IL-6受容体アンタゴニスト)やステロイドの使用が推奨されます。
2. 神経毒性の管理: 神経学的な副作用は、しばしばCRSの治療と同様に管理されますが、重症の場合は、神経科専門医による評価が必要です。必要に応じて抗てんかん薬やステロイドが使用されます。
3. 感染症予防: B細胞枯渇に対しては、定期的な免疫グロブリンの補充療法が効果的です。また、適切な予防接種と感染症に対する注意深いモニタリングが推奨されます。
4. 患者教育: 患者とその家族に対する教育は、副作用の早期発見と管理に不可欠です。治療前には、可能性のある副作用とそれらが発生した際の対処法について十分に説明することが重要です。
5. 継続的なモニタリング: 治療後の患者は、副作用の早期発見と対応のために、定期的にモニタリングする必要があります。これには、血液検査、身体検査、および必要に応じて追加的な検査が含まれます。
エフェクターT細胞治療に関連する副作用は、適切な予防策と管理戦略により効果的に対処できます。これにより、患者は治療の利益を最大限に享受しつつ、副作用のリスクを最小限に抑えることができます。
患者と医療提供者によるエフェクターT細胞治療の共同管理
エフェクターT細胞治療の共同管理は、患者と医療提供者が密接に協力することで、治療の効果を最大化し、副作用を最小限に抑えるためのアプローチです。このプロセスでは、通信、教育、相互の理解が鍵となります。
●患者の役割
1. 情報提供: 患者は自身の健康状態、過去の治療履歴、現在の症状に関する正確な情報を医療提供者に提供する必要があります。これにより、医療提供者は患者に最も適した治療計画を立てることができます。
2. 教育と自己管理: 患者はエフェクターT細胞治療の仕組み、期待される効果、可能性のある副作用について学ぶ必要があります。また、治療中に発生する可能性のある問題に対処するための自己管理スキルを身につけることが重要です。
3. 副作用のモニタリング: 患者は、治療中に発生する可能性のある副作用を正確にモニタリングし、医療提供者に報告する責任があります。これにより、早期に介入し、重大な健康問題の発生を防ぐことができます。
●医療提供者の役割
1. 患者教育: 医療提供者は、エフェクターT細胞治療のメカニズム、期待される効果、潜在的な副作用について患者に詳細な情報を提供する責任があります。これにより、患者は治療選択についてよりよく理解し、 informed consent(十分な情報に基づく同意)を提供できます。
2. 継続的なサポートとフォローアップ: 医療提供者は、治療中および治療後の患者に継続的なサポートを提供し、定期的なフォローアップを通じて患者の健康状態をモニタリングする必要があります。これにより、治療の調整や追加的な介入が必要かどうかを判断できます。
3. オープンなコミュニケーション: 医療提供者は、患者からの質問や懸念に対して、開かれた態度で対応し、透明性を持って情報を共有する必要があります。これにより、患者と医療提供者間の信頼関係が築かれます。
●共同管理の重要性
エフェクターT細胞治療の共同管理は、患者が主体的に治療プロセスに参加することを奨励し、患者と医療提供者間の協力を促進します。これは、治療の成功率を高め、患者の満足度を向上させることに寄与します。また、患者が自身の健康状態と治療選択についてより良く理解し、積極的に関与することを可能にします。