目次
BLM遺伝子(RecQ Like Helicase)は、DNA修復や複製に重要な役割を果たす遺伝子です。この遺伝子に変異が起きると、ブルーム症候群(Bloom syndrome)という遺伝性疾患を引き起こす可能性があります。遺伝子検査により、BLM遺伝子の変異を事前に知ることで、家族計画や健康管理に役立てることができます。
BLM遺伝子について知っておくべきこと
BLM遺伝子は染色体15q26.1に位置し、DNAヘリカーゼとして機能するタンパク質をコードしています。この遺伝子の両アレルに変異があると、ブルーム症候群という常染色体劣性(潜性)遺伝の疾患を引き起こします。ミネルバクリニックでは、BLM遺伝子を含む拡大版保因者検査を提供しています。
BLM遺伝子とは
BLM遺伝子(RecQ Protein-Like 3/RECQL3)は、細胞のDNA修復システムで重要な役割を担う遺伝子です。この遺伝子は、DNAヘリカーゼと呼ばれる酵素を作り出し、DNA複製や修復過程でDNAの二重螺旋構造をほどく働きをしています。ヒトゲノムでは染色体15q26.1に位置し、約98キロベース(kb)の長さを持ち、22個のエクソンからなる遺伝子です。
BLM遺伝子がコードするタンパク質は、1,417アミノ酸からなり、RecQヘリカーゼファミリーの一員です。このファミリーには大腸菌のRecQをはじめ、ヒトではRECQL(RecQLヘリカーゼ)、WRN(RECQL2)、BLM(RECQL3)、RECQL4、RECQL5の5つのヘリカーゼが含まれています。これらのタンパク質は構造的に類似しており、DNAの維持修復において相補的かつ独自の機能を持っています。
BLMタンパク質の構造的特徴
BLMタンパク質は以下の特徴的な構造を持っています:
- ヘリカーゼドメイン:ATP依存性のDNA巻き戻し活性の中核となる領域
- RecQヘリカーゼ保存領域(RQC):DNAとの結合に関与
- HRDC(Helicase and RNase D C-terminal)ドメイン:DNA構造認識に関与
- 核局在シグナル(NLS):タンパク質を細胞核に移行させる配列
- 酸性アミノ酸に富むN末端領域:他のタンパク質との相互作用に関与
- 塩基性アミノ酸に富むC末端領域:DNA結合能に関与
BLM遺伝子の進化的保存性
BLM遺伝子は、酵母からヒトまで進化的に高度に保存されています。酵母のSgs1、大腸菌のRecQ、ショウジョウバエのDmBlmなど、様々な生物種において相同遺伝子が存在し、類似した機能を持ちます。この高い保存性は、BLM遺伝子がゲノムの安定性維持において極めて重要な役割を担っていることを示しています。
BLM遺伝子の詳細な機能
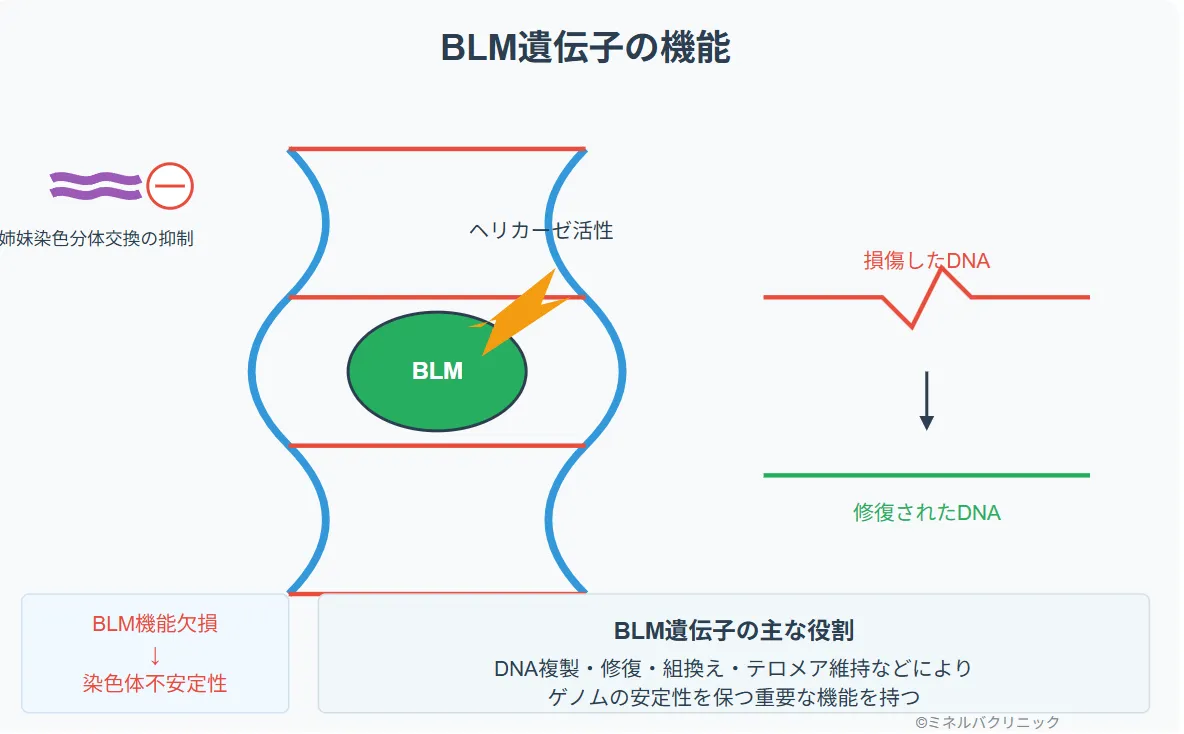
BLM遺伝子は、以下のような多岐にわたる重要な役割を持っています:
-
DNA複製時のエラー修正
DNA複製過程では、複製フォークの停止や崩壊が生じることがあります。BLMタンパク質はこのような停止した複製フォークを安定化させ、再開始を促進する役割を担っています。複製フォークが停止すると、DNA二重鎖切断や複製エラーが生じる可能性がありますが、BLMはこれを防ぐために働きます。
-
相同組換え(HR)の制御
相同組換えはDNA二重鎖切断を修復する重要なメカニズムですが、過剰な相同組換えはゲノムの不安定性を引き起こします。BLMタンパク質はホリデー接合体(Holliday junction)と呼ばれるDNA組換え中間体を認識し、これを解消(dissolution)することで、交差(crossing over)を伴わない修復を促進します。この機能はTop3α(トポイソメラーゼIIIα)やRMI1/2とともに「BTRコンプレックス」として働きます。
-
姉妹染色分体交換(SCE)の抑制
姉妹染色分体交換は遺伝的組換えの一種で、姉妹染色分体間での相同なDNA配列の物理的な交換を伴います。BLMタンパク質はこの過程を抑制する役割があり、BLM遺伝子が機能しないブルーム症候群の細胞では、SCEの頻度が著しく増加します(通常の約10倍)。これはブルーム症候群の診断マーカーとしても用いられます。
-
テロメア維持への関与
BLMタンパク質はテロメア(染色体末端)の安定性維持にも関与しています。特に、代替的テロメア伸長(ALT)を用いる細胞では、BLMはテロメアDNAの合成に関わることが示されています。テロメア結合タンパク質TRF1、TRF2との相互作用を通じて、テロメアの構造と機能の維持に貢献しています。
-
DNAトポロジーの制御
BLMタンパク質はトポイソメラーゼIIIαと相互作用し、DNAのトポロジカルな問題(超らせん、絡まりなど)を解消する役割を持ちます。これによりDNA複製や転写、修復過程でのDNA操作をスムーズに進行させることができます。
-
細胞周期チェックポイントへの関与
BLMタンパク質はDNA損傷応答経路において、ATM(Ataxia Telangiectasia Mutated)やATR(ATM and Rad3-related)キナーゼによりリン酸化され活性化されます。これにより、DNA損傷時の細胞周期チェックポイント制御に関与し、損傷DNAの修復のための時間を確保します。
BLMタンパク質の相互作用パートナー
BLMタンパク質は多くのDNA修復・複製関連タンパク質と相互作用することが知られています:
- BRCA1:乳がん感受性遺伝子1、DNA修復に関与
- FANCM:ファンコニ貧血補完群Mタンパク質
- RAD51:相同組換え修復に関与するリコンビナーゼ
- RPA:一本鎖DNA結合タンパク質複合体
- MLH1/MSH6:ミスマッチ修復タンパク質
- WRN:Werner症候群の原因遺伝子産物、RecQヘリカーゼの一つ
- Top3α:トポイソメラーゼIIIα
- RMI1/RMI2:RecQ仲介タンパク質
これらのタンパク質との相互作用ネットワークは、BLMがDNA修復やゲノム安定性維持において中心的な役割を果たしていることを示しています。
BLM遺伝子と細胞内局在
BLMタンパク質は主に細胞核内に局在しており、特に以下の場所で機能します:
- PMLボディ(PML nuclear bodies):正常細胞ではBLMはこの核内構造体に局在
- 核小体:S期(DNA合成期)の細胞ではWRNタンパク質と共に核小体にも局在
- DNA損傷部位:DNA損傷が起こるとその部位に速やかに集積
- 複製フォーク:DNA複製中の複製フォークにも局在
この遺伝子が正常に機能しないと、以下のような問題が生じます:
- 染色体の不安定性の増加(染色体切断や再編成)
- 姉妹染色分体交換(SCE)頻度の顕著な増加
- DNA損傷応答の異常
- 小核(micronuclei)形成の増加
- 細胞分裂の異常と遅延
- 発がんリスクの著しい上昇(一般集団と比較して約170~300倍)
- 細胞の早期老化
BLM遺伝子研究の最新動向
BLM遺伝子に関する研究は現在も活発に進められています:
- 抗がん剤の標的としての可能性(合成致死アプローチ)
- 遺伝子編集技術によるBLM関連疾患の治療法開発
- BLMタンパク質の構造解析と阻害剤の開発
- BLM遺伝子変異の保因者と大腸がんリスクの関連研究
- 細胞の老化とBLM機能の関連性の解明
これらの研究は、ブルーム症候群の治療法開発だけでなく、がんや老化に関する理解を深める上でも重要な意義を持っています。
BLM遺伝子の理解を深めることは、DNA修復機構やゲノム安定性維持のメカニズムの解明、そしてブルーム症候群やがんなどの疾患の理解と治療法開発につながる重要な研究分野となっています。
BLM遺伝子変異とブルーム症候群
BLM遺伝子の両アレルに病的変異がある場合、ブルーム症候群(Bloom syndrome)という希少な遺伝性疾患を引き起こします。この疾患は常染色体劣性(潜性)遺伝形式をとり、両親から変異した遺伝子を1つずつ受け継いだ場合にのみ発症します。世界的にも非常に稀な疾患で、これまでに報告された症例は約300例程度です。
ブルーム症候群の疫学
- 全体の発症頻度:約1/100,000以下
- アシュケナージ・ユダヤ人での発症頻度:約1/48,000
- アシュケナージ・ユダヤ人での保因者頻度:約1/134
- 診断時期:多くは幼少期(成長障害や皮膚症状から)
主な臨床症状
1. 成長障害
- 低出生体重:平均出生体重は通常2,000g以下
- 均整のとれた低身長:成人身長は男性で約150cm、女性で約138cm程度
- 低体重:体格は細身で、筋肉量も少ない傾向
2. 特徴的な皮膚症状
- 蝶形紅斑:顔面(特に鼻から頬にかけて)の蝶形紅斑
- 光線過敏症:紫外線により症状が悪化
- 毛細血管拡張症:紅斑部に見られる血管の拡張
3. 免疫機能低下と感染症
- 免疫グロブリン異常:IgA、IgM、IgGの低下が見られることがある
- 反復性感染症:特に上・下気道感染症や消化管感染症
4. 生殖機能障害
- 男性:無精子症や乏精子症が多く、ほとんどの男性患者は不妊
- 女性:早期閉経(30代前半)が多く、妊孕性期間が短い
5. その他の症状
- 糖尿病:約10〜15%の患者が若年〜成人早期に発症
- 特徴的な顔貌:狭い顔、突出した鼻、小さな下顎
- 慢性肺疾患のリスク上昇
ブルーム症候群と悪性腫瘍リスク
ブルーム症候群患者は、一般集団と比較して約170〜300倍の悪性腫瘍発症リスクがあります。生涯発がんリスクは約40〜50%で、平均発症年齢は約24歳(一般集団より約20年若い)です。
高リスクの悪性腫瘍
- 血液腫瘍:急性白血病、リンパ腫
- 消化器癌:大腸癌、食道癌、胃癌
- 皮膚癌:基底細胞癌、扁平上皮癌
- 女性の乳癌:若年性乳癌のリスク上昇
発がんメカニズム
BLM遺伝子変異による染色体不安定性が主な原因:
- DNA修復機能の低下による遺伝子変異の蓄積
- 姉妹染色分体交換(SCE)の頻度増加
- 染色体再編成や構造異常の増加
診断
ブルーム症候群の診断は以下の要素に基づいて行われます:
- 臨床症状と身体所見:特徴的な成長障害、皮膚病変など
- 細胞遺伝学的検査:姉妹染色分体交換(SCE)の増加(正常の約10倍)
- 遺伝子検査:BLM遺伝子の病的変異の同定
治療とマネジメント
現在のところ、ブルーム症候群に対する根治的治療法はなく、症状に対する対症療法と合併症予防が中心となります:
- 皮膚症状:日焼け止めの使用、日光暴露の制限
- 感染症:予防接種、早期の抗生物質治療
- 悪性腫瘍:定期的な癌スクリーニング、早期発見・治療
- 糖尿病:血糖モニタリング、適切な食事・薬物療法
- 心理社会的サポート:遺伝カウンセリング、家族支援
遺伝カウンセリングと家族計画
- 再発リスク:両親が保因者の場合、各妊娠で25%の発症リスク
- 保因者検査:リスクのある家族メンバーへの検査提供
- 出生前診断:絨毛検査や羊水検査による胎児診断
- 着床前遺伝子診断(PGD):体外受精と組み合わせた選択肢
ミネルバクリニックでは、BLM遺伝子を含む拡大版保因者検査と専門的な遺伝カウンセリングを提供しています。
ブルーム症候群は多くの合併症を伴う複雑な疾患ですが、早期診断と包括的な医療管理によって、患者のQOL(生活の質)を向上させることが可能です。特に、定期的な癌スクリーニングは悪性腫瘍の早期発見と生命予後の改善に寄与します。
BLM遺伝子の変異タイプ
BLM遺伝子には様々な病的変異(病的バリアント)が報告されています。特に注目すべき変異としては以下のようなものがあります:
主なBLM遺伝子変異
- 6塩基欠失/7塩基挿入(blmAsh):アシュケナージ・ユダヤ人集団に多く見られる創始者変異。この変異では、BLM遺伝子の2281位置で6塩基(ATCTGA)の欠失と7塩基(TAGATTC)の挿入が起こり、早期終止コドンが生じます。
- 3塩基欠失(631CAA):日本人の患者で報告されている変異で、186番目のアミノ酸位置で終止コドンを生じます。
- エクソン11、12の欠失:イタリア人患者で報告されている大きな欠失変異で、フレームシフトを引き起こします。
- 3181G-T変異(C1036F):1036番目のシステインがフェニルアラニンに置換される変異。
BLM遺伝子変異のタイプは多様であり、特定の集団で特定の変異が高頻度に見られることがあります。例えば、アシュケナージ・ユダヤ人集団では、約1/134の割合でblmAsh変異の保因者がいるとされています。
| 対象集団 | 保因者頻度 | 検出率 | 検査後保因確率 | 残存リスク |
|---|---|---|---|---|
| 一般集団 | 1/800 | 87% | 1/6,147 | <1/1,000万 |
| アシュケナージ・ユダヤ人集団 | 1/134 | 99% | 1/13,301 | 1/7,129,336 |
保因者検査の重要性
BLM遺伝子の保因者検査は、自分自身がブルーム症候群を引き起こす遺伝子変異を持っているかどうかを知るための検査です。特に以下のような方には検査をお勧めします:
- 家族にブルーム症候群の患者がいる方
- アシュケナージ・ユダヤ人の祖先を持つ方
- 血族結婚を予定している方
- 遺伝性疾患のリスクを知りたい方
- 将来的に子どもを持つことを計画している方
保因者であることの意味
BLM遺伝子変異の保因者は、通常はブルーム症候群を発症しません。しかし、パートナーも同じ変異の保因者である場合、お子さんがブルーム症候群を発症するリスクが25%となります。保因者検査を受けることで、このリスクを事前に知り、適切な家族計画や遺伝カウンセリングを受けることができます。
また、近年の研究ではBLM遺伝子変異の保因者は大腸がんのリスクが約2.5倍高まる可能性が示唆されています。保因者であることを知ることで、より適切な健康管理を行うことができます。
BLM遺伝子の分子遺伝学
BLM遺伝子は、RecQヘリカーゼファミリーに属する遺伝子で、DNAの修復や複製に関わる重要なタンパク質をコードしています。以下にBLM遺伝子の分子遺伝学的特徴をまとめます:
- 遺伝子座:染色体15q26.1に位置
- 遺伝子サイズ:約98kb(キロベース)
- エクソン数:22個
- コードするタンパク質:1,417アミノ酸からなるDNAヘリカーゼ
- 機能ドメイン:ヘリカーゼドメイン、核局在シグナル(NLS)、TopBP1結合ドメインなど
BLMタンパク質は、DNA複製や修復の過程で生じるDNA中間体(特にホリデー接合体と呼ばれる構造)を解消する役割を持っています。この機能が失われると、姉妹染色分体交換(SCE)の頻度が増加し、染色体の不安定性が高まります。
BLM遺伝子と他のDNA修復遺伝子との関係
BLMタンパク質は、他の重要なDNA修復タンパク質と相互作用することが知られています:
- トポイソメラーゼ III-α:DNAのトポロジカルな問題を解消する酵素
- RPA:一本鎖DNAに結合するタンパク質
- BRCA1:乳がん感受性遺伝子、DNA修復に関与
- ATM:DNA損傷応答を制御するキナーゼ
- RAD51:相同組換えに関与するタンパク質
これらのタンパク質との相互作用は、BLMがゲノムの安定性維持に重要な役割を果たしていることを示しています。
遺伝カウンセリングの重要性
BLM遺伝子変異の保因者であることがわかった場合や、ブルーム症候群のリスクが懸念される場合、遺伝カウンセリングを受けることが非常に重要です。遺伝カウンセリングでは、以下のようなサポートを受けることができます:
- 遺伝子変異の意味や健康への影響の説明
- 家族計画や出生前診断に関する情報提供
- 遺伝性疾患リスクの評価と管理
- 心理的・社会的サポート
- 最新の医学情報の提供
ミネルバクリニックの遺伝カウンセリング
ミネルバクリニックでは、臨床遺伝専門医が常駐し、BLM遺伝子を含む遺伝子変異に関する専門的な遺伝カウンセリングを提供しています。遺伝子検査の結果を正しく理解し、適切な意思決定をサポートするために、ぜひ専門家によるカウンセリングをご検討ください。
まとめ:BLM遺伝子とブルーム症候群
BLM遺伝子は、私たちの体の中でDNA修復や複製の正確性を保つ重要な役割を担っています。この遺伝子に変異があると、ブルーム症候群という希少な遺伝性疾患のリスクが高まります。ブルーム症候群は、低身長、免疫不全、若年性がんなどの特徴を持つ疾患です。
BLM遺伝子変異の保因者検査は、自分自身がこの変異を持っているかどうかを知るための重要なステップです。特にアシュケナージ・ユダヤ人の祖先を持つ方や、家族にブルーム症候群の患者がいる方は、検査を検討する価値があります。
保因者であることがわかった場合、適切な遺伝カウンセリングを受けることで、将来の健康管理や家族計画に役立てることができます。ミネルバクリニックでは、専門的な遺伝カウンセリングと拡大版保因者検査を提供しています。
ミネルバクリニックの拡大版保因者検査
ミネルバクリニックでは、BLM遺伝子を含む多数の遺伝子を対象とした拡大版保因者検査を提供しています。この検査により、ブルーム症候群を含む様々な遺伝性疾患の保因者であるかどうかを調べることができます。検査結果に基づいて、臨床遺伝専門医による専門的な遺伝カウンセリングもご利用いただけます。
参考文献
- Ellis NA, et al. The Bloom’s syndrome gene product is homologous to RecQ helicases. Cell. 1995;83(4):655-66.
- German J, et al. Bloom’s syndrome. XIX. Cytogenetic and population evidence for genetic heterogeneity. Clin Genet. 1977;12(3):169-74.
- Gruber SB, et al. BLM heterozygosity and the risk of colorectal cancer. Science. 2002;297(5589):2013.
- Calpena E, et al. Dissection of contiguous gene effects for deletions around ERF on chromosome 19. Human Mutation. 2021;42(9):1148-1160.
- Goss KH, et al. Enhanced tumor formation in mice heterozygous for Blm mutation. Science. 2002;297(5589):2051-3.