目次
AQP2遺伝子は、わたしたちの腎臓で「水を体に取り戻す」働きを担う水チャネルタンパク質「アクアポリン2」の設計図です。喉が渇いたとき、寝ている間も尿が出すぎないとき——その背後では、抗利尿ホルモン(バソプレシン)の指令を受けたAQP2が、腎臓の集合管で水分子だけを精密に通過させています。この遺伝子に変異が生じると、いくら水を飲んでも尿として大量に失われる「腎性尿崩症」を発症します。本記事では、AQP2の働きから関連疾患・最新の治療研究まで、臨床遺伝専門医がやさしく解説します。
Q. AQP2遺伝子はどのような遺伝子ですか?まず結論だけ知りたいです
A. 腎臓の集合管で水分子を選択的に通す水チャネル「アクアポリン2」をコードする遺伝子で、第12番染色体(12q13)に位置します。抗利尿ホルモン(バソプレシン)の指令に応じて細胞内から細胞膜へと素早く移動し、尿の濃縮を担います。AQP2の変異は腎性尿崩症の原因となり、常染色体劣性遺伝・常染色体顕性遺伝のいずれの形式もとり得ます。
- ➤遺伝子の基本情報 → 染色体12q13、271アミノ酸、アクアポリンファミリー
- ➤タンパク質の構造 → 4つのモノマーが集まる「ホモ四量体」と砂時計型の水通路
- ➤機能調節の仕組み → バソプレシン→cAMP→PKA→S256リン酸化→細胞膜へ移動
- ➤関連疾患 → 腎性尿崩症(AR型・AD型)、変異の場所で病態が異なる
- ➤最新治療研究 → スタチン・PDE阻害薬などのバイパス療法、エクソソーム診断
1. AQP2遺伝子とは:水を再吸収する「水のゲート」の設計図
わたしたちが1日に飲む水の量は1〜2リットル程度ですが、腎臓では1日に約180リットルもの「原尿」が作られています。これは2リットルのペットボトル90本分に相当します。もしすべてが尿として排泄されたら、人間は脱水で生きていけません。実際には、原尿の99%以上が腎臓の中で再吸収され、最終的な尿として体外に出るのは1〜1.5リットル程度です。この尿の最終濃縮を担う水のゲートが、AQP2遺伝子からつくられる「アクアポリン2」というタンパク質です。
💡 用語解説:アクアポリン(Aquaporin)
細胞膜には水分子を選択的に通す「水のトンネル」が存在します。これがアクアポリンと呼ばれる膜タンパク質ファミリーで、ヒトには13種類(AQP0〜AQP12)が知られています。1992年に米国ジョンズ・ホプキンス大学のピーター・アグリ博士によって発見され、博士はその功績で2003年にノーベル化学賞を受賞しました。アクアポリン総論はこちらで詳しく解説しています。AQP2はこのファミリーの中でも、「尿を濃くする」という極めて重要な役割を一手に引き受けている特殊なメンバーです。
AQP2は腎臓の中でも特に「集合管」と呼ばれる尿の通り道に集中して発現しています。集合管は尿の最終調整を行う場所で、ここでどれだけ水を再吸収するかが、最終的な尿量を決定します。脱水時には積極的に水を取り戻し、水分過多のときには余分な水を尿として排泄する——この精密なバランス調整の現場で、AQP2は主役を演じています。
💡 用語解説:集合管(しゅうごうかん)と主細胞
腎臓は「ネフロン」と呼ばれる微小な濾過装置の集まりです。糸球体で血液を濾過した後、濾過液(原尿)は尿細管を通り、最後に集合管へとたどり着きます。集合管は尿の濃縮を最終決定する場所で、ここを構成する細胞のうち水の再吸収に特化したのが「主細胞(しゅさいぼう/principal cell)」です。AQP2はこの主細胞の管腔側(尿側)の細胞膜に並び、水分子だけを通します。
2. AQP2遺伝子の基本情報
AQP2遺伝子の基本的なゲノム情報を以下にまとめます。
| 項目 | 内容 |
|---|---|
| 遺伝子シンボル | AQP2(別名:NDI2、AQP-CD、WCH-CD) |
| 染色体上の位置 | 第12番染色体長腕(12q13) |
| 主要転写産物 | NM_000486.6(MANE Select) |
| タンパク質長 | 271アミノ酸(標準長アイソフォーム) |
| 分子量 | 約28.8 kDa |
| 主な発現組織 | 腎髄質(集合管主細胞)が中心。78以上の細胞・組織で発現確認 |
| 所属ファミリー | MIP(Major Intrinsic Protein)/アクアポリンファミリー |
| 関連疾患 | 腎性尿崩症(OMIM #125800:AD型/OMIM #222000:AR型) |
第12番染色体の12q13という領域にはAQP2のほかにも、複数のアクアポリンファミリー遺伝子がクラスター状に近接して並んでいます。これは進化の過程で1つの祖先遺伝子が重複して新たな機能を獲得していった痕跡と考えられています。
転写制御:長期的な水分調節の仕組み
AQP2の発現量は、短時間(分単位)の細胞内移動だけでなく、数時間から数日単位の長期的な転写制御も受けています。慢性的な水制限や脱水状態が続くと、細胞内のセカンドメッセンジャーであるcAMPが上昇し、転写因子CREBがリン酸化されます。これが核内に移行してAQP2遺伝子のプロモーター領域に結合することで、新たなAQP2タンパク質が大量に合成されるのです。「短期は細胞内輸送、長期は転写量」——この二段構えの調節こそが、生体の水バランスを長期にわたり維持する仕組みの核心です。
3. アクアポリン2の構造と水透過機構
AQP2タンパク質の最大の特徴は、「水分子だけを高速で通し、イオン(特にプロトン)は絶対に通さない」という驚異的な選択性です。この選択性を生み出しているのが、巧妙な分子設計です。
4つのモノマーが集まって作る「ホモ四量体」
細胞膜上では、AQP2は4つの同じタンパク質(モノマー)が集まって「ホモ四量体(テトラマー)」を形成します。ここで一つ重要なポイントがあります——水が通るのは4つが集まる中心部ではなく、それぞれのモノマー単体が独立して持つ通路(ポア)です。つまり、1つのテトラマーには合計4つの水通路があり、それぞれが独立に動作しています。
💡 用語解説:膜貫通αヘリックスとハーフヘリックス
細胞膜は脂質の二重層でできており、その中にすっぽりと埋め込まれるタンパク質を「膜タンパク質」と呼びます。膜を貫いている部分は螺旋状のαヘリックス構造をとっており、AQP2の1つのモノマーには6本の膜貫通αヘリックスと、膜を完全には貫通せず途中で折り返す2本のハーフヘリックスが存在します。これらが立体的に組み合わさり、中央が細い「砂時計型」の水通路が形成されます。
水分子だけを通す2つの「関所」
水通路の中には、不純物を排除する「関所」が2か所設けられています。
🔐 関所① NPAモチーフ
2本のハーフヘリックスの先端に位置する、アスパラギン-プロリン-アラニン(NPA)という3つのアミノ酸の並び。膜の中央で向かい合い、最も狭い空間を作ります。ここを通過する水分子は必ず一列に並ばされ、水素結合のネットワークが分断されます。これにより、水分子の連鎖伝達によるプロトン移動(グロットゥス機構)が完全にブロックされます。
🔐 関所② ar/R選択性フィルター
通路の入口付近に設けられた、芳香族アミノ酸(aromatic)とアルギニン(Arg、R)からなる狭窄部。サイズと電荷の組み合わせにより、水以外のもの(イオンや大きな分子)は物理的・電気的に通過できません。アクアポリンファミリーのうち、グリセロールも通す「アクアグリセロポリン」と水だけを通す「水専用アクアポリン」を区別する決定的な部位です。
💡 用語解説:なぜプロトン(水素イオン)の遮断が重要なのか
細胞は内側と外側で電位差(膜電位)を保つことで、神経伝達・栄養取り込み・エネルギー産生など、ほぼすべての生命活動を行っています。もし水通路からプロトンが漏れたら、この電位差が崩れ、細胞は機能停止してしまいます。AQP2のNPAモチーフは「水だけは通すがプロトンは絶対に通さない」という、生命にとって絶対的に必要な分子設計を実現しています。
4. バソプレシンとの連携:分単位で動く水のスイッチ
AQP2が他の多くの膜タンパク質と決定的に異なるのは、「ホルモンの指令を受けて、細胞内から細胞膜へと素早く移動する」という特殊な性質です。これを「細胞内トラフィッキング(輸送)」と呼びます。
💡 用語解説:バソプレシン(AVP/抗利尿ホルモン)
脳の視床下部で作られ、脳下垂体後葉から血液中に分泌されるホルモンです。「アルギニン・バソプレシン(AVP)」または「抗利尿ホルモン(ADH)」と呼ばれます。血漿の浸透圧が上がる(=体が水不足)と分泌され、腎臓に「水を取り戻せ」と指令を出します。指令を受け取る受容体は「バソプレシン2型受容体(AVPR2)」と呼ばれ、集合管主細胞の基底膜(血管側)に発現しています。
水を取り戻す瞬間:5分から30分で起きる劇的な変化
バソプレシンが分泌されてからAQP2が細胞膜に並ぶまで、わずか5〜30分です。この間に何が起きているのか、ステップごとに見てみましょう。
バソプレシンが基底膜側のAVPR2受容体に結合。受容体はGタンパク質を介してアデニル酸シクラーゼを活性化し、ATPからcAMPが大量に作られる。
cAMPがプロテインキナーゼA(PKA)を活性化し、PKAがAQP2のC末端の256番目のセリン(S256)をリン酸化する。これが「動け」の合図。
細胞膜直下にあるF-アクチンのバリアが一時的に解除される。同時に、AQP2を内蔵した小胞が微小管・アクチンに沿って細胞膜へと運ばれる。
小胞が管腔側細胞膜と融合(エクソサイトーシス)。AQP2が膜上に展開し、原尿から水分子が細胞内→血管内へと一気に再吸収される。
逆に、十分な水分が補給されて血漿浸透圧が下がるとバソプレシンの分泌が止まり、AQP2はクラスリン媒介性エンドサイトーシスという仕組みで再び細胞内へと取り込まれます。エクソサイトーシス(出ていく)とエンドサイトーシス(戻る)の動的な綱引きによって、わたしたちの尿量は分単位で精密に調節されているのです。
5. リン酸化バーコード:4つのセリンが描く動態制御
AQP2のC末端領域(タンパク質の尾の部分)には、4つの重要なセリン残基(S256・S261・S264・S269)が並んでいます。これらがそれぞれ独立にリン酸化されたり脱リン酸化されたりすることで、AQP2の「どこに行くべきか」「どれだけ留まるべきか」「いつ分解されるべきか」が決まります。これを研究者たちは「リン酸化バーコード」と呼んでいます。
💡 用語解説:リン酸化(phosphorylation)とは
タンパク質に「リン酸基(PO4)」が付加される化学修飾です。タンパク質の中の特定のアミノ酸(セリン・スレオニン・チロシン)に、酵素(キナーゼ)がリン酸基を結合させます。これによりタンパク質の形・電荷・他のタンパク質との結合パートナーが変化し、機能が大きく変わります。リン酸化は生体内で最も普遍的なタンパク質スイッチで、AQP2のように「行き先を決める」シグナルとしても使われます。
4つのセリンの役割分担
⭐ S256:制御カスケードの起点
AVP刺激で:上昇
PKAが直接リン酸化する最重要残基。エクソサイトーシスを促進し、エンドサイトーシスを抑制。S264・S269がリン酸化されるための前提条件でもあります。
🔄 S261:分解のマーカー
AVP刺激で:低下(脱リン酸化)
他の3つとは逆の動きをする異色の残基。リン酸化されたままだと細胞内に留まり、ユビキチン化を経てプロテアソーム分解に向かうマーカーとして機能します。
🧭 S264:補助役
AVP刺激で:上昇
S256のリン酸化を前提に生じる残基。細胞膜への輸送後や、エンドソームを介したリサイクリング経路での補助的役割を担うと考えられています。
🛡️ S269:膜上での「居座り」役
AVP刺激で:上昇
S256に続いてリン酸化される残基。リン酸化されるとクラスリン・AP-2複合体との結合が阻害され、AQP2が細胞内に取り込まれるのを強力に防ぎます。膜上の安定化の決定打です。
重要なポイント:これらのリン酸化部位は「水通路の開閉」を制御しているわけではありません。あくまで「AQP2が細胞内のどこに存在すべきか」を決める局在シグナルとして機能していることが、リン酸化阻害変異体(S→A置換)と模倣変異体(S→D置換)を用いた実験から証明されています。
6. AQP2変異が引き起こす疾患:腎性尿崩症
AQP2遺伝子に病的な変異が生じると、腎性尿崩症(Nephrogenic Diabetes Insipidus / NDI)を発症します。バソプレシンは正常に分泌されているのに、腎臓側がそれに反応できないため、いくら水を飲んでも尿として大量に失われてしまう疾患です。
💡 用語解説:腎性尿崩症(NDI)の臨床像
主な症状は多尿(1日3〜20リットルの希釈尿)・激しい口渇・多飲です。乳児期発症の場合、ミルクや母乳だけでは水分を補えず、脱水・高ナトリウム血症・発熱・けいれん・発達遅延を起こすことがあります。先天性NDIの約90%はバソプレシン受容体(AVPR2)遺伝子のX連鎖劣性変異によりますが、残りの約10%がAQP2遺伝子の変異によるものです。
AQP2変異によるNDIで興味深いのは、「タンパク質自体は水を通す機能を保っているのに、適切な場所にたどり着けない」という病態であることです。これを「ミスルーティング(輸送異常)」と呼びます。変異の場所と種類によって、遺伝形式と病態メカニズムが大きく異なります。
常染色体劣性型NDI(AR-NDI):「不良品として出荷停止」
AR-NDIを引き起こす変異は、AQP2遺伝子全体に散在しています。多くは「クラスII変異」と呼ばれ、タンパク質の立体構造を狂わせます(ミスフォールディング)。たとえばG215S変異では、第6膜貫通ヘリックスの正常な折り畳みが破壊されてしまいます。
細胞内で新たに作られたタンパク質は、小胞体(ER)という工場で品質チェックを受けます。立体構造に異常があるタンパク質は「不良品」と判定され、ERから出ることを許されず、最終的にプロテアソームで分解されてしまいます。これがAR-NDIの分子病態です。
💡 用語解説:常染色体劣性遺伝(じょうせんしょくたいれっせいいでん)
2本ある染色体のうち、両方に変異がある場合のみ発症する遺伝形式です。両親はそれぞれ片方だけに変異を持つ「保因者(キャリア)」で、健康な状態。両親が保因者の場合、子に発症する確率は25%、保因者になる確率は50%、健康な子になる確率は25%です。キャリアスクリーニング検査について詳しくはこちら。
常染色体顕性型NDI(AD-NDI):「混ざって基底膜側に逃げる」
AD-NDIを引き起こす変異はC末端領域に集中し、その多くがフレームシフト変異(721delG・763-772del・812-818delなど)です。本来271アミノ酸のAQP2が、これらの変異により330〜333アミノ酸の異常に長いタンパク質へと延長されてしまいます。
この変異タンパク質の厄介な点は、立体構造の崩れが軽度であるため、正常なタンパク質と混ざり合ってヘテロ四量体を形成できることです。本来なら正常なAQP2は集合管の管腔側(尿側)に並ぶべきなのに、変異タンパク質が1つでも混じったヘテロ四量体は、基底膜側(血管側)へと誤って配送されてしまうのです。
💡 用語解説:ドミナントネガティブ効果(優性阻害効果)
変異タンパク質が、正常タンパク質の働きを積極的に妨害する現象です。AD-NDIの場合、4つのモノマーが集まる四量体のうち、純粋に正常モノマーだけで構成されるものは1/16(=½⁴)しかありません。残り15/16には変異モノマーが混じっており、これらが基底膜側へと「全体を引っ張っていく」のです。片方のアレルが正常なのに発症するのはこのためです。
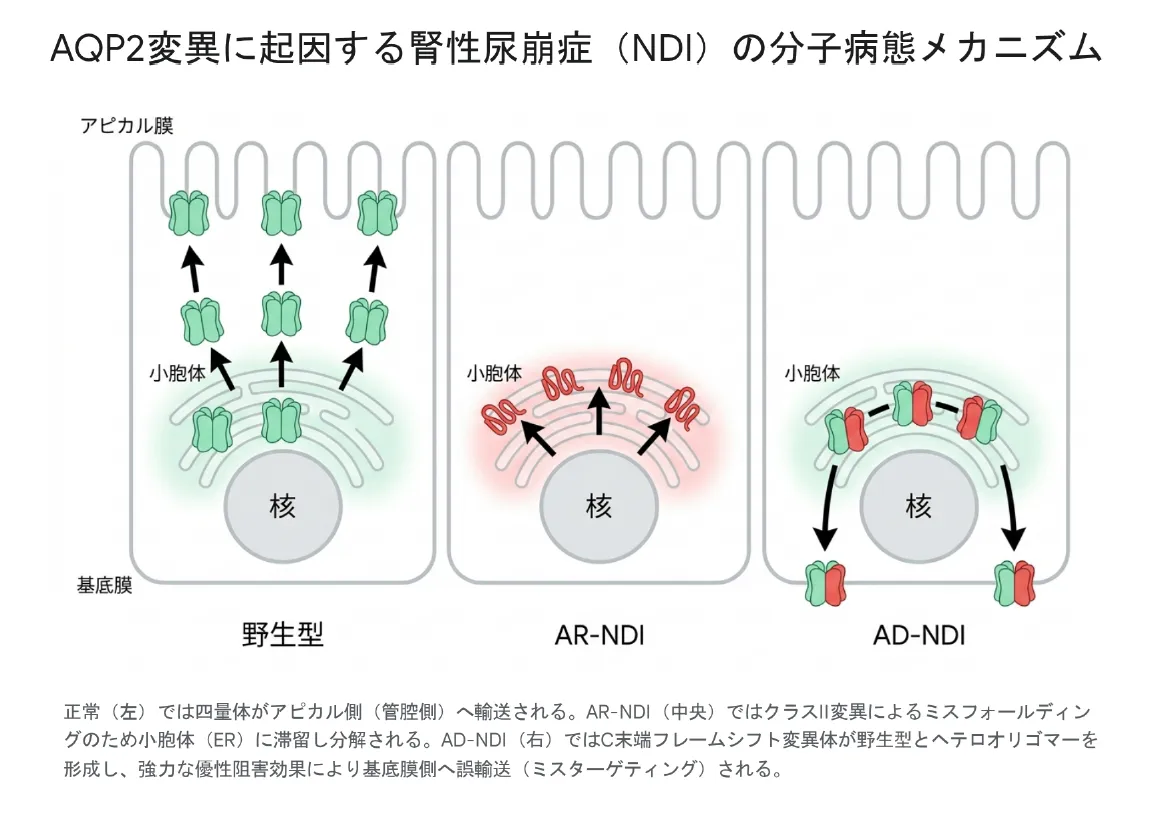
正常(左)ではAQP2の四量体がアピカル側(管腔側)へ輸送され、水分子を再吸収する。AR-NDI(中央)ではクラスII変異によるミスフォールディングのため小胞体(ER)に滞留し分解される。AD-NDI(右)ではC末端フレームシフト変異体が野生型とヘテロオリゴマーを形成し、強力な優性阻害効果により基底膜側へ誤輸送(ミスターゲティング)される。
| 特徴 | AR-NDI(常染色体劣性) | AD-NDI(常染色体顕性) |
|---|---|---|
| 変異の場所 | 遺伝子全体に散在 | C末端領域に集中 |
| 変異の種類 | 主にミスセンス変異 | フレームシフト変異が多い |
| 分子病態 | 小胞体(ER)滞留・分解 | 基底膜側への誤輸送 |
| 作用機序 | 機能喪失(ロス・オブ・ファンクション) | ドミナントネガティブ効果 |
| 発症するために必要なアレル | 両アレルの変異 | 片アレルの変異で発症 |
| 表現型の重症度 | 重症 | 部分型(やや軽症)の傾向 |
7. 診断と遺伝子検査
AQP2関連の腎性尿崩症が疑われる場合、まず臨床的に「中枢性尿崩症」との鑑別が行われます。デスモプレシン(DDAVP)負荷試験で尿浸透圧が反応しない場合に、腎性尿崩症が確定的となります。さらに病因の特定のため、AVPR2とAQP2の遺伝子検査が行われます。
💡 用語解説:トリオ全エクソーム解析(Trio-WES)
WES(Whole Exome Sequencing)とは、ヒトゲノムの中でタンパク質をコードするエクソン領域(全体の約2%)をまとめて解読する次世代シーケンス法です。「トリオ」とは患者本人+両親の3名同時解析を指し、親には存在せず子だけに新たに生じたデノボ変異を効率的に同定できます。原因不明の多尿が乳幼児期に見つかった場合、トリオWESによってAQP2のホモ接合性ミスセンス変異(c.398T>A/p.Val133Gluなど)が新たに同定された症例も近年報告されています。
遺伝カウンセリングの重要性
AQP2変異が同定された場合、家族計画や次子の見通しについての遺伝カウンセリングが極めて重要になります。AR-NDIとAD-NDIでは再発率が大きく異なるため、正確な遺伝形式の把握が不可欠です。出生前診断や着床前診断の選択肢、保因者検査などについて、臨床遺伝専門医による包括的な情報提供と心理的サポートが望まれます。
妊娠前の保因者スクリーニングは、米国人類遺伝学会(ACMG)でも推奨されています。米国人類遺伝学会の推奨内容や、女性版拡大保因者検査787・男性版拡大型保因者検査の詳細をご参照ください。
8. 最新治療研究:受容体をバイパスする新しいアプローチ
先天性NDI(特にAVPR2変異)や、リチウム製剤などによる薬剤性NDIに対しては、従来のバソプレシン補充療法(デスモプレシン)はほとんど効果がありません。受容体側が反応しないからです。そこで世界中の研究者は、「壊れたAVPR2を迂回(バイパス)して、下流のAQP2を直接動かす」という新発想の治療戦略を研究しています。
スタチン系薬剤によるアクチン骨格の再構築
脂質異常症の標準治療薬として広く使われているスタチン系薬剤(HMG-CoA還元酵素阻害薬)が、予想外にもAQP2の細胞膜集積を促進することが分かりました。スタチンは肝臓でコレステロール合成を阻害するだけでなく、副次的に細胞内のイソプレノイド(FPP・GGPP)を枯渇させます。これにより、低分子量GTPアーゼRhoAの脂質修飾(プレニル化)が阻害され、F-アクチンバリアが解除されるのです。
バソプレシンシグナルが完全に欠如した状態でも、AQP2が細胞膜へ移行する——つまり「AVPR2をスキップしてAQP2だけを動かす」という、まさに従来の常識を覆すアプローチです。既存薬の再利用(ドラッグ・リパーパシング)として、現在NDI患者を対象とした臨床試験が進められています。
PDE阻害薬によるcGMP/cAMP増幅
バソプレシン-cAMP-PKA経路を完全に迂回するもう一つの強力な経路が、NO/cGMPシグナル経路です。NO(一酸化窒素)が産生されるとcGMPが増加し、cGMP依存性キナーゼ(PKG)がPKAの代役としてAQP2のトラフィッキングを駆動します。
この経路を増幅するため、PDE5阻害薬のシルデナフィル(cGMP分解を防ぐ)や、PDE4阻害薬のロリプラム(cAMP分解を防ぐ)などが研究されています。Aqp2-F204V変異マウス(人間のAR-NDIをよく模倣する貴重な動物モデル)を用いた実験では、ロリプラムが尿浸透圧を有意に上昇させ、尿濃縮能を回復させることが証明されました。
その他の有望なアプローチ
💊 NSAIDs / EP受容体作動薬
プロスタグランジンE2(PGE2)はEP3受容体を介してアクチン重合を促進し、AQP2の膜移行にブレーキをかけます。インドメタシンなどのNSAIDsはCOXを阻害してこのブレーキを解除します。EP2・EP4選択的アゴニストもマウスモデルで有効性が示されています。
💊 EGFR阻害薬(エルロチニブ)
抗がん剤のエルロチニブが、RSK・PDK1経路を介してAQP2のS256を直接リン酸化することが2024年に解明されました。AVPと同様の膜集積効果をもたらす、まったく新しい経路の発見です。
💊 SERMs(タモキシフェン)
乳がん治療薬として知られる選択的エストロゲン受容体モジュレーターのタモキシフェンは、リチウム誘発性NDIのマウスモデルでAQP2発現低下を抑え、尿濃縮能を改善する保護効果を示しています。
💊 AI主導の薬剤再開発
AI創薬プラットフォーム(PLATO)による1882種の既存薬の逆スクリーニングから、ロイコトリエン受容体拮抗薬ザフィルルカストがAVPR2の新規アンタゴニスト候補として同定されました。1桁ナノモル濃度で作用します。
9. 尿中エクソソームAQP2:非侵襲的バイオマーカーとしての応用
AQP2の臨床応用は治療研究だけにとどまりません。近年、尿中に分泌される細胞外小胞(エクソソーム)に含まれるAQP2を解析することで、腎生検なしで腎臓深部の状態を評価する「リキッドバイオプシー」が現実のものになっています。
💡 用語解説:エクソソーム(exosome)
細胞から分泌される直径30〜150nm程度の極小な膜小胞です。中には由来細胞特有のタンパク質・RNA・DNAが安定した形で内包されており、まさに「細胞からの手紙」と言える存在です。腎集合管の主細胞からも管腔内(尿)にエクソソームが分泌されており、これを採取・解析することで細胞を直接取り出さずに分子レベルの情報を得ることができます。
📉 慢性腎臓病(CKD)
進行期CKD(ステージG4・G5)患者ではAQP1・AQP2レベルが著しく低下。AQP1+AQP2の組み合わせ評価でAUC=0.945・特異度100%という極めて高い診断精度が報告されています。
📈 糖尿病性腎症
CKDと対照的に、糖尿病性腎症ではエクソソーム内のAQP5・AQP2レベルが上昇。c-メガリンの増加と並行して観察され、初期段階の早期発見マーカーとして注目されています。
🫘 腎移植後モニタリング
移植後1日目にAQP2レベルが一時的に低下し、これは「急性利尿現象」の分子的説明として注目されています。移植腎の機能回復をリアルタイムで追跡できる可能性があります。
よくある質問(FAQ)
🏥 遺伝子検査・遺伝カウンセリングについて
AQP2遺伝子検査・腎性尿崩症の遺伝カウンセリング・
家族計画に関するご相談は、臨床遺伝専門医が在籍するミネルバクリニックへ。
関連記事
参考文献
- [1] NCBI Gene. AQP2 aquaporin 2 [Homo sapiens] (Gene ID: 359). [NCBI Gene]
- [2] UniProtKB. AQP2 – Aquaporin-2 – Homo sapiens. P41181. [UniProt]
- [3] OMIM #125800. Diabetes Insipidus, Nephrogenic, Autosomal Dominant. [OMIM]
- [4] OMIM #222000. Diabetes Insipidus, Nephrogenic, Autosomal Recessive. [OMIM]
- [5] MedlinePlus Genetics. AQP2 gene. [MedlinePlus]
- [6] Moeller HB, et al. Vasopressin and the Regulation of Aquaporin-2. Clin Exp Nephrol. 2013. [PMC3775849]
- [7] Hoffert JD, et al. Phosphorylation of aquaporin-2 regulates its endocytosis and protein–protein interactions. PNAS. 2010. [PNAS]
- [8] Frick A, et al. X-ray structure of human aquaporin 2 and its implications for nephrogenic diabetes insipidus and trafficking. PNAS. 2014. [PMC4035913]
- [9] Moeller HB, et al. AQP2: Mutations Associated with Congenital Nephrogenic Diabetes Insipidus and Regulation by Post-Translational Modifications and Protein-Protein Interactions. Cells. 2020. [MDPI Cells]
- [10] Bichet DG, et al. Hereditary Nephrogenic Diabetes Insipidus: Pathophysiology and Possible Treatment. Int J Mol Sci. 2017. [MDPI IJMS]
- [11] Li JH, et al. Bypassing vasopressin receptor signaling pathways in nephrogenic diabetes insipidus. Semin Nephrol. 2008. [PMC2494582]
- [12] Procino G, et al. A novel therapeutic effect of statins on nephrogenic diabetes insipidus. J Cell Mol Med. 2014. [PMC4407600]
- [13] Reduced urinary release of AQP1- and AQP2-bearing extracellular vesicles in patients with advanced chronic kidney disease. Physiol Rep. 2021. [PMC8387789]
- [14] Ribosomal s6 kinase is a mediator of aquaporin-2 S256 phosphorylation and membrane accumulation after EGFR inhibition with erlotinib. Am J Physiol Renal Physiol. 2024. [APS Journal]