(更新日:2025/05/26)
発達障害・自閉症・知的障害染色体シーケンス解析とは
次世代シーケンシング(NGS)の出現は、臨床遺伝子検査に革命をもたらしました。 NGS技術の進歩により、臨床遺伝学は単一遺伝子解析から多遺伝子パネル、エクソームシーケンス、さらには全ゲノムシーケンスへと発展しました。 NGSは、これまでに達成されたことのない解像度でコピー数およびシーケンスバリアントの特性解析を可能にし、その結果、診断を受ける患者数が大幅に増加しました。 発達遅延や知的障害を持つ子供の評価におけるエクソーム解析の使用により、49%という高い診断率が示されています(
【用語】
1. 次世代シーケンシング(NGS: Next-Generation Sequencing)
DNAやRNAの塩基配列を一度に大量に解析する最新の遺伝子解析技術です。従来の方法に比べて高速かつ低コストで、大量の遺伝情報を短時間で読み取ることができます。
2. 単一遺伝子解析
特定の遺伝子を対象にその配列を詳しく調べる遺伝子検査です。疾患の原因となる遺伝子変異(突然変異)を見つけるために行われ、主に遺伝性疾患の診断や家族性疾患のリスク評価に用いられます。一般的な方法にはSangerシーケンシングや次世代シーケンシング(NGS)があり、精度が高く、1つの遺伝子に特化して詳細な情報を提供します。例として、筋ジストロフィー、嚢胞性線維症、遺伝性がんなどの診断に広く使われています。迅速で比較的コストが抑えられる点が特徴です。
3. 多遺伝子パネル(Multi-Gene Panel)
複数の遺伝子を同時に解析する遺伝子検査です。特定の疾患や症状に関連する遺伝子群を一度に調べ、病気のリスクや診断、治療方針の決定に役立ちます。次世代シーケンシング(NGS)を用いることで、効率的かつ経済的に多くの遺伝子を網羅的に解析可能です。がんのリスク評価、遺伝性疾患の診断、不明な病態の解明に広く応用されています。検査結果の解釈には専門的な知識が必要で、結果に応じた適切な医療支援が重要です。
4. エクソームシーケンス(Exome Sequencing)
DNAのうちタンパク質を作る遺伝子の部分(エクソン)の配列を解析する技術です。ヒト全ゲノムの約1〜2%に相当するエクソン領域に集中し、遺伝性疾患やがんなどの原因となる遺伝子変異を効率的に見つけることができます。次世代シーケンシング(NGS)技術を使用し、数千の遺伝子を一度に解析できるため、疾患の診断精度が高まります。全ゲノム解析よりコストが低く、医療や研究分野で広く用いられていますが、非エクソン領域の変異は検出できません。
5. 全ゲノムシーケンス(Whole Genome Sequencing, WGS)
DNAのすべての塩基配列(約30億塩基対)を網羅的に解析する技術です。エクソン(タンパク質をコードする部分)だけでなく、イントロンや調節領域などの非コード領域も含め、ゲノム全体を対象とします。遺伝性疾患の診断、がんのゲノム解析、新しい遺伝子変異の発見などに利用されます。次世代シーケンシング(NGS)技術を用いて行われ、変異や構造異常の検出に優れていますが、コストやデータ解析の複雑さが課題です。
6. ゲノムワイドコピー数バリアント解析(Genome-Wide Copy Number Variant Analysis, CNV解析)
DNAのコピー数変化(欠失や重複)を全ゲノムレベルで検出する解析手法です。染色体全体を対象にし、疾患関連遺伝子や構造異常を見つけるため、遺伝性疾患、発達障害、がんの診断に広く使われます。主な手法には、マイクロアレイ(CGHアレイ)や次世代シーケンシング(NGS)があり、染色体異常の程度や位置を特定可能です。精密な解析が可能ですが、点突然変異は検出できないため、他の手法と併用することが多いです。
7. FMR1リピートエクステンション解析(FMR1 Repeat Expansion Analysis)
X染色体上のFMR1遺伝子内のCGGリピート配列の数を測定する検査です。この遺伝子の異常なリピート数の増加は、脆弱X症候群(Fragile X Syndrome)の原因となります。通常、リピート数が55回以下なら正常ですが、55〜200回は前変異、200回以上は完全変異とされ、知的障害や発達遅延などの症状を引き起こします。主な解析手法はPCRとサザンブロット法で、遺伝性疾患の診断、家族内の保因者スクリーニングに広く用いられています。
8. Integrated Reflex System(統合反射システム)
遺伝子検査や診断検査において、特定の検査結果に応じて自動的に追加検査が行われる検査プロセスのことです。
分子診断学の新たなパラダイム
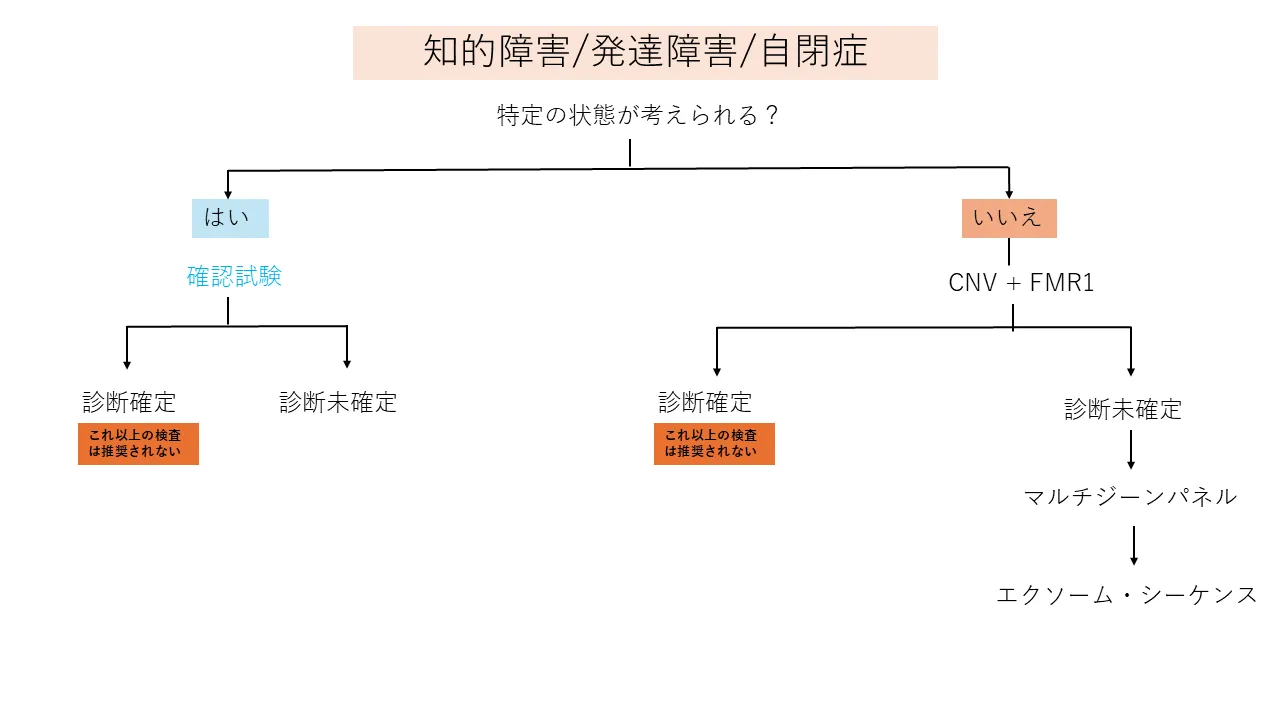
染色体シーケンス解析は、知的障害を持つ患者を対象に包括的な検査オプションを提供しています。 これまでCNV解析の標準的な手法であった染色体マイクロアレイ解析(CMA)に対し、染色体シーケンス解析は、より優れた解像度(デフォルトでは1遺伝子以上、臨床記録が提供された場合は2エクソンまで)でCNVを検出できるプラットフォームを提供しています。さらに、染色体シーケンス解析はFMR1リピート拡張解析(知的障害を持つ患者の検査で推奨される第一選択検査)を組み込んでおり、単一遺伝子、多遺伝子パネル、エクソームのいずれかにリフレックスする機能も備えているため、診断率が大幅に向上します。
米国医遺伝学会や米国小児科学会などの専門学会は、知的障害児の遺伝学的評価の最初に、コピー数多型やFMR1拡大の解析を推奨している。 染色体シーケンス解析は、これら2つの検査を1つの検査に統合し、多遺伝子パネルまたは全エクソーム解析へのリフレクションを可能にすることで、より時間と費用対効果の高い選択肢を提供します。
【用語】
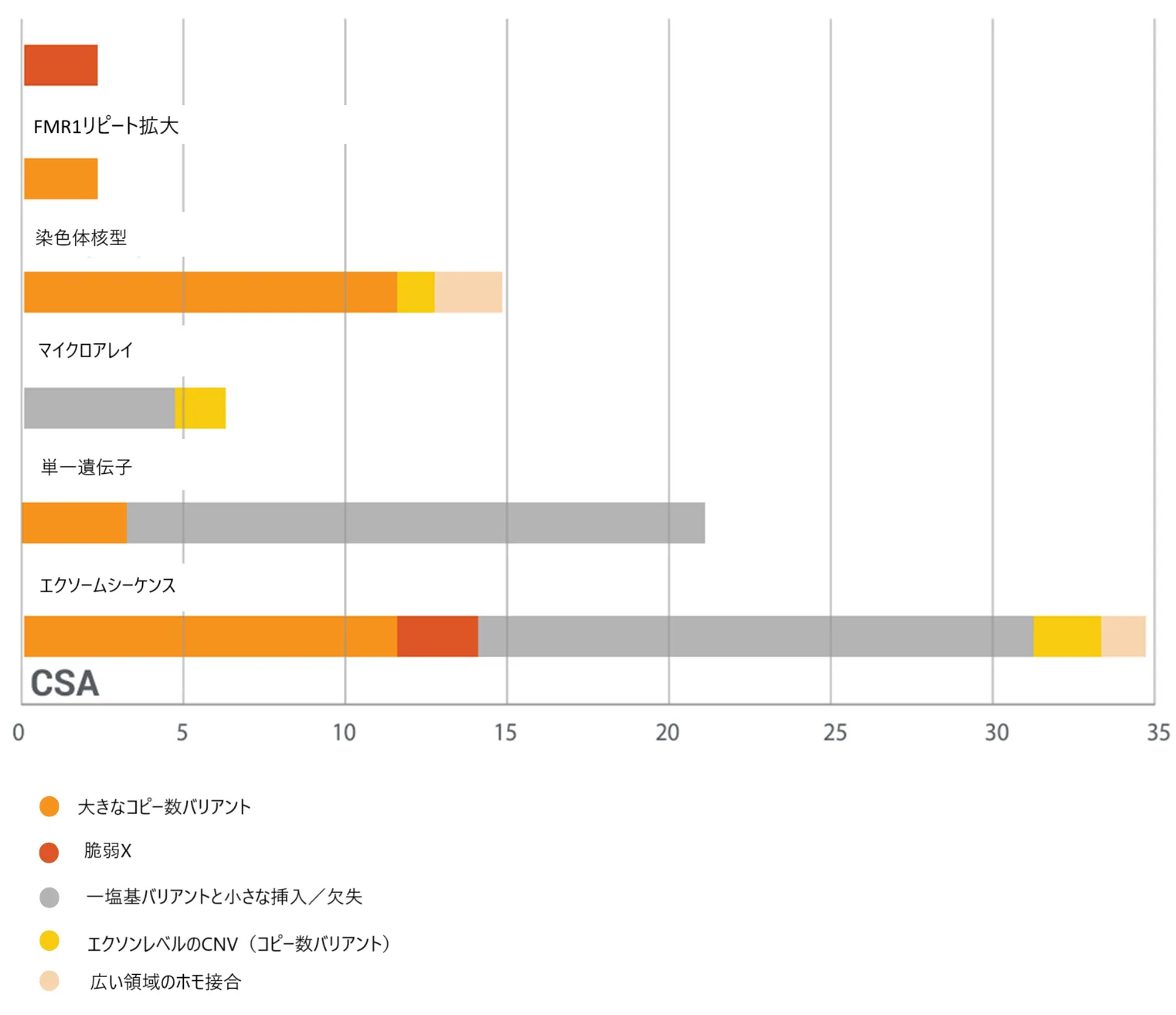
Large CNVs(ラージ コピー数変異)(大きなコピー数バリアント)
DNAの一部が大きく欠けたり(欠失)、増えたり(重複)する遺伝的な異常です。通常、DNA配列の50kb(キロ塩基対)以上の変化がLarge CNVとされます。
脆弱X症候群(Fragile X Syndrome)
X染色体上のFMR1遺伝子の異常によって起こる遺伝性疾患です。FMR1遺伝子内のCGGリピート配列が異常に増加(200回以上)すると、遺伝子の機能が停止し、知的障害、発達遅延、行動問題(自閉症様の特徴)などが現れます。通常、CGGリピートは55回以下ですが、55〜200回は前変異とされ、将来の発症リスクが高くなります。症状の重さはリピート数や性別によって異なり、男性が重症化しやすい傾向があります。早期診断と介入が、発達支援や生活の質の向上に重要です。
Single Nucleotide Variants (SNVs)
DNA配列の1つの塩基が別の塩基に置き換わる変異です。一般的な遺伝的変異の一種で、病気の原因となる場合もあります。
Small Insertions/Deletions (Indels)
DNA配列に数塩基の挿入(Insertion)または欠失(Deletion)が発生する変異です。これにより、タンパク質の構造や機能が変わることがあります。
Exon Level CNVs(エクソンレベルのコピー数変異)
遺伝子内のエクソン(タンパク質をコードするDNA配列)の欠失(失われる)または重複(増える)を指します。これにより、正常なタンパク質が作れなくなり、遺伝性疾患やがんなどの病気を引き起こす可能性があります。
Large Areas of Homozygosity(大規模なホモ接合性領域)
染色体の特定の部分で、父親と母親から受け継いだDNA配列が同一である領域を指します。この状態は、近親婚や片親性ダイソミー(UPD)の結果として発生することがあります。
1. Kuperberg, M., et al., Utility of Whole Exome Sequencing for Genetic Diagnosis of Previously Undiagnosed Pediatric Neurology Patients. Journal of child neurology, 2016. 31(14): p. 1534-1539. 2. Schaefer, G.B., et al., Clinical genetics evaluation in identifying the etiology of autism spectrum disorders: 2013 guideline revisions. Genetics in Medicine, 2013. 15(5): p. 399-407. 3. Moeschler, J.B. and M. Shevell, Comprehensive evaluation of the child with intellectual disability or global developmental delays. Pediatrics, 2014. 134(3): p. e903-e918. 4. Vissers, L.E., C. Gilissen, and J.A. Veltman, Genetic studies in intellectual disability and related disorders. Nat Rev Genet, 2016. 17(1): p. 9-18. 5. Van Karnebeek, C.D., et al., Diagnostic investigations in individuals with mental retardation: a systematic literature review of their usefulness. European journal of human genetics: EJHG, 2005. 13(1): p. 6.
Quick facts
• 染色体シーケンス解析は反射システムです。これは、多数のコピー数バリアント、エクソンレベルのコピー数バリアント、FMR1の拡大、ホモ接合領域、および表現型関連遺伝子の配列解析を含みます。
CNV(コピー数バリアント)解析 + FMR1リピート拡大
2~4週間
CNV解析 + FMR1リピート拡大 + 多遺伝子パネル
3~5週間
CNV解析 + FMR1リピート拡大 + エクソーム解析
5~7週間
• コピー数バリアントの感度:1遺伝子以上、詳細な臨床記録が提供される場合は2エクソン以上
診断率を高めるために
●希少疾患の診断課題
●希少疾患の診断と遺伝子検査の進化
希少疾患の診断は、必ずしも治療法の提供を意味するわけではありませんが、治療、緩和ケア、または支援につながる重要な一歩です。この情報が得られることで、患者と家族は安心感を得られ、将来的な家族計画の選択肢も広がります。
近年、技術と医療の進歩により、遺伝学の専門家が希少疾患の原因を特定できる機会が増えました。これにより、知的障害、先天性異常、遺伝性症候群の評価に役立つ包括的な遺伝子検査の選択肢が拡大しています。最新の染色体シーケンス解析は、複数の検査を1つのパッケージに統合し、診断の精度と臨床効率を大幅に向上させます。
●遺伝子検査の標準プロセスと課題
希少疾患の80%は遺伝性であるとされています。小児の遺伝性疾患を評価する最初のステップとして、一般的に染色体マイクロアレイ(CMA)が使用されます。CMAはDNA配列の欠失や重複を検出しますが、診断率は約12%にとどまります。残る88%の患者では、次に行うべき検査の選択が難しく、段階的な診断プロセスが課題となります。
●包括的な染色体シーケンス解析の利点
この包括的なアプローチにより、診断率は約40%に向上し、従来のCMAと比較して3倍以上の成果が得られます。最近の研究では、シーケンス分析による診断の可能性がCMAの8倍にのぼることが確認されています。
●診断精度の向上とカスタマイズ対応
検査費用
550,000(税込)
遺伝カウンセリング料金はおひとり様別途16,500円(税込)。検査を受けなくても遺伝カウンセリング料金は診察料ですのでお支払いください。
ミネルバクリニックでは患者さまへ正しい情報をお届けするために、
発達障害・学習障害・知的障害関連コラム
この記事の監修・執筆者:仲田 洋美
(臨床遺伝専門医/がん薬物療法専門医/総合内科専門医)
ミネルバクリニック院長。1995年に医師免許を取得 後、
臨床遺伝学・内科学・腫瘍学を軸に診療を続けてきました。
のべ10万人以上のご家族の意思決定と向き合ってきた臨床遺伝専門医 です。
出生前診断(NIPT・確定検査・遺伝カウンセリング)においては、
検査結果の数値そのものだけでなく、
「結果をどう受け止め、どう生きるか」までを医療の責任と捉え、
一貫した遺伝カウンセリングと医学的支援を行っています。
ハイティーンの時期にベルギーで過ごし、
日本人として異文化の中で生活した経験があります。
価値観や宗教観、医療への向き合い方が国や文化によって異なることを体感しました。
この経験は現在の診療においても、
「医学的に正しいこと」と「その人にとって受け止められること」の両立を考える姿勢の基盤となっています。
また、初めての妊娠・出産で一卵性双生児を妊娠し、
36週6日で一人を死産した経験があります。
その出来事は、妊娠・出産が女性の心身に与える影響の大きさ、
そして「トラウマ」となり得る体験の重みを深く考える契機となりました。
現在は、女性を妊娠・出産のトラウマから守る医療を使命の一つとし、
出生前診断や遺伝カウンセリングに取り組んでいます。
出生前診断は単なる検査ではなく、
家族の未来に関わる重要な意思決定です。
年齢や統計だけで判断するのではなく、
医学的根拠と心理的支援の両面から、
ご家族が後悔の少ない選択をできるよう伴走することを大切にしています。
日本人類遺伝学会認定 臨床遺伝専門医/日本内科学会認定 総合内科専門医/
日本臨床腫瘍学会認定 がん薬物療法専門医。
2025年には APAC地域における出生前検査分野のリーダーとして国際的評価を受け 、
複数の海外メディア・専門誌で特集掲載