ユビキチンを基質タンパク質に付加することをユビキチン化(またはユビキチン化、ユビキチニル化)といいます。
ユビキチンとは
ユビキチンは、真核生物のほとんどの組織に存在する小さな(8.6kDa)制御タンパク質で76個のアミノ酸からできています。ユビキチンは他のタンパクの修飾に用いられてタンパク質の分解、DNAの復や翻訳調節、シグナル伝達など多種多様な生命現象に関わっています。ユビキタスに存在している、つまりどこにでもあることからこの名称がつきました。ユビキチンは進化的な保存性が高く、すべての真核生物でほとんど同じアミノ酸配列をもっています。UBB、UBC、UBA52、RPS27Aの4つの遺伝子がユビキチンをコードしています。
ユビキチン化の役割
ユビキチン化は、プロテアソームによる分解の目印となったり、細胞内の位置を変えたり、活性に影響を与えたり、タンパク質の相互作用を促進したり阻止したりと、様々な形でタンパク質に影響を与えます。
ユビキチン化には、ユビキチン活性化酵素(E1)、ユビキチン共役酵素(E2)、ユビキチンリガーゼ(E3)による活性化、共役化、ライゲーションの3つの主なステップがあります。
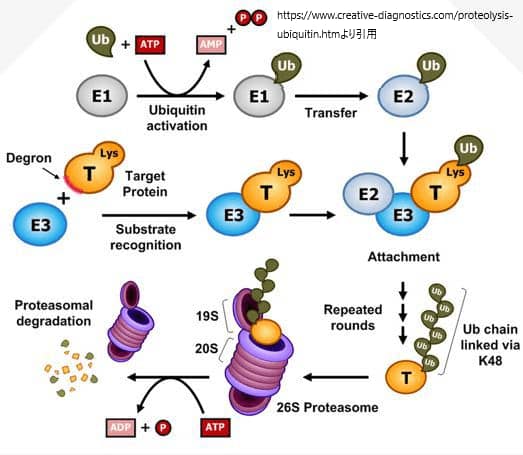
ユビキチンが各基質に結合する様式は以下の通りです。
- リジン残基:イソペプチド結合
- システイン残基:チオエステル結合
- セリン残基・スレオニン残基:エステル結合
- タンパク質のN末端のアミノ基:ペプチド結合
タンパク質の修飾は、単一のユビキチンタンパク質である場合(モノユビキチン化)と、ユビキチンの鎖である場合(ポリユビキチン化)があります。
二次ユビキチン分子は、必ず前のユビキチン分子の7つのリジン残基の一つまたはN末端のメチオニンのいずれかに連結されています。これらの「連結」残基は、「K」または「M」(それぞれリジンとメチオニンの1文字のアミノ酸表記)と、ユビキチン分子内の位置を示す数字でKたとえばM1という風に表記されます。
最初のユビキチン分子は、C末端のカルボキシル基を介して、標的タンパク質の特定のリジン、システイン、セリン、スレオニン、N末端に共有結合しています。
ポリユビキチン化は、別のユビキチンのC末端が、先に付加されたユビキチン分子の7つのリジン残基または最初のメチオニンのうちの1つに結合し、鎖を形成することで起こる。このプロセスを何度か繰り返すことで、複数のユビキチンが付加される。特定のリジン(主にK48とK29)に対するポリユビキチン化のみがプロテアソームによる分解に関係しています。
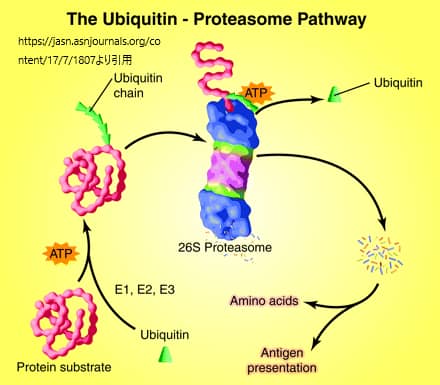
ユビキチン(Ub)-プロテアソーム経路(UPP)によるタンパク質分解。ユビキチン(Ub)は、3つの酵素が関与するATP依存性のプロセスによって、分解される予定のタンパク質に結合する。26Sプロテアソームに認識されるには、基質となるタンパク質に5個のUb分子が結合していれば十分である。ATP依存的な反応に加えて、Ubが除去され、タンパク質は直線化されてプロテアソームの中心核に注入され、そこでペプチドにまで消化される。ペプチドは、細胞質内のペプチダーゼによってアミノ酸に分解されたり、抗原提示に利用されたりする。
その他のポリユビキチン化(K63、K11、K6、M1など)やモノユビキチン化は、エンドサイト輸送、炎症、翻訳、DNA修復などのプロセスを制御していると考えられています。
この記事の著者:仲田洋美医師
医籍登録番号 第371210号
日本内科学会 総合内科専門医 第7900号
日本臨床腫瘍学会 がん薬物療法専門医 第1000001号
臨床遺伝専門医制度委員会認定 臨床遺伝専門医 第755号








