WWドメインは,約40個のアミノ酸からなり、2つの不変のトリプトファン残基を持ち、PPXY,PPLP,またはPPRモチーフを含む短いプロリンリッチ配列に結合する。トリプトファンのアミノ酸記号がWと表示されるため、WWドメインと呼ばれる。プロリン異性化酵素Pin1/Ess1とそのホモログであるスプライシング因子Prp40およびユビキチンリガーゼRsp5に含まれる小さなサブクラスのWWドメインは、有糸分裂期のリン酸化タンパク質内のホスホセリン-プロリンモチーフに特異的に結合することを示している。
WWドメインはプロリンを多く含む配列に結合する。認識する配列はSH3ドメインと類似しており、他のタンパクと相互作用して細胞内シグナル伝達などに関与する。
リン酸化特異的なWWドメインの機能は、プロリン異性化酵素であるPin1について最もよく理解されている。Pin1は、有糸分裂の進行を遅らせるタンパク質であるが、有糸分裂の終了やDNA複製チェックポイントにも必要である。Pin1は、WWドメインに加えて、そのC末端にプロリン異性化酵素(ロタマーゼ)ドメインを持ち、pSer/Thr-Pro結合の特異的なシス-トランス異性化を触媒する。Pin1の生物学的活性には、WWドメインを介したpS-Pの結合と,ロタマーゼを介したpS-Pの異性化の両方が必要である。また,Pin1は,プロテインホスファターゼによる基質の脱リン酸化を促進するが,これらの作用には、pSer-Pro結合がトランスにあることが必要である。WWドメインはトランス型の幾何異性体にしか結合できないため、その主な役割は、脱リン酸化のためにトランス型の異性体の生成物を安定化させることであると考えられる。WWドメインが促進する基質の脱リン酸化は、細胞周期の進行と転写伸長の制御の両方におけるWWドメインの機能の一般的なメカニズムであると考えられる。
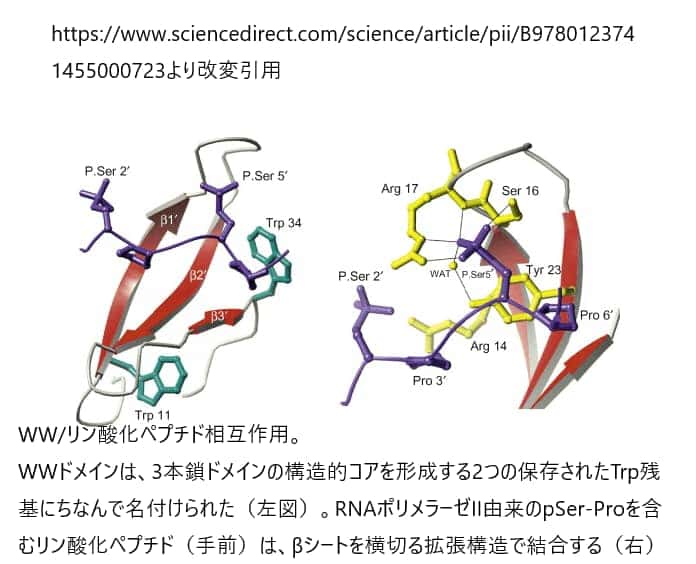
WWドメインは、3本の逆平行なβストランドに折り畳まれ、タイプIIのポリプロリンヘリックスの中でプロリンリッチなリガンドを認識する単一の溝を形成する。異なるプロリンリッチモチーフに対する特異性は,主にβ1/β2鎖とβ2/β3鎖をつなぐループ領域内の残基によって決定されるが、これはFHAドメインが利用するリガンド結合のメカニズムに似ている。Pin1のWWドメインとRNAポリメラーゼIIのCTDに存在するYpSPTpSPSペプチドとの複合体の構造解析では,すべてのリン酸接触は第2のpSerとβ1/β2ループ内のペプチドの2つの残基(Ser-16とArg-17)およびβ2鎖内の1つの残基(Tyr-23)との間で行われていることが明らかになった。これらの発見は、大多数のWWドメインがループ1内にArg残基を持たないため、少数のWWドメインしかリン酸化配列モチーフを結合できない理由を説明するものである。
この記事の著者:仲田洋美医師
医籍登録番号 第371210号
日本内科学会 総合内科専門医 第7900号
日本臨床腫瘍学会 がん薬物療法専門医 第1000001号
臨床遺伝専門医制度委員会認定 臨床遺伝専門医 第755号






