テトラトリコペプチドリピート
テトラトリコペプチドリピート領域(TPR)は、様々なタンパク質に存在する構造モチーフである(文献)。TPRは、タンパク質間相互作用や多タンパク質複合体の形成を仲介する(文献)。TPRモチーフは34アミノ酸残基の3-16個のタンデムリピートから構成されているが、個々のTPRモチーフはタンパク質配列中に分散して存在することがある。TPRモチーフの配列は、大小のアミノ酸からなるパターンによって定義されるコンセンサス配列である。TPRモチーフは、バクテリアからヒトまで、様々な異なる生物で同定されている。TPRを含むタンパク質は、細胞周期の制御、転写制御、ミトコンドリアやペルオキシソームのタンパク質輸送、神経発生、タンパク質折り畳みなど、様々な生物学的プロセスに関与している。
TPRはヘリックス-ターン-ヘリックス配列をとり、隣接するTPRモチーフが平行にパッキングし、反平行のαヘリックスが繰り返されるスパイラルになっていることが分かっている。この2つのヘリックスをヘリックスA、ヘリックスBと呼ぶ。Helix AとHelix Bのパッキング角度は、1つのTPR内で約24度であり、右巻き超らせん形状を形成している。Helix Aは、Helix Bおよび次のTPRのHelix A’と相互作用する。2つのタンパク質表面が生成され、内側の凹んだ表面は主にヘリックスAの残基によって寄与され、もう一方の表面はヘリックスAとBの両方の残基によって構成されている。
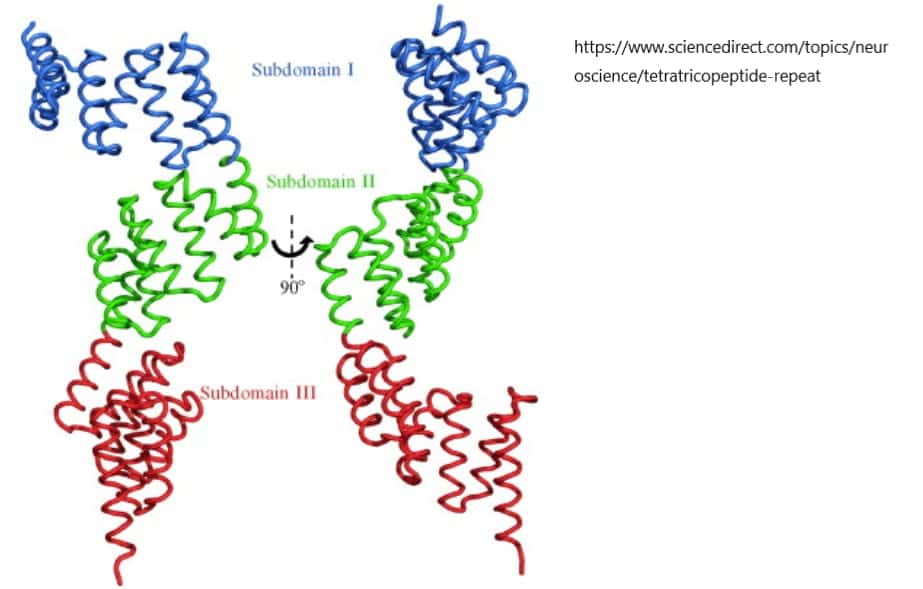
上図はP58(IPK) TPRドメインの全体構造 P58(IPK)を示している。TPRドメイン(残基35-393)には9つのTPRモチーフが存在する。TPR1-TPR3、TPR4-TPR6、TPR7-TPR9はそれぞれサブドメインI、II、IIIを構成している。3つのサブドメインは2本の長いヘリックスで連結されている。
この記事の著者:仲田洋美医師
医籍登録番号 第371210号
日本内科学会 総合内科専門医 第7900号
日本臨床腫瘍学会 がん薬物療法専門医 第1000001号
臨床遺伝専門医制度委員会認定 臨床遺伝専門医 第755号






