目次
この詳細な記事では、ヌクレオソームの基本構造と機能、その遺伝子調節における役割、およびクロマチン構造に与える影響について掘り下げます。最新の研究成果と、これらが将来の遺伝子療法にどのように応用され得るかも解説します。
ヌクレオソームの基礎
定義と基本構造
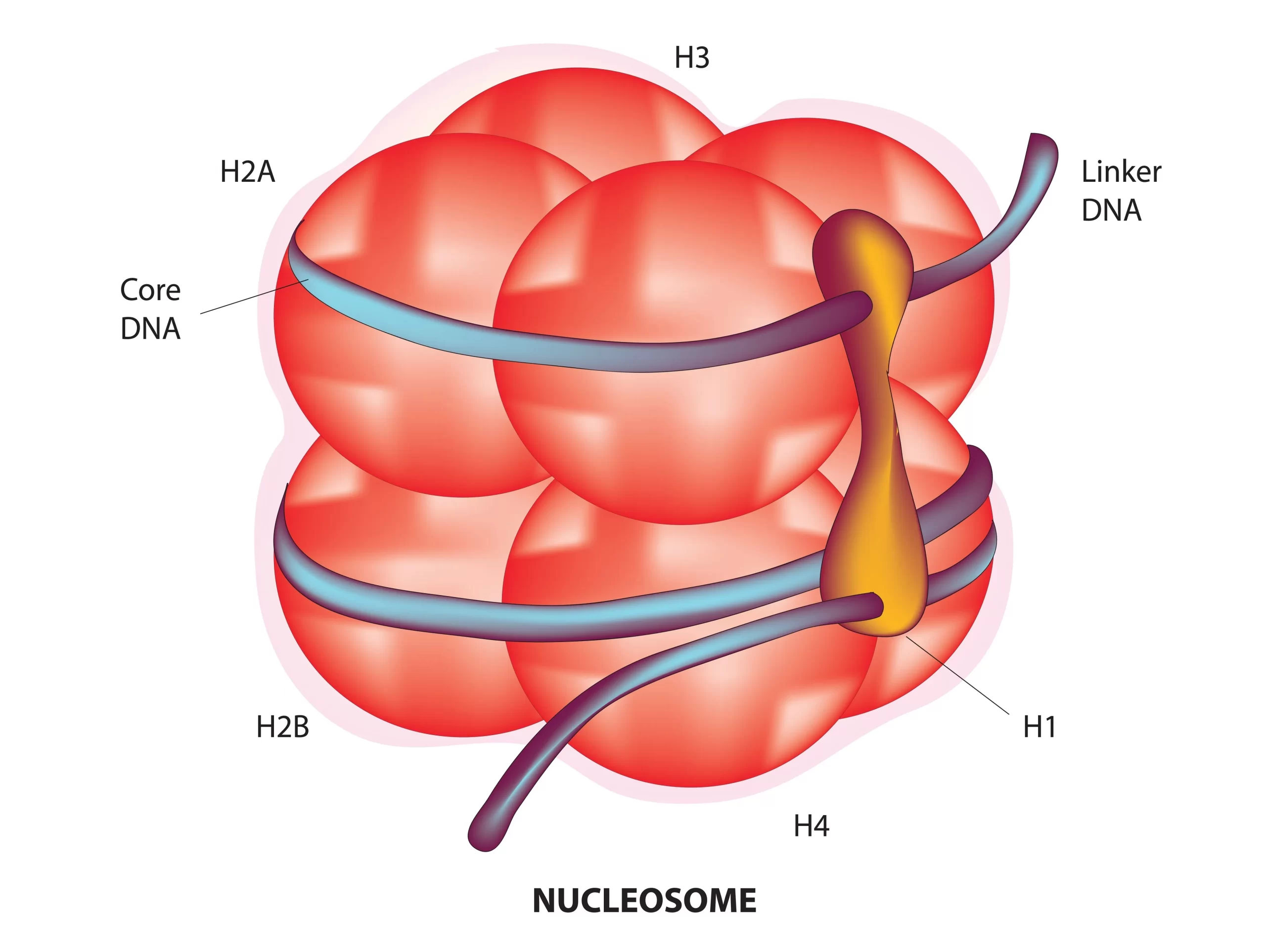
ヌクレオソームは、クロマチンの基本的な構成単位であり、約146ベースペアのDNAがヒストンタンパク質のオクタマー(8個のヒストンサブユニットから成る)を中心に1.65回螺旋状に巻きついて形成されています。この複合体は遺伝情報のコンパクト化、アクセス制御、さらには遺伝子の発現調節に重要な役割を担っています。
ヒストンオクタマーは、H2A、H2B、H3、およびH4の各ヒストンから2つずつ含まれる4種類のヒストンタンパク質で構成されています。これらのヒストンは、特にDNAとの相互作用およびヌクレオソーム間の連結に関与しており、遺伝子のオン・オフを制御する上で中心的な役割を果たしています。
ヌクレオソームの間にはリンカーDNAが存在し、その長さは細胞タイプや種によって異なりますが、通常10から80ベースペアの範囲です。このリンカーDNAの存在が、ヌクレオソーム同士の間隔を決定し、クロマチンの高次構造形成を助けます。
この構造により、DNAは細胞核内で非常にコンパクトに保管され、必要に応じて適切な遺伝情報が利用可能となります。ヌクレオソームのダイナミクスは、生物学的プロセスの中核をなす重要な要素であり、その機能と構造の詳細な理解が、遺伝学および分子生物学の分野での研究に不可欠です。
歴史的発展
ヌクレオソームの研究は、1970年代に遡ります。この分野での初期の重要な発見は、ロジャー・コーンバーグによるもので、彼は1974年にヌクレオソームがクロマチンの基本構造単位であることを初めて提案しました。彼の研究は、ヌクレオソームがDNAとヒストンタンパク質から構成されていることを示しました。これは、遺伝情報のコンパクト化と遺伝子のアクセシビリティの調節に重要な役割を果たしていることを明らかにしました。
この発見は、その後の分子生物学における多くの研究の礎を築きました。特に、ヌクレオソームが遺伝子の転写をどのように制御しているかの理解に繋がりました。また、クロマチン構造の詳細な研究により、ヒストンの修正が遺伝子表現にどのように影響を与えるかについての知見が深まりました。
1990年代に入ると、クロマチンリモデリング複合体とヌクレオソームの相互作用に関する研究が進展し、これらが遺伝的情報へのアクセスをどのように調節しているかが明らかになりました。これらの複合体は、ヌクレオソームをスライドさせることでDNAへのアクセスを可能にし、遺伝子の活性化または抑制を助けます。
21世紀に入ってからは、高度なイメージング技術と分子生物学的手法の進歩により、ヌクレオソームダイナミクスのさらに詳細な解析が可能となりました。これにより、ヌクレオソームの構造変動が細胞の発達や分化、さらには疾患の発生にどのように関与しているかの理解が進みました。
このように、ヌクレオソームの研究は分子遺伝学の中心的なテーマであり続けており、未だにその機能とメカニズムの解明に向けた研究が活発に行われています。これらの研究は、がんをはじめとする多くの疾患の治療法開発に貢献することが期待されています。
ヌクレオソームの機能と影響
遺伝子の調節における役割
ヌクレオソームは、その構造と配置によってDNAのアクセシビリティと遺伝子の活性を直接的に制御する重要な役割を果たしています。ヌクレオソームの配置とヒストンの修飾は、遺伝子の転写を可能にするか、または阻害するかを決定するため、遺伝子表現の調節において中心的な役割を担っています。
● DNAアクセシビリティの制御
ヌクレオソームはDNAを巻き付けることで、その領域の遺伝子が転写されるかどうかを影響します。ヌクレオソームが密集している領域では、転写因子や他の転写機構がDNAにアクセスしにくくなるため、遺伝子の活性が抑制されます。逆に、ヌクレオソームが緩やかに配置されているか、一部が取り除かれている領域では、DNAがよりアクセスしやすくなり、転写が促進されます。
● ヒストン修正による調節
ヌクレオソームのヒストンタンパク質に生じる化学的修正も、遺伝子のアクセシビリティを調節する重要なメカニズムです。例えば、ヒストンのアセチル化はクロマチン構造を緩め、転写因子がDNAにアクセスしやすくなります。一方で、ヒストンのメチル化はしばしばクロマチンを凝縮させ、遺伝子の発現を抑制する効果があります。
● クロマチンリモデリングとの相互作用
クロマチンリモデリング複合体は、ATPを消費してヌクレオソームをスライドさせたり、一時的に取り除いたりすることで、特定の遺伝子領域のクロマチン構造を変化させます。これにより、必要に応じて遺伝子がオンになったりオフになったりすることを可能にし、細胞の機能や発達、応答に不可欠な適応性を提供します。
これらのメカニズムにより、ヌクレオソームは細胞内での遺伝情報の利用を精密に制御し、遺伝子の発現パターンを調整して生物の発生や正常な機能維持に寄与しています。ヌクレオソームのダイナミクスとその調節は、遺伝子の適切な発現を保証するために不可欠であり、異常が生じると多くの疾患の原因となり得ます。
エピジェネティクスとの関連
ヌクレオソームはエピジェネティクス制御の中核的な役割を果たしており、ヒストンの化学的修正がどのようにして遺伝情報の表現とヌクレオソームの機能に影響を与えるかは、遺伝子調節の基本的な理解に不可欠です。
● ヒストン修正のメカニズム
ヒストンタンパク質は、そのアミノ酸の残基が様々な化学修正を受けることができます。これにはアセチル化、メチル化、リン酸化などが含まれ、これらの修正はヌクレオソームのDNAへの結合強度を変化させ、クロマチンの構造を変えることで遺伝子のアクセス可能性を調節します。
– アセチル化: ヒストンのアセチル化は、ヌクレオソームのDNAとの結合を緩和し、クロマチン構造を開いて遺伝子の転写が行いやすくなる状態にします。
– メチル化: ヒストンのメチル化は、遺伝子の活性を抑制する場合と活性化する場合があり、修正されるアミノ酸の種類とメチル基の付加される位置に依存します。
● エピジェネティクスと遺伝子の調節
ヌクレオソームのヒストン修正は、特定の遺伝子領域の転写因子に対するアクセシビリティを直接的に調節することにより、遺伝子の発現パターンに深く影響を及ぼします。これにより、細胞は発達の段階や外部からのシグナルに応じて適切な遺伝子をオンまたはオフにすることができます。
● 病態との関連
エピジェネティックな異常は多くの病態、特にがんの発生に関連しています。不適切なヒストン修正は、本来抑制されるべき遺伝子の誤った活性化や、必要な遺伝子の不活性化を引き起こし、細胞の異常な増殖や分化不全を引き起こすことがあります。
このようにヌクレオソームとエピジェネティクスの相互作用は、遺伝子の正確な調節と細胞の健康を保つために極めて重要です。ヒストンの修正を詳しく理解することは、これらのプロセスを解明し、新しい治療方法の開発につながる可能性があります。
ヌクレオソームダイナミクスの解明
構造的ダイナミクス
ヌクレオソームの構造的ダイナミクスは、クロマチンの構造と機能、特に遺伝子のアクセシビリティと転写の調節において中心的な役割を果たしています。ヌクレオソームの構造が変化することで、DNAの露出度が変わり、それによって遺伝子の転写が促進されたり抑制されたりします。
● ヌクレオソームの再配置
ヌクレオソームは、その位置を変えることによってクロマチンのアクセス可能性を調節します。この「スライディング」と呼ばれるプロセスは、特定の転写因子が遺伝子のプロモーター領域にアクセスするのを容易にするか、あるいはそれを妨げることができます。このようなダイナミクスは、細胞の発達過程や応答メカニズムにおいて重要な役割を担っています。
● ヒストンの交換
ヒストンの交換もまた、ヌクレオソームの構造的ダイナミクスに影響を及ぼす重要な要素です。古いヒストンが新しいヒストンと交換されることで、クロマチンの特定の領域がリセットされ、異なる修正パターンが導入されます。このプロセスは、遺伝子の活性化や沈黙に直接的に寄与することができます。
● 構造的変化による遺伝的安定性への影響
ヌクレオソームの構造的変化は、遺伝的安定性にも影響を及ぼします。例えば、DNAの修復過程において、ヌクレオソームの再配置やヒストンの交換が適切に行われない場合、突然変異が発生しやすくなることがあります。また、ヌクレオソームの適切な配置は、DNAの複製とセグレゲーションの精度を保つためにも重要です。
これらの構造的ダイナミクスに関する理解は、生物学的な多様性と細胞の適応能力の基礎をなしており、エピジェネティクスの研究においても中心的なテーマとなっています。ヌクレオソームの動的な性質が、生命現象を理解する鍵であることは疑いようがありません。
研究技術の進化
ヌクレオソーム研究における技術革新は、分子生物学と遺伝学の理解を飛躍的に進展させています。最新の研究手法は、ヌクレオソームの動的性質と機能的な役割を詳細に解析することを可能にし、これまでにない洞察を提供しています。
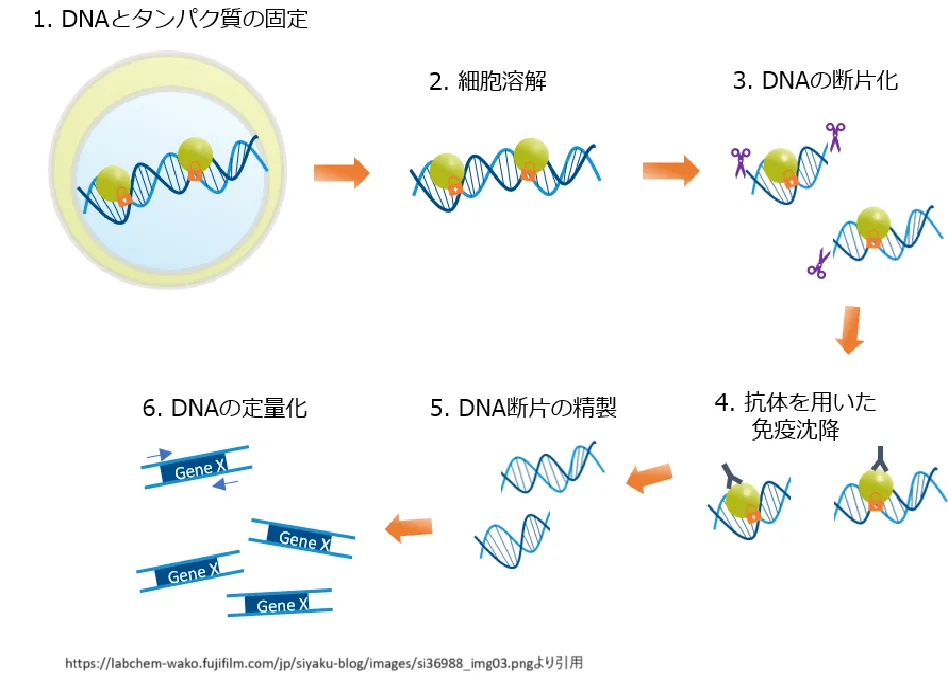
● クロマチン免疫沈降(ChIP)
クロマチン免疫沈降(ChIP)技術は、特定のヒストン修飾や結合タンパク質が関与するDNA領域を同定するために広く使用されています。この技術により、特定のヒストン修正がヌクレオソームの配置や遺伝子のアクセシビリティにどのように影響しているかを明らかにすることができます。
● 高解像度顕微鏡
フルオレセンス顕微鏡や共焦点顕微鏡を含む高解像度マイクロスコピー技術は、ヌクレオソームの実際の構造とその細胞内での位置を可視化するのに役立ちます。これにより、ヌクレオソームダイナミクスが細胞機能にどのように貢献しているかをリアルタイムで観察することが可能です。
● 次世代シーケンシング(NGS)
次世代シーケンシング技術は、ヌクレオソームの位置と遺伝子の活性パターンを高精度でマッピングするために用いられます。NGSは、大規模な遺伝子発現データとヌクレオソームの配置データを組み合わせることで、エピジェネティックな調節が遺伝子機能にどのように影響するかの解析を深めます。
● クライオ電子顕微鏡(cryo-EM)
クライオ電子顕微鏡は、ヌクレオソームとその構成タンパク質の高解像度な3D構造を提供します。この技術により、ヌクレオソームの精密な構造的詳細が明らかになり、その機能的理解が進んでいます。
これらの先進的な技術は、ヌクレオソームのダイナミクスを理解するための新たな扉を開き、将来の治療戦略や疾患理解に重要な貢献をしています。研究技術の進化により、ヌクレオソームの複雑な生物学的役割が徐々に解明されつつあります。
クロマチンとの相互作用
クロマチンリモデリングとの関係
### クロマチンリモデリングとの関係
ヌクレオソームとクロマチンリモデリング複合体との相互作用は、遺伝子のアクセスと活性化において中心的な役割を果たします。この相互作用により、DNAがよりアクセスしやすい状態になり、遺伝情報の読み取りが効果的に行われます。
● クロマチンリモデリングのメカニズム
クロマチンリモデリング複合体は、ATPをエネルギー源として使用してヌクレオソームを物理的に移動させることができます。これにより、ヌクレオソームがスライドしたり、スペースが拡大したりして、特定の遺伝子領域が転写因子によるアクセスを受けやすくなります。このプロセスは、遺伝子のオンまたはオフを切り替えるのに不可欠であり、細胞の応答や発達に必要な遺伝子表現の調整を可能にします。
● 生物学的重要性
クロマチンリモデリングは、細胞の発達、分化、および多くの生理的応答において重要な役割を担います。例えば、発達中の胚において特定の遺伝子セットがタイムリーに「オン」に設定されることで、組織の特化や器官の形成が促進されます。また、環境からのシグナルを受けて遺伝子が迅速に「オン」または「オフ」になることは、細胞の生存と適応に不可欠です。
クロマチンリモデリングの障害は、がんを含む多くの疾患の原因となることが知られています。不適切なリモデリング活動は、必要な遺伝子が正しく表現されないことにより、細胞の無秩序な増殖や異常な行動を引き起こす可能性があります。
● 研究の進展
ヌクレオソームとクロマチンリモデリング複合体の相互作用に関する研究は、遺伝子調節の更なる理解を深めるために進行中です。これには、高度なイメージング技術や分子生物学的手法が用いられ、これらの複雑なダイナミクスを詳細に解析することを目指しています。
ヌクレオソームとクロマチンリモデリング複合体との相互作用の解明は、疾患のメカニズム理解と治療法の開発に対して重要な洞察を提供します。これらの知見は、将来的に遺伝子表現を正確にコントロールする新しい疾患治療戦略を導く可能性があります。
遺伝的安定性への寄与
ヌクレオソームは、遺伝的情報の整合性と安定性を維持するために、核心的な役割を担っています。この過程では、ヌクレオソームがクロマチンの構造を維持し、DNAの損傷応答と修復に関与することが重要です。
● クロマチン構造の維持
ヌクレオソームはDNAをヒストンタンパク質の周りにコンパクトに巻きつけることで、クロマチンの構造を整えます。この構造は、DNAを物理的な損傷から保護し、化学的変性や環境由来のストレスに対する脆弱性を減少させます。適切に構成されたヌクレオソームは、DNAが過剰に凝集するのを防ぎ、複製や修復過程でのアクセスを適切に制御します。
● DNA修復過程での役割
ヌクレオソームは、DNA修復メカニズムと密接に連携しています。DNAが損傷を受けた場合、クロマチン構造は一時的に変更されることがあり、修復酵素が損傷部位にアクセスしやすくなります。ヒストンの一時的な除去や置換が行われ、修復プロセスが完了した後に元の位置に戻されることで、DNAの完全性が再び保証されます。
● 遺伝的変異の抑制
クロマチンの適切な構成とヌクレオソームの正確な配置により、遺伝的変異の発生率が低下します。ヌクレオソームが不適切に配置されたり、ヒストン修正が異常である場合、DNA複製中にエラーが発生しやすくなり、突然変異や染色体の異常が生じる可能性が高まります。
ヌクレオソームのこれらの機能は、細胞の健康を維持し、がんや遺伝性疾患などの病態の予防に寄与しています。研究者はこれらの過程をさらに詳細に理解することで、新しい治療法の開発や遺伝病のリスク管理に役立てることを目指しています。ヌクレオソームと遺伝的安定性の関連性を理解することは、分子生物学および医学研究において重要なテーマであり続けます。
臨床応用と未来への展望
病気の治療への応用
### 病気の治療への応用
ヌクレオソームの研究は、がんや遺伝性疾患など多くの病気の理解と治療法の開発に貢献しています。ヌクレオソームの動的な性質とその調節機構を理解することで、特定の疾患に関連する遺伝的変化への介入が可能になります。
● がん治療
ヌクレオソームにおけるエピジェネティックな変化は、がん細胞の成長を促進または抑制する役割を持つことが明らかになっています。例えば、特定のヒストン修正酵素を標的とした薬剤が開発されており、これにより異常なヒストン修正を正常化し、がん細胞の成長を抑制することが可能です。また、ヌクレオソームの構造を変化させることで、薬剤がDNAにアクセスしやすくなり、化学療法の効果を高めるアプローチも研究されています。
● 遺伝性疾患の治療
特定の遺伝性疾患は、ヌクレオソームの配置やヒストンの修正パターンの異常によって引き起こされることがあります。これらの疾患に対して、ヌクレオソームの配置を正常化することで症状を改善する治療法が検討されています。例えば、クロマチンリモデリング複合体を活性化または抑制することで、病気に関連する遺伝子の発現を調節し、疾患の進行を遅らせる可能性があります。
● 新しい治療戦略の開発
ヌクレオソームの研究から得られた知見は、遺伝子療法や細胞療法など、新しいタイプの治療法の開発に役立てられています。例えば、特定のヒストン修正を標的とする小分子化合物や、遺伝子の発現を制御するためにデザインされた合成ヌクレオソームの使用などが研究されています。
ヌクレオソームの詳細な研究は、これらの治療法の効果を最大化し、副作用を最小限に抑えるための重要な情報を提供します。今後の研究と臨床試験により、これらの新しい治療戦略が実用化されることが期待されています。
未来への展望
ヌクレオソーム研究の未来への展望は、エピジェネティクス、遺伝子治療、および疾患理解の深化に向けて非常に有望です。以下は、未来に向けての主な研究分野と展望です。
● エピジェネティクスの更なる解明
ヌクレオソームのエピジェネティックな調節メカニズムの理解を深めることで、特定の遺伝子の表現がどのように調節されているかの詳細な知見が得られます。特に、ヒストン修正やDNAメチル化といったエピジェネティックな変更がヌクレオソームの機能にどのように影響しているかを解明することが重要です。これにより、がんや神経変性疾患などのエピジェネティックな病態を効果的に治療する新しいアプローチが開発されることが期待されています。
● 先進的なイメージングと分子技術の進化
クライオ電子顕微鏡や次世代シーケンシングなどの技術がさらに進化し、ヌクレオソームとその周辺構造を原子レベルで解析できるようになることで、その動的な性質や相互作用の詳細が明らかになります。これにより、ヌクレオソームの構造と機能の関連をより正確に理解し、遺伝子の調節に介入する新しい方法が開発される可能性があります。
● 遺伝子編集技術との組み合わせ
CRISPR-Cas9などの遺伝子編集技術とヌクレオソーム研究を組み合わせることで、特定の遺伝的変異や疾患に関連するエピジェネティックなマーカーを直接的に修正することが可能になります。これにより、遺伝性疾患やがんなどの病態に対する根本的な治療法が提供される可能性が高まります。
● 疾患モデルへの応用
病気のモデルにおいてヌクレオソームのダイナミクスを研究することで、疾患の発症メカニズムを解明し、新しい治療ターゲットを特定することができます。特に、炎症や老化プロセスにおけるヌクレオソームの役割を理解することで、これらの条件を管理または逆転させる新しい治療法が開発されることが期待されます。
これらの進展は、ヌクレオソーム研究が今後も生命科学の多くの分野において中心的な役割を担い続けることを示しています。科学技術の進歩とともに、ヌクレオソーム研究の未来はさらに明るい展望を開くことでしょう。