目次
この記事では、ヌクレオシドアナログの基本的な特性、その製造方法、分離プロセス、および抗がんおよび抗ウイルス療法における重要な役割について詳しく解説します。また、疾患治療におけるヌクレオシドアナログの利用例と、これらがどのようにして新しい治療法の開発に貢献しているかを掘り下げます。
ヌクレオシドアナログの概要
定義と基本的な特性
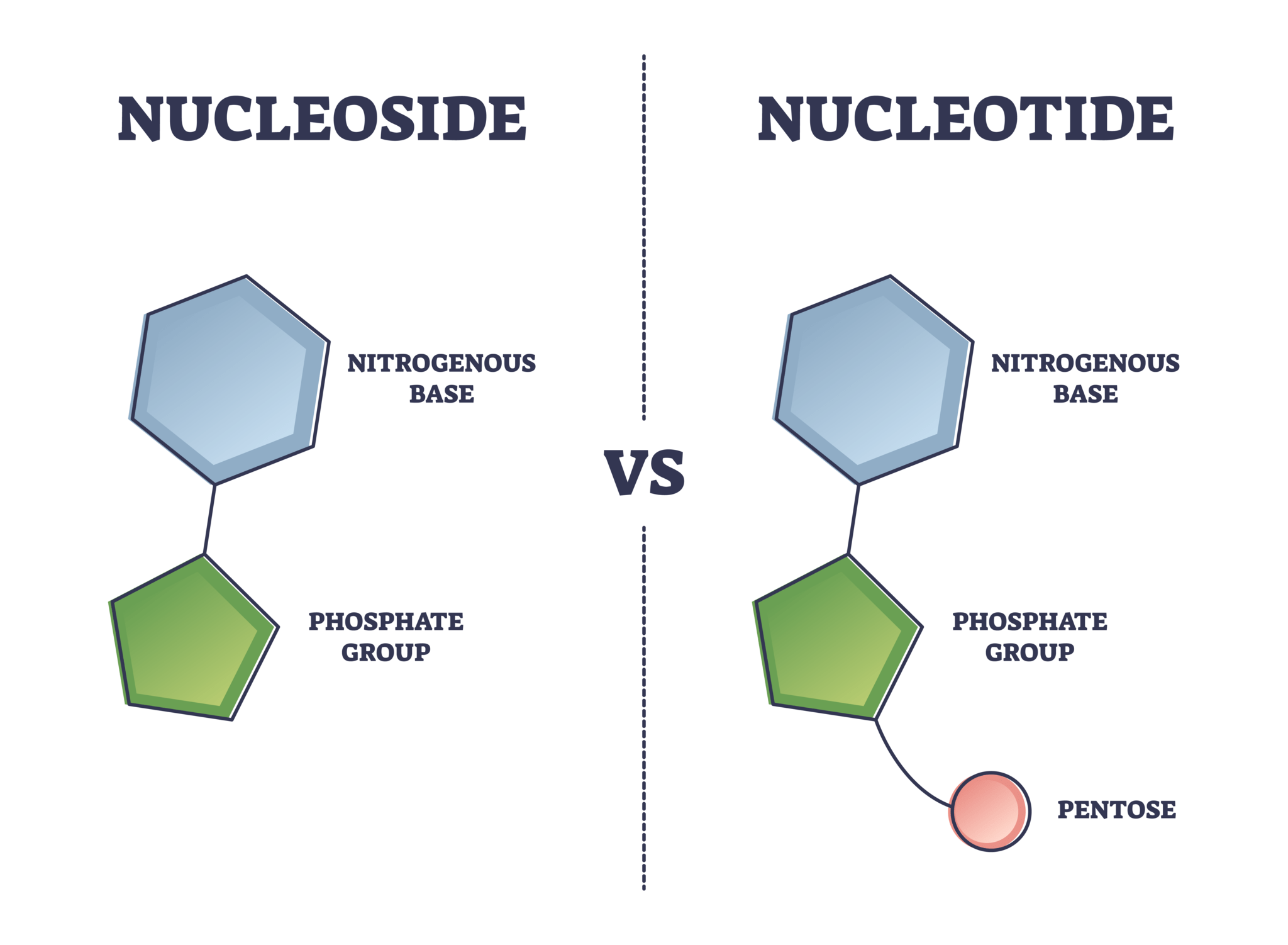
ヌクレオシドアナログは、自然界に存在するヌクレオシドの構造を模倣した化合物です。これらは主に、遺伝的情報の伝達に関与する生体内の核酸の合成を阻害するために設計されています。ヌクレオシドアナログは、医薬品として特に抗ウイルスおよび抗がん治療で広く用いられています。
● 化学的特性
ヌクレオシドアナログは、天然のヌクレオシドが持つ糖部分と塩基部分から構成されていますが、その化学構造には一部改変が加えられています。この微妙な構造変更が、DNAやRNAの合成過程に介入し、ウイルスの複製やがん細胞の増殖を阻害する機能を担います。例えば、多くのヌクレオシドアナログは、3’ヒドロキシル基が欠如しているため、DNA鎖の延長を阻害します。
● 基本的な分類
ヌクレオシドアナログはその作用機序や目的によって分類されることが多いです。主なカテゴリーには以下のようなものがあります:
1. 抗ウイルスヌクレオシドアナログ:HIVやヘルペスウイルスなど、特定のウイルスに対する抑制作用を持つアナログ。これらはウイルスのDNAポリメラーゼを標的とし、ウイルスの複製を阻害します。
2. 抗がんヌクレオシドアナログ:がん細胞のDNA合成を妨げることにより、細胞分裂を阻害し、がん細胞の成長を抑えます。
3. プロドラッグ形式のヌクレオシドアナログ:体内で活性形に変換される前駆体形式で投与され、特定の細胞や組織でのみ活性化される設計がなされています。
これらのアナログは、特に有害な副作用を最小限に抑えつつ、疾患を効果的に管理するための重要なツールとして機能します。医薬品としてのこれらの特性と応用は、継続的な研究により進化し続けており、新しい治療法の開発に不可欠な役割を果たしています。
歴史と進化
ヌクレオシドアナログは、20世紀初頭に化学療法の一環として発見され、その後、感染症とがんの治療において革新的な進展を遂げてきました。これらの化合物は、病原体やがん細胞の核酸合成を効果的に阻害することから、医薬品としての価値が高く評価されています。
● 初期の発見と応用
ヌクレオシドアナログの歴史は、1940年代にさかのぼります。最初のヌクレオシドアナログは、がん治療薬として開発されましたが、その後、抗ウイルス薬としての潜在能力が認識されるようになりました。特に、アイドクシウリジンとシタラビンは、初期の段階で発見された重要なヌクレオシドアナログであり、がんやウイルス感染症に対する有効な治療オプションとして利用されてきました。
● 抗ウイルス治療への進化
1980年代には、HIV/AIDSが世界的な健康危機として浮上しました。この時期に開発されたアジドチミジン(AZT)は、HIVの逆転写酵素を標的とすることでウイルスの複製を阻害し、抗レトロウイルス療法における画期的な薬剤となりました。この成功により、他の多くの抗ウイルスヌクレオシドアナログの開発が進められ、慢性ウイルス感染症の治療に大きな進歩をもたらしました。
● 技術の進展と最近の革新
21世紀に入ると、ヌクレオシドアナログはさらに洗練され、高度な化学技術が導入されて構造が改良されました。これにより、より少ない副作用で効果的な治療が可能となり、特にがん治療と抗ウイルス治療においてそのスペクトラムが拡大しました。また、プロドラッグ技術の導入により、薬剤の生物学的利用可能性が向上し、治療の効果が高まりました。
ヌクレオシドアナログは医薬品としての役割を拡大し続けており、新たなウイルス感染症やがんに対する治療薬として、今後も研究開発が進められることが期待されます。この進化の歴史は、ヌクレオシドアナログがいかにして現代医療の多くの課題に対処してきたかを示しており、未来の治療法の開発に向けた貴重な洞察を提供しています。
製造と分離プロセス
合成法と生物学的合成
ヌクレオシドアナログの製造には、化学合成法と生物学的合成法の両方が用いられます。これらの方法は、研究や医薬品開発において重要な役割を担っており、特定の治療目的に応じて選択されます。
● 化学合成法
ヌクレオシドアナログの化学合成は、高度に制御された化学反応を通じて行われます。このプロセスでは、自然に存在するヌクレオシドを基盤として、特定の化学基を導入することで改変されたアナログを合成します。一般的には、ヌクレオチド(ヌクレオシドにリン酸基が結合した形態)を直接合成する方法と、ヌクレオシドに後からリン酸基を結合させる方法があります。これには、ハロゲン化、アルキル化、ギルマン試薬(リチウムおよび銅の有機化合物)を使用する手法などが含まれます。
● 生物学的合成法
生物学的合成法では、微生物や酵母などの生物を利用してヌクレオシドアナログを合成します。この方法は、特定の代謝経路を利用して自然由来のヌクレオシドからアナログを合成することが特徴です。例えば、特定の微生物が持つ代謝能力を改変または強化して、必要なヌクレオシドアナログを効率よく生産します。生物学的合成は、通常の化学合成法よりも環境に優しく、コスト効率が高い場合が多いです。
これらの合成法は、ヌクレオシドアナログを製造する上でそれぞれに利点と欠点があり、用途や目的に応じて選択されます。化学合成法は製品の純度が高く、大規模生産に適していますが、複雑な化学反応を必要とすることが多いです。一方、生物学的合成法は比較的環境負荷が低く、持続可能な生産が可能ですが、生物の培養が難しい場合や所望の化合物の収率が低い場合があります。これらの方法を組み合わせることで、効率的かつ経済的にヌクレオシドアナログを製造することが可能となります。
分離技術の進化
ヌクレオシドアナログの製造過程における分離技術は、時間とともに大きく進化してきました。これにより、製品の品質と製造効率が大幅に向上しました。
● 初期の分離技術
ヌクレオシドアナログの初期の分離技術は主に単純なクロマトグラフィーや沈殿法に依存していました。これらの方法は比較的単純で実施が容易であるものの、純度や収率が常に理想的とは限らず、スケールアップが難しい問題がありました。
● 高度なクロマトグラフィー技術の導入
技術の進化とともに、より洗練されたクロマトグラフィー技術が開発されました。特に高速液体クロマトグラフィー(HPLC)の導入は、ヌクレオシドアナログの分離プロセスに革命をもたらしました。HPLCは高い解像度を提供し、複数の成分が混在する複雑なサンプルから特定のヌクレオシドアナログを迅速かつ効率的に分離できます。これにより、製品の純度が大幅に向上し、製造プロセスの再現性とスケーラビリティが改善されました。
● 分子印刷ポリマーとの組み合わせ
最近では、分子印刷ポリマー(MIP)技術が分離プロセスに導入されています。MIPは特定のヌクレオシドアナログの形状、サイズ、および機能基に合わせてカスタマイズされたポリマーベースの材料です。これにより、非常に特異的な分離が可能となり、不純物の除去効率が向上し、さらに製品の品質が保証されます。
● メモブレンフィルトレーションとその利点
また、メモブレンフィルトレーション技術の進化もヌクレオシドアナログの製造に貢献しています。この方法は、分子サイズに基づいて成分を分離するため、非常に高い選択性を持ち、特に大規模生産においてその価値が認められています。メモブレンフィルトレーションは、不純物の除去だけでなく、目的とする製品の回収率も向上させることができます。
これらの進化した分離技術により、ヌクレオシドアナログの製造プロセスはより効率的で経済的になり、医薬品としての利用拡大に寄与しています。各技術の導入は、製品の純度を最大化し、製造コストを最小化するための重要なステップとなっています。
医療における応用
抗ウイルス治療における利用
ヌクレオシドアナログは、HIVやヘルペスウイルスなどのウイルス感染症治療において重要な役割を果たしています。これらの薬剤は、ウイルスの遺伝子複製プロセスを効果的に妨げることで、感染の進行を遅らせるまたは阻止します。
HIV感染症の治療に用いられるヌクレオシド類縁体は、しばしば逆転写酵素阻害剤(NRTI)と呼ばれますが、これらは、DNA依存性とRNA依存性の両方のDNAポリメラーゼに対して活性をもっています。これらの薬剤は、ウイルスポリメラーゼの競合阻害やDNA鎖の合成終結など、いくつかのメカニズムによってウイルスの複製を阻害すると考えられています。
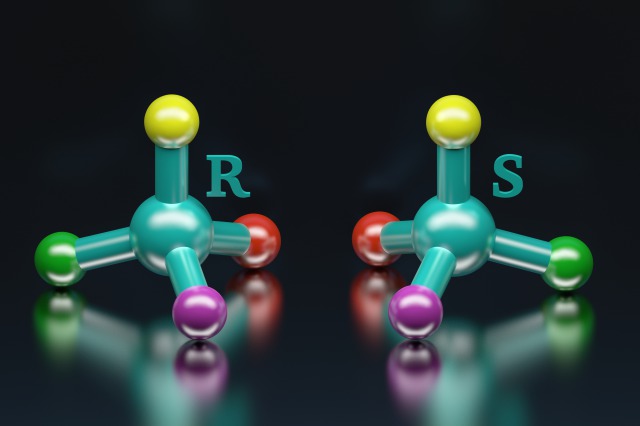
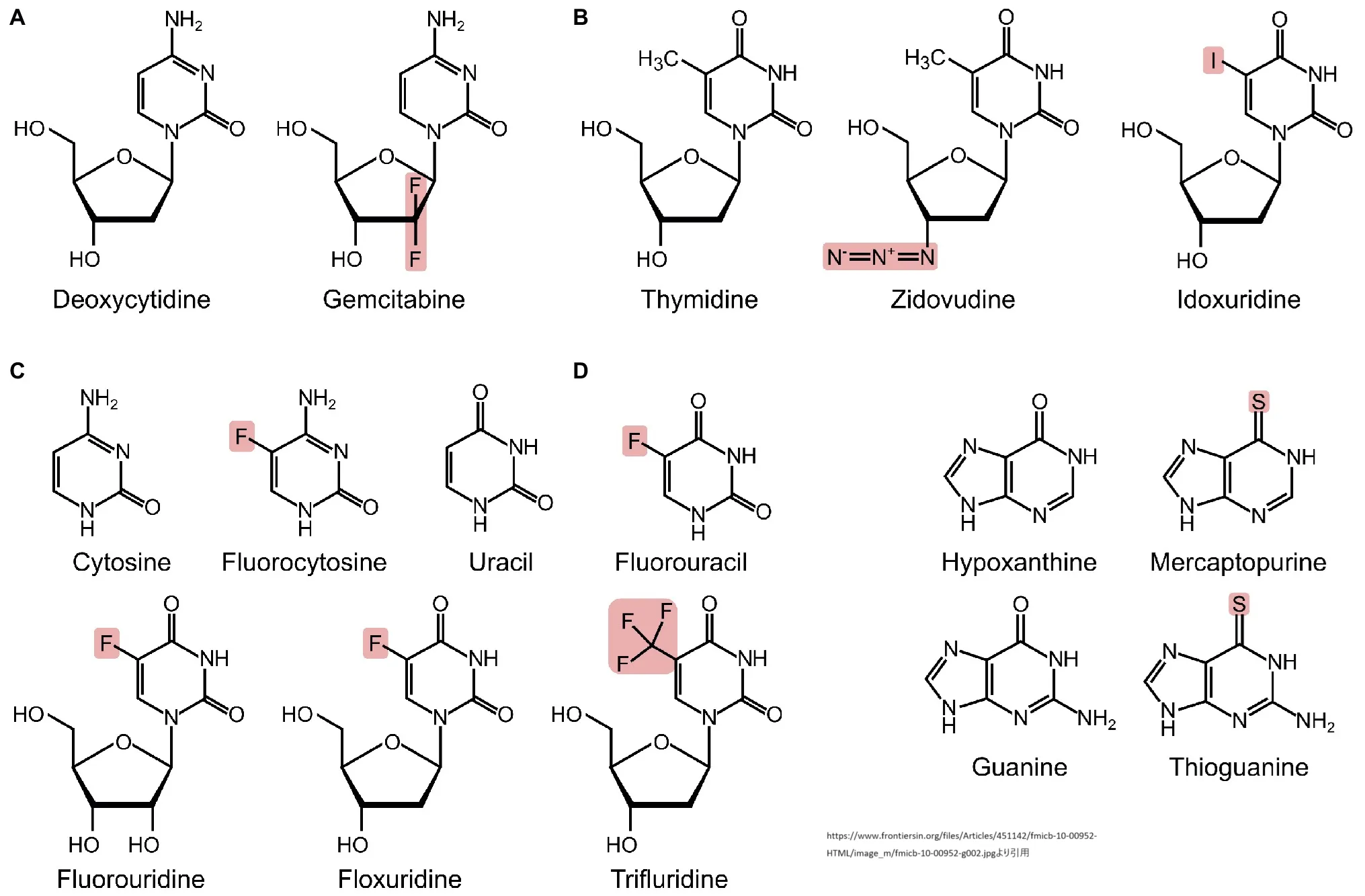
抗ウイルスヌクレオシド類似体の多くは、デオキシリボ核酸の3’ヒドロキシル基でブロックされるため、新生DNA分子の伸長が阻害されます。他の抗ウイルスヌクレオシド類似体は、天然(D形)ヌクレオシドの光学異性体(L形:ラミブジン、エムトリシタビン、テルビブジン)であり、ウイルスポリメラーゼに取り込まれたり、DNA分子に付加されたりする際に、立体構造に障害を起こして複製を妨害します。ヌクレオシドアナログの構造上のこれらの特徴は、ヒトのポリメラーゼに利用されてRNAやDNAに取り込まれる危険性があるため重要であり、これがヌクレオシドアナログの重篤な毒性の原因となっています。
● HIV治療におけるヌクレオシドアナログ
HIV治療において、ヌクレオシドアナログは逆転写酵素阻害剤(NRTI)として利用されます。NRTIは、HIVのDNAを合成する逆転写酵素の活動を阻害することで、ウイルスの複製を防ぎます。最初に承認されたヌクレオシドアナログであるアジドチミジン(AZT)は、HIVの治療を大きく変え、多くの患者の生命を延ばすことに寄与しました。この薬剤は、HIVのRNAからDNAへの転写を阻害し、ウイルスの増殖を抑制します。
● ヘルペスウイルス治療における利用
ヘルペスウイルス感染症に対しても、ヌクレオシドアナログが広く用いられています。例えば、アシクロビルはヘルペスシンプレックスウイルス(HSV)に対して高い効果を示し、特に再発性の口唇ヘルペスや性器ヘルペスの治療に効果的です。アシクロビルは、HSVが持つ特定の酵素によって活性化され、その後、ウイルスのDNAポリメラーゼを阻害してDNA鎖の伸長を停止させます。
これらのヌクレオシドアナログは、その特異的な作用機序により、特定のウイルスに対する効果的な治療選択肢を提供し、ウイルス感染症の治療における重要な進歩となっています。効果的なウイルス制御により、感染症の症状を軽減し、患者の生活の質を向上させることができます。
抗がん治療への応用
ヌクレオシドアナログは、抗がん治療においても重要な役割を果たしています。これらの化合物は、がん細胞のDNA合成を阻害することで、細胞の増殖を抑制し、がんの進行を遅らせる効果があります。
● シタラビンの使用例
シタラビンは、急性骨髄性白血病(AML)治療に広く用いられるヌクレオシドアナログの一つです。この薬剤は、がん細胞のDNAポリメラーゼを標的とし、DNA合成を妨げることで細胞分裂を阻害します。シタラビンの投与は、多くのAML患者に対して有効であり、完全寛解を達成することが報告されています。
● ジェムシタビンの治療効果
別の例としてジェムシタビンがあります。このヌクレオシドアナログは、膵臓がん、非小細胞肺がん、乳がんなど、多くの固形がんの治療に使用されています。ジェムシタビンは、がん細胞に取り込まれると代謝され、DNA合成を阻害することでがん細胞の増殖を抑制します。特に膵臓がんにおいて、ジェムシタビンは生存率の向上に寄与していると報告されています。
これらのヌクレオシドアナログは、その特異的な機序を通じてがん細胞の増殖を抑えることにより、治療の選択肢を広げ、多くのがん患者の治療成績を改善しています。各薬剤の選択と使用は、がんの種類、病期、患者の健康状態など、多くの要因を考慮して行われます。
ヌクレオシドアナログの有害事象
ヌクレオシドアナログはいくつかのメカニズムで肝障害を引き起こします。最も特徴的なのはミトコンドリア型の肝障害であり、ヌクレオシドアナログがミトコンドリアのγポリメラーゼによってミトコンドリアのDNA合成に取り込まれたり阻害されたりすることで、ミトコンドリアが枯渇したり機能が低下したりすることが原因だと考えられています。ミトコンドリア障害は、複数の組織に影響を及ぼし、ミオパシー(筋障害)、ニューロパシー(神経障害)、膵炎、骨髄抑制、肝障害などを引き起こします。
肝障害
肝障害は、乳酸アシドーシスの蓄積、微小胞性脂肪症、肝合成不全(LASH)を特徴とします。血清アミノトランスフェラーゼ値(AST, ALT)の上昇はごくわずかで、黄疸は遅れて出現します。肝ミトコンドリア障害の最も劇的な例は、ヒトを対象とした第2相試験において、治療開始から2~3ヵ月後に肝不全、乳酸アシドーシス、膵炎による死亡例が数件発生したために中止されたヌクレオシドアナログ薬のフィアルリジンです。
ヌクレオシド類似化合物は、急性過敏症や毒性中間体の生成(アロプリノール)など、他のメカニズムによっても肝障害を引き起こす可能性がありますが、これらの肝障害は特異的であり、まれです。最後に、多くのヌクレオシド類縁化合物はB型肝炎ウイルスHBVに対して強力な活性を有しており、治療中の初期、あるいは治療が突然終了してウイルスレベルが回復したときに、B型肝炎の急性増悪を引き起こすことがあります。
このように、ヌクレオシド系薬剤は、直接的な肝毒性(宿主のポリメラーゼ活性との相互作用によるミトコンドリア機能障害)、特異的な肝毒性(過敏性反応)、あるいは基礎的な肝疾患の増悪(治療中止後のB型肝炎の再活性化)のような間接的な肝毒性を引き起こす可能性があります。
研究と開発の最前線
新しいメカニズムの探求
近年の研究により、ヌクレオシドアナログの新たな作用機序が明らかにされつつあります。これらの進歩は、既存の疾患に対する新しい治療法の開発や、耐性問題の解決に向けた新たな道を開いています。
● 新しい標的の同定
最新の研究では、ヌクレオシドアナログが特定のウイルス酵素やがん関連タンパク質に対してどのように作用するかが解析されています。たとえば、一部のヌクレオシドアナログは、従来のDNAポリメラーゼや逆転写酵素以外に、RNAポリメラーゼやヘリカーゼのような新しい酵素を標的としています。これにより、これまでにない作用機序を持つ抗ウイルスや抗がん薬の開発が期待されています。
● プロドラッグの活用
また、プロドラッグ形式でのヌクレオシドアナログの利用も進んでいます。プロドラッグは、体内で活性化される前駆体形態で投与され、特定の病巣や細胞でのみ活性化されるように設計されています。このアプローチにより、副作用を最小限に抑えつつ、薬剤の効果を最大化することが可能になります。
● 分子改変の進化
さらに、ヌクレオシドアナログの分子構造を細かく改変することにより、その選択性や安全性を向上させる試みも行われています。例えば、フルオロ化ヌクレオシドや環状ヌクレオシドのような新しいクラスの化合物は、改良された薬理学的特性を持ち、耐性ウイルス株やがん細胞に対する効果が期待されています。
これらの研究成果は、ヌクレオシドアナログが持つ多様な潜在能力を示しており、新しい治療法の開発に対する期待を高めています。科学的な理解が深まるにつれて、より効果的で安全な薬剤の開発が加速されることが期待されます。
未来への展望
ヌクレオシドアナログの研究は、未来の医療技術と治療法に革命をもたらす可能性を秘めています。これらの研究は、新しいウイルスや耐性がんに対する治療法だけでなく、治療の個別化にも寄与すると考えられています。
● パーソナライズドメディシンへの応用
ヌクレオシドアナログは、個々の患者の遺伝的プロファイルに基づいてカスタマイズされた治療を提供するパーソナライズドメディシンの進展に貢献する可能性があります。遺伝子の変異や発現パターンに応じて、最適なヌクレオシドアナログを選択し、効果的かつ安全な治療を行うことが可能になるでしょう。
● 耐性問題への対応
抗ウイルスおよび抗がん治療における耐性問題への対策として、ヌクレオシドアナログの研究は重要な役割を果たします。新しいヌクレオシドアナログの開発や、既存薬剤の改良により、耐性株にも効果を発揮する治療法が開発される可能性があります。
● 組み合わせ療法の開発
さらに、ヌクレオシドアナログを他の治療薬と組み合わせることで、その効果を向上させる治療戦略が開発されています。このアプローチにより、薬剤の効果を最大化し、副作用を最小化することが可能となり、治療の成功率を高めることができます。
● 次世代のヌクレオシドアナログ
最新のナノテクノロジーやバイオテクノロジーを利用したヌクレオシドアナログの開発も進行中です。これらの技術を利用することで、より精密な薬剤配送システムや、ターゲット特異性の高い治療薬の開発が期待されています。
これらの進展は、ヌクレオシドアナログの研究が未来の医療にどのように貢献するかを示唆しています。持続的な研究と技術革新により、より効果的で安全な治療法が開発され、患者の生活の質の向上に寄与することでしょう。
課題と未来の方向性
現在の技術的課題
ヌクレオシドアナログの開発と利用には、いくつかの技術的課題が存在しています。これらの課題は、治療の効果を最大化し、副作用を最小限に抑えるための重要な障壁となっています。
● 薬剤耐性の問題
ヌクレオシドアナログはウイルスやがん細胞の迅速な進化によって効果が低下することがあります。特に、ウイルスは高い変異率を持っており、容易に薬剤耐性を獲得します。この問題に対処するためには、複数の薬剤を組み合わせた治療や、新しい標的を持つアナログの開発が必要です。
● 生物学的可用性と代謝の問題
多くのヌクレオシドアナログは、体内での生物学的可用性が低かったり、不適切な代謝によって効果が減少することがあります。これらの化合物をより効果的に細胞内に運ぶための新しい配送システムの開発が求められています。
● 副作用の管理
ヌクレオシドアナログは、特に長期間にわたる使用において、重篤な副作用を引き起こす可能性があります。これには、骨髄抑制、腎機能障害、肝機能障害などが含まれます。これらの副作用を最小化するためには、薬剤の投与量や投与スケジュールの最適化、または副作用を特異的に軽減する補助薬の開発が重要です。
● 経済的な制約
ヌクレオシドアナログの研究開発は高額な費用がかかるため、特に新しいアナログの開発は資金的な制約が大きな課題となります。さらに、開発された薬剤が広く利用されるようになるまでのプロセスは時間がかかり、多額の投資が必要です。
これらの技術的課題を克服するためには、持続的な研究と技術革新が不可欠です。また、これらの課題に対処するための国際的な協力や、政策立案者、研究者、製薬会社間の連携も重要となるでしょう。
研究における新たなアプローチ
ヌクレオシドアナログの開発と利用に関わる技術的課題を解決するために、科学界ではいくつかの革新的なアプローチが提案されています。これらの新たな研究方向性は、効果的な治療法の開発を加速すると共に、患者の安全性と治療の効果を向上させることを目指しています。
● ターゲテッドデリバリーシステムの開発
ヌクレオシドアナログの生物学的可用性と細胞内配達効率を向上させるために、ターゲット指向の薬剤送達システムが研究されています。これにはリポソームやナノ粒子を利用した技術が含まれ、薬剤を直接病変部位に運ぶことが可能です。このアプローチにより、薬剤の副作用を減少させつつ、治療効果を最大化することが期待されています。
● CRISPR-Cas9を利用した遺伝子編集
CRISPR-Cas9などの遺伝子編集技術を利用して、薬剤耐性を持つ遺伝子を標的にする新しい研究が進行中です。この技術を用いることで、ヌクレオシドアナログの効果を妨げる遺伝的要因を直接編集し、より効果的な治療成果を得ることが可能になります。
● コンピューター支援ドラッグデザイン
コンピューターを利用したドラッグデザインは、ヌクレオシドアナログの構造を最適化し、より効率的な薬剤を設計するために用いられています。このテクノロジーを活用することで、特定のタンパク質や酵素との親和性を高め、効果的なヌクレオシドアナログの開発が進められています。
● 多面的な抗耐性戦略
薬剤耐性に対抗するための新しい戦略として、複数のアクティブサイトを同時に標的とする多面的アプローチが研究されています。これにより、ウイルスやがん細胞が一つの変異によって薬剤耐性を獲得することが困難になります。
これらの研究アプローチは、ヌクレオシドアナログの未来の展望を形作るものであり、新たな治療薬の開発や既存薬の改良に向けた重要なステップです。科学技術の進展とともに、これらの方法が現実の治療オプションとして実現されることが期待されています。