目次
この記事では、ノンコーディングDNAの基本的な概念、その種類と機能、及び現代医学と研究におけるその役割について詳しく解説します。特に、最新の研究成果と将来の治療法への応用可能性に焦点を当てます。
ノンコーディングDNAとは
ノンコーディングDNA(非コードDNA)は、生物のDNAの中でタンパク質の配列をコードしていない部分を指します。このDNAは、タンパク質を直接コードする機能は持たず、その大部分はジェノムの調節機能を果たすことがわかっています。
定義と基本情報
ノンコーディングDNAの種類
ノンコーディングDNAは、タンパク質をコードしないDNAの部分を指し、人間のゲノムの大部分を占めます。これらのDNA領域は、多様な機能と重要な役割を持っており、以下のように分類されます。
● イントロン
イントロンは、遺伝子のコーディング領域(エクソン)の間に位置するDNAシーケンスです。これらは初期の転写産物からRNAスプライシングによって除去され、成熟mRNAには含まれません。イントロンは、遺伝子の調節に関与する可能性があることが示唆されています。
● レギュラトリー領域
プロモーターやエンハンサーといったレギュラトリー領域もノンコーディングDNAに含まれます。これらは遺伝子の発現を制御する重要な役割を果たし、遺伝子がいつ、どの細胞で、どのように発現されるかを決定します。
● リピート領域
ゲノム内には、単純リピートやディスパースドリピートなど、繰り返し配列が広範囲にわたって存在します。これらのリピート領域は、ゲノムの構造と機能に影響を与え、進化過程での変化や種の多様性に寄与する可能性があります。
● 非翻訳RNA
ノンコーディングRNAとして知られる多くのRNAは、タンパク質をコードしないものの、リボソームRNA、トランスファーRNA、マイクロRNAなどとして機能します。これらは遺伝子の発現を調節し、細胞の様々な生理的プロセスに関与しています。
ノンコーディングDNAのこれらの種類と機能を理解することは、生物学的なプロセスの広範な理解と、遺伝的疾患の研究において重要です。これらの領域が持つ機能や、どのように生物の進化や個体発生に貢献しているかを解明することが、今後の研究の大きな課題となっています。
ノンコーディングDNAの機能
1. 非コードRNAの転写: 一部のノンコーディングDNAは機能的な非コードRNA分子(トランスファーRNA、リボソームRNA、制御RNAなど)を転写する役割を持ちます。これらのRNAは、タンパク質の合成や遺伝情報の調節に関わる重要な役割を果たします。
2. 遺伝子の調節: ノンコーディングDNAは、タンパク質をコードする遺伝子の転写および翻訳を制御する重要な領域を含んでいます。これにはプロモーター、エンハンサー、サイレンサーなどの調節領域が含まれます。
3. 構造的な役割: ノンコーディングDNAにはセントロメアやテロメアなど、染色体の構造と維持に必要な領域も含まれています。これらは染色体の安定性と適切な分裂を支えるために不可欠です。
4. エピジェネティックな調節: ノンコーディング領域は、エピジェネティックな修飾を受ける場所としても機能します。これにより、遺伝子の発現が変化し、細胞の状態や発展に大きく影響します。
過去にはノンコーディングDNAの多くが「ジャンクDNA」と呼ばれ、無用と考えられていましたが、ENCODE(Encyclopedia of DNA Elements)プロジェクトなどの研究により、ヒトゲノムの少なくとも80%が何らかの生化学的活動に関与していることが明らかになりました。この発見は、ノンコーディングDNAが持つ潜在的な生物学的重要性とその複雑な機能を示しています。
非コードDNAの研究は、遺伝学や進化発生生物学において重要な進歩をもたらしており、今後もその機能や役割の解明が進むことが期待されています。
遺伝子調節における役割
ノンコーディングDNAは、遺伝子の発現を調節する上で重要な役割を果たしています。これらのDNA領域は、遺伝子がどのように、いつ、どこで活性化されるかを制御する多様な機能を持っています。
● プロモーターとエンハンサー
ノンコーディングDNAの中でも特に重要なのは、プロモーターとエンハンサー領域です。プロモーターは遺伝子の直前に位置し、RNAポリメラーゼとその他の転写因子が結合する場所を提供します。これにより、遺伝子の転写が開始されます。一方、エンハンサーはプロモーターから遠く離れた場所に存在することが多く、転写を増強する役割を担います。エンハンサーは転写因子が結合しやすい環境を作り出し、遺伝子の発現レベルを上昇させることができます。
● サイレンサー
サイレンサーもまたノンコーディング領域に含まれ、これは遺伝子の発現を抑制する機能を持ちます。サイレンサーに結合するタンパク質は、通常、遺伝子の活性化を妨げる役割を果たし、細胞内での遺伝子の発現パターンを精密に制御します。
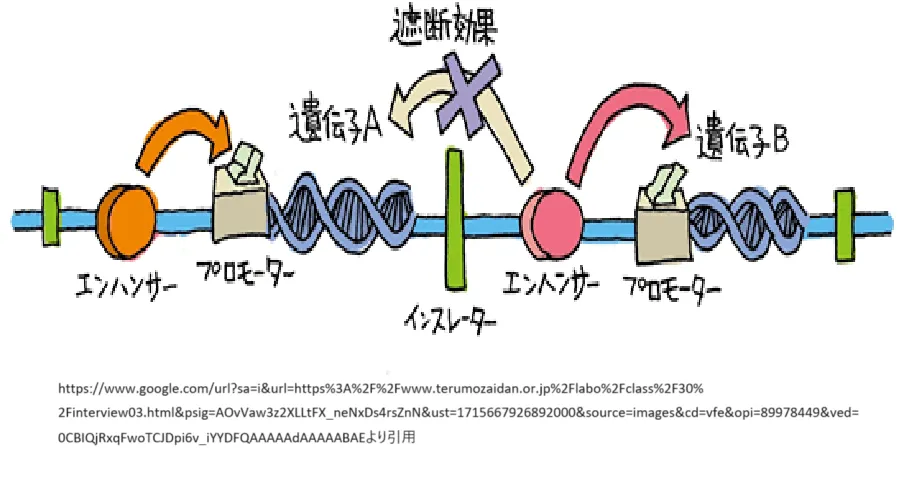
● インスレーター
インスレーターは、エンハンサーやサイレンサーが特定の遺伝子にのみ作用するように隔離するバリア機能を持つノンコーディング領域です。これにより、細胞は遺伝子の誤った発現を防ぎ、遺伝的情報の正確な使用を保証します。
これらのノンコーディングDNA領域は、細胞の種類や発達段階に応じて遺伝子の発現を調節し、生物の多様性と複雑性を支える基盤となっています。遺伝子の調節メカニズムを理解することは、遺伝病の治療や遺伝的操作の技術において非常に重要です。
RNA分子としての機能
ノンコーディングDNA領域から生成されるRNA分子は、タンパク質をコードしないものの、細胞内で重要な調節機能を果たしています。これらには、マイクロRNA(miRNA)、長鎖ノンコーディングRNA(lncRNA)などが含まれます。
● マイクロRNA (miRNA)
miRNAは、約22ヌクレオチド長の小さなRNA分子で、遺伝子の発現をポストトランスクリプションレベル(RNAがタンパク質に翻訳される過程)で抑制する役割を持っています。miRNAは特定のメッセンジャーRNA(mRNA)の3’非翻訳領域に結合し、そのmRNAの分解を促進するか、翻訳を抑制することで働きます。このプロセスにより、miRNAは細胞分化、発生、病気の進行といった多くの生物学的過程を調節します。
● 長鎖ノンコーディングRNA (lncRNA)
lncRNAは、200ヌクレオチドを超える長さを持つRNA分子で、構造、調節、または他のRNA分子の活性を変化させる多様な機能を持っています。lncRNAはクロマチンの修飾、転写の調節、mRNAの安定性の調節など、遺伝子発現の複数の段階に介入します。これらのRNAは、遺伝子のオン・オフを切り替えるスイッチの役割を果たすことがあり、特定の遺伝子が活性化または抑制されるタイミングを精密に制御することが可能です。
これらのノンコーディングRNAは、生物学的プロセスの微妙な調節に不可欠であり、細胞の正常な機能維持に対する理解を深めるとともに、がんや神経変性疾患などの病状の治療戦略を考案する上での新たな可能性を提供します。
非コードDNAのゲノムに占める割合
ゲノム内の非コードDNAの割合は、生物種によって大きく異なります。これは、各生物の遺伝的複雑さや進化の過程において非コードDNAが果たす役割が異なるためです。
● ヒトゲノムの非コードDNA
ヒトのゲノムでは、約98%が非コーディング領域とされています。この広範囲にわたる非コードDNAには、イントロン(遺伝子内の非コード領域)や遺伝子間領域が含まれます。これらの領域は、直接的にはタンパク質をコードしていませんが、遺伝子の調節、RNAの転写、クロマチン構造の形成といった重要な役割を担っています。
● 原核生物の非コードDNA
原核生物のゲノムは、ヒトなどの真核生物と比較して相対的に小さく、非コードDNAの割合も少ないです。一般的に、原核生物のゲノムでは約20%が非コーディングDNAであり、そのほとんどは遺伝子の調節領域や機能的なRNAとして機能します。
● 非コードDNAの量と生物の複雑性
生物種によるゲノムサイズの違いは、主に非コードDNAの量によって決まります。タンパク質をコードするDNA(コードDNA)の量は、多くの生物種間で比較的一定です。そのため、非コードDNAの存在は、生物の遺伝的複雑性や適応の多様性を反映していると考えられています。多くの非コードDNAがエピジェネティックな調節や遺伝的ネットワークの構築に関与しており、これが生物の進化的な発展に寄与しています。
非コードDNAはかつて「ジャンクDNA」と見なされていましたが、現在ではその多くが遺伝子発現の調節や遺伝的ネットワークの形成において重要な役割を持っていることが明らかになっています。このため、非コードDNAの研究は生物学的な理解を深め、新たな遺伝的メカニズムや治療標的を発見する鍵となるでしょう。
ノンコーディングDNA配列の種類
シス型およびトランス型調節因子
シス型とトランス型の調節因子は、遺伝子の転写を制御する方法が異なるため、遺伝子発現の調節において重要な役割を担っています。
● シス型調節因子(シスエレメント)
シス型調節因子、またはシスエレメントは、その遺伝子自体に直接連結しているDNA配列です。これらは遺伝子の近傍に位置し、直接的にその遺伝子の転写を調節します。シスエレメントは、通常、遺伝子の5’または3’の非翻訳領域(UTR)やイントロン内に存在します。シスエレメントにはプロモーターとエンハンサーが含まれます:
– プロモーター: 特定の遺伝子の転写開始点のすぐ上流に位置するDNA配列で、RNAポリメラーゼとその補助タンパク質が結合し、転写を開始する場所です。
– エンハンサー: 遺伝子の転写レベルを増加させることができる、プロモーターから離れた位置にあることも多い配列です。エンハンサーは、DNAのループ化によってプロモーターに物理的に近づき、転写因子の結合を促進します。
● トランス型調節因子(トランスエレメント)
トランス型調節因子、またはトランスエレメントは、一つの遺伝子の転写を制御するために他の遺伝子からコードされたタンパク質やRNAです。これらは、体内の異なる場所にある遺伝子の活動を遠隔操作で調節することができます。トランス調節因子には、通常、転写因子や非コーディングRNAが含まれ、これらは特定のDNA配列に結合して遺伝子の転写を促進または抑制します。
これらのシス型およびトランス型の調節機構は、遺伝子の精密な発現パターンを保証し、細胞の特定の状態や発達段階に応じた適切なタンパク質の生産を可能にします。また、これらの調節因子の相互作用は、生物の生理的および病理的プロセスにおいて重要な役割を果たします。
イントロン
イントロンは、遺伝子の構造において重要な役割を果たしている非コーディング部分です。これらは前駆体mRNA(pre-mRNA)に転写されるものの、成熟したメッセンジャーRNA(mRNA)を形成する過程で取り除かれる部分であり、このプロセスはRNAスプライシングと呼ばれます。
● イントロンの基本的な機能と重要性
1. RNAスプライシング:
– イントロンは、転写後のpre-mRNAから特定のスプライシング機構によって除去されます。スプライシングは、スプライソソームと呼ばれる大型のリボ核酸-タンパク質複合体によって行われ、正確なエクソン(コーディング領域)の結合を可能にします。
2. 遺伝子の多様性の増加:
– イントロンを含む遺伝子は、異なるスプライシングパターンを通じて複数の異なるmRNAとタンパク質を生産することが可能です。これにより、同じDNA配列から複数のタンパク質が合成され、遺伝的多様性が増加します。これは特に高等生物において顕著で、様々な生理的機能や環境適応を可能にします。
3. 遺伝子調節の制御:
– イントロン領域には、エンハンサーやサイレンサーなどの調節配列が含まれることがあり、これらは遺伝子の発現を調節する重要な役割を担います。また、イントロン自体が調節因子として機能することもあります。
4. 遺伝子の進化:
– イントロンは遺伝子の進化過程で重要な役割を果たします。イントロンの挿入や除去は、遺伝子構造の変化を引き起こし、新しい遺伝子機能や新たな調節機構の出現に寄与します。また、遺伝子の重複や遺伝子間の組み換えに影響を与えることがあります。
イントロンの存在と機能は、生物の適応と進化において中心的な役割を果たしており、生物学的な複雑さと多様性の理解に不可欠です。
シュードジーン
偽遺伝子(シュードジーン)は、進化過程で機能を失った遺伝子のことを指します。これらはもともと活動的な遺伝子から派生したものですが、様々な変異によりタンパク質をコードする能力が失われ、基本的には機能しない状態にあります。以下に、偽遺伝子の主な特徴とその起源について説明します。
● 偽遺伝子の起源と特徴
1. レトロトランスポジション:
– これは遺伝子がRNAとして転写された後、逆転写酵素によってDNAに戻され、ゲノムの別の位置に挿入される現象です。このプロセス中に、元の遺伝子とは異なる場所に挿入された遺伝子が機能を失い、偽遺伝子になることがあります。
2. ゲノム重複:
– ゲノム内の遺伝子が複製されると、一方のコピーが変異によって非機能化し、偽遺伝子となることがあります。これにより、新たに複製された遺伝子コピーは進化の過程で新しい機能を獲得するか、または機能を失う可能性があります。
3. 変異:
– 偽遺伝子は、フレームシフトや早期停止コドンの出現など、遺伝子配列内の変異によってタンパク質の正常な翻訳が妨げられるために機能を失います。これらの変異は、遺伝子の転写や翻訳プロセスを直接阻害することが多いです。
4. NUMT(ヌミット):
– ミトコンドリアの遺伝子が核ゲノムに転移して非機能化したものを指します。これらはミトコンドリアDNAの断片が核DNAに組み込まれた結果、元の機能を失った遺伝子となります。
● 偽遺伝子の機能的側面
偽遺伝子は「ゲノムの化石」とも称されますが、それらが完全に機能を失っているわけではありません。最近の研究により、多くの偽遺伝子が活発に転写され、遺伝子の調節や発現に影響を与えるRNA分子として機能することが示されています。このことは、偽遺伝子が進化的にも重要な役割を持っている可能性を示唆しており、その再活性化や新しい機能の獲得が進行中であることを示しています。
偽遺伝子の存在と機能は、生物の進化と遺伝的適応の理解を深める上で重要な要素であり、未だに多くの科学的な探求が行われている研究領域です。
トランスポゾン、レトロウイルス
トランスポゾンとレトロウイルスは、生物のゲノム進化と多様性に大きく寄与している重要な遺伝要素です。これらの要素はゲノム内での位置を変えることができるため、「ジャンピング・ジーン」とも呼ばれます。以下で、トランスポゾン、レトロトランスポゾン、および内在性レトロウイルス配列の特徴と機能について説明します。
● トランスポゾンとレトロトランスポゾン
1. トランスポゾン:
– DNAトランスポゾンとも呼ばれ、これは切断とペーストのメカニズムを使用してゲノム内を移動します。エンドヌクレアーゼと呼ばれる酵素によってDNA断片が切り出され、新しい位置に挿入されます。このプロセスは、遺伝子の重複や新しい遺伝的特徴の挿入を引き起こし、遺伝的多様性を増加させます。
2. レトロトランスポゾン:
– レトロトランスポゾンは、逆転写酵素を使用して自身のRNAをDNAに転写し、それをゲノムの新しい場所に挿入します。このグループには、長鎖核内要素(LINE)、短鎖核内要素(SINE)、およびレトロウイルスに類似したLTR(長末端反復)エレメントが含まれます。特にAlu配列(SINEの一種)はヒトゲノムにおいて最も豊富な移動性遺伝要素であり、遺伝子の転写制御に関与しています。
● 内在性レトロウイルス配列
– 内在性レトロウイルスは、感染性レトロウイルスが生殖細胞に侵入し、そのゲノムが宿主のDNAに逆転写されて組み込まれたものです。これらは通常、変異により不活性化されており、ウイルスとしての機能を失っていますが、宿主ゲノムにおいて新しい遺伝的特徴を導入することがあります。内在性レトロウイルス配列は、特定の遺伝子の発現調節や新たな遺伝的要素として機能することがあります。
● 役割と影響
トランスポゾンとレトロウイルス由来の要素は、宿主のゲノムにおいて重要な遺伝的変化を引き起こすことがあります。これらの変化は、進化の過程で新しい遺伝的特性を形成し、種の適応と生存に寄与します。また、これらの遺伝要素の活動は、遺伝病の原因となることもあり、その機能と調節の理解は遺伝学および分子生物学における重要な課題です。
テロメア
テロメアは、生物の細胞が健康に機能し続けるために重要な役割を果たしています。これらは染色体の末端に位置する特殊な構造で、反復的なDNA配列から構成されています。テロメアは細胞分裂が行われるたびに染色体が安定して維持されることを保証し、遺伝情報の損失を防ぎます。以下に、テロメアの構造と機能、さらに関連する最新の研究について詳しく説明します。
● テロメアの構造
– 反復DNA配列:
テロメアは「TTAGGG」という短いDNA配列の数千回の繰り返しで構成されています(ヒトの場合)。この反復配列は染色体の末端を形成し、その安定性を保つために重要です。
– 保護キャップの役割:
テロメアは染色体の端を保護するキャップとして機能し、DNAが不安定になることを防ぎます。この保護により、重要な遺伝情報が失われることなく、細胞分裂が安全に行われます。
● テロメアの機能
– DNA複製の保護:
DNA複製の際、DNAポリメラーゼは染色体の末端まで完全に複製することができません。テロメアはこの問題を緩和し、重要な遺伝情報が失われないようにする役割を果たします。
– 細胞老化の調節:
テロメアの長さは細胞が分裂するたびに短くなり、一定の限界に達すると細胞は分裂を停止し老化します。このメカニズムにより、細胞の寿命が決定されます。
● テロメリックリピート含有RNA(TERRA)
– テロメラーゼ活性の調節:
TERRAはテロメア自体から転写される非コーディングRNAで、テロメラーゼ活性の調節に関与しています。テロメラーゼはテロメアを延長する酵素で、特に幹細胞や癌細胞において重要です。
– 染色体の安定性の維持:
TERRAはテロメアの構造と機能を維持するために重要な役割を担っています。テロメアの保護と修復に関与し、染色体の安定性を高めます。
テロメアとTERRAの研究は、細胞の老化、がんの進行、およびその他の健康障害と密接に関連しています。これらの知見は、新たな治療法の開発や老化防止策、さらには寿命延長技術の可能性を探る上で非常に重要です。
非コードDNAが機能しているという証拠
非コードDNAが持つ機能に関する理解は近年急速に進展しており、多くの科学的研究が非コードDNA領域が持つ重要な生物学的役割を示しています。以下に、非コードDNAが機能的であるとされる証拠についてのポイントをまとめます。
● 非コードDNAの機能的証拠
1. 進化的保存性:
– 比較ゲノミクスの研究は、非コードDNAの中にも進化的に高度に保存された領域が存在することを明らかにしています。ヒトとマウスなど、進化的に離れた種間で保存されている非コード領域が存在することは、これらの領域が重要な機能を持っている可能性を示唆しています。
2. 疾患関連性:
– リンケージマッピングやゲノムワイド関連研究(GWAS)により、多くの疾患に関連する染色体領域が特定されていますが、これらの領域には機能的なコード領域の変異が見られないことがあります。このことは、疾患の原因となる遺伝子変異が非コードDNAに存在する可能性を強く示唆しています。特に、がんなどの疾患で非コード領域の変異が重要な役割を果たしている例が増えています。
3. 非コードDNAの活動的な転写:
– ENCODEプロジェクトなどの研究により、ヒトゲノムの大部分が何らかの形で転写されていることが示されています。非コードDNAからは多数の非コーディングRNAが転写され、これらが遺伝子の発現調節、エピジェネティックな修飾、染色体の構造形成など、多岐にわたる生物学的プロセスに関与しています。
4. 染色体の構造と機能:
– 非コードDNAは染色体の構造と維持にも重要な役割を果たしています。例えば、セントロメアやテロメアの構造は非コードDNAによって形成され、これらの領域は染色体の安定性と正確な細胞分裂に不可欠です。
これらの証拠は、非コードDNAが単なる「ジャンク」としてではなく、生物の発達、適応、そして疾患の発生において中心的な役割を果たしていることを示しています。このため、非コードDNAのさらなる研究は、生命科学の多くの分野における基礎的な理解を深めるだけでなく、新たな治療ターゲットや診断マーカーの発見につながる可能性があります。
ノンコーディングDNAの研究進展
疾患との関連
ノンコーディングDNAの変異は、多くの疾患の発症リスクに影響を及ぼすことが研究によって明らかにされています。これらのDNA領域は、遺伝子の発現を制御する重要な役割を担っており、その変異は直接的に遺伝子の活性化や抑制に影響を与えることができます。
● 癌との関連
ノンコーディング領域の変異は、特にがんの発生に密接に関連しています。例えば、特定のノンコーディングRNAが過剰に発現することによって、がん抑制遺伝子が不活化されたり、癌遺伝子が活性化されることがあります。これにより、細胞の増殖が異常になり、結果として腫瘍が形成されます。
● 心血管疾患
心血管疾患でも、ノンコーディング領域の変異が重要な役割を果たすことが知られています。特定のノンコーディング領域の変異が心筋の発達や血管の形成を調節する因子の発現に影響を与えることで、心血管疾患のリスクが変動します。
● 神経変性疾患
アルツハイマー病やパーキンソン病など、神経変性疾患においても、ノンコーディングDNAの変異が関与していることが示唆されています。これらの変異は、神経細胞の生存に必要な遺伝子の発現を不適切に調節することにより、疾患の発症に寄与する可能性があります。
これらの最新の研究成果は、ノンコーディングDNAが人間の健康に及ぼす影響を理解する上で非常に重要です。ノンコーディングDNAの研究はまだ進行中であり、これらの知見が将来的にはより効果的な診断手法や治療戦略の開発につながることが期待されています。
診断と治療への応用
ノンコーディングDNAの理解が深まるにつれて、その知見を診断や治療に応用するための研究が進展しています。特に、ノンコーディング領域から得られる情報は、疾患の早期発見や新たな治療法の開発に寄与しています。
● 新しい診断手法
ノンコーディングRNA、特にマイクロRNA(miRNA)や長鎖非コーディングRNA(lncRNA)は、特定の疾患状態と密接に関連しています。これらのRNA分子の発現パターンは疾患特異的であり、血液や体液中から容易に検出できるため、非侵襲的なバイオマーカーとしての使用が研究されています。例えば、特定のがんや心血管疾患、神経変性疾患の早期診断にmiRNAやlncRNAのプロファイルを利用することが検討されています。
● 治療戦略への応用
ノンコーディングDNAに基づく治療戦略も開発されており、特にRNA干渉技術を利用したアプローチが注目されています。この技術では、特定のノンコーディングRNAを標的とする小分子RNAを設計し、疾患関連遺伝子の発現を抑制することで治療効果を期待します。また、特定のノンコーディング領域を標的とするCRISPR-Cas9などのゲノム編集技術も、根本的な遺伝的原因に対処するために研究されています。
これらの進展は、個々の患者の遺伝的プロファイルに基づいたパーソナライズドメディスンの実現に向けた一歩となる可能性があります。ノンコーディングDNAの研究が進むにつれて、より効果的で副作用の少ない治療法の開発が期待されています。
ノンコーディングDNAと個別化医療
ゲノムワイドアソシエーション研究(GWAS)
ゲノムワイドアソシエーション研究(GWAS)は、広範囲の遺伝的変異と特定の疾患との関連を特定する手法です。この研究では、特にノンコーディング領域の変異がどのように疾患のリスクに寄与するかを調査します。
● GWASのプロセス
GWASは、数千から数万人の個体群のDNAサンプルを解析し、特定の疾患を持つ人々と持たない人々の間で共通の遺伝的変異を探します。このアプローチでは、ノンコーディング領域に存在する一塩基多型(SNPs)が頻繁に検出されます。これらのSNPsは、遺伝子の発現を調節する可能性があり、その結果、疾患の発生に影響を与えることがあります。
● ノンコーディング領域の重要性
多くのGWASでは、疾患に関連する遺伝的変異の大部分が、実際にはタンパク質をコードする遺伝子領域ではなく、ノンコーディング領域に位置していることが判明しています。これらのノンコーディング領域は、遺伝子の発現を制御するエンハンサーやプロモーターとして機能することがあり、遺伝子の活性化や抑制に直接影響を及ぼすことで、疾患の発症に寄与します。
● 研究の応用
ノンコーディング領域に焦点を当てたGWASの結果は、疾患の原因や発症メカニズムを理解するために非常に重要です。これにより、新しい診断マーカーや治療ターゲットの特定が可能になり、個別化医療の発展に寄与することが期待されます。また、これらの研究から得られた知見は、予防策やリスク管理戦略の改善にも役立つ可能性があります。
GWASは遺伝学と分子生物学の分野において重要なツールであり、ノンコーディングDNAの複雑な役割を解明する鍵となっています。
バイオマーカーとしての可能性
ノンコーディングDNAの領域は、多くの疾患のバイオマーカーとしての潜在的な役割を持っています。これらの領域から得られる情報は、病気の診断、進行の監視、治療応答の予測に役立つ可能性があります。
● ノンコーディングRNAの診断への応用
特に、ノンコーディングRNA(ncRNA)は、その発現パターンが特定の疾患と強く関連しているため、有効なバイオマーカーとなり得ます。例えば、特定のマイクロRNA(miRNA)は、がんや心血管疾患、アルツハイマー病など、様々な病態のバイオマーカーとして同定されています。これらのmiRNAは、病気の初期段階で異常な発現を示すことが多く、血液検査などで簡単に検出することができます。
● 長鎖非コーディングRNAの役割
また、長鎖非コーディングRNA(lncRNA)も、特定の疾患の発症と関連が見られることから、診断や予後予測のバイオマーカーとして注目されています。lncRNAは、がんの種類によって異なる発現パターンを示すことがあり、これを利用してがんのタイプや進行度を特定する研究が進められています。
● 具体的な事例
例として、miRNA-21は多くのがん種で過剰発現されており、がんの存在を示す早期診断マーカーとして利用される可能性があります。また、lncRNA PCA3は前立腺がんの診断において高い特異性を持つことが知られており、これを標的とした診断法が開発されています。
これらのバイオマーカーは、疾患の早期発見や治療のカスタマイズ、患者の管理に大きく寄与することが期待されており、ノンコーディングDNAの研究が進むことで、さらに多くの新しいバイオマーカーが発見される可能性があります。