目次
Nonsense-mediated mRNA decay(NMD)の包括的解説:基本メカニズム、生物学的役割、そして遺伝子疾患やがん治療におけるその応用について探る。最新の研究動向と未来の治療戦略を展望します。
序章: NMDとは何か?
NMDの基本概念
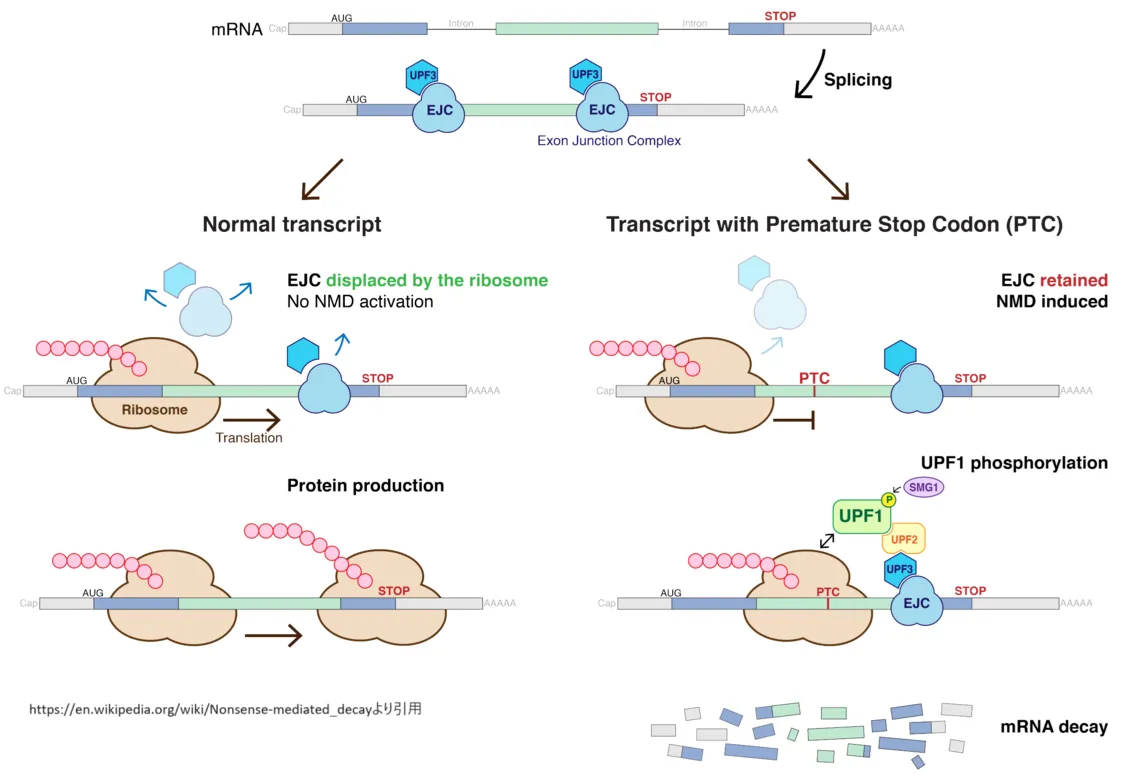
Nonsense-mediated mRNA decay(NMD)は、細胞が効率的に機能するために必要な重要な生物学的過程です。これは主に、翻訳過程中に異常が検出されたmRNAを特定し、分解する役割を担います。具体的には、遺伝子がコードするmRNA内にプレマチュア終止コドン(PTC)が存在する場合、このNMD経路が活性化されます。PTCは、通常よりも早く翻訳が終了することを意味し、しばしば機能不全のタンパク質が生成される原因となります。
NMDの主な機能は、このような非効率的または異常なmRNAをセルから除去することで、細胞内のタンパク質の質を維持し、遺伝子の発現を正確に調節することです。これにより、細胞はエネルギーを無駄にすることなく、より効率的に機能することができます。また、NMDは遺伝子の表現レベルを微調整することにより、細胞の応答性と適応性を高める役割も果たしています。このプロセスは、多くの生物学的な調整機能と連携しており、生物の健康と病気の状態に広範な影響を及ぼす可能性があります。
NMDの歴史的発見
Nonsense-mediated mRNA decay(NMD)の発見は、分子生物学における重要な進歩の一つです。この発見は、1980年代に遡ります。NMDは、当初は特定の遺伝子の異常なmRNAを研究していた中で偶然発見されました。これらのmRNAは、プレマチュア終止コドン(PTC)が存在するために通常より早く終了してしまう特性を持っていました。
この現象は、遺伝子の異常な読み取りを防ぐためのセルの自己防衛機構の一環として初めて認識されました。研究が進むにつれて、このプロセスがどのようにしてセルが機能不全のタンパク質の生成を阻止し、遺伝的安定性を維持するのに役立っているかが明らかになりました。1980年代半ばには、この過程を詳細に記述する論文が多数発表され、NMDがRNA品質管理の重要な機構であることが広く受け入れられるようになりました。
NMDのメカニズムが解明されると、その研究は遺伝学、発生生物学、疾患の研究など、生命科学の多くの分野に応用されるようになりました。NMDは、特に遺伝子疾患の原因となる異常なmRNAの除去に関与しているため、これらの疾患の治療法の開発にも貢献しています。このようにして、NMDの研究は基礎研究から臨床応用に至るまで、科学界における重要なテーマとなっています。
NMDの分子機構
主要なコンポーネントとその相互作用
Nonsense-mediated mRNA decay(NMD)は、複数のタンパク質が組み合わさって機能する複雑な分子機構です。この経路の中心的な役割を担うのは、UPF1、UPF2、そしてUPF3というタンパク質です。これらは互いに密接に作用し合い、異常なmRNAを検出して分解するプロセスを促進します。
UPF1:NMD経路の主要なタンパク質で、RNAヘリカーゼおよびATP依存性のRNA結合タンパク質として機能します。UPF1は、プレマチュア終止コドン(PTC)を含むmRNAに結合し、その分解を引き起こすために必要な分子的変更を行います。
UPF2とUPF3:これらのタンパク質は、UPF1の活動を調節する役割を持ちます。UPF2は主にUPF1と相互作用し、その活性を調節する一方で、UPF3はmRNAとリボソームの間で作用し、UPF1の結合を助けることでNMDを促進します。
これらのタンパク質は連携して、異常なmRNAが翻訳過程を通じて正常なタンパク質へと変換されることを阻止し、セルのタンパク質合成の精度を保ちます。UPF1、UPF2、およびUPF3の相互作用は、NMDが正確に機能するための基盤を形成し、これによりセルは遺伝的情報の正確な利用を保証します。このようにして、NMD経路は細胞の遺伝的安定性を維持するために不可欠な役割を果たしています。
NMD経路の活性化と制御
Nonsense-mediated mRNA decay(NMD)経路の活性化は、特定の分子的シグナルと条件に基づいています。この経路は、主にプレマチュア終止コドン(PTC)が存在するmRNAを認識し、これを効率的に除去するために機能します。活性化のプロセスは複雑で、いくつかのレギュレーターによって精密に制御されています。
活性化条件: NMDは通常、翻訳プロセス中に異常が検出された場合に活性化されます。具体的には、mRNA上の終止コドンが通常よりも早く現れた場合(PTC)、または翻訳後の複合体の配置が異常である場合にNMDが誘導されます。この異常検出は、リボソームの翻訳終了後に行われる品質管理の一環として機能します。
制御機構: NMDの調節は、複数の分子が関与することによって行われます。UPF1は、NMDの核心となるタンパク質であり、翻訳終了因子(eRF1およびeRF3)と相互作用し、PTCを含むmRNAの分解を促進します。また、UPF1のリン酸化状態は、NMDの活性化において重要な役割を果たし、リン酸化が増すことでNMD活性が高まります。その他にも、Exon-junction complex(EJC)というタンパク質複合体が、PTCの上流で結合することでNMDを助け、異常なmRNAの効率的な識別と分解をサポートします。
これらの制御機構により、NMDは細胞内の遺伝子発現レベルを微調整し、遺伝的安定性を保ちながら細胞の正常な機能を支える重要な役割を果たしています。このようにNMDは、不要または有害なmRNAを選択的に除去することで、セルの生物学的プロセスの調整に不可欠です。
NMDの生物学的役割
遺伝子発現の品質管理
Nonsense-mediated mRNA decay(NMD)は、遺伝子発現の品質管理プロセスとして重要な役割を果たしています。このプロセスでは、不完全または誤ったmRNAを効率的に検出し、分解することで、細胞内のタンパク質の品質と機能の維持に寄与します。
検出メカニズム: NMDの最初のステップは、異常な終止コドンを含むmRNAの検出です。これは通常、翻訳プロセス中にリボソームがプレマチュア終止コドン(PTC)に遭遇した際に発生します。終止コドンが遺伝子の通常のコーディングシーケンスよりも前方に位置する場合、このコドンはPTCと見なされ、NMDがトリガーされます。
分解メカニズム: PTCが検出されると、UPFプロテイン(UPF1, UPF2, UPF3)が関与する一連の反応が始まります。これらのプロテインは、PTCを含むmRNAと結合し、そのmRNAの分解を促進するために他の分解酵素を招集します。具体的には、UPF1がリン酸化され、この変化がNMDの主要な駆動力となります。リン酸化されたUPF1は、分解複合体の形成を促進し、最終的に異常なmRNAを分解します。
このようにNMDは、翻訳プロセス中に発生する可能性のあるエラーを修正し、遺伝子発現の精度を高めるための重要なメカニズムとして機能しています。このシステムにより、細胞は非効率的なタンパク質の合成を防ぎ、生物学的プロセスの正確性と効率性を保つことができます。
翻訳後調節と遺伝子サイレンシング
Nonsense-mediated mRNA decay(NMD)は、単に異常なmRNAを除去するだけでなく、遺伝子のサイレンシングや翻訳後の調節にも深く関与しています。この機能により、NMDは細胞内のタンパク質合成を微調整し、遺伝子の発現パターンを効果的に制御する役割を果たしています。
遺伝子のサイレンシング: NMDは、特定の遺伝子が過剰に発現するのを防ぐために、そのmRNAを特定し分解することで遺伝子のサイレンシングに寄与します。これにより、必要以上にタンパク質が合成されるのを防ぎ、細胞の恒常性を維持します。例えば、一部の非コードRNAや、特定の内在性レトロウイルス遺伝子由来のmRNAは、NMDによってサイレンスされることが知られています。
翻訳後の調節: NMDはまた、mRNAの翻訳プロセスが完了した後の翻訳後調節にも関与します。例えば、mRNAが翻訳された後、NMDはmRNAの半減期を短縮させることでタンパク質の合成量を調節することがあります。これは、細胞が迅速に環境の変化に対応するために重要です。
このようにNMDは、細胞の遺伝的情報が正確に使用されるようにするだけでなく、不要または潜在的に有害なタンパク質が合成されるのを防ぎ、細胞全体の機能と健康を維持するために重要な役割を果たしています。
X染色体の用量補償におけるNMDの役割
Nonsense-mediated mRNA decay(NMD)は、X染色体の用量補償において重要な役割を果たしています。用量補償は、男性がX染色体を1つ、女性が2つ持つという性染色体の数の違いにも関わらず、両性間での遺伝子発現を均等に保つメカニズムです。このバランスは、X染色体上の遺伝子から生成されるタンパク質の有害な過剰または不足を防ぐために不可欠です。
NMDは、特定のmRNAを選択的に分解することで、性別間のタンパク質生産の不均衡を防ぎ、用量補償に寄与します。研究によると、NMDは分解を目標とした特定のmRNAを通じて、X染色体の遺伝子の発現レベルを調節することができます。このターゲティングにより、X染色体からの遺伝子発現が常染色体(性染色体以外の染色体)と一致するように保たれ、細胞および生体の恒常性が維持されます。
このように、NMDは単にmRNAの誤りに対抗するだけでなく、正常な発達や細胞機能に不可欠な遺伝的発現の微調整において重要な役割を担っています。これは、NMDがX染色体の用量補償における重要な調節者であることを示しています。
特定の組織や発達段階でのNonsense-mediated mRNA decay(NMD)
特定の組織や発達段階でのNonsense-mediated mRNA decay(NMD)の活動を探る研究は、NMDが持つ生理的な多様性とその複雑な調節機構を理解する上で非常に重要です。NMDは細胞が遺伝子発現を精密に制御するために不可欠な機構であり、その活動は組織や発達の段階によって異なる可能性があります。
●NMDの多様な生理的役割
組織特異性: 組織によっては、NMDの活動が特に強く必要とされる場合があります。例えば、神経組織では、正確な遺伝子発現が神経機能の精度に直接関連しているため、NMDが積極的に関与しています。
発達段階の違い: 発達の早い段階では、細胞分化に必要な遺伝子の正確な発現が求められるため、NMDの調節が特に重要です。発達が進むにつれて、NMDの活動パターンも変化し、成熟した細胞や組織のニーズに応じて調整されます。
●NMDの調節機構
NMDの活動は、さまざまなシグナル伝達経路や因子によって細かく調節されています。これには以下のようなメカニズムが含まれます:
転写後の修飾: NMDに関わる因子自体が、リン酸化や他の化学的修飾を受けることで活性が変化することがあります。
環境因子への応答: 細胞外のシグナルやストレス条件がNMDの活動を調節することもあり、これにより細胞は環境の変化に迅速に対応できます。
このような研究を通じて、NMDがどのようにして細胞の生理的状態や発達プロセスに適応し、遺伝的安定性を保ちながら適切なタンパク質生産を支援しているのかの理解が深まります。これにより、特定の疾患に対する治療法の開発や、細胞の機能を改善する新たな戦略を考案する手がかりを得ることができるでしょう。
NMDと疾患
遺伝子疾患でのNMDの役割
Nonsense-mediated mRNA decay(NMD)は、遺伝子疾患の発生と進行に重要な役割を果たしています。特に、プレマチュア終止コドン(PTC)による異常なmRNAを除去することで、疾患の症状の軽減や進行の防止に寄与することがあります。例として、シャルコー・マリー・トゥース病(CMT)などの神経変性疾患が挙げられます。
シャルコー・マリー・トゥース病では、特定の遺伝子変異が神経細胞の機能不全を引き起こし、これが疾患の症状に直結します。NMDは、これら変異を含むmRNAを標的とし、不完全なタンパク質が合成されるのを防ぐことにより、細胞の損傷を最小限に抑えることができます。しかし、NMDが過剰に活性化されると、必要なタンパク質まで分解されてしまう可能性があり、その結果、症状が悪化することもあります。
このように、NMDは遺伝子疾患のコンテキストで二重の役割を果たしています。一方で、異常な遺伝情報の流出を防ぎ、細胞の正常な機能を支える保護的な役割を果たします。他方で、必要な遺伝情報が誤って排除されることで、病態を悪化させる可能性もあります。したがって、NMDの精密な調節は、遺伝子疾患治療において重要な研究対象となっています。
がんにおけるNMDの二重性
Nonsense-mediated mRNA decay(NMD)はがん細胞の成長と進行に影響を及ぼすことが示されており、がん治療においてNMDを標的とするアプローチが研究されています。NMDの役割はがんのタイプや状態によって異なるため、その二重性が特に注目されています。
がん細胞の成長への影響: NMDは通常、異常なmRNAを除去することで細胞の遺伝的安定性を維持し、がんの抑制に寄与します。しかし、一部のがん細胞では、NMDが不完全に機能することがあり、これが異常なタンパク質の蓄積を許し、がん細胞の成長や生存を促進することがあります。参考文献
がん治療におけるNMDの標的化: NMD経路の特定のコンポーネントを標的とすることで、がん細胞の増殖を抑制する新しい治療戦略が開発されています。例えば、特定のNMD因子の活性を抑制することで、がん細胞内の不正なmRNAが分解されず、結果的に細胞死を誘導する可能性があります。また、NMDを抑制することで新たな免疫原性ペプチドが生産され、がん免疫療法の効果を高めることが期待されています(参考文献)。
このように、NMDはがん細胞の生物学において重要な役割を果たしており、その精密な調節ががん治療に新たな可能性をもたらすことが示されています。今後の研究により、NMDを利用した治療の最適化が進むことが期待されます。
研究と治療への応用
最新の研究成果と挑戦
Nonsense-mediated mRNA decay(NMD)に関する最近の研究は、この重要な生物学的経路の理解を大きく前進させていますが、同時に新たな科学的課題も明らかになっています。
最新の研究成果: 近年の研究では、NMDが単に異常なmRNAを除去するだけでなく、細胞の発達、免疫応答、および病態生理におけるその役割が広がっていることが明らかにされています。特に、NMDが特定のがんタイプで異常に活性化され、がん細胞の生存と増殖を支援していることが示されています参考文献。また、異なる組織や発達段階でNMDの活性がどのように変化するかについての研究も進められており、これにより個別化医療におけるNMDの潜在的な役割が探求されています参考文献。
現在直面している課題: 一方で、NMD経路の複雑さとその生物学的な多様性は、研究者にとって大きな課題となっています。例えば、NMDが関与する疾患の範囲が広がるにつれて、どのようにしてこの経路を特定の疾患の治療に利用できるかを理解することが求められています。また、NMDの調節機構を正確に操作する方法を開発することも重要な課題です。
これらの研究成果と課題は、NMDに関するさらなる研究を促進し、将来的には新しい治療法の開発につながる可能性があります。科学者たちは、NMDの精密なメカニズムを解き明かし、それを医療に応用する方法を模索しています。
治療目標としてのNMD
Nonsense-mediated mRNA decay(NMD)は、遺伝子治療の新しいアプローチとして注目されています。NMDの調節を通じて疾患の治療に利用する試みが進んでおり、特に遺伝子異常が原因である種類の疾患に対して有効な可能性があります。
新しい治療戦略: NMDの標的化は、特に遺伝的異常を含むmRNAを制御することにより、疾患の原因となるタンパク質の生産を抑制する戦略です。例えば、特定の遺伝子疾患において、異常なmRNAがNMDによって除去されずにタンパク質が生産されることが問題となる場合、NMDの活性を高めることでこれを防ぐ試みが行われています参考文献。
持つ可能性: また、NMDを抑制することで、通常はNMDによって分解される有益なタンパク質が細胞内で保持されることを利用した治療法も研究されています。このアプローチは、特定のがんタイプにおいて、免疫系による認識を高め、より効果的ながん治療が期待できるとされています参考文献。
これらのアプローチには、NMDの精密な制御と個々の病態に合わせた調節が必要です。今後の研究で、NMDを標的とした治療法がさらに発展し、多くの疾患に対して新たな治療オプションとして実用化されることが期待されています。
Nonsense-mediated mRNA decay (NMD)を標的とした治療方法は、特定の遺伝子疾患に対して実用化されつつあります。例えば、筋ジストロフィーや一部のがん治療において、NMDの機構を利用して異常なmRNAを減少させることが研究されています。
NMDは、異常なmRNAがタンパク質に翻訳されるのを防ぐことにより、病気の進行を遅らせるかもしれないと考えられています。具体的には、がん細胞においてNMDを抑制することで、新しい抗原(ネオアンチゲン)の生成を増やし、これにより免疫系の反応を強化する可能性があります。このアプローチは、免疫チェックポイント阻害剤との併用により、がん治療における新たな戦略として注目されています。
さらに、特定のアンチセンスオリゴヌクレオチドを用いてNMD経路を標的にする方法も研究されており、これにより特定の遺伝子からのmRNAの分解を防ぎ、必要なタンパク質の生産を促進することが可能になるかもしれません。
これらの治療法の発展により、NMDを利用した新しい治療戦略が今後さらに拡がることが期待されています。