ミリストイル化
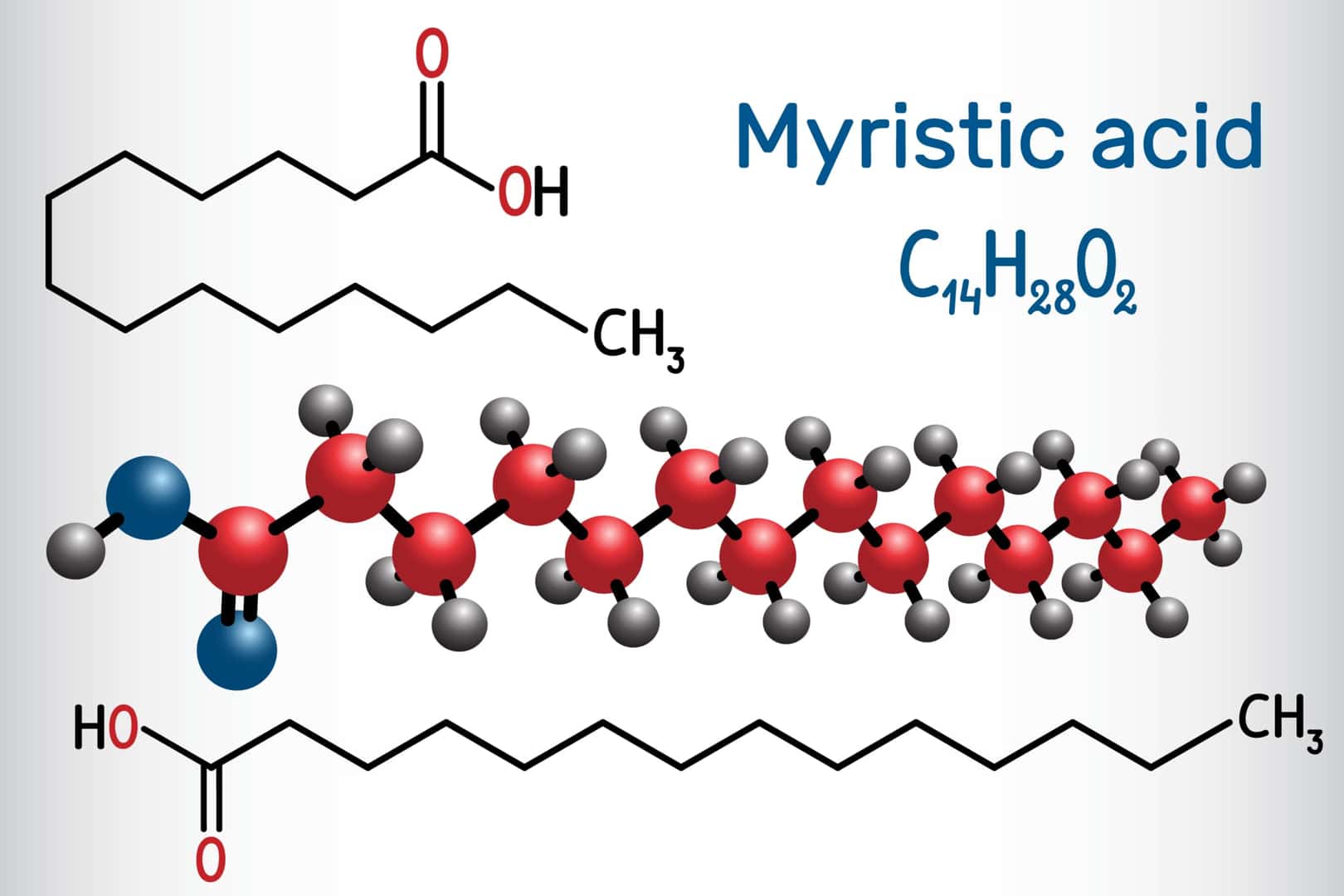
ミリストイル化とは、N末端のグリシン残基のα-アミノ基にミリスチン酸由来のミリストイル基をアミド結合で共有結合させるタンパクの脂質修飾である。ミリスチン酸は,n-テトラデカン酸という系統名を持つ炭素数14の飽和脂肪酸である。この修飾は、共翻訳的にも翻訳後にも付加される。N-myristoyltransferase (NMT) Nミリストイル転移酵素と呼ばれる酵素が細胞質内でミリスチン酸付加反応を触媒する。ミリストイル化は脂肪のアシル化の中で最も多く見られるタイプであり、多くの生物に共通して見られる。ミリストイル化は、タンパク質-タンパク質およびタンパク質-脂質の弱い相互作用を可能にし、膜のターゲティング、タンパク質-タンパク質の相互作用に必須の役割を果たし、様々なシグナル伝達経路で広く機能している。
ミリストイル化のメカニズム
蛋白質の正電化を帯びた塩基性残基が、膜上の負電荷を帯びたリン脂質と相互作用し、ミリストイル依存性の膜結合を安定化させる。
ミリストイル化されたタンパク質にリガンドが結合すると、ミリスチル基が露出し、膜との結合が可能になる。
ミリストイル-静電スイッチを特徴づけるのは疎水性のミリストイル基と「ベーシックパッチ」(タンパク質上の高陽性荷電領域)である。ベーシックパッチは、膜の負電荷を帯びたリン脂質の頭部と、結合するタンパク質の正電荷を帯びた表面との間に、有利な静電的相互作用を生じさせる。これにより、タンパク質の結合が強固になり、局在化が促進される。
ミリストイル化の役割
ミリストイル化は、タンパク質-タンパク質およびタンパク質-脂質の弱い相互作用を可能にし、膜のターゲティング、タンパク質-タンパク質の相互作用に不可欠な役割を果たし、様々なシグナル伝達経路で広く機能している。
ミリストイル基の最大の機能は、膜への結合と修飾タンパク質の細胞内局在化である。ミリストイル化は「分子のスイッチ」のようなものである。
ミリストイル・コンフォーメーション・スイッチにはいくつかの形態があり、このような構造変化は、細胞内での局在化、膜タンパク質間、タンパク質間の相互作用のシグナルとして利用できる。
- 1.ミリストイル基が封鎖されたミリスチル化タンパク質にリガンドが結合すると、タンパク質のコンフォメーションが変化し、ミリスチル基が露出する。
- 2.ミリスチル化タンパク質が細胞内のグアニンヌクレオチド交換因子によってGDPがGTPに交換されることで活性化される。GTPがミリスチル化タンパク質に結合すると、活性化されてミリスチル基が露出する。
ミリストイル化されたタンパク質はその後さらに二重修飾を受ける
N-ミリスチル化タンパク質にさらに修飾を受ける。ミリストイル化とパルミトイル化は一般的に連結した修飾である。ミリストイル化だけでは、一過性の膜相互作用が起こり、タンパク質は膜に固定されるが、簡単に解離してしまう。パルミトイル化されると、膜にしっかりと固定され、必要に応じて膜からゆっくりと解離するようになる。この特異的な二重修飾はGタンパク質共役型受容体経路において重要であり、「二重脂肪アシル化スイッチ」と呼ばれる。
ミリストイル化の後には近傍の残基がリン酸化されることが多い。同じタンパク質にさらにリン酸化が起こるとミリスチル化されたタンパク質の膜に対する静電的親和性が低下し膜から解離したタンパク質が細胞質に移動してしまうことがある。
シグナル伝達とミリストイル化
ミリストイル化は膜へのターゲティングやシグナル伝達に重要な役割を果たしている。また,Gタンパク質を介したシグナル伝達では,αサブユニットのパルミトイル化、γサブユニットのプレニル化とミリストイル化が、Gタンパク質が受容体と相互作用できるようにGタンパク質を細胞膜の内側に繋ぎ止めることに関与している。
この記事の著者:仲田洋美医師
医籍登録番号 第371210号
日本内科学会 総合内科専門医 第7900号
日本臨床腫瘍学会 がん薬物療法専門医 第1000001号
臨床遺伝専門医制度委員会認定 臨床遺伝専門医 第755号






