目次
mGluR(Metabotropic glutamate receptor)とは
mGluR(メタボトロピックグルタミン酸受容体)は、神経伝達物質であるグルタミン酸に反応するGタンパク質共役受容体(GPCR)の一種です。これらの受容体は、イオンチャネルではなく、生化学的カスケードを活性化して他のタンパク質、例えばイオンチャネルの修飾を行い、シナプスの興奮性の変化を引き起こします[1]。
mGluRは、中枢および末梢神経系で多様な機能を果たしており、学習、記憶、不安、痛覚の知覚などに関与しています。これらは、海馬、小脳、大脳皮質などの脳の部位や、末梢組織において、プレシナプスおよびポストシナプスのニューロンに存在します[1]。
mGluRは8種類(mGluR1からmGluR8)が存在し、これらは構造と生理活性に基づいてI群、II群、III群の3つのグループに分類されます。各グループは異なるシグナル伝達経路を介して作用し、神経伝達物質の放出の抑制や細胞の興奮性の調節など、異なる生理的効果をもたらします[1]。
また、mGluRはホモダイマーまたはヘテロダイマーとして機能することが知られており、これらのダイマー形成は受容体の薬理学的および機能的特性に影響を与えます[2][4]。これらの受容体は、特定の脳疾患や神経障害の治療において潜在的な標的とされており、例えば、mGluR2/3のアゴニストは一般化不安障害の治療に有効であることが示されています[1]。
グルタミン酸と中枢神経
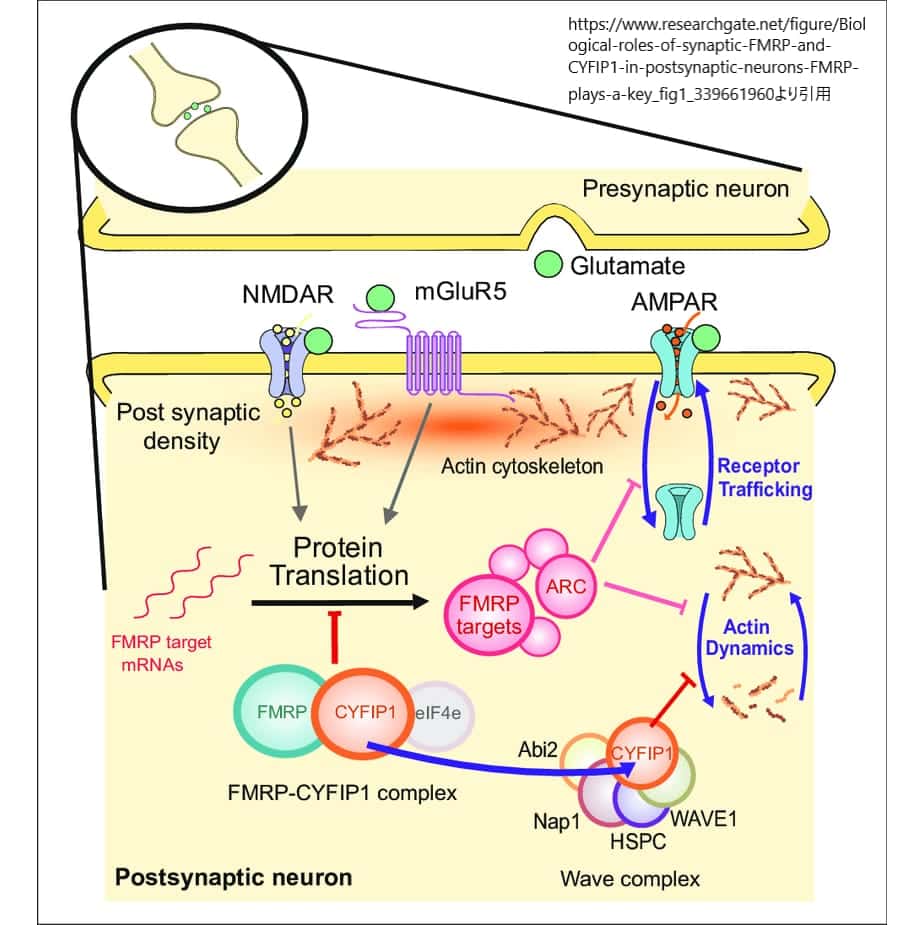
グルタミン酸は、哺乳類の中枢神経系で最も重要な興奮性の神経伝達物質の一つです。この物質は、記憶の形成、神経細胞の発達、そしてシナプスの可塑性といった脳の基本的な機能に必要不可欠です。しかし、グルタミン酸が過剰に放出されると、神経細胞が死に至ることもあります。
グルタミン酸受容体には大きく分けて、イオンチャンネル型と代謝型の2種類があります。代謝型グルタミン酸受容体(mGluR)は、8つのサブタイプと3つのグループに分類され、Gタンパク質に依存するか非依存するかによって細胞のシグナル伝達を活性化します。これにより、グルタミン酸の活動が細かく調整され、脳のシナプス可塑性に影響を与えます。
mGluRは神経発達障害や精神疾患、神経変性疾患による認知機能の低下といった問題の治療に役立つ可能性があることが研究で示されています。また、mGluRはシナプス前の神経伝達を調節することで、神経細胞の発火や神経伝達物質の放出を活動依存的に制御しています。これにより、脳内の情報の流れがスムーズに調整されるのです。
mglurの役割は何ですか?
mGluR(メタボトロピックグルタミン酸受容体)は、中枢神経系において重要な役割を果たしています。これらの受容体は、学習や記憶のプロセス、神経伝達の調節、シナプスの可塑性に関与しており、神経系の健康と機能に不可欠です[1][2][3][4][5][6][7][8]。
具体的には、mGluRは以下のような多様な機能を持っています:
1. 学習と記憶: mGluRは学習と記憶の形成に関与しています。これらの受容体は、シナプスの可塑性、つまり神経細胞間の接続の強度が経験に基づいて変化する能力に影響を与えることで、記憶の形成と保持を助けます[1][2][6]。
2. 神経伝達の調節: mGluRは神経伝達物質の放出を調節し、神経細胞の興奮性を制御します。これにより、神経系の全体的な活動バランスが保たれ、過剰な興奮や抑制が防がれます[1][2][7]。
3. シナプス前膜とシナプス後膜の調節: mGluRはシナプス前膜およびシナプス後膜に存在し、シナプス伝達の効率を調節することで、神経回路の微調整を行います[1][2]。
4. 精神疾患の治療標的: mGluRは統合失調症や不安障害、てんかんなどの精神疾患の治療標的としても研究されています。これらの受容体を標的とする薬物は、これらの疾患の症状を改善する可能性があります[6][7]。
これらの役割は、mGluRが神経系の健康と機能において中心的な役割を果たしていることを示しています。
- 参考文献・出典
-
[1] www.abcam.co.jp/content/glutamate-receptors-1
[2] www.abcam.co.jp/content/metabotropic-glutamate-receptors-1
[3] www.jstage.jst.go.jp/article/fpj/144/2/144_76/_pdf
[4] www.jstage.jst.go.jp/article/fpj/144/2/144_76/_article/-char/ja/
[5] ja.wikipedia.org/wiki/%E4%BB%A3%E8%AC%9D%E5%9E%8B%E3%82%B0%E3%83%AB%E3%82%BF%E3%83%9F%E3%83%B3%E9%85%B8%E5%8F%97%E5%AE%B9%E4%BD%93
[6] photo1.biophys.kyoto-u.ac.jp/shichida/interests/mglur_activation_jp.html
[7] www.nips.ac.jp/research/seminar/2005/06/post-61.html
mGluRの分子構造
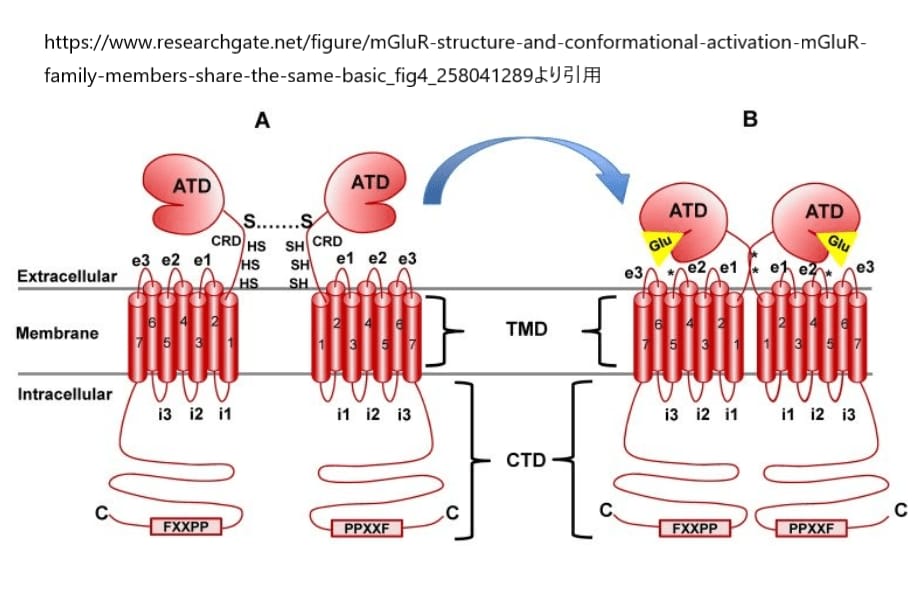
mGluR(代謝型グルタミン酸受容体)ファミリーは、その基本的な構造が共通しています。この構造は、N末端(N)から始まり、アミノ末端ドメイン(ATD)、システインリッチドメイン(CRD)、7つの膜貫通ドメイン(TMD)、そしてC末端ドメイン(CTD)が続きます。i1、i2などは膜貫通ドメイン間の細胞内ループを、e1、e2などは細胞外ループを指します。特に、ループe2にあるシステイン残基は、Gタンパク質複合体に活性化情報を伝達する際に重要な役割を果たします。
左側のパネルAは、mGluR1aの自然な休止状態の分子構造を示しており、CRDのシステイン残基がS-S結合を介して二量体化を助けることが描かれています。グルタミン酸が結合すると、右側のパネルBのように、CRDを含むATDの構造が変化し、結果として結合したGタンパク質が活性化されるのです。
mGluRにはどのような種類がありますか
mGluR(メタボトロピックグルタミン酸受容体)には、8種類の異なるタイプが存在し、これらは3つのグループに分類されます[1][2][3]。
1. グループ I:
– mGluR1 (GRM1)
– mGluR5 (GRM5)
– このグループの受容体は、主にナトリウムイオンとカリウムイオンの流れを増加させ、グルタミン酸の放出を減少させることで、主にシナプス後部で活動します。また、神経毒性プロセスである興奮毒性において中心的な役割を果たします。
2. グループ II:
– mGluR2 (GRM2)
– mGluR3 (GRM3)
– このグループの受容体は、主にシナプス前膜に位置し、アデニル酸シクラーゼ活性を阻害することで興奮性神経伝達を抑制します。これらは、海馬、皮質、側座核、線条体、扁桃体などに高レベルで発現しています。
3. グループ III:
– mGluR4 (GRM4)
– mGluR6 (GRM6)
– mGluR7 (GRM7)
– mGluR8 (GRM8)
– このグループの受容体も主にシナプス前膜に位置し、アデニル酸シクラーゼ活性を阻害することで興奮性神経伝達を抑制します。mGluR4とmGluR7は脳全体に、mGluR6は主に網膜に、mGluR8は主に低レベルで海馬、視床下部、嗅球などに発現しています。
これらの受容体は、シグナル伝達のメカニズムや機能によって異なる生理的および病理的プロセスに関与しています[1][2][3]。
mglurの種類ごとにどのような薬物が使用されるのですか?
mGluR(メタボトロピックグルタミン酸受容体)の種類ごとに使用される薬物は、それぞれの受容体の機能や関与する病態に基づいて異なります。以下に、いくつかのmGluRタイプとそれに関連する薬物の例を示します。
1. mGluR1:
– 拮抗薬: mGluR1拮抗薬は、非定型抗精神病薬であるクロザピンが拮抗作用を示す一方で、定型抗精神病薬であるハロペリドールは拮抗作用を示さないという特性があります[10][12]。
2. mGluR2/3:
– 作動薬: mGluR2への作用を模倣した薬物は、強力な抗精神病薬となる可能性があります[11]。
– 拮抗薬: グループII mGlu受容体拮抗薬は、抗うつ作用を示すことが動物モデルで確認されています[7][9]。
– アゴニスト: mGluR2アゴニストは、コカイン依存症の治療の可能性を開いています[13]。
3. mGluR5:
– 拮抗薬: mGluR5の働きをMPEPという薬剤で予めブロックすることにより、覚せい剤によるドーパミン放出異常を抑制する効果があります[4]。
4. mGluR6:
– 作動薬: mGluR6には特に高いアゴニスト選択性を持つ薬物があり、網膜における役割が研究されています[5]。
5. mGluR7:
– 拮抗薬: mGluR7拮抗薬は、抗うつ作用を示す可能性があります[7]。
6. mGluR8:
– 拮抗薬: mGluR8拮抗薬に関する具体的な情報は示されていませんが、グループIIIの受容体として興奮性神経伝達を抑制する役割があります[5]。
これらの薬物は、mGluRの機能を調節することで、統合失調症、うつ病、依存症、神経保護などの治療に応用される可能性があります。また、mGluRを標的とした治療薬の開発は、精神疾患や神経疾患の治療において新たなアプローチとなることが期待されています[8][9][10][11][12][13][14][15][16][17][18][19][20]。
- 参考文献・出典
-
[4] www.qst.go.jp/site/qms/1623.html
[5] www.abcam.co.jp/content/metabotropic-glutamate-receptors-1
[6] www.qst.go.jp/site/press/20230403.html
[7] www.jstage.jst.go.jp/article/jsbpjjpp/27/1/27_27/_article/-char/ja/
[8] www.jstage.jst.go.jp/article/fpj/144/2/144_76/_pdf
[9] www.jstage.jst.go.jp/article/jsbpjjpp/27/1/27_27/_pdf
[10] www.jstage.jst.go.jp/article/fpj/142/6/142_280/_pdf
[11] www.natureasia.com/ja-jp/nature/highlights/18247
[12] www.jstage.jst.go.jp/article/fpj/142/6/142_280/_article/-char/ja/








