目次
本記事では、細胞分裂における重要な構造であるキネトコアについて詳しく解説します。キネトコアの形成、その機能、セントロメアとの関係、および染色体の正確な分配を支える機構に焦点を当て、最新の研究成果も紹介します。ライフサイエンス分野における重要な発見とその影響について理解を深めましょう。
第1章: キネトコアとは
キネトコアの定義と基本構造
「キネトコア」という用語は英語の “kinetochore” から来ており、これはギリシャ語の「kinesis」(運動)と「choros」(場所)から派生しています。これはキネトコアが染色体の動きを調節する場所であることを反映しています。
キネトコアは、真核生物の細胞分裂時に染色体のセントロメアと呼ばれる領域に形成される重要なタンパク質構造です。この構造は、細胞分裂中に姉妹染色分体を引き離す役割を担っており、紡錘糸が結合する部位として機能します[5][7]。
● 基本構造と機能
キネトコアは、複数のタンパク質から成る複合体であり、その主な機能は染色体を細胞の両極に均等に分配することです。このプロセスは、細胞の遺伝情報が正確に新しい細胞に伝えられることを保証します。キネトコアの構造は、細胞分裂の有糸分裂および減数分裂の際に特に重要で、紡錘体の微小管ポリマーへ染色体を連結する役割を果たします[5][7]。
キネトコアのタンパク質は、姉妹染色分体をつなぎとめることにも関与し、染色体の正確な分配を助けるとともに、染色体の編集にも関与しています[5]。また、キネトコアはセントロメア上で組み立てられ、その形成と機能は細胞の遺伝的安定性にとって非常に重要です[6]。
● 研究と発見
最近の研究では、キネトコアの構造と機能についての新たな発見があり、これらの知見は染色体分配のメカニズムをより深く理解するのに寄与しています。例えば、キネトコアのタンパク質CENP-Cの多量体化がキネトコアの機能に重要であることが明らかにされています[3]。
このように、キネトコアは細胞分裂の正確な制御に不可欠な構造であり、その複雑な機能と構造は生物学的な研究の重要な対象となっています。

キネトコアは染色体DNAと紡錘体・微小管のポリマーとの間の相互作用を仲介する大きなタンパク質構造体です。これまでに100種類以上のキネトコアタンパク質が同定されています。キネトコアの構造基盤は、ヒストンH3の変異体であるCENP-Aを含む特殊なヌクレオソームによって形成されており、これは配列に依存しないエピジェネティックなメカニズムによってセントロメアに誘導されます。
キネトコアは微小管との接点を形成し、コアの付着部位の生成、キネトコアの動きと微小管の分解との結合、キネトコアに結合した微小管の重合動態への影響、そして紡錘状微小管に沿った移動の促進など、様々な機能を提供します。これにより、染色体の正確な分離が可能になります。
さらに、キネトコアの機能の忠実性とタイミングは、分裂期チェックポイントや複数の分裂期キナーゼなど、いくつかのシグナル伝達経路によって厳密に制御されています。この複雑な調節機構は、細胞分裂が正確に行われることを保証し、遺伝子の安定性を維持します。
セントロメアとの関連性とその役割
染色体の正確な分離には、DNAのユニットが染色体分離装置によって認識されるプロセスが必要です。セントロメアは、ほとんどの真核生物において各染色体の単一の領域に位置しており、これが機能しない場合、キネトコアはDNA上に適切に集まらず、結果として有糸分裂時に染色体が正しく分離されません。また、染色体の遠位部に複数の動原体が形成されると、紡錘体の力によって断片化が起こることがあります。セントロメアの正確な位置決めは、細胞の健康と遺伝情報の正確な伝達にとって極めて重要です。
セントロメアDNAの性質やサイズは、生物種によって大きく異なります。例えば、ヒトのセントロメアは、171bpのα-サテライトリピートが数千回から数万回繰り返されることによって構成されています。これらのリピート配列はセントロメアに関連してはいるものの、実際にはほとんどの生物ではセントロメアのDNA配列に固有の要件は存在しないことが知られています。
特に興味深いのは、脊椎動物におけるセントロメアの性質です。研究により、セントロメアがα-サテライト・リピートのない染色体領域に新しく形成された事例(ネオセントロメア)があり、これはセントロメアが塩基配列に依存しないことを示しています。また、α-サテライト配列が存在しても機能的なセントロメアとして機能しない場合もあり、これらのリピート配列はセントロメアの指定には必要でも十分でもないことが示されています。
脊椎動物のセントロメアが塩基配列に依存しないことは、エピジェネティックに定義されるセントロメアの概念を支持します。このプロセスにおいて重要なのは、ヒストンH3のバリアントであるCENP-Aで、これはセントロメアに特有の特殊なヌクレオソームを形成し、セントロメアの機能と位置を決定します。
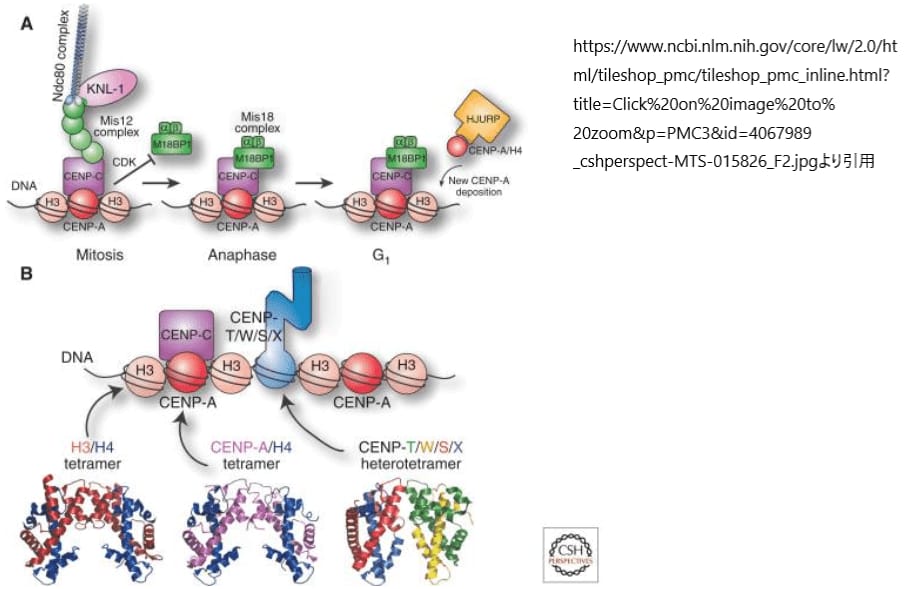
CENP-Aターゲティングドメイン(CATD)は、その独特な構造的特性により、ヌクレオソームが特殊な沈着因子によって認識される基盤となります。CENP-Aがセントロメアに限定されることを確実にするために、いくつかのメカニズムが連携して、CENP-Aヌクレオソームの適切な沈着を確保します。脊椎動物の細胞では、CENP-Aの沈着はG1期に行われ、これはサイクリン依存性キナーゼ(CDK)の活性による負の制御によって、ヒストンH3を含むヌクレオソームが沈着するS期には起こりません。この細胞周期による制限は、CENP-Aの沈着の時期を特定する重要な因子です。
Mis18α、Mis18β、M18BP1/KNL2からなるMis18複合体は、HJURPをセントロメアにリクルートします。HJURPは特殊なヒストンシャペロンであり、CENP-A/ヒストンH4二量体と結合して完全なヌクレオソームを組み立てます。CENP-Aヌクレオソームは、内側キネトコアタンパクであるCENP-Cと相互作用し、CENP-CはMis18複合体の取り込み装置のセントロメア受容体として機能します。この精密な相互作用により、CENP-Aの組み込みは高い忠実度で行われます。もしCENP-Aがセントロメア以外のクロマチンに誤って組み込まれた場合、これらのヌクレオソームはクロマチンから取り除かれ、分解の対象となります。これによって、各染色体上にCENP-Aでマークされた単一の部位が確実に存在し、動原体構造の組み立てを指示することになります。
CENP-A以外にも、セントロメアには特殊なDNA結合タンパク質が存在しており、その一例がCENP-T-W-S-X複合体です。この複合体は通常のヌクレオソームとは異なる配列を持ちますが、その構造はヌクレオソーム内のヒストンと類似しています。研究によれば、これらのタンパク質はヌクレオソーム様の構造を形成し、その表面にDNAを巻きつけることが示唆されています。CENP-T-W-S-X複合体の局在化はCENP-Aの下流で起こりますが、これらのヌクレオソーム様粒子の局在化を制御する因子はまだ完全には解明されていません。
これらのDNA結合タンパク質は、キネトコアが各染色体の特定の領域と安定した相互作用を形成することを可能にし、分離装置が各染色体を効果的に「認識」できるようにしています。特にCENP-Tは、DNAとの結合だけでなく、NDC80複合体とも直接相互作用します。この相互作用は、分裂期に核膜が破壊されると顕著になり、NDC80複合体が染色体にアクセスしやすくなり、キネトコアに集合することが可能になります。このプロセスは、細胞分裂時の染色体の正確な分離と配分を保証するために重要です。
キネトコアとセントロメアは、細胞分裂時の染色体の正確な分配に不可欠な構造であり、それぞれが独自の重要な役割を果たしています。
● セントロメアの役割
セントロメアは染色体の一部で、姉妹染色分体を結びつける役割を持ちます。この領域は、特に細胞分裂時に重要で、キネトコアの組み立ての場として機能します。セントロメアは、特定のDNA配列とそれに結合するタンパク質から構成されており、その構造は種によって異なることがあります。セントロメアDNAは、キネトコアタンパク質が結合する基盤を提供し、細胞分裂時に染色体が正しく分配されることを保証します[1][2][6].
● キネトコアの役割
キネトコアは、セントロメアに形成される複合タンパク質構造で、紡錘体微小管と染色体を結びつける役割を持ちます。この結合により、染色体は細胞分裂時に細胞の両極に引き寄せられ、均等に分配されます。キネトコアは、細胞分裂の各段階で微小管の結合状態を監視し、染色体が正確に分配されるまで細胞周期の進行を遅らせることができる重要な機能を持っています[1][2][4][6].
● 相互作用と調節
キネトコアとセントロメアの相互作用は、細胞分裂の正確性を保つために極めて重要です。セントロメアにはCENP-Aという特殊なヒストンが含まれており、これがキネトコアの組み立てを促進します。CENP-Aはキネトコアタンパク質の結合サイトとして機能し、キネトコアの構造と機能の基盤を形成します[1][2][6].
● 研究と応用
キネトコアとセントロメアの研究は、がんや遺伝病など、染色体分配異常に関連する疾患の理解と治療に寄与しています。不正確な染色体分配は細胞の異常増殖や死につながるため、これらの構造の詳細な研究は医学的にも重要です[1][2][6].
このように、キネトコアとセントロメアは細胞の生命活動において中心的な役割を担い、その複雑な相互作用と調節機構が細胞分裂の精度を保つために不可欠です。
- 参照・引用
-
[1] www.nature.com/scitable/topicpage/chromosome-segregation-in-mitosis-the-role-of-242/
[2] www.ncbi.nlm.nih.gov/pmc/articles/PMC3687001/
[3] academic.oup.com/femsre/article/38/2/185/497120
[4] www.cell.com/fulltext/S0092-8674%2803%2900115-6
[5] www.youtube.com/watch?v=5CM-KUywh84
[6] en.wikipedia.org/wiki/Centromere
第2章: キネトコアの分子メカニズム
キネトコア形成の分子構成要素
キネトコアの形成は、染色体上で特定されると、脊椎動物の細胞で構成される100種類以上のタンパク質による複雑な多タンパク質構造の構築へと移行します。これらのタンパク質はキネトコアごとに複数のコピーが存在し、その相対的な空間的局在と機能の違いに基づき、大きく3つの主要なカテゴリーに分類されます。
1. 内側キネトコアタンパク質は染色体DNAとの直接的な結合を形成し、キネトコアの基本的なプラットフォームを組み立てます。これにより、染色体の正確な動きと配置が可能になります。
2. 外側キネトコアタンパク質は、主に微小管との結合を担い、細胞分裂中に染色体を適切な位置に移動させるための物理的なつながりを提供します。
3. 制御タンパク質は、キネトコアの構造と機能を監視し、細胞周期に応じてその活動を調整・制御します。
これらのタンパク質間の完全な分子結合とその構造的な詳細を解明することは、高次のキネトコア構造の構築において重要な課題です。現在までのところ、この分野では多くの進歩がありましたが、DNAと微小管を物理的につなぐキネトコア内の全ての分子的相互作用を完全に理解するには至っていません。この解明は、細胞分裂の精密なメカニズムを理解するための鍵となり、将来的には遺伝病やがんなどの治療に対する新たなアプローチを提供する可能性があります。
キネトコアは、染色体の正確な分配を保証するために不可欠な細胞構造であり、細胞分裂時に染色体を紡錘体の微小管に接続する役割を果たします。この構造は、セントロメア領域に形成され、複数のタンパク質から成る複合体です。キネトコアの形成と機能には、特定のタンパク質が重要な役割を担っています。
● 主要な分子構成要素
1. CENP-T-W-S-X複合体
– CENP-T-W-S-Xは、キネトコアの形成に必要なタンパク質複合体であり、DNAとの結合部位がヒストンと類似しています。この複合体は、DNAに結合し、キネトコアの構造的基盤を形成するのに寄与します[1]。
2. CENP-C
– CENP-Cは、キネトコアの重要な構成要素であり、セントロメアのDNAに特異的に結合し、キネトコアの組み立てと機能の中心的な役割を果たします。特に、CENP-Cの多量体化はキネトコアの構造的整合性を保持するのに重要です[2]。
3. CENP-A
– CENP-Aはセントロメア特異的なヒストンH3のバリアントで、キネトコアの形成において中心的な役割を果たします。CENP-Aヌクレオソームは、キネトコアタンパク質が結合する基盤を提供し、セントロメアの構造と機能の核となります[4]。
4. ミクロチューブル
– キネトコアは、細胞の分裂装置である紡錘体の微小管と結合します。この結合は、染色体が細胞分裂中に姉妹染色体を均等に分配するために必要です[6]。
● 機能と相互作用
キネトコアのタンパク質は、複雑な相互作用を通じてキネトコア複合体を形成し、染色体のセントロメアに局在します。これらのタンパク質は、紡錘体微小管との物理的な接続を確立し、染色体の動きを調節して正確な染色体分配を促進します。CENP-CやCENP-Tなどのタンパク質は、キネトコアの構造的整合性と機能的活性を維持するために、特定の調節機構によって制御されます[2][4]。
これらの分子構成要素とその相互作用の詳細な理解は、細胞分裂のメカニズムを解明し、染色体分配異常に関連する疾患の治療法開発に寄与する可能性があります。
- 参照・引用
-
[1] user.spring8.or.jp/sp8info/?p=23551
[2] resou.osaka-u.ac.jp/ja/research/2023/20230609_1
[3] resou.osaka-u.ac.jp/ja/research/2018/20181113_1
[4] kaken.nii.ac.jp/ja/file/KAKENHI-PROJECT-18K06084/18K06084seika.pdf
[5] kaken.nii.ac.jp/ja/grant/KAKENHI-PROJECT-21K06048/
[6] ja.wikipedia.org/wiki/%E5%8B%95%E5%8E%9F%E4%BD%93
動原体との相互作用
キネトコアと動原体(キネトコア)は、細胞分裂時に染色体の正確な分配を保証するために重要な役割を果たします。キネトコアは、染色体のセントロメア上に形成される複合体であり、細胞分裂中に紡錘体微小管と結合して染色体を細胞の両極に引っ張る役割を担います[6][15]。
● キネトコアと動原体の基本機能
キネトコアは、細胞分裂時に染色体を正確に分配するための重要な構造です。この構造は、細胞のセントロメアに位置し、紡錘体微小管と結合して染色体を細胞の両極に引き寄せる役割を果たします[6][15]。キネトコアの形成と機能は、細胞の遺伝情報が正確に次世代に伝えられることを保証するために不可欠です。
● 相互作用の詳細
キネトコアの主要な機能は、紡錘体微小管との結合を通じて染色体の動きを制御することです。この結合は、染色体が細胞分裂中に均等に分配されることを確実にするために重要です。キネトコアは、複数のタンパク質から構成される複合体であり、これらのタンパク質は微小管との物理的な接続を提供し、染色体の移動を助けます[14][15]。
● 研究の進展
最近の研究では、キネトコアと動原体の相互作用に関する新たな知見が明らかにされています。例えば、キネトコアの構成要素であるCENP-Cタンパク質が、キネトコアの形成と機能において中心的な役割を果たしていることが分かっています[3][4]。また、キネトコアの動的な構造と微小管との相互作用が染色体の正確な分配を助けるメカニズムについても研究が進んでいます[14]。
● 社会への影響
キネトコアと動原体の相互作用の理解は、がんや遺伝病など、染色体分配異常に関連する疾患の治療法開発に寄与する可能性があります。正確な染色体分配メカニズムの解明は、これらの疾患の予防や治療に向けた新たなアプローチを提供することが期待されています[3][4]。
このように、キネトコアと動原体の相互作用は細胞分裂の基本的なプロセスにおいて中心的な役割を果たし、生命科学の多くの分野において重要な研究対象となっています。
- 参照・引用
-
[3] resou.osaka-u.ac.jp/ja/research/2023/20230609_1
[4] resou.osaka-u.ac.jp/ja/research/2019/20191031_2
[5] kaken.nii.ac.jp/ja/file/KAKENHI-PROJECT-18K06084/18K06084seika.pdf
[6] kotobank.jp/word/%E5%8B%95%E5%8E%9F%E4%BD%93-103485
[14] webview.isho.jp/journal/detail/abs/10.15105/J01677.2013167623
[15] ja.wikipedia.org/wiki/%E5%8B%95%E5%8E%9F%E4%BD%93
[16] www.nig.ac.jp/nig/pdf/research/lab_fukagawa.pdf
第3章: キネトコアの機能と重要性
染色体の正確な分配を如何にして実現するか
キネトコアは、細胞分裂時に染色体の正確な分配を保証するための重要な役割を果たします。この複雑なタンパク質構造は、細胞の遺伝情報が正確に娘細胞に伝えられることを確実にするため、染色体と紡錘体微小管との間の重要な接点として機能します。
● キネトコアの基本構造と機能
キネトコアは、染色体のセントロメア領域に位置し、多数のタンパク質から構成されています。この複合体は、紡錘体微小管が染色体を細胞の両極に引っ張る際の「つかみどころ」として機能します。キネトコアの主要な構成要素には、CENP-A、CENP-C、Ndc80複合体などがあり、これらは微小管との結合や、細胞周期におけるチェックポイントの調節に不可欠です[7][9][10][12][20].
● 染色体分配の精度を高めるメカニズム
キネトコアは、紡錘体微小管との正確な結合を通じて、染色体が細胞の中央に配置されるメタフェーズプレートに整列することを支援します。このプロセスは、姉妹染色体がそれぞれ反対側の極に引き寄せられる「バイオリエンテーション」と呼ばれます。キネトコアの機能不全は、染色体の不正確な分配、さらには異数体やがんの原因となる可能性があります[1][2][3].
● 紡錘体組立チェックポイント(SAC)
キネトコアは、紡錘体組立チェックポイント(SAC)の重要な部分としても機能します。これは、すべての染色体が適切に紡錘体微小管に結合するまで、細胞周期の進行を一時的に停止させる安全装置です。不適切な結合が存在すると、キネトコアはSACを活性化し、細胞分裂を遅らせることで、エラーの修正が可能になります[4][7][11].
● テンションセンシングとエラー修正
キネトコアは、微小管との結合において生じる力(テンション)を感知する能力も持っています。適切なテンションがかかると、安定した結合が促進され、エラーがある場合は修正メカニズムが働きます。このプロセスは、染色体が正確に分配されることを保証し、遺伝的安定性を維持するのに重要です[4][6][11].
● 研究と臨床への応用
キネトコアの研究は、がんや遺伝病の治療に向けた新たなアプローチを提供する可能性を持っています。例えば、キネトコアの異常が関与する疾患の治療に向けて、特定のキネトコアタンパク質を標的とした治療法の開発が進められています[5][8][14][15].
キネトコアの機能とその重要性を理解することは、細胞生物学だけでなく、医学研究においても極めて重要です。この複雑なタンパク質構造の詳細な解析は、生命科学の多くの分野における基礎的な知識の拡張に寄与しています。
- 参照・引用
-
[1] www.frontiersin.org/articles/10.3389/fcell.2023.1096333/full
[2] bmcbiol.biomedcentral.com/articles/10.1186/s12915-015-0172-y
[3] lumicks.com/kinetochore-mediated-chromosome-segregation-c-trap/
[4] www.mdpi.com/1422-0067/22/16/8818
[5] pubmed.ncbi.nlm.nih.gov/36755973/
[6] www.ncbi.nlm.nih.gov/pmc/articles/PMC3813865/
[7] en.wikipedia.org/wiki/Kinetochore
[8] study.com/academy/lesson/kinetochore-definition-structure.html
[9] byjus.com/neet/kintechore-structure-and-function/
[10] www.ncbi.nlm.nih.gov/pmc/articles/PMC5721348/
[11] rupress.org/jcb/article/200/5/557/37082/The-functions-and-consequences-of-force-at
[12] academic.oup.com/femsre/article/38/2/185/497120
[13] kaken.nii.ac.jp/ja/file/KAKENHI-PROJECT-18K06084/18K06084seika.pdf
[14] resou.osaka-u.ac.jp/ja/research/2018/20181113_1
[15] www.eurekalert.org/news-releases/567012?language=japanese
[16] www.healthcare.nikon.com/ja/ss/joicoaward/award/award15/
[17] resou.osaka-u.ac.jp/ja/research/2023/20230609_1
[18] kaken.nii.ac.jp/file/KAKENHI-PROJECT-20870004/20870004seika.pdf
[19] seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2022.940433/data/index.html
[20] www.kazusa.or.jp/news/re_info-2015-1111/
キネトコア障害が引き起こす細胞分裂異常
キネトコアは、細胞分裂時に染色体を正確に分配するために不可欠な構造であり、その障害は細胞分裂異常を引き起こし、さまざまな病態につながる可能性があります。キネトコアの機能不全は、染色体の不正確な分配、すなわち異数体の形成を引き起こすことが知られています。異数体は、正常な染色体数と異なる細胞が生じる状態で、これが発癌のリスクを高めることが示されています[2][17]。
● キネトコアの基本構造と機能
キネトコアは、染色体のセントロメア領域に形成される複合体で、紡錘体微小管と染色体を結びつける役割を果たします。この結合により、細胞分裂時に姉妹染色体が均等に分配されることが保証されます。キネトコアは、内キネトコアと外キネトコアの二つの主要な部分から構成されており、それぞれが異なるタンパク質サブユニットで構成されています。内キネトコアはセントロメアDNAに直接結合し、外キネトコアは紡錘体微小管に結合します[1][12]。
● キネトコア障害による細胞分裂異常
キネトコアの障害は、細胞分裂の精度に直接影響を及ぼします。例えば、キネトコアが正しく機能しない場合、紡錘体微小管が染色体に適切に結合できず、これが染色体の不均等な分配や遅延を引き起こす可能性があります。このような分裂異常は、細胞の異常増殖やアポトーシス抑制、さらには腫瘍形成につながる可能性があります[2][19]。
● キネトコア障害と疾患
キネトコアの障害は、特定の遺伝病やがんの発生に関連しています。例えば、キネトコアの異常は、モザイク変異性異数体症候群(MVA)などの疾患の原因となることがあります。この症候群は、細胞が異なる数の染色体を持つことによって特徴づけられ、発達遅延や先天異常を引き起こす可能性があります[2]。
● 研究と治療への応用
キネトコアの研究は、細胞分裂の基本的なメカニズムを理解する上で重要であり、特にがん治療において重要な意味を持ちます。キネトコア機能の抑制は、がん細胞の分裂を阻害する新たな治療戦略として考えられています。また、キネトコアの構造や機能に関する詳細な理解は、染色体分配異常に基づく疾患の診断や治療に役立つ可能性があります[1][2][17]。
このように、キネトコアの正確な機能は細胞の健康と直接関連しており、その障害は多くの病理学的状態に寄与する可能性があります。そのため、キネトコアの研究は医学研究の重要な分野であり続けます。
第4章: キネトコア研究の最新進展
新たな発見と技術の進化
# キネトコアの構造と機能の解明
キネトコアは染色体の正確な分配を担う重要な構造であり、その機能不全は染色体異常や疾患の原因となります。最近の研究では、キネトコアの分子構造と機能に関する新たな知見が明らかにされています。
● CENP-Cの多量体化とキネトコアの形成
大阪大学の研究グループは、キネトコアの形成に必要なタンパク質CENP-Cの多量体化メカニズムを解明しました。CENP-Cが自己集合して多量体を形成することが、キネトコアの構造形成に不可欠であることが示されました[1]。この発見は、染色体の正確な分配メカニズムの理解を深めるものであり、染色体異常に起因する疾患の治療法開発に寄与する可能性があります。
● キネトコアと紡錘体微小管の結合機構
2018年の研究では、キネトコアが紡錘体微小管と結合する際の新たな分子メカニズムが発見されました。特に、CENP-Tの制御がキネトコアの機能に重要であることが示され、これまでのCENP-C中心の理解を更新しました[2]。
# 技術の進化とその応用
● クライオ電子顕微鏡(クライオEM)の進展
キネトコアの研究において、クライオ電子顕微鏡技術が重要な役割を果たしています。この技術により、キネトコア複合体の高解像度構造が明らかにされ、その動的な機能を理解する上での新たな道が開かれました[1]。
● 人工キネトコアの構築
ゲノム工学的手法を用いて、人工的なキネトコア構造が構築され、その機能が自然のキネトコアと同等であることが確認されました[18]。この技術は、染色体工学や疾患モデルの開発に応用される可能性があります。
# 今後の展望
キネトコアの研究は、基礎生物学だけでなく、医学的な応用にも大きな影響を与える分野です。特に、キネトコアの異常が引き起こす疾患の治療法開発や、新たな抗がん剤の開発に向けた基盤が築かれつつあります。また、人工キネトコアの構築技術は、染色体操作技術としての応用が期待されています。
これらの進展は、染色体生物学の未来を形作る重要なステップであり、遺伝子の安定伝達と疾患治療の新たなアプローチを提供することでしょう。
キネトコア研究における未解決の問題点
キネトコアは染色体の正確な分配を担保するために不可欠な構造であり、その研究は遺伝学、細胞生物学、分子生物学の分野で重要な位置を占めています。最新の研究進展により、キネトコアの構造と機能に関する理解が深まっていますが、依然として解決すべき多くの問題点が存在します。
● キネトコアの分子構造の完全な解明
キネトコアは複数のタンパク質から構成される複雑な構造体であり、その詳細な分子構造の解明は進行中です。特に、キネトコアを形成するタンパク質間の相互作用や、その動的な変化を理解することが重要です。例えば、CENP-Aヌクレオソームの認識機構や、細胞周期に依存するキネトコアの構造変化についての詳細はまだ完全には解明されていません[15]。
● キネトコアの機能的多様性と調節機構
キネトコアの機能は、染色体の分配だけに留まらず、細胞周期のチェックポイント制御や紡錘体微小管との結合調節にも関与しています。これらの機能がどのように統合され、調節されるのかは、依然として活発に研究されているテーマです。特に、異なる細胞タイプや生物種でのキネトコアの機能的違いについての理解も進められています[19]。
● 疾患との関連
キネトコアの異常は染色体不安定性(CIN)を引き起こし、がんをはじめとする多くの疾患の原因となり得ます。キネトコアの異常がどのように疾患に寄与するのか、また、そのメカニズムの解明は、新たな治療法の開発につながる可能性があります。キネトコア機能の抑制や調節が疾患治療にどのように応用できるかについての研究が求められています[17]。
● 技術的課題
キネトコアの研究には高度なイメージング技術や分子生物学的手法が必要ですが、これらの技術のさらなる発展が研究の進展を加速させる鍵となります。特に、生細胞内でのキネトコアの動態をリアルタイムで観察する技術や、単一分子レベルでの解析技術の向上が期待されています[18][19]。
これらの未解決の問題点に対する研究は、キネトコアの完全な理解に向けて不可欠であり、将来的には遺伝病の診断や治療に貢献する可能性を秘めています。
- 参照・引用
-
[15] kaken.nii.ac.jp/ja/grant/KAKENHI-PROJECT-21K06048/
[16] www.nsc.nagoya-cu.ac.jp/~jnakayam/_src/sc733/pubj13.pdf
[17] seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2022.940433/data/index.html
[18] www.jstage.jst.go.jp/article/jpros/2/2/2_59/_pdf/-char/ja
[19] www.jhupo.org/data/proteomeletters/17202.pdf
第5章: キネトコアの臨床的応用と未来
がん治療におけるキネトコアの標的化
キネトコアは、細胞分裂の際に染色体を正確に分配するために不可欠な構造であり、がん細胞の増殖と関連していることが知られています。キネトコアと微小管の接続(KT-MT接続)の調節は、染色体不安定性(CIN)を引き起こし、がんの発生に寄与する可能性があります。このため、キネトコアはがん治療の新たな標的として注目されています。
研究によると、キネトコア関連タンパク質の過剰発現は、がん細胞の染色体不安定性を引き起こし、これががんの特徴であるとされています。例えば、キネトコアタンパク質BubR1のGLE2p結合配列ドメインや新たに発見されたBuGZは、グリオブラストーマ(GBM)の治療標的としての可能性があるとされています[1]。また、キネトコア遺伝子のミスエクスプレッションは、がん患者の生存率や放射線治療および化学療法への反応を予測する指標となり得ることが示されています[2][4][11]。
キネトコアタンパク質Hec1は、がん細胞で頻繁に過剰発現されており、Hec1のN末端にEGFPタグを付けた変異体の発現は、がん細胞の増殖を完全に阻害し、腫瘍の成長を強く抑制することが示されています[3]。このような研究結果は、キネトコアタンパク質を標的とすることで、がん細胞を死滅させる新たな治療戦略となり得ることを示唆しています。
さらに、キネトコアタンパク質の機能を標的とすることで、がん細胞の染色体不安定性を利用し、がん細胞のゲノムを不安定化させることができる可能性があります[13][20]。このアプローチは、がん細胞を選択的に死滅させるための新しい治療法の開発につながるかもしれません。
キネトコアの研究は、がん治療における新たな治療薬の開発に不可欠な基礎となっています。キネトコア関連タンパク質の機能や調節機構の理解を深めることで、がん細胞の増殖を阻害し、患者の生存率を向上させる可能性があります。現在、キネトコアを標的とした治療法の開発に向けた研究が進行中であり、将来的にはより効果的で副作用の少ないがん治療薬が登場することが期待されています。
- 参照・引用
-
[1] aacrjournals.org/clincancerres/article/21/2/233/244999/Molecular-Pathways-Regulation-and-Targeting-of
[2] www.eurekalert.org/news-releases/626145
[3] www.ncbi.nlm.nih.gov/pmc/articles/PMC4675780/
[4] www.nature.com/articles/ncomms12619
[11] www.ncbi.nlm.nih.gov/pmc/articles/PMC5013662/
[20] www.sciencedirect.com/science/article/pii/S193652332300089X
将来の研究方向と期待される成果
キネトコアは細胞分裂時に染色体を均等に分配するために不可欠な構造であり、その研究はがん治療、遺伝病の理解、および細胞生物学の基本的なメカニズムの解明に対して重要な意味を持っています。将来の研究方向としては、キネトコアの構造と機能のさらなる解明、異常なキネトコア機能による疾患の治療法の開発、およびキネトコアタンパク質の新たな臨床応用の探求が期待されています。
● キネトコアの構造と機能の解明
キネトコアの詳細な構造解析を進めることで、細胞分裂の制御におけるその役割をより深く理解することができます。特に、キネトコアタンパク質の相互作用や、紡錘体微小管との結合メカニズムの詳細な解析が重要です。これにより、染色体分配の精度を向上させる新しい戦略が開発される可能性があります[14]。
● 疾患治療への応用
キネトコアの機能不全は、がんや先天性疾患など多くの健康問題に直接関連しています。キネトコアの異常が引き起こす疾患メカニズムを解明することで、特定のキネトコアタンパク質を標的とした新しい治療薬の開発が進むことが期待されます。例えば、キネトコアの異常による染色体の不均等分配を正常化することで、がん細胞の増殖を抑制する治療法が考えられます[12][17]。
● 新たな臨床応用の探求
キネトコア研究は、細胞の生存と増殖に必要な基本的なプロセスを理解する上での突破口となり得ます。この知識を基に、細胞周期の制御を効果的に操作することで、組織再生医療や細胞ベースの治療法に応用する新たなアプローチが開発される可能性があります。また、キネトコア機能の人工的な調節により、特定の疾患状態における細胞分裂の制御が可能になるかもしれません[16][18].
これらの研究方向は、キネトコアの基本的な生物学的理解を深めるだけでなく、がんや遺伝疾患の治療に直接的な応用が期待されるため、生命科学および医学分野において重要な進展をもたらすことでしょう。
- 参照・引用
-
[12] www.eurekalert.org/news-releases/567012?language=japanese
[13] bsw3.naist.jp/research/index.php?id=2591
[14] www.nig.ac.jp/nig/ja/research/interviews/close-up-interviews/close-up-interviews12
[15] kaken.nii.ac.jp/ja/file/KAKENHI-AREA-3506/3506_kenkyu_seika_hokoku_ja.pdf
[16] www.jsps.go.jp/file/storage/grants/j-grantsinaid/37_topics/data/00020-14401-60321600.pdf
[17] seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2016.880748/data/index.pdf
[18] www.kri.or.jp/know/img/nw_pressrelease_20221014a.pdf
細胞分裂とキネトコア
真核生物の細胞分裂では、複製されたゲノムの分離が極めて重要です。このプロセスの中核を担うのがキネトコアで、この複雑なタンパク質複合体は、紡錘体微小管に中心染色体DNAを結合させる役割を持っています。これまでに80以上のキネトコア構成要素が同定され、これらがどのように高次のキネトコア構造に組織化され、適切な染色体分離を実現するかが明らかにされつつあります。
有糸分裂において、キネトコアは染色体DNAと紡錘体微小管ポリマーの両方に結合し、染色体の整列と分離を指示する重要な役割を果たします。この複雑なプロセスは、精密に調整された多段階の活動を必要とし、以下の主要なステップを含みます。
1. DNAの各ユニットを特異的に認識・検出する
真核生物の染色体分離では、セントロメアと呼ばれる特定のDNA領域が分離装置によって認識される必要があります。この領域はキネトコアの組み立ての起点となり、精密な染色体の動きを保証します。
2. DNAと他の細胞構造とを物理的に接続して分配を媒介する
キネトコアは、セントロメア上に形成されるタンパク質複合体で、DNAと細胞の構造体を物理的に結びつけます。これにより、染色体は紡錘体微小管に接続され、分裂時に正確に娘細胞に配分されるようになります。キネトコアは、100種類以上の異なるタンパク質成分が協調して機能することを必要とします。
3. DNAを娘細胞に空間的に移動させるための力を発生させる
紡錘体微小管は、染色体を分離する際に必要な力を提供します。これは主に微小管のポリマーの解重合によって生じ、キネトコアはこれらの微小管との相互作用を通じて、染色体を新しい細胞核に向けて動かすための力を発生させます。
この複雑で調整されたプロセスは、細胞分裂の正確性を保証し、遺伝的安定性を維持するために不可欠です。キネトコアと微小管の間の精密な相互作用は、生命の基本的なメカニズムの中で極めて重要な役割を担っています。
紡錘体微小管とキネトコアの結合
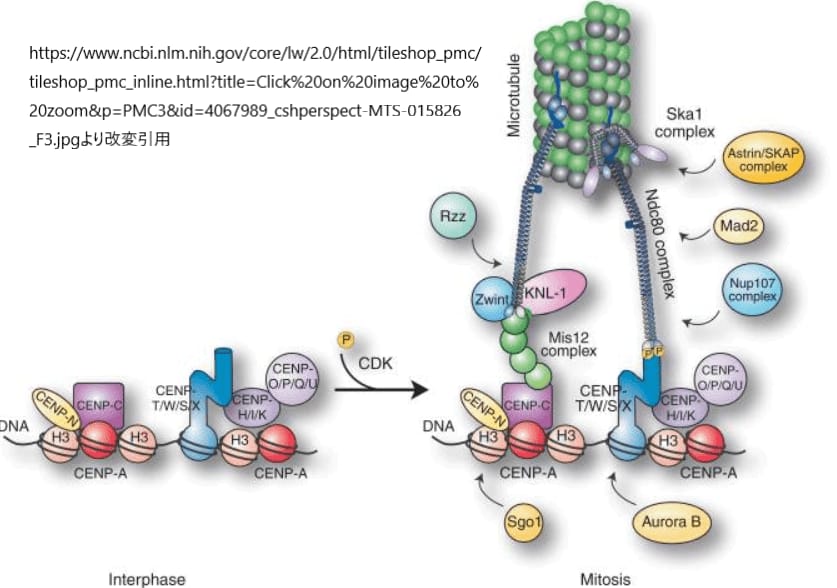
キネトコアタンパク質の中で、NDC80複合体は特に重要な役割を果たします。この4サブユニットからなる複合体は、キネトコアにおける微小管付着活動の中心として機能し、染色体の正確な移動と分離を支援します。NDC80複合体は、微小管との強固な相互作用を形成することで知られており、この相互作用は細胞分裂時に染色体を正確に娘細胞へと分配するために不可欠です。
しかし、微小管は静止した構造ではなく、その長さは重合と脱重合を繰り返すことで絶えず変化します。このダイナミックなプロセスに適応するため、キネトコアは微小管ポリマーが延長または収縮する際にも安定して結合し続ける必要があります。そのための重要な役割を担うのが、脊椎動物で見られるSka1複合体です。この複合体は、解重合する微小管の末端に結合し続けることで、キネトコアが紡錘体微小管との適切な接続を維持するのを助けます。
この相互作用により、細胞は細胞分裂中に染色体を正確に分離し、紡錘体微小管との安定した結合を維持しながら、必要に応じて微小管の長さの変動に対応することが可能になります。このように、NDC80複合体とSka1複合体の連携は、キネトコア機能の効率性と精度を高めるために重要な役割を果たしています。
染色体の移動
キネトコアと微小管の相互作用は、細胞分裂の各段階において非常に重要な役割を果たします。この相互作用は、単純な静的な結合ではなく、微小管のダイナミックな性質に適応して、絶えずその長さの変化に対応する必要があります。
1. メタフェーズ前半期
キネトコアは微小管ポリマーに捕らえられ、細胞の中央にあるメタフェーズプレートに向かって移動します。このプロセスは、染色体が紡錘体極に向かって整列することを確実にし、次の分裂に備えます。
2. メタフェーズ
この段階で、ペアになった姉妹染色分体が微小管によって対向する紡錘体極に付着します。この配置は、染色体が等しく娘細胞に分配されるための基礎を形成します。
3. アナフェイズA
アナフェイズの開始とともに、キネトコアは紡錘体に引き寄せられ、これによって染色体が中央から細胞の両極に向かって引き離されます。このプロセスは、遺伝物質が正確に2つの娘細胞に分配されることを保証します。
染色体の移動は、キネトコアが微小管ポリマーとの相互作用を通じて発生する力に依存しています。この力は微小管の解重合によって生じ、キネトコアによって効率的に利用されます。この複雑なダイナミクスは、染色体の正確な分離と細胞分裂の成功に不可欠であり、生物学的プロセスの精緻さを示しています。
キネトコアが微小管ポリマーに付着する方法
キネトコアが微小管ポリマーに付着する方法は2種類あります。
微小管の側面に結合
キネトコアは、細胞分裂の過程で重要な役割を果たす微小管ポリマーとの横方向の相互作用を形成します。この相互作用は、微小管の側面にキネトコアが結合することによって行われ、神経細胞の軸索微小管に沿った小胞輸送との類似性が指摘されています。当初は、このような横方向の相互作用を通じて、キネトコアの「貨物」を微小管ポリマーが提供するトラックに沿って移動させる微小管ベースの分子モーターが関与していると考えられていました。
実際に、プラス端指向のキネシンであるCENP-Eや、微小管マイナス端指向のモーターである細胞質ダイニンなど、複数の微小管ベースのモーターがキネトコアに局在しています。特にCENP-Eは、隣接する微小管ポリマーとの横方向の相互作用を利用して、紡錘体の極近くにある染色体を紡錘体の中央に運びます。CENP-Eが機能しない場合、少なくとも一部の染色体は紡錘体極周辺にとどまることが知られています。一方、ダイニンは、微小管繊維に沿った染色体の移動だけでなく、微小管の捕捉、キネトコアのシグナル伝達、紡錘体の構成にも関与しています。
さらに、DNAに結合するクロモキネシンも重要な役割を担い、横方向の相互作用を利用して染色体を極から遠ざける力を発揮し、メタフェースプレートへの染色体の合体に貢献します。これらの相互作用は細胞分裂の精密な制御と正確な遺伝物質の分配に不可欠であり、キネトコアの複雑な動態を理解する上で重要な要素です。
微小管とのエンドオン結合
キネトコアと微小管の横方向の相互作用は、初期段階でキネトコアが微小管を捕捉し、その後分子モータータンパクを用いて微小管のポリマーに沿って移動する能力を有します。しかし、微小管の持続的な重合と解重合によりその長さや形が絶えず変化するため、より強固な相互作用を確立するためにはエンドオンアタッチメントが必要です。このアタッチメントでは、微小管のプラス端がキネトコアに直接埋め込まれる形で結合します。
微小管ベースのモータータンパク質は、染色体の分離やキネトコア-微小管の相互作用の制御には重要ですが、染色体の物理的な移動や分配には直接的には必要ではないとされています。代わりに、キネトコアが微小管とエンドオンで結合することにより、微小管ポリマー自体が染色体を動かすモーターとして機能すると考えられています。このプロセスでは、染色体の移動が主に微小管の重合と解重合によって行われます。
対になった姉妹染色体のキネトコアと、反対側の紡錘体極から伸びた微小管とがエンドオンで結合すると、染色体の移動は微小管のダイナミクスに大きく依存します。この複雑な相互作用を維持するためには、キネトコアの微小管結合タンパク質が微小管の動的な性質に対応し、継続的に結合を保ちながら、その解重合によって生じる力を利用して染色体の動きを誘導することが必須です。これにより、細胞分裂中に染色体が正確に分配され、遺伝的な情報が均等に娘細胞に伝えられることが保証されます。この複雑なメカニズムの理解は、細胞生物学および遺伝学の重要な分野を形成し、さらなる研究が期待されています。
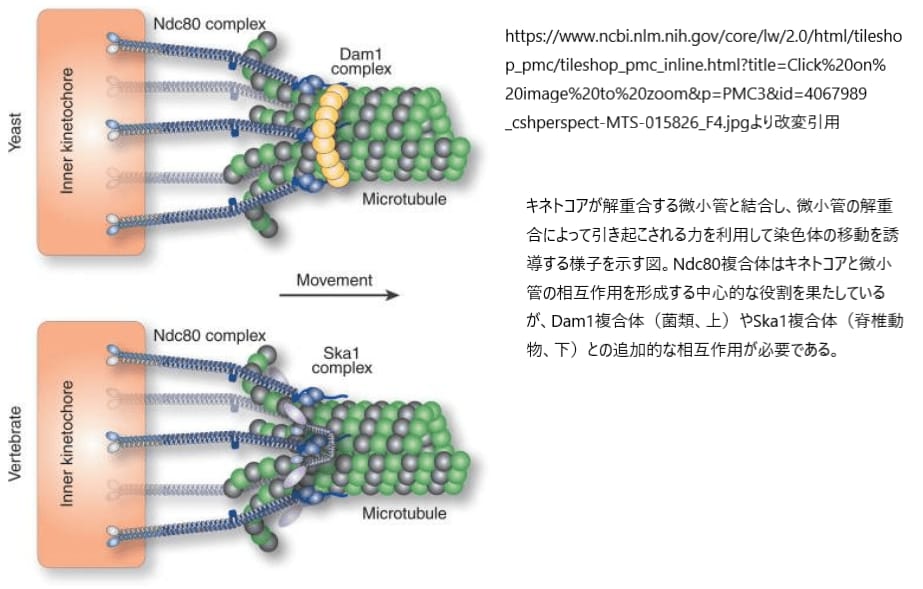
微小管のダイナミクスは細胞分裂中の染色体の動きを大きく左右するため、キネトコアがこれを適切に制御することが非常に重要です。キネトコアには微小管の重合状態に直接影響を与えるタンパク質が存在し、これらのタンパク質は、微小管の重合や解重合を調節し、細胞分裂中の染色体の正確な配列と分離を実現します。
キネトコアの機能には、微小管の成長を促進するタンパク質や、解重合を促進するタンパク質などが含まれます。例えば、Aurora Bキナーゼなどのタンパク質は微小管の安定性を調節し、キネトコアと微小管の相互作用の強度を変更することができます。このような調節は、微小管が染色体を引っ張る力を適切に調整し、細胞分裂時に染色体が均等に分配されることを保証します。
さらに、キネトコアは、微小管から発生する力を利用して、染色体の移動を効果的に指揮する役割も果たします。これには、微小管の動的な性質に応じてキネトコアが適応的に反応し、必要に応じて微小管との結合を強化したり緩めたりする能力が含まれます。この複雑な調節メカニズムにより、キネトコアは微小管から発生する力を最大限に利用し、染色体の精密な配列と分離を実現することが可能になります。
このように、キネトコアと微小管の相互作用は単なる物理的な結びつきを超えた、高度に調整されたプロセスであり、細胞分裂の成功に不可欠な役割を担っています。
- キネシン13ファミリー
- Kif2c/MCAK、微小管のカタストロフィー(脱重合への切り替え)を促進。
- キネシン8ファミリー
- Kif18a、脱重合酵素として作用。
- チューブリン重合促進因子
- CLASP(Clasp1およびClasp2)やTOGドメイン含有タンパク質(ヒトではch-TOG)などの一連の重合促進因子は、チューブリン二量体を微小管プラス端に送り込んで重合を促進する。
キネトコアの調節と細胞周期
キネトコアの精密な調節は、細胞分裂時の染色体分離の忠実性を保証するために必須です。有糸分裂におけるわずかな欠陥でも細胞にとって致命的な結果、すなわち染色体の数が不正確になるという事態を招きます。このため、キネトコアは染色体を単に動かすだけではなく、染色体の分離が高い精度で行われるよう監視し、必要に応じて修正も行う役割を担っています。
キネトコアと姉妹染色体の間に結合エラーが発生した場合、細胞は問題を感知し、それを修正するためのメカニズムを持っています。このプロセスは「スピンドルアセンブリチェックポイント」として知られており、キネトコアの機能が厳密に制御され、キネトコアと微小管の結合が適切に形成されることを保証します。このチェックポイントは、エラーが修正されるまで、細胞がアナフェイズへ進行することを遅らせることによって、染色体の不正確な分配を防ぎます。
このシステムにより、細胞は染色体の完全なセットが次世代の細胞に正確に伝えられるようにし、遺伝的安定性を維持します。キネトコアの調節が不十分だと、無秩序な細胞分裂が進行し、がんなどの疾患のリスクが高まるため、この精緻な調節機構は生物学的にも医学的にも極めて重要です。
キネトコアと微小管の結合の制御
キネトコアの機能は、細胞分裂の正確さを保証するために、一連のプロテインキナーゼによって厳密に制御されています。これらのキナーゼは、キネトコアの構造と活動を調整し、特にキネトコアと微小管の正確な結合を確保するために重要な役割を果たします。
主要なプロテインキナーゼの一つであるオーロラBは、キネトコアと微小管の結合を監視し、不適切な結合がある場合にはそれを修正するための信号を送ります。これによって、染色体が正しく分離されることを確実にし、染色体不安定性を防ぎます。Plk1(ポロライクキナーゼ1)もまた、キネトコアの結合状態とスピンドルアセンブリの調整に重要な役割を果たし、特に細胞分裂の進行において中心的な役割を担います。
Mps1はキネトコアの組み立てとスピンドルアセンブリチェックポイントの活性化に必須であり、キネトコアが正しく組み立てられているかを監視し、エラーがある場合には細胞周期の進行を停止させます。Bub1はキネトコアの構造的完整性を保ちながら、姉妹染色体の適切な分離を支援することで、遺伝的安定性を維持するのに役立ちます。
CDK(サイクリン依存性キナーゼ)は、細胞周期の異なる段階においてキネトコアの機能とアセンブリ状態を調整します。CDKによるリン酸化は、細胞周期の特定の時点でキネトコアの活性を変化させ、その結果、細胞分裂の様々な段階で適切な応答が可能になります。
これらのキナーゼはそれぞれ、キネトコアに局在し、リン酸化によってキネトコアの基質を修正します。これにより、キネトコアの機能が適切に調整され、細胞分裂時に染色体の正確な分離が保証されるのです。この精密な制御システムは、細胞の生存と遺伝的安定性にとって不可欠なものであり、適切な機能不全はさまざまな疾患、特にがんの発生に繋がる可能性があります。
オーロラBキナーゼ
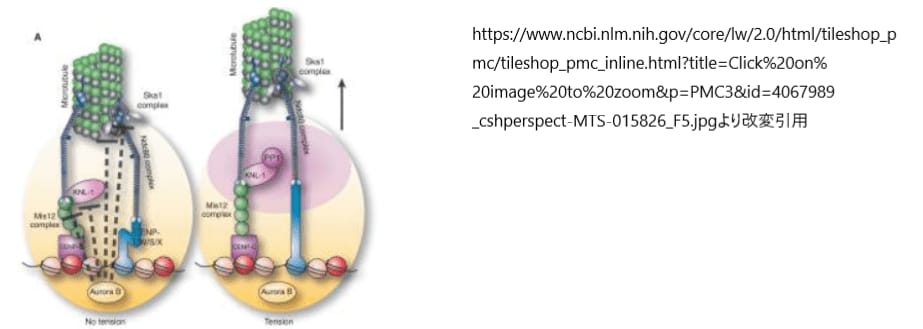
キネトコアの機能とその正確な微小管付着を制御するために、不適切な付着を解消するオーロラBキナーゼの活動は不可欠です。このキナーゼは、セントロメア内側、すなわちキネトコアの基部に位置し、外側キネトコアにある基質とは空間的に分離されています。キネトコアに双方向の張力がかかると、オーロラBは外側のキネトコアタンパク質をリン酸化し、これによって微小管との結合能力が低下します。このリン酸化は、NDC80複合体やSka1複合体など、キネトコアと微小管の境界面にある複数の構成要素の活性を直接阻害します。このように、オーロラBのリン酸化による複合的な効果がキネトコアと微小管の誤った結合を解消し、キネトコアを未結合の基底状態にリセットし、新たな正しい結合が形成されるように促します。
リン酸化はキネトコアのアセンブリを促進し、不適切な微小管の相互作用を防ぐ重要な役割を果たしますが、その機能が完了した後は、速やかに除去される必要があります。この逆転プロセスは、脱リン酸化酵素であるPP1(protein phosphatase 1)とPP2A(protein phosphatase 2)によって行われます。これらの酵素はキネトコアに局在し、リン酸化酵素標的化因子が適切なタイミングでキネトコア基質のリン酸化を解除できるようにします。この精緻な調整によって、キネトコアはその機能を適切に行い、細胞分裂中の染色体の正確な分配を保証するのです。
このように、リン酸化と脱リン酸化のダイナミックなバランスは、細胞分裂の調整と染色体の適切な分離に極めて重要であり、生物学的プロセスの正確性を保持するために不可欠です。








