目次
CCC複合体(Cullin-RING ligase complex)とは
CCC複合体(Cullin-RING ligase complex)は、タンパク質のユビキチン化とプロテアソームによる分解を担う重要な生物学的機構の一部です。この複合体は、タンパク質の選択的な分解を通じて細胞内のタンパク質の恒常性を維持し、多くの細胞プロセスを調節しています。
CCC複合体は、カリン(Cullin)、セレブロン(Cereblon、CRBN)、およびRINGボックスタンパク質(Rbx)から構成されます。カリンは、複合体の骨格を形成し、他のサブユニットを結合する役割を果たします。セレブロンは、タンパク質のユビキチン化において基質認識サブユニットとして機能し、特定のタンパク質を選択的に認識してユビキチン化の標的とします。RINGボックスタンパク質は、ユビキチンをタンパク質に転移させる酵素活性を持つ部分です。
CCCという名称は、おそらくCullin3型リガーゼ複合体の略称として用いられている可能性があります。
セレブロン(CRBN)は、特に注目されているタンパク質で、サリドマイドおよびその類似体であるイミド(IMiDs)の作用標的として知られています。サリドマイドは、かつて催奇形性が問題となった薬剤ですが、その後、多発性骨髄腫などの治療薬として再評価されました。サリドマイド類似体は、セレブロンに結合することで、特定のタンパク質のユビキチン化と分解を誘導し、抗腫瘍効果を発揮します[5][6][10]。
また、セレブロンは、タンパク質分解やユビキチン–プロテアソームシステムの文脈で重要な役割を果たしています。セレブロンは、ユビキチンリガーゼの一部として機能し、タンパク質の選択的な分解を促進することで、細胞のシグナル伝達や細胞周期制御などに関与しています[9][12]。
遺伝子の観点から見ると、CCC複合体に関連する遺伝子は、タンパク質のユビキチン化と分解に関与する遺伝子群の一部であり、これらの遺伝子の変異や異常は、がんをはじめとする多くの疾患の発症に関連している可能性があります[6][11][15]。
このように、CCC複合体は、遺伝子からタンパク質への情報の流れを制御し、細胞の機能と運命を決定する上で中心的な役割を担っています。
[5] www.ubiquitin.jp/images/common/chemo_ubiquitin_vol1.pdf
[6] seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2017.890525/data/index.html
[10] showa-u-rheum.com/2022/04/4268/
[11] www.jstage.jst.go.jp/article/nogeikagaku1924/65/3/65_3_699/_pdf/-char/ja
[12] patents.google.com/patent/JP2020506922A/en
[15] kaken.nii.ac.jp/ja/file/KAKENHI-PROJECT-20K21583/20K21583seika.pdf
CCC複合体(Cullin-RING ligase complex)の構造
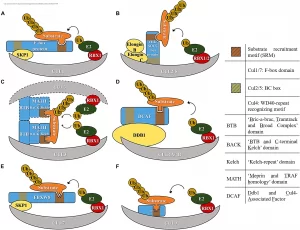
上図の説明:図1. CullinファミリーのE3ユビキチンリガーゼ複合体を表す図。(A)Cul1ベースのE3リガーゼ。(B)Cul2/5ベースのE3リガーゼ。(C)Cul3ベースのE3リガーゼ。(D)Cul4ベースのE3リガーゼ。(E)Cul7ベースのE3リガーゼ。(F)Cul9ベースのE3リガーゼ。
Cullin-RING ligase complex(CRL)は、E3ユビキチンリガーゼの大きなファミリーであり、タンパク質のユビキチン化とその後のプロテアソームによる分解を媒介する重要な役割を果たしています。CRLは、Cullin(Cul)と呼ばれるスキャフォールドタンパク質、RINGボックスタンパク質(Rbx1またはRbx2)、アダプタータンパク質、および基質認識サブユニット(SR)から構成されています[1][2][3][4]。
● Cullinスキャフォールド
CullinはCRLの中心的なスキャフォールドタンパク質であり、CRLのアーキテクチャーを形成します。Cullinタンパク質は、N末端ドメイン(NTD)とC末端ドメイン(CTD)の2つの主要なドメインから構成されています。NTDはアダプタータンパク質と結合し、CTDはRINGボックスタンパク質と結合します[3][4]。
● RINGボックスタンパク質
RINGボックスタンパク質(Rbx1またはRbx2)は、ユビキチン結合酵素(E2)と相互作用し、ユビキチンの転移を促進します。RINGドメインは2つの亜鉛イオンを結合し、その構造を安定化させます[3][4]。
● アダプタータンパク質
アダプタータンパク質は、CullinのN末端に結合し、基質認識サブユニット(SR)への結合を仲介します。例えば、Cul1ベースのE3リガーゼでは、Skp1がアダプタータンパク質として機能し、F-boxタンパク質と結合します[2][3]。
● 基質認識サブユニット(SR)
SRは、特定の基質タンパク質を認識し、CRLに結合させる役割を持ちます。SRは多様なタンパク質-タンパク質相互作用ドメインを持ち、特定の基質のデグロンと呼ばれる配列を認識します[4]。
● Neddylation
Cullinタンパク質は、NEDD8というユビキチン様タンパク質によって修飾されることがあります。この修飾は、CRLの活性化に関与しており、CullinのC末端リジン残基にNEDD8が共有結合的に結合します[1][3]。
● CRLの構造的特徴
CRLはアーチまたはバナナ形のアーキテクチャーを持ち、Cullinが中心に位置し、その両端にアダプタータンパク質とSR、およびRINGボックスタンパク質が配置されます。CullinのNTDはヘリックスバンドルから構成され、CTDは4ヘリックスバンドル、α/βドメイン、および2つのウィングドヘリックスドメインを含みます。これらのドメインは、Rbx1とのV字型の結合ポケットを形成します[3]。
● CRLの多様性
CRLは、異なるCullinタンパク質(Cul1からCul5、および非典型的なCullinであるAPC2、PARC、Cul7)と、様々なアダプタータンパク質およびSRを組み合わせることで、多様なE3リガーゼを形成します。これにより、CRLは細胞内で広範な基質特異性を持ち、多くの生物学的プロセスを調節することができます[1][2][4]。
[1] en.wikipedia.org/wiki/Cullin
[2] www.frontiersin.org/journals/physiology/articles/10.3389/fphys.2019.01144/full
[3] www.ncbi.nlm.nih.gov/pmc/articles/PMC7205596/
[4] www.ncbi.nlm.nih.gov/pmc/articles/PMC3070871/
CCC複合体(Cullin-RING ligase complex)の機能
CCC複合体(Cullin-RING ligase complex)は、細胞内でタンパク質のユビキチン化とその後のプロテアソームによる分解を担う重要な役割を果たしています。この複合体は、Cullin(カリン)と呼ばれる骨格タンパク質、RING指蛋白質(RING protein)、そして様々な基質認識サブユニットから構成されています。Cullin-RING E3ユビキチンリガーゼ(CRL)は、細胞内のタンパク質恒常性の維持、細胞周期の制御、シグナル伝達の調節、DNA損傷応答など、多岐にわたる生物学的プロセスに関与しています。
CRLの活性化は、Cullinタンパク質のNEDD8という小さなユビキチン様タンパク質による修飾(neddylation)によって行われます。NEDD8の共有結合的な付加は、CRLの構造的な変化を引き起こし、E2ユビキチン結合酵素との相互作用を促進し、結果として基質タンパク質へのユビキチンの転移効率を高めます。一方、COP9シグナルソーム(CSN)によるneddylationの逆反応(deneddylation)は、CRLの活性を抑制します。
CRL複合体は、その構成要素の多様性により、非常に多くの基質タンパク質を認識し、ユビキチン化することができます。例えば、CRL1(またはSCF複合体)は、Skp1、Cullin1(CUL1)、F-boxタンパク質、およびRING指蛋白質Rbx1から構成され、細胞周期の進行に関与するサイクリンやCDK阻害因子など、多くの基質を認識します。他のCRL複合体も、異なるCullinタンパク質(CUL2、CUL3、CUL4A/B、CUL5など)と特異的な基質認識サブユニットを用いて、特定の基質タンパク質を標的とします。
CRL複合体の機能不全は、がん、神経変性疾患、感染症など、多くの疾患の発症に関連しています。例えば、特定のCullinタンパク質の過剰発現や、基質認識サブユニットの変異は、不適切なタンパク質の蓄積や細胞の異常な増殖を引き起こす可能性があります。このため、CRL複合体は、新たな治療標的として注目されています。
総じて、CCC複合体は、細胞内のタンパク質の選択的なユビキチン化と分解を通じて、細胞の機能と恒常性の維持に不可欠な役割を果たしています。
CCC複合体(Cullin-RING ligase complex)の機能不全
CCC複合体(Cullin-RING ligase complex)は、細胞内でタンパク質の分解を担う重要な役割を果たしています。この複合体は、ユビキチン-プロテアソームシステムの一部として機能し、特定のタンパク質にユビキチンタグを付加することで、それらのタンパク質をプロテアソームによる分解へと導きます。CCC複合体の機能不全は、タンパク質の適切なターンオーバーが妨げられることにより、細胞の正常な機能に影響を及ぼす可能性があります。
CCC複合体の機能不全は、細胞のシグナル伝達経路の誤調節、細胞周期の異常、アポトーシスの障害など、さまざまな細胞機能の障害を引き起こすことが知られています。これらの障害は、がんをはじめとする多くの疾患の発症に関与していると考えられています。例えば、CCC複合体の一部であるCullinタンパク質の変異や発現の異常は、がん細胞の増殖や生存に影響を与えることが示されています。
また、CCC複合体は、細胞ストレス応答や免疫応答にも関与しており、その機能不全は自己免疫疾患や炎症性疾患の発症にも関連している可能性があります。さらに、神経変性疾患においても、CCC複合体の機能不全が神経細胞の損傷や死につながるメカニズムとして注目されています。
CCC複合体の機能不全による疾患の治療には、ユビキチン-プロテアソームシステムの調節を目的とした薬剤の開発が進められています。これらの薬剤は、CCC複合体の機能を正常化することで、疾患の進行を抑制または逆転させることを目指しています。
CCC複合体(Cullin-RING ligase complex)をターゲットとした研究開発
CCC複合体(Cullin-RING ligase complex)は、タンパク質のユビキチン化を担うE3ユビキチンリガーゼの一種であり、がん治療、薬剤耐性、疾患メカニズムの研究において重要なターゲットとなっています。これらの複合体は、Cullin(Cul)を中心とした構造を持ち、様々なサブユニットの組み合わせによって多様な基質を認識し、ユビキチン化することができます[1][2]。
● Cullin-RING Ligase Complexの構造と機能
Cullin-RING ligase complexは、Cullinを骨格とし、Rbx1やRbx2といったRING-Boxタンパク質、アダプタータンパク質、基質認識サブユニットから構成されます。CullinのC末端はRING-Boxタンパク質を結合し、E2ユビキチン結合酵素との相互作用を可能にします。一方、N末端はアダプタータンパク質を介して基質認識サブユニットに結合し、特定の基質タンパク質を認識します[4]。
● がん治療におけるCCC複合体の役割
がん治療においては、CCC複合体がタンパク質のユビキチン化と分解を通じて、細胞周期の調節、シグナル伝達、転写制御などの重要な生物学的プロセスに関与しています。例えば、Cullin3型リガーゼ複合体は、BTBドメインを持つタンパク質を介して基質を認識し、がん関連タンパク質の分解を促進することが知られています[2]。また、Cullin4を含むE3ユビキチンリガーゼ複合体は、Bcl-2タンパク質の分解を促進することで、癌処置に寄与する可能性があります[3]。
● 疾患メカニズムの解明
CCC複合体は、疾患のメカニズムを解明するための研究にも利用されています。例えば、Cullin3 E3リガーゼ複合体は、Nrf2という抗酸化応答に関与する転写因子と結合し、神経保護効果に関する研究において重要な役割を果たしています[9]。
● 薬剤耐性の研究
薬剤耐性に関する研究では、CCC複合体が特定の薬剤に対する耐性の発達に関与している可能性があります。例えば、抗CD33抗体やその複合体が、薬剤耐性の研究において重要なターゲットとなっています[10]。
● 研究開発の方向性
CCC複合体をターゲットとした研究開発は、新しいがん治療薬の開発、疾患のメカニズム解明、薬剤耐性の克服といった分野で進められています。これらの複合体の構造と機能の詳細な解析を通じて、特定の疾患に関連するタンパク質のユビキチン化と分解を調節する新しい治療戦略が開発されることが期待されます。また、CCC複合体の異常が疾患の原因となる場合、これらの複合体の活性を調節することで、疾患の進行を抑制または逆転させる可能性があります。
[1] www.yodosha.co.jp/jikkenigaku/keyword/2465.html
[2] www.yodosha.co.jp/jikkenigaku/keyword/1857.html
[3] patents.google.com/patent/JP2021511342A/ja
[4] www.frontiersin.org/journals/physiology/articles/10.3389/fphys.2019.01144/full
[9] naist.repo.nii.ac.jp/record/11592/files/R009358.pdf
[10] ipforce.jp/patent-jp-A-2021-19599
CCC complexに属する遺伝子
CCDC22
CCDC93
COMMD1
COMMD3
COMMD4
COMMD6
COMMD7
COMMD8
COMMD9
COMMD10