目次
カルシウム電位依存型チャネルα1サブユニットとは
カルシウム電位依存型チャネルα1サブユニットは、電位依存性カルシウムチャネル(Voltage-dependent calcium channels, VDCC)の主要な構成要素であり、チャネルの孔(ポア)を形成し、細胞外から細胞内へのカルシウムイオン(Ca2+)の流入を仲介します。このサブユニットは、チャネルの主たる生物物理学的および薬理学的特性を決定し、細胞の電気的興奮をCa2+依存的な生理応答に変換する役割を担います[5]。
電位依存性カルシウムチャネルは、膜電位の脱分極によって開口し、細胞外から細胞内へCa2+を選択的に透過させるイオンチャネルです。これらのチャネルは、神経細胞や筋細胞を始めとする興奮性細胞において、神経伝達物質放出、筋収縮、遺伝子発現など様々なCa2+依存性の細胞応答を制御する重要な役割を果たします[3]。
α1サブユニットには10種類のアイソフォームが存在し、これらは高電位活性化型と低電位活性化型の2つの大きなグループに分類されます。高電位活性化型にはL型を構成する4種類のCaV1(CaV1.1-CaV1.4)、P/Q、N及びR型を構成する3種類のCaV2(CaV2.1-CaV2.3)、低電位活性化型にはT型を構成する3種類のCaV3(CaV3.1-CaV3.3)が含まれます[4]。
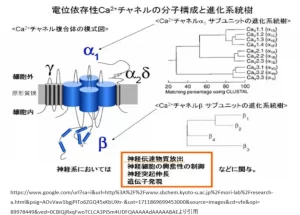
α1サブユニットは、約2,000アミノ酸残基からなる膜タンパク質で、6回膜貫通領域(S1-S6)の構造単位が4回繰り返す構造を有しています。各構造単位のS5とS6領域がCa2+を選択的に透過させるポア領域を形成し、S1-S4領域は電位センサー領域を形成します[4]。
このように、カルシウム電位依存型チャネルα1サブユニットは、細胞の生理的機能において中心的な役割を果たす重要なタンパク質であり、その構造と機能の理解は、神経伝達や筋収縮などの生命現象を解明する上で不可欠です。
[3] bsd.neuroinf.jp/wiki/%E9%9B%BB%E4%BD%8D%E4%BE%9D%E5%AD%98%E6%80%A7%E3%82%AB%E3%83%AB%E3%82%B7%E3%82%A6%E3%83%A0%E3%83%81%E3%83%A3%E3%83%8D%E3%83%AB
[4] www.sbchem.kyoto-u.ac.jp/mori-lab/research-a.html
[5] webview.isho.jp/journal/detail/abs/10.11477/mf.2425101029
カルシウム電位依存型チャネルα1サブユニットの構造
電位依存性カルシウムチャネルのα1サブユニットは、細胞の電気的興奮をカルシウム依存的な生理応答に変換する役割を担っています。このサブユニットは、細胞外から細胞内へカルシウムイオン(Ca2+)を選択的に透過させるイオンチャネルの主要な構成要素です。α1サブユニットの構造と機能に関する研究は、神経伝達物質の放出、筋収縮、遺伝子発現など、多様な生理的プロセスの理解に不可欠です。
● 構造
α1サブユニットは、約2,000アミノ酸残基からなる大きな膜タンパク質で、6回膜貫通領域(S1-S6)を持つ構造単位が4回繰り返される構造を有しています。各構造単位のS5とS6領域がカルシウムイオンを選択的に透過させるポア領域を形成し、S1-S4領域は電位センサー領域を形成します。この構造により、α1サブユニットは細胞膜の電位変化に応じてイオン透過孔の開閉を調節し、カルシウムイオンの細胞内への流入を制御します[5]。
● 分類
α1サブユニットには10種類のアイソフォームが存在し、これらは高電位活性化型と低電位活性化型の2つの大きなグループに分類されます。高電位活性化型にはL型を構成する4種類のCaV1(CaV1.1-CaV1.4)、P/Q、N及びR型を構成する3種類のCaV2(CaV2.1-CaV2.3)、低電位活性化型にはT型を構成する3種類のCaV3(CaV3.1-CaV3.3)の3つのサブファミリーに分類されています[5]。
● 機能調節と細胞内局在
α1サブユニットの機能調節と細胞内局在は、α2/δ、βおよびγサブユニットによって重要な役割を果たされます。これらのサブユニットは、α1サブユニットの発現調節、機能調節や細胞内局在に影響を与え、複数の遺伝子によってコードされています。特にβサブユニットは、α1サブユニットに細胞質側から会合し、VDCCの活性に必要不可欠なサブユニットです[5]。
このように、電位依存性カルシウムチャネルのα1サブユニットは、その複雑な構造と多様なアイソフォーム、および他のサブユニットとの相互作用により、細胞の様々な生理的プロセスにおいて重要な役割を果たしています。
[5] www.sbchem.kyoto-u.ac.jp/mori-lab/research-a.html
カルシウム電位依存型チャネルα1サブユニットの機能
カルシウム電位依存型チャネル(Voltage-dependent calcium channels, VDCC)は、細胞の電気的興奮をカルシウム(Ca2+)依存的な生理応答に変換する役割を担っています。これらのチャネルは、細胞外から細胞内へCa2+を選択的に透過させるイオンチャネルであり、神経細胞や筋細胞を始めとする興奮性細胞において、神経伝達物質放出、筋収縮、遺伝子発現など様々なCa2+依存性の細胞応答を制御します[3]。
VDCCの中心機能は、孔を形成するα1サブユニットが担っており、このサブユニットはチャネルの主たる生物物理学的および薬理学的特性を決定します[6]。α1サブユニットは、約2,000アミノ酸残基からなる膜タンパク質であり、6回膜貫通領域(S1-S6)の構造単位が4回繰り返す構造を有しています。各構造単位のS5とS6領域がCa2+を選択的に透過させるポア領域を形成し、S1-S4領域は電位センサー領域を形成します[4]。
VDCCは、開口する電位により高電位活性化型と低電位活性化型の2つに分類されます。高電位活性化型のVDCCは、α1、α2/δ、βおよびγサブユニットから構成されており、α1サブユニットには10種類のアイソフォームが存在します。高電位活性化型にはL型を構成する4種類のCaV1(CaV1.1-CaV1.4)、P/Q、N及びR型を構成する3種類のCaV2(CaV2.1-CaV2.3)、低電位活性化型にはT型を構成する3種類のCaV3(CaV3.1-CaV3.3)の3つのサブファミリーに分類されています[4]。
α1サブユニットは、VDCCの機能調節や細胞内局在に重要な役割を果たすα2/δ、βおよびγサブユニットと相互作用します。特にβサブユニットは、α1サブユニットのリピートIとIIをつなぐ細胞内リンカーに結合し、α1サブユニットの形質膜における機能的な発現に重要であり、Ca2+チャネル電流の活性化・不活性化の速度や電位依存性を修飾することが知られています[3][5]。
以上のように、カルシウム電位依存型チャネルα1サブユニットは、VDCCの構造と機能の中心を担い、細胞の生理応答において重要な役割を果たしています。
[3] bsd.neuroinf.jp/wiki/%E9%9B%BB%E4%BD%8D%E4%BE%9D%E5%AD%98%E6%80%A7%E3%82%AB%E3%83%AB%E3%82%B7%E3%82%A6%E3%83%A0%E3%83%81%E3%83%A3%E3%83%8D%E3%83%AB
[4] www.sbchem.kyoto-u.ac.jp/mori-lab/research-a.html
[5] www.jstage.jst.go.jp/article/fpj/144/5/144_211/_pdf
[6] webview.isho.jp/journal/detail/abs/10.11477/mf.2425101029
カルシウム電位依存型チャネルα1サブユニットの機能不全
カルシウム電位依存型チャネルα1サブユニットの機能不全は、神経伝達物質の放出、筋収縮、遺伝子発現など、生命活動における基本的な機能に影響を及ぼす可能性があります。カルシウム電位依存型チャネルは、細胞膜の脱分極に応答して活性化し、細胞外から細胞内へカルシウムイオン(Ca2+)を選択的に透過させるイオンチャネルです。これらのチャネルは、α1、α2/δ、β、およびγの4種類のサブユニットから構成されており、その中でもα1サブユニットがイオン透過孔の形成と電位センサーの機能を担っています[4][7]。
α1サブユニットの機能不全は、神経系や筋肉系の疾患に関連しています。例えば、CaV2.1(P/Q型カルシウムチャネル)のα1サブユニットに変異があるrockerマウスは、運動失調や動眼運動異常などの神経疾患を呈します。この変異は、シナプス後部のAMPA受容体の密度及び総数の減少や、プルキンエ細胞樹状突起の形態変化など、シナプス機能異常に関連していることが示されています[5]。
また、電位依存性カルシウムチャネルのα2δサブユニット1の上昇は、神経障害性疼痛の分子メカニズムに関与していることが示されています[8]。これは、α1サブユニットだけでなく、他のサブユニットの異常も神経系の機能不全に関連していることを示唆しています。
さらに、電位依存性カルシウムチャネル病においては、チャネルの機能異常と症状の関係が不明なものが多いですが、骨格筋α1サブユニット遺伝子(CACNL1A3)の異常が関連していることが知られています[10]。これらの研究結果から、カルシウム電位依存型チャネルα1サブユニットの機能不全は、神経系や筋肉系の疾患の発症メカニズムに深く関わっていることが理解されます。
[4] bsd.neuroinf.jp/wiki/%E9%9B%BB%E4%BD%8D%E4%BE%9D%E5%AD%98%E6%80%A7%E3%82%AB%E3%83%AB%E3%82%B7%E3%82%A6%E3%83%A0%E3%83%81%E3%83%A3%E3%83%8D%E3%83%AB
[5] www.nips.ac.jp/release/2007/01/post_78.html
[7] www.sbchem.kyoto-u.ac.jp/mori-lab/research-a.html
[8] www.jstage.jst.go.jp/article/jacd/34/3/34_307/_pdf/-char/ja
[10] imis.igaku-shoin.co.jp/contents/reference/dic_00582-02/582/dic_00582-02_a004b004c066z0011/
カルシウム電位依存型チャネルα1サブユニットをターゲットとした研究開発
カルシウム電位依存型チャネルα1サブユニットは、電位依存性カルシウムチャネル(Voltage-Dependent Calcium Channels, VDCC)の主要な機能単位であり、細胞の電気的興奮をカルシウムイオンの流入に変換する役割を担っています。これらのチャネルは、神経伝達、筋収縮、ホルモン分泌、遺伝子発現など多岐にわたる生理的プロセスに関与しており、特に心筋細胞における収縮機能の調節に重要な役割を果たしています[17][19][20]。
研究開発の観点から、カルシウム電位依存型チャネルα1サブユニットは、心血管疾患、神経疾患、疼痛管理などの治療薬の開発において重要なターゲットとなっています。例えば、心筋細胞におけるL型Ca2+チャネルは、心臓の収縮力を調節するために重要であり、これを標的とした薬剤は高血圧や狭心症の治療に用いられています[18]。
また、α1サブユニットの異なるアイソフォームは、組織特異的な発現パターンを持ち、それぞれが異なる生理的機能を持っているため、特定のアイソフォームを標的とすることで、副作用を最小限に抑えつつ治療効果を高めることが可能です[17][19]。
さらに、α1サブユニットは、β、α2/δ、γといった他のサブユニットと複合体を形成し、これらの補助サブユニットはα1サブユニットの機能を調節することが知られています。これらの補助サブユニットもまた、新たな治療薬の開発における標的としての可能性を秘めています[18][19][20]。
研究開発においては、これらのチャネルの構造や機能の詳細な解明、異なるアイソフォームや補助サブユニットの特定、およびこれらの相互作用の理解が重要です。これにより、疾患のメカニズムの解明や新たな治療薬の開発につながる可能性があります。
さらに、カルシウムチャネルブロッカーとして知られる薬剤群は、これらのチャネルの機能を阻害することで、心血管疾患の治療に広く用いられています。これらの薬剤の改良や新規薬剤の開発においても、α1サブユニットは中心的な役割を果たしています[18][19][20]。
総じて、カルシウム電位依存型チャネルα1サブユニットをターゲットとした研究開発は、心血管疾患、神経疾患、疼痛管理などの分野において、新たな治療薬の開発に大きな影響を与える可能性があります。
[17] www.sbchem.kyoto-u.ac.jp/mori-lab/research-a.html
[18] www.jstage.jst.go.jp/article/fpj/144/5/144_211/_pdf
[19] webview.isho.jp/journal/detail/abs/10.11477/mf.2425101029
[20] www.jstage.jst.go.jp/article/fpj/144/5/144_222/_pdf
Calcium voltage-gated channel alpha1 subunitsに属する遺伝子
CACNA1A
CACNA1B
CACNA1C
CACNA1D
CACNA1E
CACNA1F
CACNA1G
CACNA1H
CACNA1I
CACNA1S