目次
BIN1遺伝子とは:基本情報と機能
BIN1(Bridging Integrator 1)遺伝子は、細胞膜の形成や神経伝達、筋肉機能に重要な役割を果たすタンパク質をコードしています。この遺伝子は第2染色体長腕(2q14.3)に位置し、様々な組織で発現していますが、特に脳と筋肉での機能が重要視されています。1996年にMYCタンパク質(がん遺伝子産物)と相互作用するタンパク質として初めて同定されました。
BIN1遺伝子の基本情報
- 正式名称: Bridging Integrator 1
- 別名: AMPH2(Amphiphysin II)、BOX-dependent MYC-interacting protein 1
- 染色体位置: 2q14.3
- ゲノム座標 (GRCh38): 2:127,048,023-127,107,154
- 遺伝子構造: 20個のエクソンからなり、選択的スプライシングにより少なくとも10種類のアイソフォームが存在
- タンパク質構造: 約451アミノ酸(アイソフォームにより異なる)、約50kDaの分子量
BIN1遺伝子の進化的保存性と構造
BIN1遺伝子は進化的に高度に保存されており、ヒトとマウスのBIN1タンパク質は約95%の配列同一性を持っています。この高い保存性は、BIN1が生物学的に重要な機能を持つことを示唆しています。
BIN1タンパク質には複数の重要な機能ドメインが存在します:
- BAR(BIN1/Amphiphysin/RVS167)ドメイン: 膜の湾曲を感知し促進する役割を担います
- MYC結合ドメイン: がん遺伝子産物であるMYCタンパク質と相互作用します
- SH3(SRC homology-3)ドメイン: 他のタンパク質と相互作用するために重要な領域です
- 核局在シグナル: タンパク質を細胞核へ輸送するための配列を含みます
- プロリンリッチ領域: さまざまなタンパク質との相互作用に関与します
BIN1タンパク質は「橋渡しタンパク質」とも呼ばれ、細胞内の様々なタンパク質と相互作用し、重要な細胞プロセスを調整します。特に注目すべき機能として:
筋肉組織における主要な機能
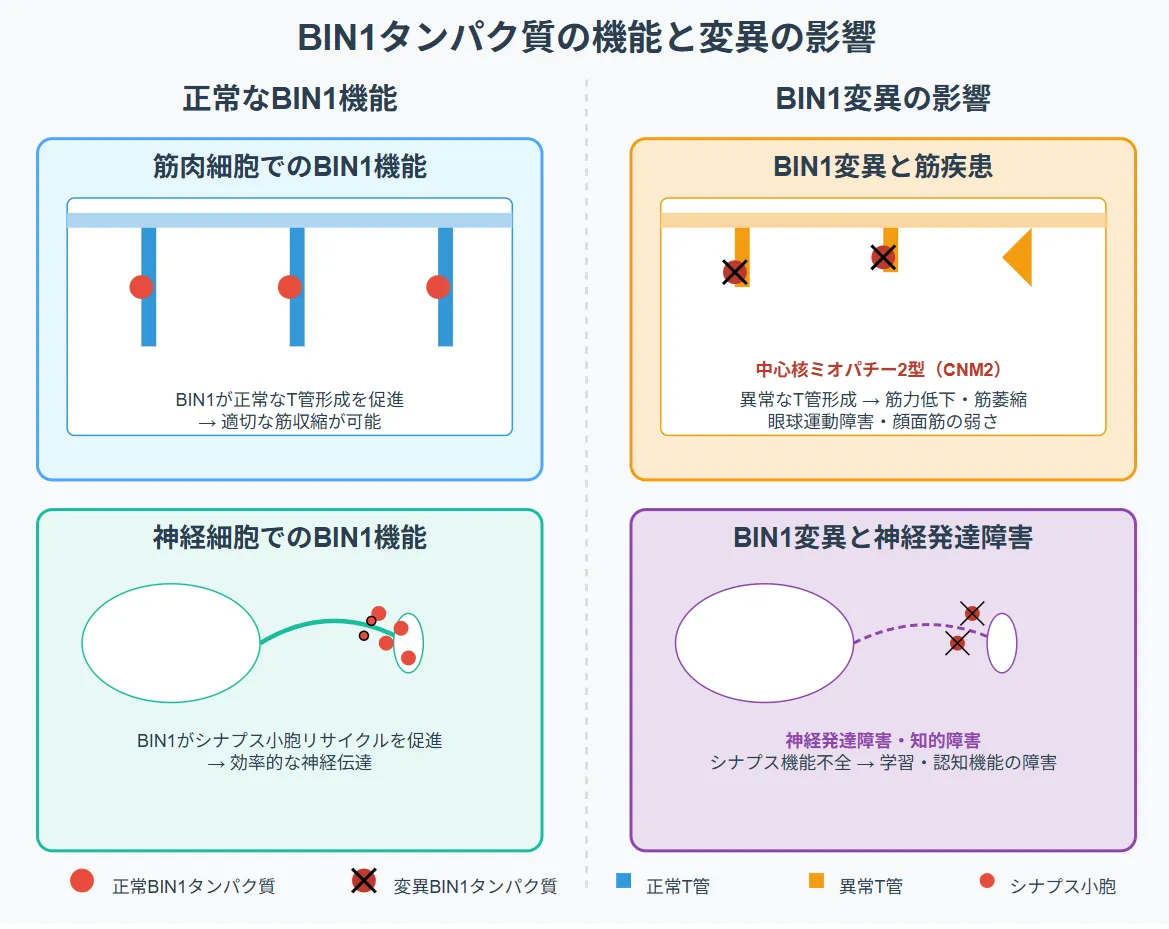
- T管(横行小管)の形成と維持: T管は筋肉細胞の特殊な膜構造で、筋収縮に必須のカルシウムシグナルを伝達します。BIN1はT管の形成と維持に不可欠であり、特にエクソン11によってコードされる部分がホスホイノシチドとの結合に関与しています。T管の異常は筋力低下や筋萎縮の原因になります。
- 筋分化の制御: 筋肉の発達過程において、BIN1の発現は分化に伴って増加します。BIN1は筋分化のマスター制御因子と連携して機能し、細胞周期の停止や筋特異的タンパク質の発現を促進します。
神経系における主要な機能
- エンドサイトーシスの調節: 細胞が物質を取り込む過程を制御し、特に神経伝達物質を含むシナプス小胞のリサイクルに関与しています。
- シナプス小胞のリサイクル: 神経細胞間の情報伝達において、シナプス小胞の再利用を促進し、効率的な神経伝達を維持します。
- 神経突起の形成: 神経細胞の発達過程で、軸索や樹状突起の形成に関与することが示唆されています。
- ミクログリアにおける機能: 脳の免疫細胞であるミクログリアにおいて特異的な役割を持ち、神経炎症プロセスに関与している可能性があります。これはアルツハイマー病との関連が示唆されています。
細胞分裂と腫瘍抑制における役割
- MYCタンパク質(がん遺伝子産物)との相互作用: BIN1はMYCの腫瘍形成活性を抑制する能力を持ち、腫瘍抑制タンパク質として機能します。
- 細胞周期の制御: 酵母のRVS167(BIN1の相同体)と同様に、細胞周期の負の調節因子として機能する可能性があります。
- 免疫監視の調節: BIN1の喪失は免疫系による腫瘍細胞の認識を妨げる可能性があることが、マウスモデル研究で示されています。
タンパク質間相互作用ネットワーク
BIN1は以下のような多様なタンパク質と相互作用することが知られています:
- ダイナミン2(DNM2): 膜分裂に関与するGTPaseで、BIN1とともにT管の形成に重要です。DNM2の変異も中心核ミオパチーを引き起こします。
- インテグリン: 特にラミニン受容体として機能するインテグリンα1、α3、α6BとBIN1は相互作用し、細胞-細胞外マトリックス間の接着を調節します。
- Rab8-Ehbp1l1複合体: この複合体とBIN1の相互作用は、極性細胞における膜輸送に重要です。
これらの多様な機能により、BIN1遺伝子は筋肉の正常な収縮機能や神経細胞の情報伝達、細胞の形態維持において中心的な役割を担っています。組織特異的なアイソフォームの発現パターンにより、BIN1は異なる組織で特化した機能を果たすことができます。
BIN1遺伝子と疾患:筋疾患から知的障害まで
BIN1遺伝子変異が引き起こす主な疾患
BIN1遺伝子の変異は、主に常染色体劣性遺伝形式で中心核ミオパチー2型(CNM2)を引き起こすことが知られています。また、アルツハイマー病のリスク因子としても研究が進んでいます。近年の研究では、知的障害や神経発達障害との関連も示唆されています。
1. 中心核ミオパチー2型(CNM2)
中心核ミオパチー2型はBIN1遺伝子の両アレル(父方と母方の両方)に病的バリアント(変異)がある場合に発症する筋疾患です。主な特徴としては:
- 出生時からの筋力低下や筋緊張低下
- 近位筋(体幹に近い筋肉)の進行性の筋力低下
- 筋生検で特徴的な「中心核」が見られる(筋線維の中心に核が位置する異常な所見)
- 眼球運動障害
- 顔面筋の弱さ
興味深いことに、CNM2患者の一部には軽度から中等度の知的障害を伴うケースが報告されています。これはBIN1遺伝子が筋肉だけでなく、脳の機能にも関与していることを示唆しています。
2. アルツハイマー病との関連
全ゲノム関連解析(GWAS)研究により、BIN1遺伝子の特定のバリアントがアルツハイマー病のリスク増加と関連していることが示されています。BIN1タンパク質はタウタンパク質の病理学的蓄積や神経炎症に関与している可能性があります。
3. 知的障害と神経発達障害
複数の研究がBIN1遺伝子の変異と知的障害の関連を示唆しています:
- モロッコ人の中心核ミオパチー患者で、BIN1遺伝子のR154Q変異と軽度知的障害の併発が報告されています
- BIN1タンパク質は脳の発達期に高レベルで発現しており、神経細胞の形成や成熟に関与している可能性があります
- マウスモデル研究では、Bin1遺伝子の欠損がシナプス機能異常や学習障害を引き起こすことが示されています
症例報告
Claeys et al.(2010)は、BIN1遺伝子にR154Q変異を持つ21歳のモロッコ人男性の症例を報告しています。この患者は幼少期からの筋力低下と筋萎縮に加えて、軽度の知的障害も示していました。これはBIN1遺伝子の変異が筋肉だけでなく認知機能にも影響を与える可能性を示唆しています。
BIN1遺伝子変異のメカニズム
BIN1遺伝子の変異がどのように疾患を引き起こすのかについては、いくつかのメカニズムが提案されています:
BIN1遺伝子変異の病態メカニズム
- T管形成の障害:BIN1タンパク質は筋肉のT管形成に必須であり、その機能不全は筋収縮障害につながります
- 膜の湾曲能の低下:多くのBIN1変異は膜を変形させる能力を損なうため、細胞膜の再構成に影響します
- タンパク質相互作用の喪失:BIN1はDNM2などの他のタンパク質と相互作用しますが、変異によりこの能力が損なわれます
- スプライシング制御の破綻:特定のエクソンのスプライシング異常は、組織特異的な機能障害を引き起こす可能性があります
- 神経細胞での機能不全:脳でのBIN1機能不全はシナプス小胞リサイクルや神経ネットワーク形成に影響する可能性があります
特に知的障害との関連では、BIN1遺伝子が神経細胞の発達やシナプス機能に重要な役割を果たしていると考えられています。マウスモデル研究では、Bin1欠損がシナプス小胞リサイクルの障害や学習能力の低下と関連していることが示されています。
BIN1遺伝子変異の遺伝形式
BIN1遺伝子の病的バリアントによる疾患の遺伝形式についての理解は重要です:
BIN1関連疾患の遺伝形式
- 常染色体劣性遺伝:中心核ミオパチー2型(CNM2)は常染色体劣性遺伝形式をとります。つまり、両親からそれぞれ1つずつ、計2つの変異アレルを受け継いだ場合に発症します。
- 保因者(キャリア):1つの変異アレルのみを持つ親(保因者)は通常症状を示しませんが、子どもに変異を伝える可能性があります。
- 再発リスク:両親が保因者の場合、子どもが疾患を発症するリスクは25%、保因者になるリスクは50%、変異を全く受け継がないリスクは25%です。
スペインのロマ民族では、BIN1遺伝子のR234C変異が創始者効果(founder effect)によって高頻度で見られることが報告されています。これは特定の集団に特有の変異が広がることで、その集団内での疾患の発生率が高くなる現象です。
モザイク変異と低頻度モザイク
一部の症例では、親の体細胞の一部のみにBIN1遺伝子変異が存在する「モザイク」状態が報告されています。これは次世代への遺伝に重要な影響を与える可能性があります:
- 親の体の細胞の一部のみに変異が存在する場合でも、その変異が生殖細胞(卵子や精子)に含まれると、子どもに伝わる可能性があります
- 低頻度モザイク(例:全体の2%の細胞のみが変異を持つ)であっても、子どもへの伝達リスクは「ゼロか1」の二択となります
- これは遺伝カウンセリングにおいて考慮すべき重要な点です
BIN1遺伝子検査の臨床的意義
BIN1遺伝子検査は、以下のような状況で臨床的に意義があります:
- 中心核ミオパチーが疑われる患者の確定診断
- 原因不明の筋力低下を伴う知的障害の評価
- 家族歴がある場合のリスク評価
- 将来の妊娠に関する遺伝カウンセリングのための情報提供
遺伝子検査の種類
ミネルバクリニックでは、知的障害や神経発達障害の原因となる遺伝子変異を検出するために複数の検査オプションを提供しています:
- 知的障害遺伝子検査パネル:BIN1遺伝子を含む、知的障害に関連する多数の遺伝子を同時に解析します
- 自閉症遺伝子検査パネル:自閉症スペクトラム障害と関連する遺伝子変異を検出します
- 発達障害・自閉症・知的障害染色体シーケンス解析:より広範囲なゲノム解析により、大きな染色体異常も検出できます
これらの検査は、症状の原因を特定し、適切な医療管理計画や将来の家族計画のための情報を提供するのに役立ちます。
遺伝カウンセリングの重要性
BIN1遺伝子変異が特定された場合、専門的な遺伝カウンセリングを受けることが重要です。遺伝カウンセリングでは以下のような情報提供と支援が行われます:
遺伝カウンセリングで提供される情報
- 遺伝子変異の意味と健康への影響についての説明
- 疾患の自然経過と予後に関する情報
- 家族内の他のメンバーへのリスク評価
- 将来の家族計画に関するオプションの説明
- 最新の研究や治療法に関する情報
- 適切な専門医や支援サービスの紹介
ミネルバクリニックでは、臨床遺伝専門医が常駐しており、BIN1遺伝子を含む遺伝性疾患に関する専門的な遺伝カウンセリングを提供しています。検査結果に基づいた個別化された情報提供と心理的サポートにより、患者さんとご家族が適切な意思決定ができるようサポートしています。
BIN1遺伝子研究の最新動向
BIN1遺伝子に関する研究は活発に進められており、以下のような最新の研究動向があります:
アルツハイマー病との関連に関する研究
Nott et al.(2019)は、アルツハイマー病に関連するBIN1遺伝子バリアントが、主に脳のミクログリア(特殊な免疫細胞)で機能していることを発見しました。これはアルツハイマー病における神経炎症プロセスとBIN1の関連を示唆しています。
治療法の開発に関する研究
Giraud et al.(2023)は、マウスモデルでMTM1タンパク質(別の筋疾患に関連するタンパク質)の過剰発現が、Bin1欠損による筋力低下を改善できることを示しました。これは将来の治療法開発に重要な意味を持つ可能性があります。
構造と機能の解明
Nakajo et al.(2016)は、BIN1タンパク質がRab8やEhbp1l1などの他のタンパク質と複合体を形成し、エンドソームリサイクリングセンター(ERC)での膜輸送に関与していることを明らかにしました。これはBIN1の細胞内での詳細な機能メカニズムの解明に貢献しています。
今後の研究課題
BIN1遺伝子に関する今後の研究課題としては、以下のような点が挙げられます:
- BIN1遺伝子変異と知的障害の直接的な因果関係の解明
- 組織特異的なBIN1アイソフォームの役割の詳細な解析
- BIN1を標的とした治療法の開発
- アルツハイマー病におけるBIN1の役割のさらなる解明
ミネルバクリニックでの遺伝子検査
ミネルバクリニックでは、BIN1遺伝子を含む知的障害関連遺伝子の検査を提供しています。当院の特徴は以下の通りです:
- 臨床遺伝専門医による直接の診察と説明
- 最新の次世代シーケンサーを用いた高精度な遺伝子解析
- 検査前・検査後の丁寧な遺伝カウンセリング
- 個々の患者さんに合わせた医療管理計画の提案
- 長期的なフォローアップとサポート体制
検査を受けるメリット
遺伝子検査によりBIN1遺伝子変異が確認されると、以下のようなメリットがあります:
- 症状の原因を特定することによる「診断の旅」の終了
- 疾患の自然経過に関する情報の取得
- 将来起こりうる合併症への備え
- 適切な治療やリハビリテーションプランの立案
- ご家族の遺伝的リスクの評価
- 同じ遺伝子変異を持つ患者さん同士のコミュニティへのアクセス
遺伝子検査をご希望の方は、まずはミネルバクリニックまでお気軽にご相談ください。臨床遺伝専門医が丁寧にご説明し、適切な検査をご案内いたします。
まとめ:BIN1遺伝子と遺伝カウンセリングの重要性
BIN1遺伝子は、細胞膜の形成や筋肉・神経細胞の機能に重要な役割を果たしています。この遺伝子の変異は、中心核ミオパチー2型などの筋疾患や、知的障害、アルツハイマー病リスクとの関連が報告されています。
疾患を引き起こすBIN1遺伝子バリアントには:
- K35N(リジン35アスパラギン置換)
- D151N(アスパラギン酸151アスパラギン置換)
- R154Q(アルギニン154グルタミン置換)- 知的障害との関連が報告されている
- R234C(アルギニン234システイン置換)- スペインのロマ民族での創始者変異
- K575X(リジン575終止コドン)
これらの変異は主に常染色体劣性遺伝形式で疾患を引き起こします。発症メカニズムには、T管形成障害、膜湾曲能の低下、タンパク質相互作用の喪失などが含まれます。
遺伝子検査によりBIN1遺伝子変異が確認された場合、専門的な遺伝カウンセリングを受けることが重要です。ミネルバクリニックでは、臨床遺伝専門医による丁寧な説明と心理的サポートを提供し、患者さんとご家族が適切な意思決定ができるようサポートしています。
ミネルバクリニックからのメッセージ
遺伝子検査の結果は、時に予期せぬものかもしれません。しかし、その情報はあなたとお子さんの健康管理に役立つ大切な知識です。どのような結果であっても、当院の臨床遺伝専門医が丁寧に説明し、最適な医療とサポートへの道を一緒に考えていきます。疑問や不安がありましたら、いつでもご相談ください。
BIN1遺伝子を含む知的障害関連遺伝子検査についてさらに詳しく知りたい方は、下記のリンクから情報をご覧いただけます。
参考文献
- Sakamuro D, et al. BIN1 is a novel MYC-interacting protein with features of a tumour suppressor. Nat Genet. 1996;14(1):69-77.
- Wechsler-Reya R, et al. The putative tumor suppressor BIN1 is alternatively spliced in human tumors. Cancer Res. 1997;57(14):3126-31.
- Nicot AS, et al. Mutations in amphiphysin 2 (BIN1) disrupt interaction with dynamin 2 and cause autosomal recessive centronuclear myopathy. Nat Genet. 2007;39(9):1134-9.
- Claeys KG, et al. Phenotype of a patient with recessive centronuclear myopathy and a novel BIN1 mutation. Neurology. 2010;74(6):519-21.
- Lee E, et al. Amphiphysin 2 (Bin1) and T-tubule biogenesis in muscle. Science. 2002;297(5584):1193-6.
- Fugier C, et al. Misregulated alternative splicing of BIN1 is associated with T tubule alterations and muscle weakness in myotonic dystrophy. Nat Med. 2011;17(6):720-5.
- Cabrera-Serrano M, et al. Novel BIN1 mutation causing centronuclear myopathy with myasthenic features. Neuromuscul Disord. 2018;28(7):610-4.
- Nott A, et al. Brain cell type-specific enhancer-promoter interactome maps and disease-risk association. Science. 2019;366(6469):1134-9.
- Giraud MN, et al. MTM1 Gene Therapy Rescues Muscle Force and T-tubule Architecture in a Bin1 Deficient Murine Model of Centronuclear Myopathy. Mol Ther. 2023;31(2):557-68.
- Di Paolo G, et al. Decreased synaptic vesicle recycling efficiency and cognitive deficits in amphiphysin 1 knockout mice. Neuron. 2002;33(5):789-804.
- Muller AJ, et al. Inhibition of indoleamine 2,3-dioxygenase, an immunoregulatory target of the cancer suppression gene Bin1, potentiates cancer chemotherapy. Nat Med. 2005;11(3):312-9.
- Nakajo A, et al. EHBP1L1 coordinates Rab8 and Bin1 to regulate apical-directed transport in polarized epithelial cells. J Cell Biol. 2016;212(3):297-306.
- Wixler V, et al. Identification of novel interaction partners for the conserved membrane proximal region of alpha-integrin cytoplasmic domains. FEBS Lett. 1999;445(2-3):351-5.
- DuHadaway JB, et al. Immunohistochemical localization of Bin1/Amphiphysin II in human tissues: diverse sites of nuclear expression and losses in prostate cancer. J Cell Biochem. 2003;88(3):635-42.
- Wechsler-Reya RJ, et al. Structural analysis of the human BIN1 gene. Evidence for tissue-specific transcriptional regulation and alternate RNA splicing. J Biol Chem. 1997;272(50):31453-8.